3 грудня, 2021
Роль дефіциту калію і магнію у розвитку порушень ритму серця та шляхи корекції
На сьогодні відомо та докладно вивчено чимало факторів ризику розвитку серцево-судинних захворювань (ССЗ), зокрема порушень серцевого ритму. Їх слід враховувати як при первинній, так і вторинній профілактиці ССЗ, а також у комплексному лікуванні. Та чи завжди лікарі зважають на ймовірні порушення електролітного балансу, зокрема таких макроелементів, як калій (К) та магній (Mg)? Чи часто дефіцит К та/або Mg є фактором розвитку аритмій? Які механізми цієї асоціації? Як ефективно корегувати вказані порушення електролітного балансу? Пропонуємо до вашої уваги огляд джерел, присвячених відповідям на ці запитання.
Калій
Калій – один із найважливіших мікроелементів у людському організмі, при цьому більша його частина (приблизно 98%) міститься у клітинах. Він задіяний у регуляції кислотно-лужної рівноваги крові, водного балансу міжклітинної та внутрішньоклітинної рідини, водно-сольового балансу, осмотичного тиску.
Окрім того, калій має такі властивості:
- забезпечує створення мембранного потенціалу, необхідного для скорочення скелетних і серцевого м’язів;
- бере участь у передачі нервових імпульсів та нервовій регуляції серцевих скорочень;
- активує роботу деяких ферментів, вуглеводний і білковий обмін;
- необхідний для синтезу білка, перетворення глюкози на глікоген, видільної функції нирок.
У багатьох фізіологічних процесах К діє синергічно із Mg, та дефіцит останнього часто супроводжується дефіцитом калію (Дудар, 2018).
У дисертаційній роботі K. Tazmini (2020) детально вивчено клітинну патофізіологію та клінічні прояви у хворих з електролітним дисбалансом з акцентом на гіпокаліємію. Ґрунтуючись на власних та інших релевантних дослідженнях, автор зазначає, що порушення електролітного балансу часто зустрічаються і пов’язані зі збільшенням захворюваності, смертності та зниженням якості життя.
Серед інших видів електролітного дисбалансу гіпокаліємія є одним із найпоширеніших і асоційована, зокрема, з підвищеним ризиком розвитку аритмій. У даній роботі наведені переконливі докази того, що гіпокаліємія підвищує схильність до аритмій за різними механізмами у передсердних і шлуночкових кардіоміоцитах. Цікаво, що в деяких тематичних дослідженнях проілюстровано відновлення синусового ритму при фібриляції передсердь на тлі гіперкаліємії, при цьому науковці припускають, що підвищення рівня калію у плазмі може мати терапевтичний потенціал при аритміях.
Дефіцит К ініціює складні біохімічні процеси, як-от зниження активності Na+/K+-АТФази, що згодом призводить до перевантаження Ca2+, активації Ca2+/кальмодулінзалежної кінази II та деполяризації, що у кінцевому підсумку спричиняє зростання ризику шлуночкових аритмій і раптової серцевої смерті при СН (Scogestad, Aronsen, 2018).
Тяжка гіпокаліємія може погіршити тенденцію та прогноз аритмії (Mattsson et al., 2016). Так, що нижчим є рівень калію, то більша ймовірність виникнення шлуночкових аритмій. У дослідженнях N. Mattsson et al. (2016) та C. Bird et al. (2017) було продемонстровано, що у пацієнтів із тяжким дефіцитом К (≤3,1 ммоль/л) спостерігався підвищений ризик надшлуночкової аритмії та ектопії шлуночків.
Магній
Магній – найпоширеніший внутрішньоклітинний бівалентний катіон, необхідний для підтримання нормальної клітинної фізіології та обміну речовин. Mg діє як кофактор численних ферментів, регулює роботу іонних каналів та вироблення енергії. У серці Mg відіграє ключову роль у модуляції збудження нейронів, внутрішньосерцевої провідності та скорочення міокарда шляхом регулювання низки іонних транспортерів, зокрема калієвих та кальцієвих каналів. Дані спостережень продемонстрували зв’язок між низькими концентраціями магнію у сироватці крові та розвитком атеросклерозу, ішемічної хвороби серця, аритмій, серцевої недостатності (СН) (Tangvoraphonkchai, Davenport, 2018).
На додаток, Mg модулює запалення і окислювальні процеси, що, як відомо, є тригерами атерогенезу і ССЗ. Також магній є:
- фізіологічним антагоністом кальцію (Ca), що забезпечує модифікацію мембранного потенціалу (Wu Lipsius, 1990; Madden et al., 1984);
- регулятором агрегації та адгезії тромбоцитів (Hwang et al., 1994; Rukshin et al., 2002);
- модулятором ендотеліальної функції (Pearson et al., 1998; Maier et al., 2004).
Таким чином, магній потенційно має суттєвий вплив на патогенез ССЗ, зокрема порушень ритму.
Дефіцит магнію – проблема світового масштабу. Так, згідно з результатами дослідження NHANES (2001‑2006), майже половина дорослих американців споживають недостатню кількість магнію з їжею та водою. За даними епідеміологічного дослідження H.F. Schimatschek та R. Rempis (2001), у Німеччині середня поширеність нестачі магнію становила 14,5%.
Цікаво, що серед госпіталізованих пацієнтів у 42% виявляється гіпомагніємія. Проте лікарі призначають аналіз рівня Mg лише у 7% випадків. Клінічно зазвичай вимірюють вміст магнію у сироватці крові, хоча менш ніж 1% магнію існує позаклітинно; отже, сироватковий магній не завжди точно відображає загальний рівень Mg в організмі. Фактично, сироватковий рівень Mg може бути нормальним, незважаючи на виснаження його загального вмісту в організмі (Di Nicolantonio et al., 2018; Van Laecke, 2019).
Як і гіпокаліємія, дефіцит магнію призводить до зменшення активності Na-K-АТФази, що зумовлює зниження рівня Mg і К у кардіоміоцитах (Di Nicolantonio et al., 2018). Внаслідок таких змін підвищується схильність коронарних артерій до спазму, що може спричиняти розвиток інфаркту міокарда й аритмій (Kubena et al., 1990).
Наведені дані свідчать про те, що визначення цього іону можна використовувати для скринінгу та профілактики ССЗ. Своєю чергою препарати Mg є потенційним додатковим компонентом до фармакотерапії ССЗ, зокрема аритмій.
У новому фремінгемському дослідженні вивчали співвідношення доза – відповідь натрію (Na), K, Mg та Ca із ризиком розвитку ССЗ, а також комбіновану дію цих мінералів (Pickering et al., 2021). Загалом у дослідженні взяли участь чоловіки та жінки віком 30‑64 роки (n=2362) без ССЗ на початковому етапі. Тривалість спостереження становила 12 років.
За результатами випробування, низьке споживання Na (<2500 vs ≥3500 мг/добу) не асоціювалося із нижчим ризиком ССЗ. Споживання Ca ≥700 (vs <500) мг/добу корелювало зі статистично незначущим кардіоваскулярним ризиком. На противагу, споживання калію ≥3000 (vs <2500) мг/добу було пов’язано із 25% зменшенням серцево-судинного ризику, а Mg ≥320 (vs <240) мг/добу – привело до зменшення ймовірності розвитку ССЗ на 34% (рис. 1).
Рис. 1. Співвідношення доза – відповідь між споживаннями мінералів та частотою ССЗ
Примітка: ВР – відносний ризик. Пунктирні лінії представляють 95% довірчий інтервал.
Корекція порушень електролітного балансу
Для корекції описаних порушень електролітного балансу часто недостатньо лише збалансованої дієти чи застосування біологічних добавок. У більшості випадків гіпокаліємії та магніємії необхідні препарати з адекватним вмістом К та Mg, задовільною біодоступністю і низькою токсичністю.
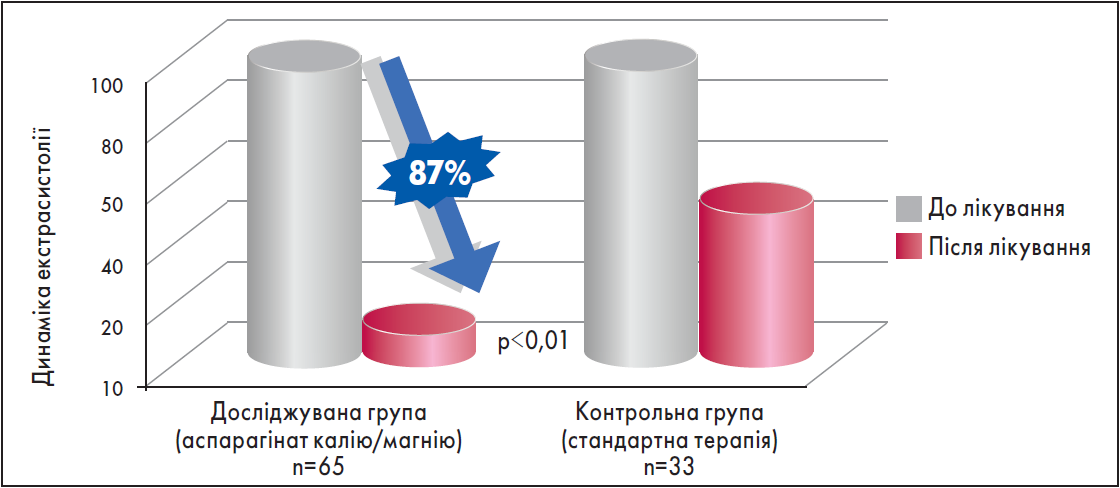
У даному контексті привертає увагу лікарський засіб Панангін Форте, що містить 280 магнію аспарагінату та 316 мг калію аспарагінату. Показано, що використання аспарагінату калію та аспарагінату магнію приводить до зменшення екстрасистолії у пацієнтів з ІХС на 87% (рис. 2) (Zhi et al., 2007).
Рис. 2. Антиаритмічний ефект препарату Панагін форте у пацієнтів з ІХС
Крім того, вказане дозування є зручним, виваженим та дозволяє спростити схему приймання препарату (1 таблетка тричі на день забезпечує добову дозу К та Mg), що, закономірно, покращує комплаєнс пацієнтів. До того ж калій та магній у вигляді аспарагінату мають низку переваг, серед яких (Manz, Susilo, 2002; Громова, 2006; Zhi et al., 2007):
- Вища біодоступність порівняно з неорганічними сполуками: 35 та 8% відповідно.
- Низька токсичність (LD50 >400 мг/кг).
- Поєднання калію, магнію та аспарагінат-аніону сприяє захисту міокарда й додатково забезпечує зниження ризику розвитку аритмій.
Підготувала Наталія Нечипорук