31 січня, 2022
Ведення пацієнтів із тикозними розладами: сучасні підходи до діагностики та лікування
 Тикозний розлад є хронічною психоневрологічною патологією, що зазвичай розвивається у дитинстві. Антипсихотичні препарати, такі як рисперидон, галоперидол, тіаприд та сульпірид, широко використовують у лікуванні тиків. Однак їх застосування є обмеженим через поширені побічні ефекти, такі як екстрапірамідні реакції, надмірна вага, нудота тощо. Відповідно, існує незадоволена потреба в ефективних та безпечніших ліках для терапії тиків, особливо у дітей.
Тикозний розлад є хронічною психоневрологічною патологією, що зазвичай розвивається у дитинстві. Антипсихотичні препарати, такі як рисперидон, галоперидол, тіаприд та сульпірид, широко використовують у лікуванні тиків. Однак їх застосування є обмеженим через поширені побічні ефекти, такі як екстрапірамідні реакції, надмірна вага, нудота тощо. Відповідно, існує незадоволена потреба в ефективних та безпечніших ліках для терапії тиків, особливо у дітей.
Епідеміологія та класифікація
Тикозні розлади зустрічаються у 0,3‑1% населення планети. Зазвичай симптоми з’являються у віці 2‑15 років, а пік маніфестації припадає на 6‑8 років (Марценковський, 2017). Отже, тики – це раптові, повторювані, стереотипні та неритмічні рухи, які переважно спостерігаються в дітей та підлітків. Належний збір анамнезу та феноменологія є ключем до встановлення правильного діагнозу, оскільки буває складно відрізнити тики від інших гіперкінетичних розладів.
Залежно від симптомів тики можуть бути моторними чи звуковими (фонічними). Моторні проявляються рухами тіла, такими як посмикування голови, кінцівок, гримасами обличчя. Натомість фонічні тики виникають унаслідок повторюваних скорочень м’язів гортані, глотки, носа або дихальних шляхів, тобто це звуки, що «не стосуються справи», такі як пирхання, кашель, відкашлювання, клацання, дзижчання або свист.
За даними досліджень, частота хронічних моторних тикозних розладів коливається від 3 до 50, тоді як голосових – від 2,5 до 9,4 на 1 тис. осіб. Загалом транзиторні тики зустрічаються досить часто і вражають до 20% дітей шкільного віку. Своєю чергою поширеність синдрому Туретта, що характеризується численними моторними тиками та хоча б одним фонічним, коливається в межах 2,6‑38 на 1 тис. дітей (Scahill et al., 2014).
Згідно з феноменологічною класифікацією моторних тиків J. Jankovic et al. (1997), тики класифікуються наступним чином:
- клонічні, що зачіпають лише один м’яз або групу м’язів, викликаючи короткі ривки;
- дистонічні – повільніші, виникають через короткочасне збереження ненормальної (нефізіологічної) пози;
- тонічні – відображають ізометричне скорочення, що зазвичай проявляється короткочасною напругою м’язів живота або кінцівок.
Отже, прикладами рухових тиків є мигання, закочування очей, кивання головою, знизування плечима та стиснення живота. Дистонічні тики включають окулогіричні рухи (судоми погляду), тривале відкривання рота, блефароспазм та кривошию. Складні рухові тики є скоординованими моделями рухів за участю більш ніж однієї групи м’язів: нахили, стрибки, стусани, плювки, непристойні жести (копропраксія) тощо. Складні звукові тики представлені висловлюваннями: словами, фразами, ненормативною лексикою або образами за расовою ознакою (копролалія), повторенням чужих (ехолалія) чи власних слів (палілалія).
Тикозні розлади характеризуються запобіжним позивом перед моторним або звуковим тиком із тимчасовим полегшенням позивів за рахунок тику. Пацієнти пояснюють передчуття позивів як відчуття дискомфорту, стискання чи парестезії зсередини.
Прояви тиків зазвичай загострюються на тлі тривоги та стресу. Цілком можливо, що під час стресу здатність пригнічувати тики знижується. Анатомічний розподіл тиків змінюється з віком. Частота і тяжкість симптомів також варіюють із плином часу.
Поведінкові особливості
Приблизно 65% дітей і підлітків із хронічними руховими або вокальними тиками мають супутні розлади. Приблизно у 90% пацієнтів із тикозними розладами спостерігається один чи кілька коморбідних психічних станів. Імовірність наявності супутніх розладів зростає з посиленням тяжкості тиків, раннім початком і обтяженим сімейним анамнезом (Марценковський, 2017).
Зокрема, обсесивно-компульсивні симптоми часто пов’язані з тикозними розладами (Rothenberger, Roessner, 2019). До того ж вважається, що за етіологією обсесивно-компульсивний (ОКР) та тикозний розлади тісно взаємопов’язані (Perez-Vigil et al., 2016).
Поведінкові симптоми, такі як синдром дефіциту уваги з гіперактивністю (СДУГ) й ОКР, зазвичай спостерігаються у пацієнтів із синдромом Туретта і часто передують руховим та звуковим тикам як початкові прояви (Mittal, 2020). Симптоми ОКР у дітей із синдромом Туретта стають серйознішими у більш пізньому віці та зберігаються частіше, ніж симптоми тику.
Вочевидь, ці супутні поведінкові стани нерідко заважають навчанню та знижують успішність. Під час дослідження у 21% американських школярів було виявлено тики й супутні помітні поведінкові симптоми, такі як ОКР, СДУГ, тривога розлуки, надмірне занепокоєння, проста фобія, соціальна фобія, агорафобія, манія, велика депресія та опозиційна поведінка (Carter et al., 2000).
Встановлення діагнозу та диференціальна діагностика
Застосування специфічних опитувальників або напівструктурованих інтерв’ю для скринінгу власне симптоматики тикозних розладів, таких як єльська шкала оцінки тикозних проявів (YGTSS) та шкала оцінки тяжкості синдрому Туретта (TSSS), не є обов’язковим для встановлення діагнозу (Leckman et al., 1989; Walkup et al., 1992). Водночас вони рекомендовані для визначення клінічних особливостей і тяжкості розладу. За допомогою переглянутого єльського списку симптомів синдрому Туретта (TSSL-R) можна провести додаткову оцінку зі слів батьків або самооцінку (Марценковський, 2017).
За потреби проводять ретельне фізичне і неврологічне обстеження, зокрема електроенцефалографію. Основною метою є виключення інших захворювань, які можуть викликати подібні симптоми, наприклад фокальної епілепсії. У разі підозри на органічне ураження головного мозку використовують магнітно-резонансну томографію.
Проведення електрокардіографії, аналіз функціонування щитоподібної залози або інших процедур (наприклад, метаболічних тестів) за відсутності ознак, що дозволяють запідозрити відповідні порушення, не рекомендовані. Також не рекомендовано оцінювати рівень інтелекту пацієнта, якщо немає інших даних, які свідчать про наявні проблеми у цій сфері. Інформація із заповнених анкет надає хорошу можливість проаналізувати його стан у складних ситуаціях, навіть якщо ремісія є тривалою (Марценковський, 2017).
Стани, що потребують проведення ретельної диференціальної діагностики, наступні:
- міоклонус;
- дистонія;
- атетоз;
- хорея;
- стереотипії;
- синдром неспокійних ніг;
- судоми.
Сенсорний феномен позивів із полегшенням після руху також спостерігається при акатизії, стереотипії та синдромі неспокійних ніг. Усі гіперкінетичні розлади, особливо акатизія, та функціональні рухи можуть пригнічуватися, але меншою мірою, ніж тики (Tnenganat et al., 2019). Якщо рухи мультифокальні або мають мігруючий характер, слід враховувати міоклонус та хорею. Тики іноді зберігаються під час сну, а порушення сну зустрічаються і в пацієнтів із синдромом Туретта (Kirov et al., 2014).
Описано кілька випадків тиків після застосування варенікліну, який є частковим агоністом α4β2-нікотинових ацетилхолінових рецепторів нейрона, що посилює вивільнення дофаміну та зазвичай використовується як препарат для лікування тютюнової залежності. Тож про нього також не слід забувати при зборі анамнезу (Mittal et al., 2017).
Терапевтичні стратегії
Лікування тиків – це спільна й індивідуалізована терапія, що потребує психоосвіти пацієнтів і членів їхніх родин, клінічної оцінки та обговорення доступних методів, як-то поведінкові чи фармакологічні. Зокрема, слід звертати особливу увагу на ефективність лікарських засобів та профілі їх безпеки (Mittal, 2020). Для пацієнтів із тяжкими тиками при синдромі Туретта, стійкими до медикаментозної та поведінкової терапії, можна також застосовувати глибоку стимуляцію мозку (Pringsheim et al., 2019).
За наявності коморбідних розладів важливо оцінити, який саме розлад найбільшою мірою впливає на соціальне функціонування дитини і зумовлює потребу в нагальному лікуванні. Наприклад, лікування коморбідного гіперкінетичного розладу може сприяти поліпшенню здатності пригнічувати тики, тоді як призначення психостимуляторів, насамперед метилфенідату, – спровокувати посилення тикозної симптоматики. В інших випадках метилфенідат здатний знизити тяжкість екстрапірамідних побічних ефектів та асоційованих із ними рухових порушень: усунути виникнення окулогіричних кризів, дискінезій та акатазії у дітей і підлітків, що отримують терапію антипсихотиками.
Загалом фармакологічне лікування слід проводити шляхом повільного нарощування доз, оцінюючи ефективність та переносимість медикаменту через однакові проміжки часу. Після підбору оптимальної дози препарат варто приймати систематично протягом принаймні одного року. Надалі, наприкінці підліткового віку, дозування поступово зменшують. При визначенні необхідності продовження терапії слід враховувати високий рівень імовірності спонтанного досягнення ремісії (Марценковський, 2017).
Хронічні тики та синдром Туретта: положення рекомендацій Американської академії неврології
У 2019 р. Американська академія неврології (AAN) оновила настанову з лікування тиків у осіб із синдромом Туретта та хронічними тиками (Pringsheim et al., 2019). Зокрема, поведінкова терапія та застосування α-агоністів (як-то гуанфацин і клонідин) рекомендовані як препарати першої лінії при тикозних розладах легкого та помірного ступенів тяжкості. Стосовно антипсихотичної терапії в рекомендаціях зазначається, що галоперидол, рисперидон, арипіпразол і тіаприд із більшою ймовірністю, ніж плацебо зменшують тяжкість тиків, тоді як доказів щодо визначення відносної ефективності пімозиду, зипразидону та метоклопраміду бракує.
Натомість наявні дані щодо вищого ризику рухових розладів порівняно із плацебо внаслідок застосування галоперидолу, пімозиду та рисперидону, збільшення маси тіла – рисперидону й арипіпразолу, сонливості – рисперидону і тіаприду, подовження інтервалу QT – пімозиду та зростання рівня пролактину – галоперидолу, пімозиду й метоклопраміду.
Систематичні огляди випробувань та когортних досліджень демонструють збільшення ймовірності рухових розладів, спричинених лікарськими засобами (включно із пізньою дискінезією, медикаментозним паркінсонізмом, акатизією, гострою та пізньою дистонією), підвищення ваги, несприятливі метаболічні ефекти, а також підвищення рівня пролактину за пролонгації приймання антипсихотиків першого й другого покоління (Leucht et al., 2013). Зокрема, тривале використання метоклопраміду пов’язане з пізньою дискінезією. При цьому відносна схильність до зазначених побічних ефектів залежить від лікарського засобу та часто – від його дози. Своєю чергою різке припинення застосування антипсихотиків може спричинити дискінезію відміни.
Загалом антипсихотики можна призначати для лікування тиків, коли користь від нього перевищує ризики (Pringsheim et al., 2019). При тиках слід приймати антипсихотики у найнижчих ефективних дозуваннях, щоб знизити ймовірність розвитку несприятливих явищ. Лікарі мають контролювати рухові розлади, спричинені препаратами, а також метаболічні та гормональні побічні ефекти антипсихотиків, використовуючи протоколи моніторингу, що ґрунтуються на фактичних даних.
Необхідно проводити електрокардіографію та вимірювати інтервал QT до і після початку приймання пімозиду або зипразидону, або якщо антипсихотики призначають одночасно з іншими ліками, які можуть подовжувати інтервал QT.
При прийнятті рішення щодо відміни антипсихотиків у пацієнтів із тиками лікарі мають поступово знижувати дозування протягом декількох тижнів або місяців, щоб уникнути дискінезії відміни.
Призначення ін’єкцій ботулінічного токсину для лікування підлітків та дорослих із локалізованими й набридливими простими руховими тиками можливе у випадках, коли користь від терапії переважує ризики (рівень доказовості C). Ін’єкції ботулотоксину можуть викликати слабкість та гіпофонію, але ці ефекти є тимчасовими.
У рекомендаціях AAN запропоновано застосовувати топірамат у таких випадках:
- у пацієнтів із тиками помірної тяжкості, якщо вони є обтяжливими;
- бракує задовільної відповіді на втручання;
- наявні несприятливі наслідки інших методів лікування.
Для осіб із легкими тиками, але такими, що викликають занепокоєння, за відсутності задовільної відповіді від інших методів терапії чи побічних ефектів топірамат може бути корисною альтернативою. Препарат зазвичай добре переноситься у низьких дозах (25‑150 мг/добу) (Pringsheim et al., 2019).
Топірамат – антиконвульсант другої генерації широкого спектра дії
Топірамат – це препарат для моно- та комбінованої протисудомної терапії, що є часто застосовуваним антиконвульсантом широкого спектра дії (Nevitt et al., 2019). Натепер накопичено значну базу даних щодо балансу ефективності топірамату та профілю побічних ефектів, яка свідчить на користь його застосування як препарату першої лінії при низці неврологічних розладів (есенціальному треморі, розладах епілептичного ґенезу, мігрені тощо).
Як антиконвульсант другого покоління топірамат діє за множинними механізмами:
- обмежує повторні розряди нейронів, впливаючи на вольтажзалежні натрієві канали;
- потенціює гальмування, опосередковане γ-аміномасляною кислотою, чинить вплив на її рецептори;
- блокує глутамат-опосередковане збудження нейронів через дію на рецептори α-аміно‑3-гідрокси‑5-метилізоксазол‑4-пропіонової кислоти (АМПК) та каїнатні рецептори;
- помірно знижує амплітуди вольтажзалежного кальцієвого току завдяки взаємодії з кальцієвими каналами;
- є антагоністом ізоензимів II і IV, оскільки впливає на карбоангідразу.
Зазначені механізми дії визначають ефективність топірамату при різних типах нападів та епілептичних синдромах: фокальних, середньо-генералізованих, деяких ідіопатичних генералізованих епілепсіях. Препарат застосовують у педіатричній практиці і при лікуванні дорослих пацієнтів у режимі монотерапії та як засіб допоміжного лікування (Омельяненко та співавт., 2012; Okuyama et al., 2016).
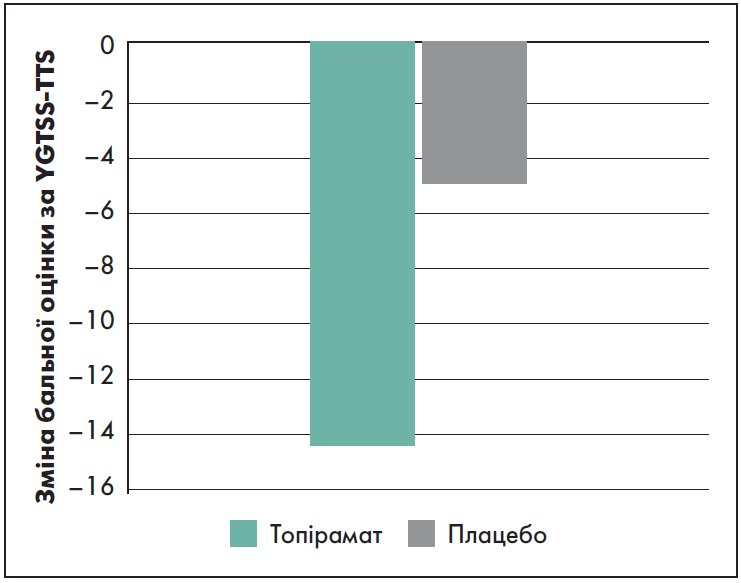
Топірамат порівняно із плацебо показав статистично значуще зниження балів за єльською глобальною шкалою тяжкості тиків (YGTSS-ТТS) у пацієнтів із синдромом Туретта (Jankovic et al. 2010). У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні взяли участь 29 пацієнтів (26 чоловіків та 3 жінки) віком від 7 до 65 років (середній вік – 16,5 років), що мали симптоми від помірних до тяжких. Первинною кінцевою точкою був загальний показник тяжкості тиків, який поліпшився у групі топірамату (середня доза – 118 мг) на 14,29 бала порівняно з вихідним рівнем до 5-го візиту (на 70-ту добу), тоді як на тлі плацебо – лише на 5 балів (рисунок). Відмінностей у частоті небажаних явищ між двома групами лікування не спостерігалося.
Рисунок. Зменшення тяжкості тиків за шкалою YGTSS-ТТS у пацієнтів із синдромом Туретта на тлі терапії топіраматом порівняно із плацебо
Адаптовано за Jankovic et al., 2010
Місце топірамату в лікуванні тикозних розладів
Дані двох метааналізів підтвердили, що ефективність топірамату при тикозних розладах була вищою, ніж у галоперидолу або тіаприду, при цьому його застосування супроводжувалося меншою кількістю побічних ефектів (Yang et al. 2013; Zheng et al. 2015). Слід зазначити, що нині атипові антипсихотики (такі як арипіпразол) широко використовують для лікування тиків (Wang et al., 2017; Yang et al., 2019). Зокрема, арипіпразол вважається препаратом першої лінії при тикозних розладах у Японії (Hamamoto et al., 2019). При цьому лише в одному дослідженні з невеликою вибіркою арипіпразол порівнювали з топіраматом, і між ними не було виявлено значних відмінностей (Wang 2015).
Останніми роками було проведено кілька нових рандомізованих контрольованих випробувань топірамату при лікуванні тикозних розладів, які підтвердили його ефективність та сприятливий профіль безпеки. Нещодавній метааналіз даних 14 досліджень продемонстрував, що топірамат порівняно із галоперидолом і тіапридом є перспективним засобом із кращою ефективністю для застосування у дітей із тикозними розладами (Yu et al., 2020). Своєю чергою до метааналізу даних щодо безпеки було включено результати 15 досліджень. Відносний ризик небажаних явищ становив 0,56 (95% довірчий інтервал 0,44‑0,72; p=0,03), що свідчило про вельми високу гетерогенність підгруп за різними умовами порівняння.
Загалом результати метааналізу підтвердили ефективність топірамату при лікуванні тикозних розладів. Було показано, що топірамат є дієвішим порівняно з галоперидолом і тіапридом та спричиняє меншу кількість несприятливих явищ (Yu et al., 2020).
Окрім того, в деяких публікаціях повідомлялося, що топірамат може посилювати транспорт глюкози й ефект інсуліну та пригнічувати апетит за рахунок антагонізму гіпоталамічних рецепторів АМПК (Okuyama et al., 2016; Cicek et al., 2018). Таким чином, на додаток до посилення дії антипсихотиків, топірамат можна використовувати як ад’ювантний препарат з атиповими антипсихотиками у пацієнтів із тикозними розладами, в яких спостерігається підвищення ваги, особливо резистентних до лікування. Завдяки клінічному ефекту щодо зменшення маси тіла, він також є перспективним засобом для осіб із тикозними розладами та ожирінням (Герджикова та співавт., 2018).
У багатьох дослідженнях було показано, що топірамат можна використовувати для лікування пацієнтів з ОКР, зокрема резистентними формами (Mowla et al., 2010; Berlin et al., 2011; Afshar et al., 2014). Метааналіз підтвердив, що топірамат є ефективним допоміжним засобом для лікування стійких до терапії компульсивних розладів (Zhou et al., 2019).
Висновки
Топірамат є перспективним препаратом для моно- та комбінованої терапії дітей і дорослих, що страждають на тикозні розлади. Дані досліджень підтверджують, що топірамат ефективніший, ніж галоперидол і тіаприд при лікуванні тикозних розладів у дітей. Також топірамат є потенційним засобом вибору для пацієнтів із тиками, які мають ожиріння або ОКР.
UA-TOPI-PUB-122021-011
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 4 (59) 2021 р.