2 лютого, 2022
Вторинна інфекція в пацієнтів із COVID-19, госпіталізованих до відділень реанімації та інтенсивної терапії
21-23 жовтня відбувся VIIІ Національний конгрес анестезіологів України.
Традиційно чималу увагу було приділено проблемним питанням ведення пацієнтів із тяжким перебігом COVID‑19. Про особливості лікування пацієнтів із коронавірусною хворобою, госпіталізованих до відділень реанімації та інтенсивної терапії (ВРІТ), розповів завідувач кафедри анестезіології та інтенсивної терапії Національного університету охорони здоров’я України ім. П. Л. Шупика (м. Київ), доктор медичних наук, професор Олег Анатолійович Лоскутов.
 На початку своєї доповіді професор нагадав, що однією з основних причин летальних наслідків при COVID‑19 є т. зв. цитокіновий шторм, який характеризується надмірним синтезом і вивільненням цитокінів із подальшим формуванням гіперімунної системної запальної відповіді. Лабораторним підтвердженням цитокінового шторму є суттєве підвищення рівнів IL‑6, С‑реактивного білка, фактора некрозу пухлини.
На початку своєї доповіді професор нагадав, що однією з основних причин летальних наслідків при COVID‑19 є т. зв. цитокіновий шторм, який характеризується надмірним синтезом і вивільненням цитокінів із подальшим формуванням гіперімунної системної запальної відповіді. Лабораторним підтвердженням цитокінового шторму є суттєве підвищення рівнів IL‑6, С‑реактивного білка, фактора некрозу пухлини.
Клінічний прояв цитокінового шторму – підвищення проникності капілярів (синдром системного капілярного витоку), що зумовлює вихід рідини та білків в інтерстиціальний простір і набряк тканин. З боку дихальної системи типова ознака цитокінового шторму – розвиток гострого респіраторного дистрес-синдрому (ГРДС) та дихальної недостатності.
Характерна особливість патогенезу SARS-CoV-2 – піроптоз, що являє собою одну із форм запрограмованої загибелі клітини. В основі механізму піроптозу лежить активація каспази‑1, яка сприяє утворенню інтерлейкінів IL‑1β і IL‑18. Зазначені прозапальні медіатори вбудовуються в ліпідну мембрану клітини та спричиняють її перфорацію і руйнування. Порушення цілісності мембрани супроводжується загибеллю клітини та вивільненням її вмісту.
На сьогодні цитокіновий шторм і піроптоз вважаються основною причиною смертності при COVID‑19. Сучасні терапевтичні стратегії, спрямовані на стримування проявів цитокінового шторму та піроптозу при COVID‑19, передбачають застосування глюкокортикоїдів, а також антагоністів IL‑6, зокрема тоцилізумабу.
Глюкокортикоїди в лікуванні COVID‑19
Для досягнення сприятливого результату в пацієнтів із тяжким перебігом COVID‑19 важливий час прийому та дозування глюкокортикоїдів; занадто раннє їх введення гальмує запуск механізму імунного захисту організму, збільшуючи в такий спосіб вірусне навантаження та підвищуючи ризик несприятливих наслідків.
Інгібування надмірного запалення на ранній стадії цитокінового шторму (своєчасне виявлення зростання рівня IL‑6) за допомогою введення глюкокортикоїдів ефективно запобігає розвитку ГРДС і порушенню функцій інших органів.
Для пацієнтів із прогресуючим погіршенням показників оксигенації та надмірною запальною відповіддю доцільно використовувати глюкокортикоїд нетривалим курсом (3-5 днів); рекомендована доза метилпреднізолону – 1-2 мг/кг/добу (Zhou Y. H. et al., 2020).
Антагоністи IL‑6
Тоцилізумаб – антагоніст IL‑6, що пригнічує функцію імунної системи; його застосування є ефективним за умови введення на ранніх етапах розвитку цитокінового шторму.
Стартова доза препарату становить 4-8 мг/кг. Рекомендується розчиняти 400 мг тоцилізумабу в 100 мл з 0,9% хлориду натрію та вводити внутрішньовенно крапельно протягом щонайменше 1 год.
Для пацієнтів із низькою ефективністю першої дози додаткова доза може бути застосована через 12 год (доза така сама, як і початкова) з максимальною кумулятивною дозою не більше двох.
Але на тлі призначення тоцилізумабу існують побоювання клініцистів щодо зростання ризику приєднання вторинної бактеріальної інфекції у зв’язку із пригніченням імунної відповіді. Наразі дані клінічних досліджень не надають однозначної відповіді на це запитання, що спонукало українських фахівців провести власне ретроспективне дослідження ефективності та безпеки тоцилізумабу в пацієнтів із тяжким перебігом COVID‑19. Як первинну кінцеву точку було обрано частоту розвитку вторинної бактеріальної інфекції у пацієнтів із COVID‑19 на тлі призначення тоцилізумабу. До випробування не залучали пацієнтів із цитопенією, хворих із бактеріальною або грибковою інфекцією при госпіталізації, осіб, котрі отримують імуносупресивну терапію.
Пацієнти основної групи отримували 400 мг тоцилізумабу внутрішньовенно з можливістю повторного введення залежно від клінічної відповіді (8 мг/кг). Пацієнти контрольної групи отримували лікування згідно зі стандартизованим протоколом.
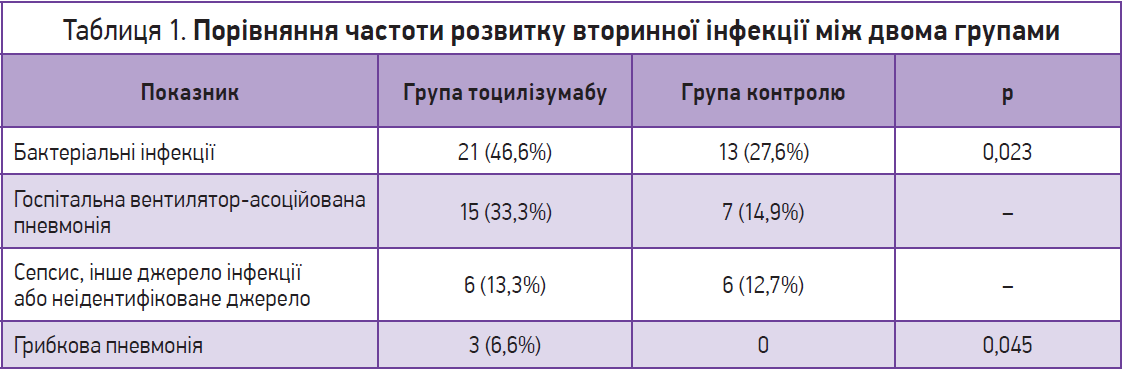
Частота розвитку вторинних бактеріальних інфекцій становила 46,6% у групі тоцилізумабу та 27,6% у групі контролю. Також у групі тоцилізумабу спостерігалася вища частота госпітальних пневмоній та грибкових пневмоній (табл. 1).
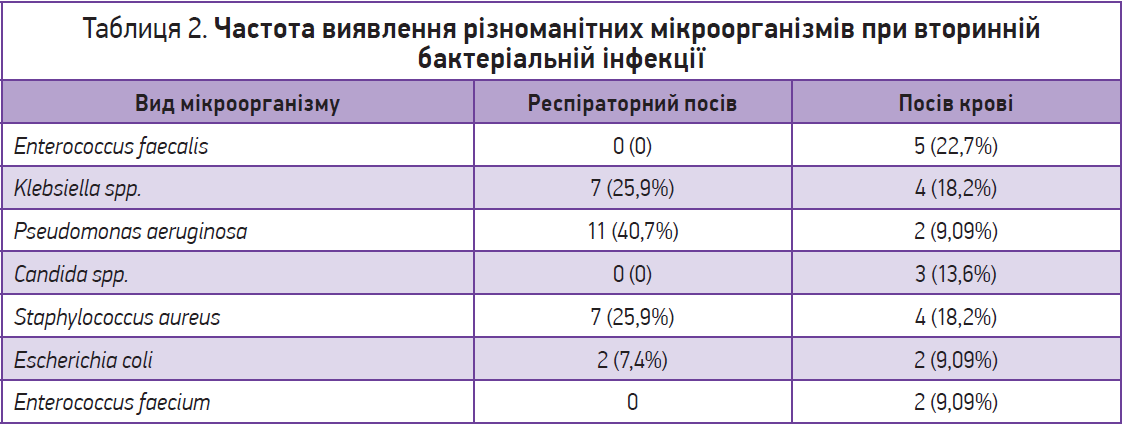
Найчастіше виявлялися такі збудники, як Enterococcus faecalis, Klebsiella spp., Pseudomonas aeruginosa, Candida spp. (табл. 2).
Порівняння абсолютної кількості лімфоцитів між двома досліджуваними групами пацієнтів продемонструвало суттєве їх зниження в групі тоцилізумабу.
Отже, результати проведеного дослідження продемонстрували, що протизапальні методи лікування коронавірусної інфекції із застосуванням тоцилізумабу можуть ефективно зменшувати прояви цитокінового шторму, але водночас сприяють зростанню ризику вторинного інфікування пацієнтів із тяжким перебігом COVID‑19.
На сьогодні є досить багато даних щодо розповсюдженості вторинної бактеріальної інфекції у пацієнтів із COVID‑19. За даними T. M. Rawson і співавт. (2020), ≈8% пацієнтів із коронавірусною хворобою під час госпіталізації мали бактеріальну / грибкову коінфекцію. Вторинний аналіз лікування таких пацієнтів продемонстрував доцільність призначення антибактеріальних засобів із широким спектром дії більше ніж у половині випадків, незважаючи на недостатність доказів бактеріальної коінфекції.
Зазначені дані свідчать про необхідність втілення зваженої політики щодо призначення протимікробних препаратів і відповідних стратегічних втручань в умовах пандемії COVID‑19.
В останніх рекомендаціях Мічиганського медичного університету (США) щодо лікування пацієнтів дорослого та дитячого віку з COVID‑19 (від 10 жовтня 2021 року) запропоновано керуватися такими положеннями:
- в пацієнтів, госпіталізованих із підозрою на пневмонію при COVID‑19 (очікуються результати тестування), рішення про початок антибактеріальної терапії має ґрунтуватися на локальних рекомендаціях із лікування пневмонії та оцінці рівня прокальцитоніну;
- продовження / початок антибактеріальної терапії лише у зв’язку із підтвердженням COVID‑асоційованої пневмонії не показане;
- підвищення рівня прокальцитоніну достовірно не пов’язане з бактеріальною інфекцією, особливо в умовах супутньої дисфункції нирок. Емпіричну антибактеріальну терапію зазвичай припиняють одразу після того, як у пацієнта буде підтверджено наявність COVID‑19, але вона може бути показана хворим із лейкоцитозом та/або гемодинамічною нестабільністю. Слід розглянути питання щодо деескалації/припинення прийому антибіотиків на підставі клінічних і мікробіологічних даних.
У пацієнтів із тяжкою інфекцією COVID‑19, госпіталізованих до клініки Мічиганського медичного університету, які потребували проведення штучної вентиляції легень (ШВЛ):
- у 40% випадків розвинулася бактеріальна суперінфекція;
- у 32% випадків виявлено бактеріальну пневмонію;.
- середній час до розвитку інфекції становив 8-10 днів після початку ШВЛ.
У 3,5% усіх пацієнтів із COVID‑19 була виявлена бактеріальна коінфекція на момент госпіталізації (табл. 3).
Отже, перевага в лікуванні бактеріальної пневмонії у пацієнтів, котрі перебувають у ВРІТ, надається цефепіму.
Цефепім – β-лактамний цефалоспориновий антибіотик IV покоління широкого спектра дії; характеризується високою стійкістю до більшості β-лактамаз. Цефепім має здатність швидко проникати всередину грамнегативних бактеріальних клітин. Ступінь зв’язування цефепіму з пеніцилін-зв’язувальним білком значно перевищує спорідненість інших цефалоспоринів для парентерального застосування.
На українському фармацевтичному ринку цефепім представлений високоякісним генеричним препаратом Квадроцеф виробництва АТ «Київмедпрепарат», Корпорація «Артеріум».
Згідно із протоколом надання медичної допомоги для лікування коронавірусної хвороби (COVID‑19) відповідно до наказу Міністерства охорони здоров’я України від 2 квітня 2020 року № 762 (у редакції наказу Міністерства охорони здоров’я України від 13 травня 2021 року № 930; останні зміни внесені 30 грудня 2021 року) антибіотикотерапія пацієнтам із COVID‑19 показана у випадку розвитку пізньої госпітальної пневмонії.
За пізньої госпітальної пневмонії, якщо антибіотики призначаються емпірично, насамперед необхідно враховувати епідемічну ситуацію у відділенні (яка мікрофлора переважає та до яких антибіотиків вона чутлива).
Рекомендується застосовувати такі антибіотики:
→ цефалоспорини III покоління (цефтріаксон, цефотаксим, цефтазидим, цефіксим, цефоперазон, цефподоксим) + макроліди (азитроміцин або кларитроміцин);
→ респіраторні фторхінолони (левофлоксацин або моксифлоксацин) як монотерапія або в комбінації з цефалоспоринами III покоління;
→ за потреби (зазвичай з метою ротації призначуваних антибіотиків у відділенні) варто розглянути захищені цефалоспорини (цефоперазон/сульбактам, цефтріаксон/сульбактам, цефтріаксон/тазобактам, цефотаксим/сульбактам) або піперацилін/тазобактам.
З огляду на суттєве зростання призначень антибіотиків цефалоспоринового ряду, що спостерігається в умовах пандемії COVID‑19, очікується значне зростання антибіотикорезистентності до препаратів цієї групи.
Отже, доцільними є ротація антибіотиків і надання переваги антибактеріальним засобам із посиленою стійкістю до β-лактамаз. Приклад такого засобу – препарат Гепацеф Комбі виробництва АТ «Київмедпрепарат», Корпорація «Артеріум», до складу якого входять сульбактам натрію та цефоперазон натрію.
Сульбактам натрію, що є похідним основного пеніцилінового ядра, незворотно інгібує β-лактамазу. Цефоперазон натрію – напівсинтетичний цефалоспориновий антибіотик III покоління широкого спектра дії. Цефоперазон натрію діє шляхом пригнічення біосинтезу мукопептиду клітинної стінки, тоді як сульбактам захищає його від руйнування β-лактамазами мікроорганізмів, резистентних до β-лактамних антибіотиків. Окрім того, спостерігається синергізм дії (зниження мінімальних концентрацій антибіотиків, що входять до складу комбінації; пригнічує мікроорганізми набагато сильніше порівняно з такими ж концентраціями для кожного компонента окремо).
Гепацеф Комбі активний проти всіх мікроорганізмів, чутливих до цефоперазону; крім того, виявлено синергізм дії (зниження мінімальних концентрацій комбінацій, здатних пригнічувати мікроорганізми в ≈4 рази порівняно з такими концентраціями для кожного компонента окремо). Гепацеф Комбі чинить найвираженішу дію проти таких мікроорганізмів, як Haemophilus influenzae, види Bacteroides, види Staphylococcus, Acinetobacter calcoaceticus, Enterobacter aerogenes, Escherichia coli, Proteus mirabilis, Klebsiella pneumoniae, Morganella morganii, Citrobacter freundii, Enterobacter cloacae, Citrobacter diversus.
Підготував В’ячеслав Килимчук