3 лютого, 2022
Антибіотикотерапія при COVID‑19
У рамках IV міжнародного конгресу Antibiotic resistance STOP! (13-14 листопада 2021 року) провідні вітчизняні й закордонні експерти обговорювали нюанси антибіотикотерапії (АБТ) та особливості застосування антибактеріальних препаратів (АБП). «Попри тотальне призначення фахівцями первинної ланки АБП пацієнтам із COVID‑19, для переважної більшості хворих ця тактика не є доцільною. Ані підвищена температура тіла, ані наявність симптомів протягом ≥5 днів, ані прагнення запобігти розвитку бактеріальної коінфекції не вважаються науковим обґрунтуванням для використання АБП. На користь застосування АБП свідчать клініко‑лабораторні дані, котрі підтверджують наявність бактеріальної інфекції. Нагадаю, що на вірус, який спричиняє COVID‑19, АБП не діють», – наголосив завідувач кафедри анестезіології та інтенсивної терапії Національного медичного університету ім. О. О. Богомольця (м. Київ), доктор медичних наук, професор Сергій Олександрович Дубров, розпочинаючи свою доповідь на конгресі.
Слова професора С.О. Дуброва підтверджує й світова статистика: 70% пацієнтів отримують АБП на амбулаторному етапі та в стаціонарі (Hassan Z. et al., настанова ISARIC, 2020; Langford B. J. et al., 2021). У 90-95% (!) випадків призначення недоцільні або неправильні (Knight G. et al., 2021).
Занадто багато хворих на COVID‑19 отримують АБП «про всяк випадок» – такий висновок зробили американські вчені під керівництвом V. M. Vaughn, що провели ретроспективний аналіз даних більш ніж 1700 пацієнтів із 38 госпіталів. Його результати, опубліковані 2020 року, вразили медичну спільноту. Виявилося, що понад 50% осіб із підозрою на COVID‑19 отримували АБП, однак антибактеріальну флору виділили лише в 3,5% пацієнтів (у 96,5% хворих виявили вірусну інфекцію).
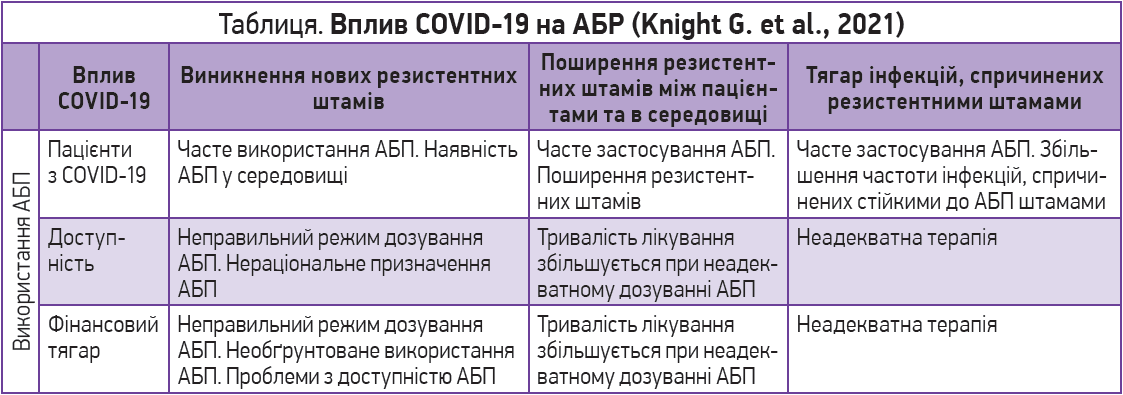
Пандемія COVID‑19 погіршує ситуацію з АБР (табл.).
«Якщо в «доковідну» епоху проблема АБР стосувалася переважно збудників нозокоміальних інфекцій (НКІ), то нині фахівці чимраз частіше стикаються з випадками АБР на позалікарняному етапі», – акцентував увагу колег С. О. Дубров.
Як відомо, за останні десятиліття не з’явилося жодного принципово нового АБП. Імовірність того, що найближчим часом ученим вдасться створити АБП широкого спектра дії, активний стосовно полі- та панрезистентних штамів збудників (критично важливі й мають статус пріоритетних карбапенемрезистентні штами Acinetobacter baumannii, карбапенемрезистентні штами Pseudomonas aeruginosa, карбапенемрезистентні штами та штами Enterobacteriaceae, що продукують β-лактамази розширеного спектра – БЛРС), стрімко прямує до нуля.
За словами доповідача, тяжкий перебіг COVID‑19 відповідає критеріям міжнародного консенсусу Sepsis‑3 і може розглядатись як вірусний сепсис. Роль бактеріальної коінфекції недостатньо вивчена, але відомо, що вторинна інфекція відіграє головну роль у захворюваності в умовах нестачі ресурсів, особливо в пацієнтів, які перебувають на штучній вентиляції легень (ШВЛ). Рівень смертності від COVID‑19 високий, існують розбіжності залежно від доходу: в країнах, де він низький/середній, ситуація гірша. В Україні рівень смертності під час першої хвилі не відрізнявся від такого в країнах із високим економічним розвитком, але нині він у 4-6 разів вищий порівняно з державами Європейського Союзу, Великою Британією, Ізраїлем, де охоплення вакцинацією становить понад 70%. Резистентні штами, НКІ й організаційні аспекти є важливими чинниками, що впливають на ймовірність виникнення сепсису, рівень смертності; найперше слід корегувати ці чинники.
Частоту виникнення бактеріальних інфекцій під час проведення ШВЛ оцінювали в європейському багатоцентровому дослідженні A. Rouze та співавт. (2021) за участю 1576 пацієнтів із COVID‑19, грипом або без вірусної інфекції. Частота виникнення вентиляторасоційованої пневмонії бактеріального генезу становила 50,5% у групі COVID‑19, 30,3% – за наявності грипу, 25,3% – у пацієнтів без вірусних інфекцій. Показник летальності при вентиляторасоційованій пневмонії вищий серед хворих, у яких діагностовані вірусні інфекції.
У рекомендаціях Американського товариства інфекційних хвороб (IDSA, 2020) щодо лікування грамнегативних резистентних бактеріальних інфекцій містяться такі положення:
- штами Enterobacteriaceae, що продукують БЛРС, і карбапенемрезистентні штами, а також тяжкі інфекції, зумовлені P. aeruginosa, визначені CDC як невідкладні або серйозні загрози, що спричиняють летальні наслідки;
- основна мета настанови – надати допомогу клініцистам у виборі АБП для лікування інфекцій, спричинених штамами Enterobacteriaceae, які продукують БЛРС, і карбапенемрезистентними штамами, а також тяжких для лікування інфекцій, зумовлених P. aeruginosa;
- обираючи емпіричну терапію, клініцисти повинні враховувати умови інфікування (позалікарняна чи НКІ); попередні випадки інфікування та дані про чутливість до АБП протягом останніх 6 міс; анамнез застосування АБП за останні 30 днів (якщо використовували піперацилін/тазобактам, варто розглянути АБП із впливом на грамнегативну флору, як-от меропенем).
Відповідно до наказу МОЗ України № 3094, за підозри чи підтвердженої інфекції COVID‑19 із легким/середньотяжким перебігом не варто призначати АБП без наявності клінічної підозри на бактеріальну інфекцію. За підозри чи підтвердженої інфекції COVID‑19 із тяжким перебігом потрібно застосовувати АБП як емпіричну терапію проти ймовірних патогенів на підставі клінічного діагнозу (наприклад, негоспітальна/госпітальна пневмонія), епідеміологічних даних і регіональних/місцевих даних щодо АБР. У пацієнтів у тяжкому стані слід розпочинати емпіричну АБТ проти ймовірних патогенів якомога швидше (за можливості протягом 1 год від виявлення сепсису та не пізніше 4 год від встановлення діагнозу бактеріальної пневмонії). При встановленні діагнозу вторинної бактеріальної пневмонії потрібно звертати увагу на погіршення самопочуття, лихоманку, появу гнійного мокротиння, вологих хрипів, а також зміну лабораторних показників (найвагоміший – прокальцитонін, також інформативні лейкоцитоз, зсув лейкоцитарної формули вліво). Зазвичай за наявності ізольованої COVID‑19 навіть у разі суттєвих полісегментарних змін у легенях за даними рентгенографії чи комп’ютерної томографії кашель сухий, надсадний, мокротиння відсутнє або слизового характеру, хрипи не вислуховуються.
АБТ при позалікарняній бактеріальній пневмонії
За легкого перебігу рекомендована монотерапія захищеними пеніцилінами (амоксицилін/клавуланат, ампіцилін/сульбактам), або макролідами (азитроміцин, кларитроміцин), або цефалоспоринами II покоління.
У разі середньотяжкого перебігу показані захищені пеніциліни (амоксицилін/клавуланат) + макроліди (азитроміцин чи кларитроміцин)
або
цефалоспорини II-III покоління (цефуроксим, цефтріаксон, цефотаксим, цефтазидим, цефіксим, цефоперазон, цефподоксим) + макроліди (азитроміцин чи кларитроміцин)
або (в разі алергії на β-лактами)
респіраторні фторхінолони (левофлоксацин або моксифлоксацин).
АБТ у разі тяжкого перебігу:
цефалоспорини III покоління (цефтріаксон, цефотаксим, цефтазидим, цефіксим, цефоперазон, цефподоксим) + макроліди (азитроміцин чи кларитроміцин)
або
респіраторні фторхінолони (левофлоксацин або моксифлоксацин) як монотерапія чи в комбінації з цефалоспоринами III покоління.
За потреби рекомендується розглянути захищені цефалоспорини: цефоперазон/сульбактам, цефтріаксон/сульбактам, цефтріаксон/тазобактам, цефотаксим/сульбактам.
Нозокоміальна пневмонія бактеріального генезу
• Рання: цефалоспорини III покоління (цефтріаксон, цефотаксим, цефтазидим, цефіксим, цефоперазон) + макроліди (азитроміцин чи кларитроміцин)
або
респіраторні фторхінолони (левофлоксацин або моксифлоксацин) як монотерапія чи в комбінації з цефалоспоринами III покоління. Також можливе призначення захищених цефалоспоринів III покоління.
! Якщо АБП призначають емпірично, варто враховувати епідемічну ситуацію у відділенні та результати бактеріоскопії.
• Пізня: цефалоспорини III покоління (цефтріаксон, цефотаксим, цефтазидим, цефіксим, цефоперазон, цефподоксим) + макроліди (азитроміцин чи кларитроміцин)
або
респіраторні фторхінолони (левофлоксацин або моксифлоксацин) як монотерапія чи в комбінації з цефалоспоринами III покоління.
За потреби розглядають захищені цефалоспорини: цефоперазон/сульбактам, цефтріаксон/сульбактам, цефтріаксон/тазобактам, цефотаксим/сульбактам або піперацилін/тазобактам.
У разі наявності полірезистентної флори радять застосовувати 2-3 АБП, карбапенеми (наприклад, меропенем) або тайгециклін, особливо при тяжкому перебігу.
За умови поширення у відділенні грампозитивної полірезистентної мікрофлори (MRSA) потрібно призначати ванкоміцин або лінезолід. Карбапенеми слід використовувати емпірично тільки у відділеннях інтенсивної терапії (у виняткових випадках – в інших відділеннях, але рішення приймають комісійно, за належного обґрунтування) у хворих із тяжким перебігом. «У пацієнтів із патологією нирок, ожирінням, цукровим діабетом, артеріальною гіпертензією лінезолід є безпечнішим порівняно з ванкоміцином», – підкреслив доповідач.
Неприпустима тактика – емпірично застосовувати колістин, фосфоміцин внутрішньовенно. Потрібно регулярно оцінювати можливість зменшення інтенсивності АБТ і переходу на пероральне введення.
У пацієнтів із тяжкою бактеріальною інфекцією / коінфекцією обов’язковим є мікробіологічне дослідження з метою визначення чутливості збудника та корекції АБТ.
Запитання – відповідь
? Як діяти, коли пацієнт приймає АБП після призначення іншим лікарем за відсутності показань?
– У нашій практиці такі ситуації не рідкість. Якщо в пацієнта немає зміни лабораторних показників (прокальцитонін та інші маркери – в межах референтних значень) і продуктивного кашлю з гнійним мокротинням, ми скасовуємо призначення АБП (попри численні наполягання родичів хворого). Після цього забезпечуємо постійний моніторинг стану пацієнта.
За відсутності бактеріальної мікрофлори дострокове припинення курсу АБТ не впливає на АБР.
? Яка частота призначення АБП у реанімаційному та коронавірусному відділеннях вашого медичного закладу?
– У ковідному інфекційному відділенні на 50 ліжок частота призначення АБП – 0-3%. Показник використання АБП у разі COVID‑19 до 3-ї хвилі становив 16,7%, тоді як в інших медичних закладах країни перевищував 90%.
? Чи доцільно призначати АБП, якщо в пацієнта показник прокальцитоніну 1 нг/мл і протягом кількох днів спостерігається т. зв. сіре вікно (лейкоцити загалом і нейтрофільні лейкоцити на пороговому рівні)?
– Якщо лейкоцити в межах норми, немає зсуву лейкоцитарної формули вліво, відсутні продуктивний кашель і гнійне мокротиння, а прокальцитонін не перевищує 1 нг/мл, особисто я утримався би від призначення АБП і через кілька днів повторно оцінив би рівень прокальцитоніну.
? Наскільки здешевлюють лікування COVID‑19 адекватна діагностика й відмова від необґрунтованої АБТ?
– Проводився порівняльний аналіз результатів терапії пацієнтів із COVID‑19 у нашому закладі (120 осіб за 9 міс) і хворих з інших лікарень. Витрати на АБП становили 40 і 486 тис. грн відповідно, тобто відрізнялися у 12 (!) разів (рис.).
Рис. «Воронка» АБТ
Підготувала Олександра Марченко