14 лютого, 2022
Лікування постінсультної депресії: аналіз відповіді пацієнтів на есциталопрам
Постінсультна депресія (ПІД) є вельми поширеним станом, що погіршує клінічний результат та якість життя хворих. Ефективність фармакотерапії, зокрема антидепресантами, у пацієнтів із симптомами ПІД варіює. E.-J. Lee et al. мали на меті вивчити, як впливає есциталопрам на ПІД залежно від індивідуальних симптомів депресії та локалізації вогнища інсульту. Отримані результати опубліковані у виданні Journal of Geriatric Psychiatry and Neurology (2021; 34 (6): 565‑573).
Фармакотерапія ПІД часто є недостатньо ефективною, що, ймовірно, пов’язано з гетерогенними механізмами цього стану (Kim, 2016; Lee et al., 2020). ПІД може частково розвиватися через пошкодження нейромедіаторних волокон, що простягаються від стовбура мозку до лобової кори (Terroni et al., 2011; Numasawa et al., 2017). Тож ефективність медикаментозного лікування, зокрема селективними інгібіторами зворотного захоплення серотоніну (СІЗЗС), у пацієнтів із симптомами ПІД може варіювати залежно від локалізації інсульту.
Крім того, різна терапевтична відповідь може асоціюватися з невідповідним використанням діагностичних інструментів у хворих після перенесеного інсульту. Більшість методик оцінки ПІД призначені для осіб із психічними розладами без структурних пошкоджень мозку і стосуються таких симптомів, як швидка стомлюваність, порушення сну, труднощі з концентрацією уваги тощо. У пацієнтів із гострим інсультом такі симптоми можуть бути вторинними щодо неврологічних розладів, змін навколишнього середовища чи приймання ліків. Тому хворі, в яких наявні переважно саме такі симптоми, можуть бути менш чутливими до терапії антидепресантами.
У даному контексті E.-J. Lee et al. (2020) припустили, що дія СІЗЗС змінюється залежно від виразності нейроповедінкових симптомів та вогнища інсульту. Щоб перевірити цю гіпотезу, вони виконали ретроспективний аналіз даних нещодавнього клінічного випробування ефекту есциталопраму, в якому вивчали локалізацію уражень при інсульті та різноманітні симптоми депресії у пацієнтів із гострим інсультом.
Матеріали й методи
Дизайн дослідження та інструменти оцінки
Ретроспективний аналіз включав дані рандомізованого подвійного сліпого плацебо-контрольованого багатоцентрового клінічного випробування EMOTION, проведеного в період 2011‑2014 рр. (Kim et al., 2017). У дослідження увійшли 478 пацієнтів, що відповідали таким критеріям:
- вік ˃20 років;
- перенесений гострий інсульт протягом 21 дня (у 456 – ішемічний, у 22 – геморагічний);
- наявність неврологічного дефіциту (≥2 бали за шкалою Ренкіна);
- надання інформованої згоди на участь.
Критеріями виключення були: діагностована депресія або інші психічні розлади в анамнезі до епізоду інсульту; змінений психічний статус, тяжка деменція та/або афазія, що призвели до виникнення труднощів у спілкуванні (Winblad, Poritis, 1999). Пацієнти з симптомами депресії під час скринінгу були включені у дослідження, але особи з виразними суїцидальними думками – виключені.
Учасники протягом 12 тижнів отримували есциталопрам у початковій дозі 5 мг/добу, яку з 2-го тижня поступово збільшували до 10 мг/добу за відсутності побічних явищ, або плацебо. Потім вони перебували під наглядом ще 12 тижнів без застосування досліджуваних препаратів.
Первинне обстеження хворих проводили після стабілізації неврологічного стану, порушеного внаслідок інсульту (зазвичай через три дні). Симптоми ПІД оцінювали за допомогою шкали депресії Монтгомері – Асберг (MADRS) від 0 до 6 балів (чим вищий бал, тим тяжчі прояви депресії) (Khan et al., 2004). Показники MADRS аналізували на початку та через 12 тижнів із метою визначення ефекту есциталопраму під час лікування. Неврологічний дефіцит оцінювали за шкалою інсульту Національних інститутів охорони здоров’я США (NIHSS) (Brott et al., 1989).
Локалізація вогнища інсульту
Локалізацію осередку інсульту (лобова, тім’яна, скронева, потилична, підкіркова ділянка, таламус, середній, довгастий мозок, міст і мозочок) було підтверджено за даними магнітно-резонансної чи комп’ютерної томографії (Kim et al., 2017). Автори розподілили локалізації вогнищ інсульту на три групи: пошкодження середнього мозку чи моста, лобної або підкіркової ділянки мозку та інші (Paxinos et al., 2012). Пацієнти із множинними ураженнями за різними категоріями (n=5) не були включені до аналізу локалізації осередку інсульту.
Статистичний аналіз
Аналіз проводили на основі ІТТ-популяції (всі рандомізовані пацієнти відповідно до призначеного лікування). Вихідні характеристики та клінічні змінні порівнювали між групами лікування та локалізації інсульту за допомогою критерію хі-квадрат (або точного критерію Фішера) для категорійних змінних та t-критерію Стьюдента (чи U-критерію Манна – Уїтні) – для безперервних. Вплив есциталопраму на основний результат (зміну загального бала за MADRS через 12 тижнів) досліджували за допомогою лінійної регресії з множинними змінними. Також для груп локалізації ураження були розраховані середні значення за методом найменших квадратів, щоб визначити величину незалежного впливу кожної з них на зміни симптомів депресії. Двобічні p<0,05 вважалися статистично значущими.
Результати
Із загальної кількості учасників оцінювання за MADRS упродовж 12 тижнів пройшли 73,8%. Кількість вибулих із дослідження протягом цього періоду була порівнянною між групами (плацебо та есциталопраму – 65 vs 60 осіб відповідно).
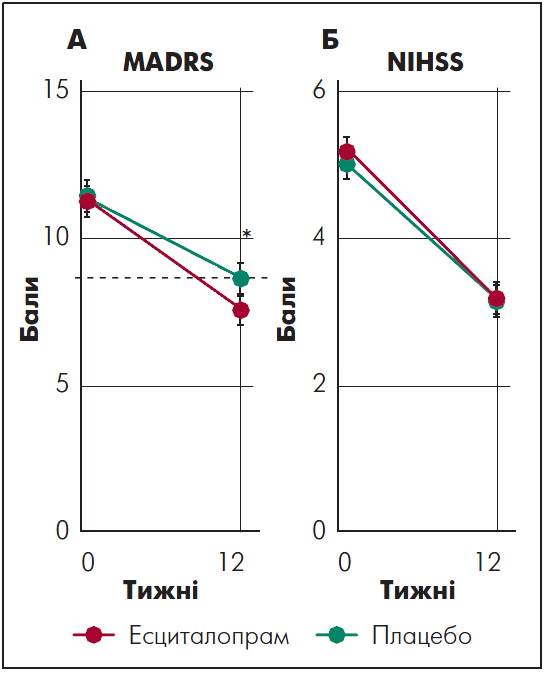
Вихідна тяжкість симптомів депресії у групах плацебо й есциталопраму, оцінена за MADRS, була однаковою. Оскільки неврологічний дефіцит із часом зменшувався, також мало місце полегшення симптомів депресії. При цьому зміна загального бала за MADRS була значно виразнішою у пацієнтів, які отримували есциталопрам (рисунок). Серед окремих симптомів у групі есциталопраму полішилися показники за трьома пунктами MADRS, як-то явний смуток, повідомлення про сумні думки та песимістичний настрій.
Рисунок. Симптоми депресії та неврологічний дефіцит у пацієнтів із ПІД протягом 12 тижнів
Примітки: Пунктир відповідає середнім значенням, відрізки – стандартним похибкам; * р<0,05 при порівнянні змін балів від вихідного рівня між досліджуваними групами.
Адаптовано за E.-J. Lee et al., 2021
Серед пацієнтів, включених до аналізу локалізації вогнища інсульту (n=473), 101 мав ураження середнього мозку / моста, а 278 – лобно-підкіркової зони. Неврологічний дефіцит у цих групах був вищого ступеня, ніж у хворих з іншими ураженнями. Згідно з отриманими результатами, було продемонстровано ефективність есциталопраму в осіб із лобно-підкірковими порушеннями.
Есциталопрам загалом добре переносився (Kim et al., 2017). Міжгрупова прихильність до лікування була зіставною (для плацебо та есциталопраму – 86,3 vs 89,3% відповідно).
Обговорення
E.-J. Lee et al. (2020) виявили, що фармакологічний ефект стосовно ПІД варіював залежно від індивідуальних симптомів депресії та локалізації вогнищ інсульту, які не враховувалися у попередніх дослідженнях.
Було показано, що есциталопрам значно зменшував прояви явного смутку, повідомлення про сумні думки та песимістичний настрій (McNutt et al., 2012). Своєю чергою змін щодо труднощів із концентрацією уваги, зниження сну/апетиту та стомлюваності не відбулося. Імовірно, це пов’язано з тим, що учасники дослідження перенесли гострий інсульт, а симптоми когнітивного або нейровегетативного характеру могли бути частково спричинені інсультом та пов’язаними з ним факторами (наприклад, зміною навколишнього середовища, прийманням ліків), а тому – й менш чутливими до есциталопраму.
Тож автори припустили, що відповідь на лікування антидепресантами у пацієнтів із гострим інсультом за допомогою діагностичних інструментів, що використовують вегетативні симптоми для характеристики ПІД, могла бути недооціненою з огляду на те, що частота цих симптомів є вищою на ранніх, ніж на пізніх стадіях ПІД (Tateno et al., 2002).
Крім того, СІЗЗС можуть бути ефективнішими при ПІД залежно від тяжкості симптомів. Оскільки у поточній роботі використовували лише есциталопрам, необхідні додаткові дослідження із залученням інших антидепресантів для з’ясування властивих їм відмінностей фармакологічних ефектів щодо кожного з симптомів депресії.
На додаток, автори висунули гіпотезу, що дія СІЗЗС варіює залежно від локалізації вогнища інсульту. Дійсно, значуща відповідь на фармакотерапію спостерігалася у пацієнтів із ураженнями в лобно-підкірковій зоні, на відміну від таких у середньому мозку й мості. Одним із можливих пояснень цієї невідповідності може бути те, що ступінь і кількість пошкоджених серотонінових волокон відрізняються між групами, що могло призвести до різної терапевтичної відповіді на СІЗЗС (Stahl, 1998).
Висновки
За результатами дослідження E.-J. Lee et al. (2020) було продемонстровано, що терапевтичний ефект при ПІД залежить від окремих симптомів депресії та локалізації вогнищ інсульту. Тож у майбутніх клінічних випробуваннях слід враховувати різну фармакологічну ефективність залежно від тяжкості симптомів і локалізацій уражень. Застосування індивідуальних стратегій лікування при веденні хворих із симптомами депресії після перенесеного інсульту забезпечить максимальну ефективність терапії.
Підготувала Олена Коробка
Тематичний номер «Інсульт» № 1 2022 р.