20 липня, 2022
Антигістамінна дія і профіль безпеки фексофенадину
Систематичний огляд і метааналіз рандомізованих контрольованих досліджень
Як антигістамінний препарат (АГП) нового покоління фексофенадин широко використовують при алергічних захворюваннях (АЗ). Однак досі немає сукупних даних щодо ефективності і безпеки (побічні і седативні ефекти та вплив на когнітивні/психомоторні функції) фексофенадину проти інших АГП і плацебо. Метою цієї роботи стала систематична оцінка відповідних рандомізованих контрольованих досліджень (РКД) у базах Embase, Cochrane і PubMed з моменту створення препарату до 1 січня 2018 року. В аналіз було включено 51 дослідження (n=14 551).
Ключові слова: фексофенадин, ефективність, безпека, небажані явища, алергічні захворювання, порівняльний аналіз.
Актуальність АЗ і місце АГП ІІ покоління в їх лікуванні, вимоги до безпеки й ефективності АГП
Поширеність таких АЗ, як алергічний риніт (AР), алергічна бронхіальна астма (АБА), хронічна ідіопатична кропив’янка (ХІК) і атопічний дерматит (AД), продовжує зростати в усьому світі останні кілька десятків років [1]. Симптоми, які супроводжують АЗ, значно погіршують якість життя і працездатність пацієнтів [2]. Для терапії АЗ як засоби першої лінії традиційно використовують АГП, але АГП І покоління більше не рекомендовані через побічні ефекти (ПЕ), у тому числі гепато- і кардіотоксичність, седативну дію, антихолінергічні ефекти і недостатню селективність щодо H1-рецепторів [4].
Сьогодні перевагу віддають АГП ІІ покоління завдяки їхній помірній седативній дії та більш вираженому і стійкому лікувальному ефекту. Однак деякі АГП ІІ покоління використовують рідко через очевидну кардіотоксичність цих засобів [5].
Як АГП нового покоління і активний метаболіт терфенадину – високоселективного антагоніста H1-рецепторів – фексофенадин виявляє виражену антигістамінну дію [6] без кардіотоксичного ефекту і з мінімальними ПЕ з боку печінки, оскільки в ній метаболізується лише близько 5% фексофенадину [7].
Фексофенадин не долає гематоенцефалічний бар’єр (ГЕБ), тому не здатен чинити седативну дію і зумовлювати інші небажані ефекти з боку центральної нервової системи.
Мета цього дослідження – проаналізувати антигістамінні ефекти і безпеку фексофенадину в здорових осіб і пацієнтів з АЗ, у тому числі AР, АБА, ХIК і AД, порівнюючи з іншими АГП або плацебо.
Аналіз даних численних досліджень щодо ефективності фексофенадину
Були включені РКД, в яких порівнювали антигістамінні ефекти і безпеку фексофенадину з такими інших АГП або плацебо. Учасниками цих РКД були здорові добровольці і пацієнти з АЗ, які потребували антигістамінної терапії. АГП оцінювали за ступенем інгібування гістамін-індукованих пухирів і гіперемії (через 24 год після лікування); безпеку оцінювали за частотою ПЕ, седативних ефектів і зміни показників когнітивної/психомоторної функції (через 3-5 год після лікування). Оцінка когнітивних/психомоторних функцій охоплювала дослідження критичної частоти злиття світлового мерехтіння (critical flicker fusion; CFF), час прийняття вибору (choice reaction time; CRT), тест на компенсаторне відслідковування (compensatory tracking test; CTT), лінійні аналогові рейтингові шкали для седативного ефекту (line analogue rating scales for sedation; LARS) і візуальні аналогові шкали (visual analogue score; VAS) сонливості, які використовували для оцінки здатності до обробки інформації, швидкості реакції, ступеня концентрації уваги, пильності і стомлюваності, а також сонливості. Із 96 знайдених повнотекстових робіт лише 51 було залучено до метааналізу за відповідністю критеріям включення. Із них 20 (39,2%) досліджень були паралельними, а 31 (60,8%) – перехресними. Загальна кількість учасників становила 14 551 особу (45,0% – чоловіки), середній вік становив 31,7 року. Серед досліджуваних було 3024 здорові особи, 10 521 випадок AР, 536 випадків ХIК, 470 – полінозу.
Антигістамінні ефекти
- Пригнічення гістамін-індукованих висипань.
Про пригнічення індукованих гістаміном висипань (пухирів) на тлі застосування фексофенадину повідомлялося в 6 роботах – в 1 порівнювали з АГП І покоління, у 5 – з АГП ІІ покоління і в 5 – з плацебо. Порівняння фексофенадину і АГП І покоління не увійшло до метааналізу, оскільки було знайдено тільки 1 дослідження. Якщо порівнювати з АГП ІІ покоління, рівні інгібування індукованих гістаміном висипань не розрізнялися (зважена середня різниця (ЗСР) = -17,56; 95% ДІ від -44,77 до 9,65; р=0,21). Гетерогенність становила 99%, що може бути зумовлене несумісними дозами фексофенадину й АГП ІІ покоління. Як було показано, проти плацебо фексофенадин значно швидше інгібував зумовлені гістаміном висипання (рис. 1).
Рис. 1. Частота супресії гістамін-індукованих висипань: фексофенадин (FEX) проти АГП ІІ покоління
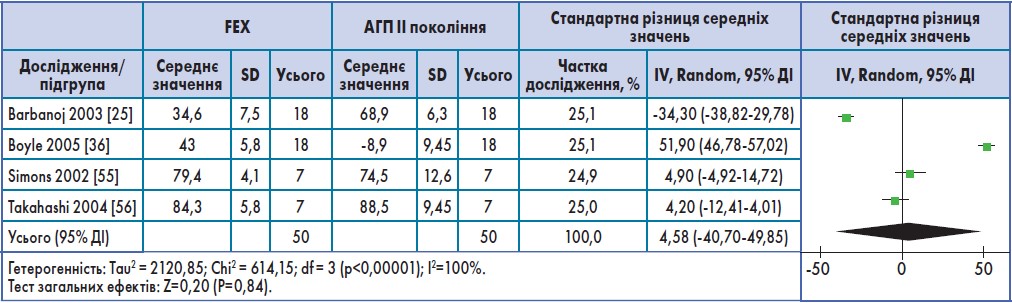
- Пригнічення гістамін-індукованої гіперемії (вазодилатації).
Про пригнічення гістамін-індукованої гіперемії (вазодилатації) на тлі прийому фексофенадину повідомлялося в 6 дослідженнях. Лише в 4 із них порівняння проводили з АГП ІІ покоління, ступінь інгібування ними гіперемії не відрізнявся (ЗСР=4,58; 95% ДІ 40,70-49,85; р=0,84). У 5 дослідженнях, в яких порівняння проводили з плацебо, фексофенадин значно швидше інгібував гістамін-індуковану гіперемію (ЗСР=35,75; 95% ДІ 18,67-52,83; р<0,00001) (рис. 2). Гетерогенність може бути зумовлена несумісними дозами фексофенадину та АГП ІІ покоління. Аналіз чутливості показав, що результати метааналізу були аналогічними.
Рис. 2. Частота супресії гістамін-індукованої гіперемії: фексофенадин (FEX) проти АГП ІІ покоління
Безпека
- Частота ПЕ.
У 41 дослідженні аналізували ПЕ після прийому фексофенадину. Із них 10 робіт порівнювали фексофенадин з АГП І покоління, 22 – з АГП ІІ покоління і 37 – із плацебо. Проти АГП І покоління фексофенадин показав значуще меншу частоту ПЕ (ВШ=0,446; 95% ДІ 0,214-0,929; р=0,031). Частота ПЕ при застосуванні фексофенадину та АГП ІІ покоління була порівнянною (ВШ=0,987; 95% ДІ 0,815-1,195; р=0,890). При порівнянні з плацебо частота ПЕ у групах не відрізнялася (ВШ=0,999; 95% ДІ 0,863-1,156; р=0,987).
- Частота седативних ефектів.
Аналіз седативних ефектів на тлі застосування фексофенадину проводили в рамках 46 досліджень. Із них 10 робіт порівняння проводили з АГП І покоління, 27 – з АГП ІІ покоління і 38 – із плацебо. Проти АГП І покоління фексофенадин продемонстрував значно нижчу частоту седативних ефектів (ВШ=0,265; 95% ДІ 0,072-0,976; р=0,046). Проти АГП ІІ покоління в групі фексофенадину частота седативних ефектів також була нижчою (ВШ=0,578; 95% ДІ 0,369-0,906; р=0,017). У групах плацебо і фексофенадину частота седативних ефектів була порівнянною (ВШ=1,608; 95% ДI 0,884-2,924; р=0,120).
Когнітивна/психомоторна функція CFF – дослідження, під час якого при певній частоті світлових спалахів мерехтіння зливається і сприймається людиною як безперервне світло. Що швидше відбувається злиття, то нижча здатність обробляти інформацію. Цей параметр досліджували в 6 з наведених досліджень.
Було показано, що фексофенадин приводив до значно меншої зміни CFF проти АГП І покоління (ЗСР=1,73; 95% ДI 1,14-2,32; р<0,00001), а аналіз підгрупи показав, що фексофенадин у дозі 120 мг/добу спричинював значно меншу зміну CFF проти прометазину (ЗСР=1,62; 95% ДІ 1,33-1,91; р<0,00001). Показник CFF не відрізнявся в групах прийому фексофенадину та АГП ІІ покоління (ЗСР=0,20; 95% ДІ 0,16-0,56; р=0,28), а аналіз підгрупи продемонстрував значно меншу зміну CFF проти олопатадину (ЗСР=0,37; 95% ДІ 0,24-0,49; р<0,00001). Також CFF був однаковим у групах прийому плацебо і фексофенадину (ЗСР= -0,15; 95% ДІ 0,37-0,06; р=0,17).
CRT оцінювали в 7 дослідженнях. Це чутливий тест для виявлення змін швидкості психомоторних реакцій. Вимірюють час вибору в ситуації з двома опціями. Що він більший, то нижча швидкість вибору відповіді. В усіх цих дослідженнях фексофенадин показав найменший CRT проти АГП І покоління (ЗСР= - 61,41; 95% ДІ від -81,87 до -40,96; р<0,00001). У 4 дослідженнях із 7 показано однаковий CRT у разі прийому фексофенадину та АГП ІІ покоління (ЗСР=5,28; 95% ДІ від -3,07 до 13,63; р=0,22) і в 6 із 7 робіт не виявили відмінностей у CRT між фексофенадином і плацебо (ЗСР=3,68; 95% ДІ 2,95-10,32; р=0,28).
CTT проводять для оцінки розподіленої уваги і здатності до концентрації. Що вищий бал, то нижча здатність до концентрації. У 3 дослідженнях серед здорових осіб СТТ порівнювали між групами АГП І покоління, АГП ІІ покоління і плацебо. Проти АГП І покоління фексофенадин значно менше змінював СТТ (ЗСР= -21,79; 95% ДІ від -42,44 до -1,14; р=0,04), так само як і проти АГП ІІ покоління (ЗСР= -2,43; 95% ДІ від -3,67 до -1,18; р=0,0001). У групах плацебо і фексофенадину СТТ не відрізнявся (ЗСР=0,11; 95% ДІ 3,81-4,02; р=0,96).
LARS – суб’єктивна оцінка пацієнтом «втомлюваності», «сонливості» і «пильності». Що вища оцінка (у мм), то менший ступінь бадьорості і вищий ступінь втомлюваності/сонливості у випробовуваних. Цю шкалу використовували в 7 дослідженнях, де порівнювали фексофенадин із плацебо і АГП І покоління, у 3 із них – з АГП ІІ покоління. Фексофенадин призводив до значно менших змін LARS проти АГП І покоління (ЗСР= -6,34; 95% ДІ від -10,53 до -2,15; р=0,003), АГП ІІ покоління (ЗСР= -7,75; 95% ДІ від -12,56 до -2,93; р=0,002) і плацебо (ЗСР= -2,67; 95% ДІ від -3,99 до -1,35; р<0,0001).
VAS – у 3 дослідженнях повідомлялося про сонливість у пацієнтів після прийому фексофенадину відповідно до балів VAS. Із 3 досліджень за участю здорових добровольців у 2 препарат порівнювали з АГП І покоління, ще у 2 – з АГП ІІ покоління, і в усіх – із плацебо. Порівняння фексофенадину і АГП ІІ покоління не було залучено до метааналізу, оскільки було знайдено лише 2 дослідження з високою гетерогенністю. Проти АГП І покоління фексофенадин спричинював значно меншу зміну сонливості за VAS (ЗСР= -15,72; 95% ДІ від -17,33 до -14,11; р<0,00001). При порівнянні з плацебо оцінка сонливості за VAS не відрізнялася (ЗСР=7,18; 95% ДІ 0,64-14,99; р=0,07). Резюме результатів щодо вивчення безпеки фексфенадину представлені в таблиці.
Обговорення
Цей перший метааналіз, проведений з метою оцінки антигістамінних і седативних ефектів фексофенадину, вказує на кращий профіль безпеки фексофенадину проти АГП ІІ покоління [8]. Антигістамінні ефекти (швидкість інгібування гістамін-індукованого пухиря і гіперемії) фексофенадину були значно вищі за такі плацебо і не дуже відрізнялися від інших представників АГП ІІ покоління.
Це важливий критерій оцінки ефективності АГП при лікуванні АЗ. Ґрунтуючися на об’єднаному аналізі, ми виявили, що антигістамінні ефекти і тривалість дії фексофенадину, порівнянні з такими АГП ІІ покоління і перевищують плацебо. Аналогічні дані були отримані в недавньому систематичному огляді і метааналізі; було показано, що фексофенадин ефективно усуває назальні симптоми в пацієнтів із сезонним АР (САР), але обмеженням цієї роботи було включення в дослідження лише пацієнтів із САР.
Наведений метааналіз охоплює ширше коло пацієнтів, у ньому враховані всі РКД, в яких використовували фексофенадин і порівнювали ефекти з такими інших АГП або плацебо, шляхом оцінки ступеня пригнічення гістамін-індукованого пухирів і гіперемії [9-59]. Таким чином, фексофенадин, що виявляє позитивну антигістамінну дію, підходить більшості пацієнтів, які потребують терапії АГП. Варто зазначити деякі невідповідності в результатах окремих досліджень. Так, одна з робіт показує, що рівень інгібування гістамін-індукованого пухиря і гіперемії у фексофенадину нижчий за такий лоратадину, тоді як в іншому дослідженні було показано, що фексофенадин забезпечував значно вищий рівень інгібування гістамін-індукованого пухиря і гіперемії проти лоратадину [36]. Причиною цього можуть бути різні дози фексофенадину (60 і 180 мг/добу) і однакова доза лоратадину (10 мг/добу) у двох випробуваннях [55]. Отже, необхідні подальші дослідження для визначення безпечнішої й ефективнішої, проти лоратадину, дози фексофенадину.
ПЕ, які оцінювали в цьому метааналізі: головний біль, сонливість, втомлюваність, інфекції верхніх дихальних шляхів, астма, фарингіт, сухість у роті, кашель, нудота, шлунково-кишкові болі, діарея, висип, носова кровотеча, синусит, біль у спині, лейкопенія та ін. Головний біль – найчастіший ПЕ у пацієнтів, які отримували фексофенадин. Загалом препарат добре переносився, через ПЕ його прийом припинили лише <5% пацієнтів [63].
Усі АГП І покоління і більшість АГП ІІ покоління є кардіотоксичними внаслідок пригнічення мускаринових холінорецепторів (M-ХР), які можуть регулювати частоту серцевих скорочень, серцевий ритм і роботу серцевого м’яза [64]. Попереднє дослідження показало, що фексофенадин не подовжує інтервал QT і не спричинює аритмію, коли використовується окремо або в поєднанні з іншими препаратами, такими як кетоконазол і еритроміцин [65].
Проведений систематичний огляд і метааналіз продемонстрували відсутність гепато- і кардіотоксичного ефекту в осіб, які отримували фексофенадин, також не було значущої різниці в частоті ПЕ між фексофенадином і плацебо в пацієнтів із САР [66]. Стосовно ПЕ – профіль безпеки фексофенадину вищий за такий АГП І покоління і зіставний з іншими представниками АГП ІІ покоління, а головне – із плацебо.
Седативний ефект – одна з серйозніших проблем, пов’язаних із ПЕ [67]. Поточне дослідження демонструє, що ризик розвитку седативної дії при застосуванні фексофенадину нижчий у порівнянні з представниками інших АГП і порівняний з таким у плацебо.
Було показано відсутність або легкий седативний ефект фексофенадину, оскільки він не може проникати крізь ГЕБ [68]. Це значуща перевага фексофенадину, тому що, наприклад, левоцетиризин, за даними недавнього метааналізу, має легку седативну дію, попри те що належить до АГП нового покоління. Тому за сукупністю отриманих даних фексофенадин, який не має седативної дії, є одним з найкращих АГП нового покоління.
З огляду на той факт, що фексофенадин здатен не виявляти седативного ефекту, відповідно до консенсусу експертів у США, Національне управління з аеронавтики і дослідження космічного простору (НАСА) дозволило пілотам у разі потреби використовувати фексофенадин [70].
Когнітивна психомоторна функція – ще одна важлива проблема ПЕ. Дане дослідження демонструє, що фексофенадин рідше спричинює когнітивні/психомоторні порушення, якщо порівнювати з АГП І та іншими представниками ІІ покоління, і їх частота є такою самою, як і в плацебо [71].
Недавній систематичний огляд показав, що на японському ринку фексофенадин був визнаний АГП, що найменше спричинює психомоторні порушення проти всіх інших АГП. У наведений метааналіз були включені АГП, які використовують в усьому світі. Це додатково підтверджує, що фексофенадин здатен не спричинювати когнітивних/психомоторних порушень.
Стосовно CFF було виявлено, що пацієнти, які отримують фексофенадин, краще здатні обробляти інформацію проти тих, хто застосовує прометазин. Аналогічним чином дослідження показало, що здатність обробляти інформацію була вищою після лікування фексофенадином у дозі 120 мг/добу або 60 мг/добу проти олопатадину в дозі 10 мг/добу або 5 мг/добу [28, 49].
У цьому дослідженні є кілька потенційних обмежень. Визначення підгруп щодо дози/тривалості/типу АГП було недоступне через обмежену кількість досліджень. Для порівняння антигістамінних ефектів і когнітивних/психомоторних функцій не було проведено РКД з великою вибіркою, що може збільшити ризик систематичної помилки. Спосіб вимірювання результатів, таких як частота небажаних явищ і седативних ефектів, був іншим.
Висновки
Дані систематичного огляду і метааналізу досліджень свідчать про виражену антигістамінну дію фексофенадину, що робить його препаратом вибору при лікуванні низки АЗ. Ще одним украй важливим аспектом є сприятливий профіль безпеки фексофенадину, а також той факт, що він є одним із кращих серед АГП ІІ покоління через відсутність впливу на когнітивні функції і седативного ефекту.
Таким чином, фексофенадин може бути рекомендований особам, чия діяльність пов’язана з безпекою і необхідністю концентрації уваги. Однак для глибшого розуміння ефективності й безпеки фексофенадину необхідні додаткові багатоцентрові дослідження з великою вибіркою, довгострокове спостереження і добре сплановані клінічні дослідження.
Реферативний огляд Huang C. et al. Antihistamine effects and safety
of fexofenadine: a systematic review and Meta-analysis of randomized controlled trials. BMC Pharmacology and Toxicology. 2019.
Підготувала Ірина Чумак
Повну версію див.: https://bmcpharmacoltoxicol.biomedcentral.com/articles/10.1186/s40360-019-0363-1