21 липня, 2022
Причины, особенности и тактика ведения COVID‑19-ассоциированной пневмонии, осложнившейся острым респираторным дистресс-синдромом

В 1967 г. Ashbaugh и соавт. впервые описали синдром острого повреждения легких (СОПЛ) [1]. Авторы наблюдали 12 больных, семь из которых умерли. Клиническая картина соответствовала острому респираторному дистрессу в виде диффузного цианоза, резистентности к дотации О2, снижения комплаенса легких и обнаружения диффузных инфильтратов на обзорной рентгенограмме легких. Тогда же и был применен термин «респираторный дистресс-синдром взрослых», что подразумевало его отличие от респираторного дистресс-синдрома новорожденных. В дальнейшем это состояние имело множество синонимов: «некардиогенный отек легких», «тяжелое легкое», «шоковое легкое» и др. [2]. В 1946 г. группа американских военных врачей ввела термин «влажные легкие», использовав положительное давление в конце выдоха (ПДКВ) [5], а в 1994 г. на Американо-европейской согласительной конференции (АЕСК) это состояние было названо острым респираторным дистресс-синдромом (ОРДС) [3].
С позиций патофизиологии ОРДС стал пониматься как мозаичное ателектазирование легких, нарушение диффузии газов через альвеолярно-капиллярную мембрану и возрастание внутрилегочного шунтирования крови. Цель применения ПДКВ при ОРДС состояла в предотвращении коллабирования альвеол в фазу выдоха, то есть в поддержании альвеол в расправленном состоянии в течение всего дыхательного цикла [4].
Что касается СОПЛ, то на протяжении последующих десятилетий после описания изучались его патогенез, методы лечения, диагностические критерии, эпидемиология, что, в свою очередь, побудило пересмотреть и название. Поэтому вначале применялся термин «респираторный дистресс-синдром взрослых», а в последующем СОПЛ рассматривался как ОРДС, что подчеркивало остроту его развития.
В англоязычной литературе используется аббревиатура ARDS (acute respiratory distress syndrome). Обоснованием к изменению определения явилось внедрение системы количественной оценки степени повреждения легких, включающей четыре параметра: уровень ПДКВ (PEEP – positive end-expiratory pressure), отношение парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода, выраженное в десятых долях (например, 50% концентрация соответствует примерно FiO2 = 0,5; РаО2/ FіO2), легочный комплаенс (показатель растяжимости легочной ткани, определяющий способность легких расширяться при дыхательных движениях грудной клетки, С = deltaV/P) и объем (процент) альвеолярного поражения.
Другие факторы, которые были использованы в оценке выраженности ОРДС, включали поражение не только респираторного аппарата, но также других органов и систем человека. Такой подход сыграл большую роль в оценке эффективности тех или иных методов лечения. Однако недостатком была невозможность определить прогноз исхода в первые два дня развития ОРДС.
Наконец, современный этап определения этого синдрома включает один из центральных патогенетических механизмов его развития – повреждение альвеоло-капиллярной мембраны, что и обусловливает повышенную проницаемость эндотелиальных и эпителиальных клеток, регулирующих водно-электролитный обмен дистального отдела дыхательных путей. Клиническим проявлением этих нарушений является развитие некардиогенного отека легких [5]. Таким образом, СОПЛ является равнозначным ОРДС с отличием в степени гипоксемии (РаО2/FiO2 Ќ 300 мм рт. ст.). В англоязычной литературе чаще используется аббревиатура ALІ/ARDS (acute lung injury and the acute respiratory distress syndrome).
Новой сложной и противоречивой проблемой в понимании ОРДС явилось его лечение при COVID‑19. Многочисленные исследования показали вероятность атипичной патофизиологии для объяснения спектра легочных и системных проявлений, вызванных возбудителем данного заболевания. Главный парадокс COVID‑19-ассоциированной пневмонии – наличие тяжелой гипоксемии с сохраненной легочной механикой. Данные, полученные из опыта нескольких центров в мировом масштабе, показали, что первоначальные клинические меры должны быть направлены на то, чтобы избежать искусственной вентиляции легких у пациентов с гипоксемией, обусловленной COVID‑19. С другой стороны, пациенты с COVID‑19, состояние которых прогрессирует до ОРДС или достигает явного ОРДС с типичным снижением легочного комплаенса, это еще одна клиническая загадка для многих клиницистов.
Итак, SARS-CoV‑2-инфекция, вызвавшая тяжелый ALІ/ARDS, является беспрецедентной клинической проблемой, а уникальность течения этой инфекции с необычной патофизиологей ставит под сомнение эффективность существующих терапевтических подходов. Данная статья представляет собой обзор современного клинического опыта и не предназначена для использования в качестве стандарта лечения, учитывая, что доказательная база, лежащая в основе клинического подхода у пациентов с COVID‑19-ассоциированной пневмонией, быстро развивается. Да и, собственно, традиционное определение бактериальной «пневмонии» как экссудации в альвеолы не соответствует поражению паренхимы легких в виде «матовых стекол» с ее патоморфологическими характеристиками (рис. 1-4).
Рис. 1. Вирусная «пневмония» при COVID-19. Компьютерная томография органов грудной клетки (КТ ОГК) демонстрирует
двусторонние помутнения в виде «матового стекла», смешанные с пятнистыми областями консолидации
Рис. 2. Бактериальная пневмония. Участок консолидации легочной ткани слева, широким основанием прилегающий
к костальной плевре и имеющий конусовидную форму
Учитывая лучевые и морфологические характеристики при CОVID‑19 и бактериальном (пневмококковом) поражении легочной ткани, применение антибактериальных препаратов в первом случае (рис. 1 и 3) необоснованно.
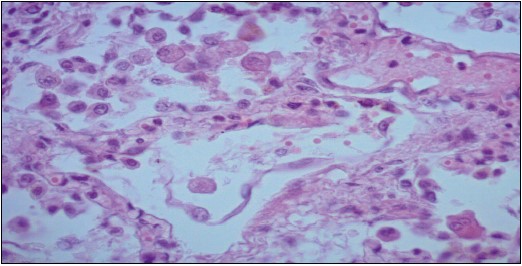
Рис. 3. Паренхима легкого умершего от COVID-19. Ранняя фаза экссудации. В просветах альвеол и интерстиции
легкого инфильтрат, представленный мононуклеарами, преимущественно макрофагами (крупные округлые
клетки), сегментоядерные лейкоциты отсутствуют; ×400. Окраска гематоксилин-эозин
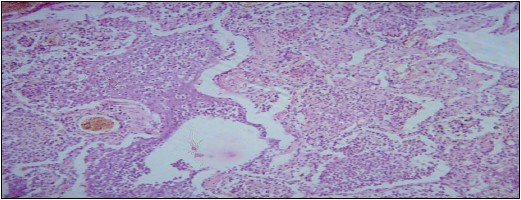
Рис. 4. Легочная паренхима умершего от пневмококковой пневмонии. Микроскопически – диффузная гнойная
пневмония: межальвеолярные перегородки не утолщены, в просвете альвеол фибринозно-гнойный экссудат, без богатой белком жидкости; ×100. Окраска гематоксилин-эозин
Механизмы, лежащие в основе патофизиологии COVID‑19-ассоциированной «пневмонии», осложнившейся ОРДС, постоянно исследуются и развиваются. Вопрос, имеют ли пациенты с COVID‑19 сходную патофизиологию с «типичным» ОРДС и соответствуют ли они определению Берлинских критериев (ARDS; CPAP – постоянное положительное давление в дыхательных путях; FiO2 – фракция кислорода во вдыхаемой смеси; РаО2 – парциальное давление артериального кислорода; ПДКВ (РЕЕР), остается предметом дискуссий.
На основании имеющихся в настоящее время результатов исследований были описаны следующие патофизиологические механизмы.
Гипоксемическая дыхательная недостаточность: прямые цитопатические эффекты вируса на пневмоциты, отличающиеся от бактериального воспалительного процесса, и вызванное вирусом уменьшение сурфактанта, провоцирующее развитие ателектаза, являются одними из уникальных патологических находок, наблюдаемых у пациентов с COVID‑19. Описаны также традиционные диффузные альвеолярные кровотечения и образование гиалиновых мембран [6]. Гипоксемия является паттерном легочного поражения, однако во многих случаях пациенты с COVID‑19 продемонстрировали наличие значительной гипоксемии без признаков респираторного дистресса («тихая гипоксемия») [7, 8].
В свете этих результатов Gattinoni и соавт. описали два фенотипа пневмонии при COVID‑19. Тип 1 (или тип L, «без ОРДС»): пациент с нормальным или высоким комплаенсом дыхательной системы (>50 мл/см вод. ст.), низкой эластичностью легких, низким весом легких и низкой способностью к раскрытию (рекрутингу) легких. Считается, что гипоксемия связана с нарушением кровотока и гипоксической вазоконстрикцией легких, что приводит к значительному несоответствию вентиляции и перфузии. Тип 2 (или тип H, «типичный ОРДС»): когда у больного отмечается тяжелая гипоксемия и заметно сниженный комплаенс дыхательной системы (<40 мл/см вод. ст.), высокая эластичность легких, большой вес легких (>1,5 кг) и высокая способность к рекрутингу. Перекрестные характеристики обоих этих типов могут присутствовать у больного в качестве промежуточной стадии [9, 10]. Однако в когортном исследовании Ziehr и соавт. представлены 66 интубированных пациентов с COVID‑19, имеющих аналогичную легочную механику «типичного» ОРДС, основанную на снижении эластичности легких, мертвом пространстве и реакции на положение лежа. Следовательно, необходимы дальнейшие исследования для определения «нетипичной» модели ОРДС.
Гиперцитокинемия, или цитокиновый шторм, – нарушение регуляции и чрезмерный иммунный ответ, который может привести к значительному системному повреждению. Мононуклеарные клетки, такие как нейтрофилы и моноциты, в тканях легких и периферической крови продуцируют повышенные уровни провоспалительных цитокинов: интерлейкина‑6 (IL‑6), IL‑1 и фактора некроза опухоли. Доказательства подтверждают заметное высвобождение цитокинов при COVID‑19, напрямую связанное с тяжестью заболевания и смертностью от него, и это особенно отражается в высоких уровнях IL‑6, ферритина и С-реактивного белка (CРБ) [11, 12].
Гиперкоагуляция, связанная с COVID-19, описана как отчетливое протромботическое состояние, в отличие от незначительной коагулопатии, вторичной по отношению к заметно повышенным уровням фибрина и фибриногена. Этот механизм синергичен с цитокиновым штормом и вирусной эндотелиальной дисфункцией. Следовательно, сывороточные уровни D-димера являются весомым прогностическим фактором плохого исхода [13, 14].
Клиническая картина и лабораторные данные
Частота лихорадки у больных варьирует в пределах 43-98%, поэтому отсутствие лихорадки не исключает заражения COVID‑19. Кашель – второй по частоте симптом (59-72%), за ним следуют миалгия (15%) и слабость (23%). Желудочно-кишечные симптомы (диарея, тошнота и рвота) наблюдались у 10% пациентов, как правило, до появления лихорадки и одышки [15]. Описано, что ОРДС развивается у 17-41% этих больных, при этом среднее время от появления первого симптома до прогрессирования ОРДС составляет 8 дней [15, 16].
Что касается первоначальных лабораторных данных, то количество лейкоцитов обычно в норме, а лимфопения присутствует у 80% пациентов [17]. Было также обнаружено, что уровень СРБ постоянно повышается у пациентов с COVID‑19 и имеет обратную зависимость от уровня потребности в кислороде; его можно использовать для прогнозирования смертности [18]. Другими прогностическими лабораторными показателями, имеющими прямую связь со смертностью от COVID‑19, являются IL‑6, LDH, сывороточный ферритин и D-димер. Уровни прокальцитонина у этих пациентов умеренно повышены и не всегда связаны с прогнозированием смертности [17]. В дополнение к полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) при COVID‑19 необходимо выполнять обычные посевы крови и вирусную панель, чтобы исключить присутствие любого другого патогена в качестве основного виновника или коинфекции.
Результаты лучевой диагностики
Рентгенограмма ОГК демонстрирует типичные пятнистые затемнения в виде «матового стекла», которые имеют периферическую (субплевральную) и базальную локализацию, но ее чувствительность составляет около 59% [19]. Что касается КТ ОГК, то ее чувствительность зависит от симптоматики пациента на момент проведения исследования: 86-97% – у пациентов с респираторными симптомами и 50% – у пациентов только с конституциональными симптомами [20, 21].
Чжоу и соавт. в когорте из 100 пациентов с COVID‑19 провели 272 КТ ОГК и выявили преобладающее периферическое распределение «матовых стекол» (62%), за которым следовало комбинированное периферическое и центральное распределение (38%). Большинство больных имели двустороннее поражение легких (92%) и значительное поражение средних, нижних и задних сегментов [22].
Не всем пациентам с подозрением на COVID‑19-ассоциированную пневмонию требуется КТ ОГК. Безусловно, вопрос спорный, так как КТ, в отличие от обзорной рентгенограммы ОГК, точна в проценте поражения, верификации паттерна «матовое стекло», консолидации и др. Поэтому решение о проведении этого обследования должно приниматься в индивидуальном порядке на основе суждения врача.
Также описывается УЗИ легких у тяжелых пациентов с COVID‑19-ассоциированной пневмонией; его результаты ограничены периферическими изменениями и не всегда коррелируют с результатами КТ. Peng и соавт. описали наличие рассеянных B-линий, которые имеют тенденцию сливаться по мере прогрессирования заболевания. Описано утолщение плевральных листков, а также плевральный выпот [23].
Внутрибольничное распространение и аэрозолизация
Экологический контроль имеет первостепенное значение при начальной оценке больных с пневмонией, обусловленной COVID‑19. Меры предосторожности против воздушно-капельной передачи регламентируются многими организациями. Всемирная организация здравоохранения и протоколы, изданные МЗ Украины, рекомендуют меры предосторожности, связанные с воздушным переносом, когда у пациентов с COVID‑19 ожидаются процедуры, сопровождающиеся образованием аэрозолей, в том числе: вентиляция с помощью маски для лица, неинвазивная вентиляция, эндотрахеальная интубация, отсасывание из дыхательных путей, аэрозольный путь введения лекарств, бронхоскопия, отключение пациента от аппарата искусственной вентиляции легких (ИВЛ) и сердечно-легочная реанимация. Несмотря на высокий риск заражения во время этих процедур, имеющиеся данные свидетельствуют о том, что тщательное использование средств индивидуальной защиты эффективно для предотвращения инфицирования медицинского персонала [24, 25].
У пациентов со спонтанным дыханием важно контролировать респираторный драйв и усилия для выявления ранних фаз респираторного поражения. Хотя неинвазивная вентиляции легких (НИВ) использовалась у пациентов с COVID‑19-ассоциированной пневмонией, данные литературы относительно адекватного периода интубирования противоречивы. Большинство авторов соглашаются с тем, что при наличии нарушений дыхательной механики, возникновении респираторного ацидоза не следует откладывать контроль психического статуса, и при неадекватности коррекции сатурации и кислотно-щелочного равновесия необходима ИВЛ [9].
Для пациентов со спонтанным дыханием, сопровождающимся одышкой и гипоксемией легкой и средней степени тяжести, невосприимчивых к назальной канюле с низким потоком, начальный подход может включать использование назальной канюли с высоким потоком (HFNC) в состоянии бодрствования на основе ограниченных клинических данных. HFNC поначалу вызывала споры из-за ее проблемной способности к оксигенации, однако в дальнейших исследованиях было обнаружено, что она безопасна, при этом биоаэрозольная дисперсия существенно не отличается от обычных назальных канюль [26]. Ян и и соавт. продемонстрировали более высокую выживаемость пациентов с HFNC по сравнению с пациентами с другими средствами ИВЛ, как неинвазивными, так и инвазивными [27]. Cостояние бодрствования предполагает лежание пациента на животе в качестве метода улучшения дренирования секрета и предупреждения образования легочных ателектазов в нижних долях легких [28].
Постоянное положительное давление в дыхательных путях методом CPAP или двухуровневым положительным давлением в дыхательных путях (BiPAP) использовались у пациентов с COVID‑19 в качестве последнего средства перед эндотрахеальной интубацией после неудачной HFNC и в бодрствующем положении, хотя официальные рекомендации относительно их использования были разрешены из-за риска аэрозолизации [24].
CPAP, по-видимому, имеет наибольшее преимущество среди НИВ у пациентов с COVID‑19-ассоциированной пневмонией, поскольку обеспечивает наибольшее среднее давление в дыхательных путях, что приводит к более эффективному раскрытию (рекрутированию) альвеол по сравнению с BiPAP. Последний вариант оказался более подходящим для определенной группы пациентов с сопутствующими заболеваниями (например, хроническая обструктивная болезнь легких, застойная сердечная недостаточность) [9]. В связи с аэрозольным потенциалом традиционных методов НИВ было предложено использование «шлемового CPAP» в качестве средства неинвазивной вентиляции [29].
Крайне важно внимательно следить за кислородной передозировкой у больных с COVID‑19, которые самостоятельно дышат (независимо от использования HFNC или NIV). В контексте раннего ОРДС, ассоциированного с COVID‑19, высокий респираторный драйв может привести к генерации высокого транспульмонального давления и стрессу легких с последующим повышенным риском развития «самопроизвольного повреждения легких пациентом» (P-SILI) [30].
Подход к интубированному больному с COVID‑19
ИВЛ должна быть произведена как можно скорее, независимо от фенотипа пневмонии при COVID‑19, когда признаки ОРДС связаны с тяжелой гипоксемией. Приведенные ниже стратегии вентиляции представляют собой экспертное мнение, основанное на текущих и быстро развивающихся данных о больных с ОРДС, в этой связи требуется дополнительная информация для подтверждения эффективности этих методов ведения.
Управление механической вентиляцией
Гаттинони и соавт. предложили адаптированные модификации к традиционным принципам лечения ОРДС, основанные на фенотипах COVID‑19-ассоциированной пневмонии. У интубированных больных с I фенотипом лечение гипоксемии должно быть направлено на улучшение несоответствия вентиляции/перфузии за счет дерегуляции дыхательных объемов (идеальная масса тела 7-8 мл/кг массы тела, чтобы избежать ателектаза резорбции), ограниченных уровней ПДКВ (8-10 см вод. ст.) и поддержание частоты дыхания <20 в минуту [31].
По мере прогрессирования поражения легких с появлением II фенотипа и «типичного» ОРДС (двусторонние инфильтраты, снижение податливости дыхательной системы и увеличение веса легких) стандартный подход щадящей вентиляции легких связан с низким дыхательным объемом (идеальная масса тела 6 мл/кг массы тела), уровень ПДКВ (<10 -15 см вод. ст.), а также пермиссивная гиперкапния продемонстрировали, что это оптимальное вмешательство при ОРДС, ассоциированном с COVID‑19 [38]. Цель состоит в том, чтобы избежать повреждения легких, вызванного аппаратом, за счет снижения нагрузки на легкие и сосуды [32]. В то время как некоторые авторы выступают за высокие уровни ПДКВ (<15 см вод. ст.) при II фенотипе, на основе высокой эластичности легких и увеличения неоксигенированной легочной ткани [8], в одноцентровом наблюдательном исследовании показали плохое раскрытие альвеол, несмотря на высокие уровни ПДКВ. «Раскрытие легких» было более очевидным после прон-позиции в анализируемой популяции [33].
Вентиляция с переменным давлением в дыхательных путях (APRV) может рассматриваться в ранний период интубации у пациентов с умеренным и тяжелым ОРДС с целью обеспечения адекватного раскрытия альвеол. Применение APRV по-прежнему ограничено, учитывая, что многие производители не знакомы с этим режимом вентиляции или методикой его выбора [34]. Поэтому данные о полезности APRV у пациентов с ОРДС, ассоциированным с COVID‑19, еще только исследуются.
Положение на животе способствует облегчению тяжелой гипоксемии за счет уменьшения чрезмерно раздутых областей легких, что способствует рекрутированию альвеол и уменьшению несоответствия вентиляции/перфузии [33]. Испытание «The Proning Severe ARDS Patients» у тяжелых пациентов с ОРДС (PROSEVA), проведенное Guerin и соавт., продемонстрировало значительное снижение 28- и 90-дневной смертности у пациентов с тяжелым ОРДС [35].
Положение лежа рекомендуется у интубированных больных с ОРДС, ассоциированным с COVID‑19. Pan и соавт. продемонстрировали повышенную рекрутируемость легких и улучшение PaO2/FiO2 в положении лежа на животе у пациентов с умеренным ОРДС, ассоциированным с COVID‑19 [33]. Основным препятствием по-прежнему является его внедрение в лечебные учреждения. Обученный и квалифицированный высший, средний и младший медперсонал респираторной терапии является наиболее важным фактором для получения успешных результатов, поскольку в любой момент могут произойти опасные для жизни события (самоэкстубация, гемодинамическая нестабильность, отсутствие адекватной седации, пролежни).
Что касается нервно-мышечной блокады, то она рекомендуется для предупреждения вентиляторной диссинхронизации, регулировки дыхательных объемов и снижения сопротивления дыхательных путей, что уменьшает воспаление паренхимы легких. Нервно-мышечные блокаторы были введены как часть альтернативной терапии тяжелого ОРДС [36]. Пока не опубликовано ни одного официального клинического исследования или каких-либо доказательств относительно использования нервно-мышечной блокады у пациентов с ОРДС, ассоциированным с COVID‑19. Кампания Surviving Sepsis Campaign рекомендует использовать периодические дозы нервно-мышечных блокаторов для облегчения вентиляции легких у пациентов с COVID‑19 [24].
Оценивая противовоспалительную терапию больных с ОРДС, ассоциированным с COVID‑19, исследование RECOVERY продемонстрировало, что у пациентов в группе вмешательства (то есть принимавших дексаметазон в дозе 6 мг в течение 10 дней, энтерально или внутривенно) смертность снижалась на треть среди госпитализированных пациентов с тяжелыми респираторными осложнениями от COVID‑19. Эффект был более заметным у пациентов, находящихся на ИВЛ, и промежуточным у тех, кому требовалась только дотация кислорода. Исследование не показало какой-либо пользы от дексаметазона у пациентов, которым не требовалась кислородная дотация [37].
Считается, что селективная вазодилатация легких улучшает течение ОРДС путем перераспределения крови из плохо вентилируемых зон в зоны с более высокой вентиляцией, тем самым уменьшая шунтирование и корректируя гипоксемию. Оксид азота и простагландины (например, PGI2, эпопростенол), несмотря на вызываемую им легочную артериальную дилатацию, не продемонстрировал уменьшения смертности при ОРДС [44]. Использование оксида азота у пациентов с COVID‑19 вызывает споры [45]. Некоторые авторы выступают за его потенциальную противовирусную активность на основании результатов исследования, проведенного во время вспышки SARS-CoV в 2004 г. [46]. В настоящее время нет рекомендаций по применению легочных вазодилататоров у пациентов с ОРДС, ассоциированным с COVID‑19, в случаях экстренной помощи при рефрактерной гипоксемии [37].
Когда наступает рефрактерная гипоксемия и альтернативные методы лечения оказываются неэффективными, уместным становится использование экстракорпоральных приемов. Несмотря на то что частота случаев применения экстракорпоральной мембранной оксигенации (ЭКМО) значительно увеличилась за последние десятилетия, ее использование по-прежнему остается спорным.
Два крупных многоцентровых рандомизированных клинических исследования предоставили противоречивые данные по использованию ЭКМО при ОРДС. Испытание CESAR (традиционная ИВЛ в сравнении с ЭКМО при тяжелом ОРДС) в исследовании Peek и соавт. (2009) представило обнадеживающие результаты, демонстрирующие значительную выживаемость без тяжелой инвалидности через 6 месяцев. Авторы этого исследования пришли к выводу, что пациентам с тяжелым ОРДС с потенциально обратимыми параметрами, не поддающимися традиционному лечению, следует назначать ЭКМО. С другой стороны, в исследовании EOLIA (ECMO to Rescue Lung Injury in ARDS), проведенном Combes и соавт. (2018), обнаружилось, что 60-дневная смертность не была значительно ниже у пациентов в группе ЭКМО, и поэтому испытание было остановлено в соответствии с заранее определенными правилами, хотя апостериорный байесовский анализ этого испытания продемонстрировал апостериорную вероятность увеличения смертности при ЭКМО у больных с очень тяжелым ОРДС [38].
В свете этих противоречивых результатов и в разгар всемирной пандемии, вызванной COVID‑19, когда ожидается, что у пациентов разовьется тяжелый ОРДС, Организация экстракорпорального жизнеобеспечения (ELSO) выпустила согласованное руководство по применению ЭКМО у этих пациентов. ELSO подчеркивает, что опыт центра, а также подготовка медработников и команды являются наиболее важными факторами, определяющими использование экстракорпоральных методов у пациентов с COVID‑19. Что касается приоритизации пациентов в применении этого метода, то руководство ELSO рекомендует отдавать приоритет более молодым пациентам с незначительными сопутствующими заболеваниями или без них. Также рекомендуется не включать больных с терминальным течением какого-либо заболевания или тяжелым поражением центральной нервной системы.
Чтобы определить соответствие пациента критериям отбора, консенсус ELSO при ОРДС, ассоциированном с COVID‑19, предоставляет четкий алгоритм для пациентов с PaO2/FiO2 <150 мм рт. ст., ориентированный на обеспечение консервативного лечения (положение на животе, нервно-мышечная блокада, легочные вазодилататоры, высокие уровни ПДКВ, маневры с положением тела). Если у пациента развивается прогрессирующая рефрактерная гипоксемия (соотношение PaO2/FiO2 <80 мм рт. ст. в течение >6 ч или соотношение PaO2/FiO2 <50 мм рт. ст., а PaCO2 >60 мм рт. ст.), следует рассмотреть ЭКМО при отсутствии противопоказаний. Кроме того, для пациентов с соотношением PaO2/FiO2 >150 мм рт. ст., но с признаками плохой тканевой перфузии и гиперкапнией необходимо выбрать ЭКМО как лучший вариант.
В заключение следует отметить, что ведение COVID‑19-ассоциированной пневмонии, осложненной ОРДС, представляет собой серьезную клиническую, логистическую, реанимационную и этическую проблему. В основе развития ОРДС/СОПЛ лежит воспалительная реакция, повреждающая альвеоло-капиллярную мембрану, что приводит к некардиогенному отеку легких, снижению легочного комплаенса, увеличению шунтирования в малом круге и, как следствие, – к тяжелой дыхательной и полиорганной недостаточности.
Сама по себе гипоксемия не является показанием для интубации, если легочная механика сохранена. Напротив, пролонгация дыхательных нарушений, возникших спонтанно либо на фоне НИВ, приводит к психическим нарушениям и развитию респираторного ацидоза. Диагностические мероприятия, направленные на выявление больных с ОРДС, требующих ИВЛ, являются актуальными, поскольку задержка в проведении этого вмешательства связана с трагическим исходом. Создание специализированного протокола для такого контингента больных может иметь первостепенное значение.
Литература
- Ashbaugh D.G., Bigelow D.B., Petty T.L. et al. Acute respiratory distress in adults. Lancet. 1967;12(7511):319–323.
- Ranieri V.M., Rubenfeld G.D., Thompson B.T. et al. Acute respiratory distress syndrome: the Berlin Definition. J.A.M.A. 2012;307(23):2526-2533.
- Bernard J.R., Artigas A., Brigham K.L. et al. The American-European Consensus Conference on ARDS. Definitions, mechanisms, relevant outcomes, and clinical trial coordination. Am J Res Crit Care Med. 1994;149:818–824.
- Глумчер Ф.С. Острый респираторный дистресс-синдром: определение, патогенез, терапия. Мистецтво лікування. 2004. № 9. С. 30-35.
- Чучалин А.Г. Синдром острого повреждения легких. РМЖ. 2006. № 22.
- Xu Z, Shi L, Wang Y, Zhang J, Huang L, Zhang C, et al. Pathological findings of COVID‑19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020;8(4):420-422. https://doi.org/10.1016/S2213–2600(20)30076-X.
- Xie J, Tong Z, Guan X, Du B, Qiu H. Clinical characteristics of patients who died of coronavirus disease 2019 in China. JAMA Netw Open. 2020;3(4): e205619. https://doi.org/10.1001/jamanetworkopen.2020.5619.
- Gattinoni L, Coppola S, Cressoni M, Busana M, Rossi S, Chiumello D. Covid-19 does not Lead to a «typical» acute respiratory distress syndrome. Am J Respir Crit Care Med. 2020;201(10):1299-1300. https://doi.org/10.1164/ rccm.202003–0817LE.
- Gattinoni L, Chiumello D, Rossi S. COVID‑19 pneumonia: ARDS or not? Critical care (London, England). 2020;24(1):154. https://doi.org/10.1186/ s13054–020–02880-z.
- Marini JJ, Gattinoni L. Management of COVID‑19 respiratory distress. JAMA. 2020. https://doi.org/10.1001/jama.2020.6825. 9
- Mehta P, McAuley DF, Brown M, Sanchez E, Tattersall RS, Manson JJ. COVID‑19: consider cytokine storm syndromes and immunosuppression. Lancet. 2020;395(10229):1033-1034. https://doi.org/10.1016/S0140–6736(20)30628–0.
- Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID‑19 in Wuhan, China: a retrospective cohort study. Lancet (London, England). 2020;395(10229):1054-1062.
- Han H, Yang L, Liu R, Liu F, Wu KL, Li J, et al. Prominent changes in blood coagulation of patients with SARS-CoV‑2 infection. Clin Chem Lab Med. 2020;58(7):1116–20. https://doi.org/10.1515/cclm‑2020–0188.
- Spiezia L, Boscolo A, Poletto F, Cerruti L, Tiberio I, Campello E, et al. COVID‑19-related severe hypercoagulability in patients admitted to intensive care unit for acute respiratory failure. Thromb Haemost. 2020;120(6):998–1000. https://doi.org/10.1055/s‑0040–1710018.
- Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020;323(11):1061-1069. https://doi.org/10.1001/jama. 2020.1585.
- Rationale for Prolonged Corticosteroid Treatment in the Acute Respiratory Distress Syndrome Caused by Coronavirus Disease 2019. Available at: https://journalslww.com/ccejournal/fulltext/2020/04000/rationale_for_ prolonged_corticosteroid_treatment18aspx. Accessed in April 20, 2020.
- Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, He JX, et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020. https://doi.org/10. 1056/NEJMoa2002032.
- Young BE, Ong SWX, Kalimuddin S, Low JG, Tan SY, Loh J, et al. Epidemiologic features and clinical course of patients infected with SARSCoV‑2 in Singapore. JAMA. 2020. https://doi.org/10.1001/jama.2020.3204.
- Shi H, Han X, Jiang N, Cao Y, Alwalid O, Gu J, et al. Radiological findings from 81 patients with COVID‑19 pneumonia in Wuhan, China: a descriptive study. Lancet Infect Dis. 2020;20(4):425-434.
- Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. Correlation of chest CT and RT-PCR testing in coronavirus disease 2019 (COVID‑19) in China: a report of 1014 cases. Radiology. 2020. https://doi.org/10.1148/radiol. 2020200642.
- Kanne JP, Little BP, Chung JH, Elicker BM, Ketai LH. Essentials for radiologists on COVID‑19: an update-radiology scientific expert panel. Radiology. 2020. https://doi.org/10.1148/radiol.2020200527.
- Zhou S, Zhu T, Wang Y, Xia L. Imaging features and evolution on CT in 100 COVID‑19 pneumonia patients in Wuhan, China. Eur Radiol. 2020:1–9. https://doi.org/10.1007/s00330–020–06879–6
- Peng QY, Wang XT, Zhang LN. Findings of lung ultrasonography of novel corona virus pneumonia during the 2019–2020 epidemic. Intensive Care Med. 2020;46(5):849–50. https://doi.org/10.1007/s00134–020–05996–6.
- Alhazzani W, Moller MH, Arabi YM, Loeb M, Gong MN, Fan E, et al. Surviving Sepsis campaign: guidelines on the management of critically ill adults with coronavirus disease 2019 (COVID‑19). Crit Care Med. 2020;48(6): e440-469. https://doi.org/10.1097/CCM.0000000000004363.
- The Australian and New Zealand Intensive Care Society COVID‑19 Guidelines. Available at: https://www.anzicscom.au/wp-content/uploads/202 0/03/ANZICS-COVID‑19-Guidelines-Version‑1pdf. Access on June 17, 2020.
- Li J, Fink JB, Ehrmann S. High-flow nasal cannula for COVID‑19 patients: low risk of bio-aerosol dispersion. Eur Respir J. 2020;55(5):2000892. https://doi. org/10.1183/13993003.00892–2020.
- Yang X, Yu Y, Xu J, Shu H, Xia J, Liu H, et al. Clinical course and outcomes of critically ill patients with SARS-CoV‑2 pneumonia in Wuhan, China: a singlecentered, retrospective, observational study. Lancet Respir Med. 2020;8(5):475-481. https://doi.org/10.1016/S2213–2600(20)30079–5.
- Sun Q, Qiu H, Huang M, Yang Y. Lower mortality of COVID‑19 by early recognition and intervention: experience from Jiangsu Province. Ann Intensive Care. 2020;10(1):33. https://doi.org/10.1186/s13613–020–00650–2.
- Lucchini A, Giani M, Isgro S, Rona R, Foti G. The «helmet bundle» in COVID‑19 patients undergoing non invasive ventilation. Intensive Crit Care Nurs. 2020;58:102859. https://doi.org/10.1016/j.iccn.2020.102859. 3.
- Spinelli E, Mauri T, Beitler JR, Pesenti A, Brodie D. Respiratory drive in the acute respiratory distress syndrome: pathophysiology, monitoring, and therapeutic interventions. Intensive Care Med. 2020;46(4):606-618.
- Management of COVID‑19 Respiratory Distress. Available at: https:// jamanetwork.com/journals/jama/fullarticle/2765302. Accessed on June 16, 2020.
- Brower RG, Matthay MA, Morris A, Schoenfeld D, Thompson BT, Wheeler A. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000;342(18):1301-1308.
- Pan C, Chen L, Lu C, Zhang W, Xia JA, Sklar MC, et al. Lung Recruitability in COVID‑19-associated acute respiratory distress syndrome: a single-center observational study. Am J Respir Crit Care Med. 2020;201(10):1294-1297.
- Lim J, Litton E. Airway pressure release ventilation in adult patients with acute hypoxemic respiratory failure: a systematic review and meta-analysis. Crit Care Med. 2019;47(12):1794-1799.
- Guerin C, Reignier J, Richard JC, Beuret P, Gacouin A, Boulain T, et al. Prone positioning in severe acute respiratory distress syndrome. N Engl J Med. 2013;368(23):2159-2168.
- Papazian L, Forel JM, Gacouin A, Penot-Ragon C, Perrin G, Loundou A, et al. Neuromuscular blockers in early acute respiratory distress syndrome. N Engl J Med. 2010;363(12):1107-1116.
- Randomised Evaluation of COVID‑19 Therapy. https://www.recoverytrial.net/ results. Accessed on June 19, 2020.
- Goligher E.C., Tomlinson G, Hajage D, Wijeysundera DN, Fan E, Juni P., et al. Extracorporeal membrane oxygenation for severe acute respiratory distress syndrome and posterior probability of mortality benefit in a post hoc Bayesian analysis of a randomized clinical trial. JAMA. 2018;320(21):2251-2259.
Уперше опубліковано в журналі «Клінічна імунологія. Інфектологія. Алергологія», №7-8 (136-137), 2021 р.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (57), 2021 р.