17 жовтня, 2022
Дисбаланс електролітів у пацієнтів з COVID-19 та його клінічне значення
Електролітні порушення доволі часто виявляють у хворих на COVID-19. Сьогодні достеменно відомо про ризик розвитку гіпомагніємії та гіпокаліємії на тлі коронавірусної інфекції. Недостатність зазначених мікроелементів може обтяжувати перебіг коронавірусної інфекції та сприяти розвитку ускладнень цього захворювання.
Фізіологічна роль магнію
Роль магнію в метаболізмі клітин і тканин є складною та багатофакторною; насамперед він має роль ключового сигнального елемента й метаболіту для забезпечення фізіологічних процесів на клітинному рівні [1-4]. Відомо, що магній – кофактор >600 ферментів й активатор ≈200 біохімічних реакцій. Магній є незамінним у підтримці низки таких життєво важливих функцій: формування кісткової тканини, нервово-м’язова активність, сигнальні шляхи, біоенергетика, метаболізм глюкози, ліпідів і білків, стабільність ДНК/РНК, проліферація клітин [5].
Загальна кількість магнію в організмі дорослої людини становить ≈25 г, з яких 50-60% міститься в кістках, решта 40-50% – у м’яких тканинах, <1% – у крові. Магній здебільшого всмоктується тонким кишечником і меншою мірою – товстим кишечником та виводиться нирками [6]. Дефіцит магнію через недостатнє споживання з їжею в практично здорових людей є відносно рідкісним явищем, оскільки нирки дуже чутливо регулюють його екскрецію; концентрація магнію в сироватці крові може бути ефективно буферизованою за рахунок ниркової екскреції, а також (частково) – за рахунок його вивільнення з кісткової тканини, тому показник концентрації магнію в сироватці крові в межах референтного діапазону не може виключати стану системного виснаження магнію, а клінічний вплив дефіциту магнію можна легко недооцінити [7-9]. Однак за відсутності репрезентативного та легко вимірюваного біомаркера для оцінки забезпеченості магнієм слід покладатися на рівень магнію в сироватці крові.
Зв’язок між дефіцитом магнію та патогенезом COVID‑19
Відомо про важливу роль магнію в захисті від вірусних інфекцій, оскільки адекватні внутрішньоклітинні його концентрації необхідні для забезпечення цитотоксичної активності Т‑лімфоцитів, а також природних клітин-кілерів [10]. Водночас слід згадати, що магній потрібний для синтезу, транспортування й активації вітаміну D, який є імуномодулювальним гормоном [11]. Дефіцит вітаміну D пов’язують з різними інфекційними захворюваннями, в т. ч. з інфекціями верхніх дихальних шляхів [12].
Магній стабілізує мембрани мастоцитів, локалізованих у підслизовій оболонці дихальних шляхів і альвеолярних перегородках, запобігаючи тим самим їхній дегрануляції та вивільненню численних прозапальних медіаторів; регулює активність нейтрофілів і макрофагів, пригнічує окислювальний стрес [13].
Окрім потенціювання та гармонізації імунної функції, рівень магнію може впливати на початкову фазу інфекції SARS-CoV‑2. Відомо, що білок вірусного шипа (S) зв’язується з рецептором ангіотензинперетворювального ферменту‑2 (АПФ‑2), який експресується в багатьох тканинах. Щоб відбулося злиття між вірусною та клітинною мембранами, білок S має бути протеолітично розщеплений протеазами клітини-хазяїна – здебільшого трансмембранною серин-протеазою‑2 (TMPRSS2) і конвертазою фурином [14]. Магній відіграє певну роль у пригніченні активності цих ферментів. Попередні результати демонструють, що додаткове застосування магнію посилює метилювання промотора TMPRSS2; саме це перешкоджає транскрипції та знижує експресію цього ферменту [15]. Крім того, завдяки своїй антагоністичній дії щодо кальцію магній може перешкоджати активізації кальційзалежного фурину [16]. Отже, дефіцит магнію може сприяти посиленню інвазивності вірусу SARS-CoV‑2.
Слід зазначити, що низький рівень магнію також асоціюється зі збільшенням концентрації медіаторів запалення, сприяючи розвитку т. зв. цитокінового шторму, який лежить в основі патогенезу складних клінічних проявів SARS-CoV‑2 [17, 18]. У разі додаткового введення магнію реалізується ефект блокування кальцієвих каналів. Це перешкоджає притоку кальцію до імунокомпетентних клітин, унаслідок чого обмежуються активація ядерного фактора NF‑κB і продукція прозапальних цитокінів, зокрема IL‑6, який вважається ключовим ініціатором цитокінового шторму [19-21]. Систематичні огляди рандомізованих контрольованих досліджень продемонстрували зворотний зв’язок між прийомом магнію, рівнями С‑реактивного білка та вираженістю проявів системного запалення [22, 23]. На моделі гострого ураження легень уведення магнію зменшувало навколобронхіальну інфільтрацію клітинами запалення, альвеолярну септальну інфільтрацію й альвеолярний набряк [24].
Відомо, що низький уміст магнію спричиняє посилене вивільнення β-тромбоглобуліну та тромбоксанів, що сприяє агрегації тромбоцитів, розвитку тромбоемболічних ускладнень [25]. Ушкодження ендотелію, стан гіперкоагуляції є ключовими компонентами тріади Вірхова та пояснюють високу частоту тромбоемболічних подій у пацієнтів з COVID‑19.
Крім того, інші симптоми, про які повідомляють пацієнти з COVID‑19, як-от астенія, міалгії, тривога, депресія, безсоння, можуть бути пов’язані з дефіцитом магнію [26].
Завдяки своїм судинорозширювальним, протизапальним і антитромботичним ефектам магній здатен зменшувати респіраторні симптоми та покращити функцію легень у пацієнтів з COVID‑19. Усі ці ефекти можуть сприяти зменшенню невідповідності вентиляції та перфузії, яка є однією з найважливіших причин гіпоксемії у пацієнтів з COVID‑19, а також покращенню оксигенації у цих хворих [27].
Нещодавно проведене дослідження продемонструвало, що низький уміст магнію знижує функцію діафрагми в експериментальній моделі сепсису [28]. Отримані результати свідчать про те, що дефіцит магнію може зумовити необхідність проведення штучної вентиляції легень через порушення скоротливості діафрагми.
Також слід згадати, що дефіцит магнію впливає на мікробіоту кишечнику, мікробіоту дихальних шляхів та імунну відповідь [29]. Наразі продовжується вивчення зв’язку між дисбактеріозом і тяжкістю перебігу COVID‑19 [30].
Оптимальний статус магнію необхідний для синтезу, транспортування та активації вітаміну D, який є імуномодулювальним гормоном [31]. Дефіцит вітаміну D пов’язують з різними інфекційними захворюваннями, в т. ч. з інфекціями верхніх дихальних шляхів [32]. Сьогодні опубліковано чимало ретроспективних досліджень, котрі свідчать про значну поширеність дефіциту вітаміну D серед пацієнтів із COVID-19 [33]. Дослідження у 20 європейських країнах підтвердило зв’язок дефіциту вітаміну D з показниками смертності від коронавірусної інфекції [34]. Призначення вітаміну D уже тривалий час застосовується в клінічній практиці для профілактики/лікування COVID-19. У пацієнтів із недостатністю магнію сироватковий рівень 1,25(OH)D часто залишається низьким, незважаючи на прийом препаратів вітаміну D [33].
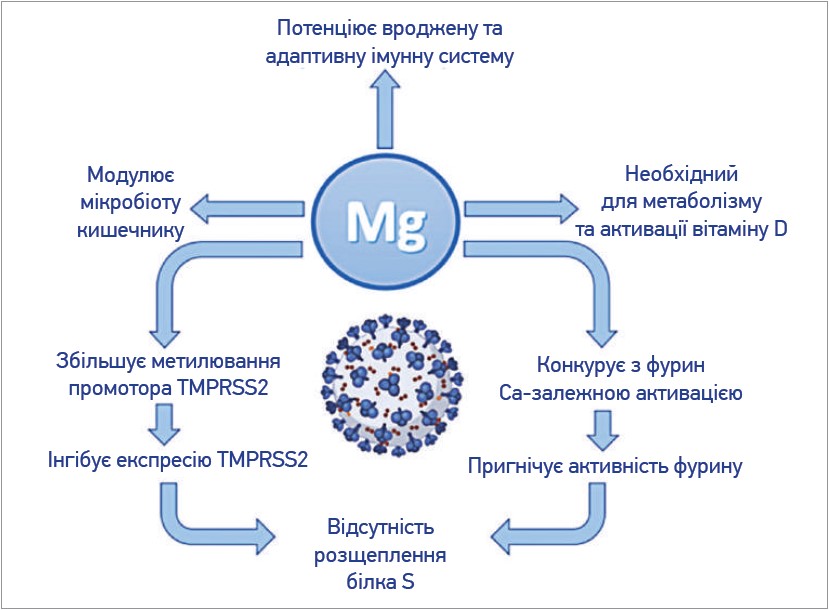
Можливі механізми впливу магнію на патогенез COVID-19 представлено на рисунку.
Рис. Можливі механізми впливу магнію на патогенез COVID-19
Магній при COVID‑19: клінічні дослідження
Ключова роль магнію в підтримці належної імунної, судинної, легеневої функції теоретично підтверджує гіпотезу про те, що статус магнію може впливати на сприйнятливість до SARS-CoV‑2 та відповідь на інфекцію. В декількох останніх дослідженнях проаналізували рівень магнію в пацієнтів з COVID‑19 і оцінили їхній зв’язок із результатами захворювання. Zeng і співавт. вивчили наслідки лікування 300 пацієнтів з COVID‑19 та виявили, що складні випадки захворювання (насичення киснем ≤93% у спокої або необхідність лікування у відділенні інтенсивної терапії) демонструють значно нижчі рівні магнію, ніж випадки легкого та помірного ступенів. Така різниця виявлялася з початку розвитку COVID‑19 та зберігалася постійно протягом клінічного перебігу захворювання [34].
Крім того, низький рівень магнію виявився предиктором ризику смерті пацієнтів з COVID‑19. Ретроспективне дослідження продемонструвало, що у 63 осіб із летальним наслідком рівень магнію під час госпіталізації був значно нижчим, ніж у 396 тих, хто вижив (1,61±0,19 проти 1,81±0,23 мг/дл відповідно) [35].
Частим спотворювальним фактором у таких дослідженнях є те, що люди із супутніми захворюваннями, як-от гіпертонія, серцево-судинні захворювання, діабет і ожиріння, які більш схильні до розвитку тяжкої форми COVID‑19, часто мають низький рівень магнію. Для виключення цього впливу Sarvazad і співавт. провели когортне дослідження, проаналізувавши електролітний статус у пацієнтів із COVID‑19 під час госпіталізації. Хворих із раком, діабетом, гіпертонією, серцево-судинними або ж з нирковими захворюваннями в анамнезі не залучали до дослідження. У 32% госпіталізованих без супутнього основного захворювання була виявлена гіпомагніємія (1,26% – 1,7 мг/дл), у 6% – тяжка гіпомагніємія (<1,25 мг/дл), у 14% – гіпермагніємія (>2,6 мг/дл). Виявилося, що пацієнти з гіпомагніємією частіше потребували лікування в умовах відділення інтенсивної терапії [36].
На жаль, наразі недостатньо випробувань, які б вивчали вплив додаткового призначення магнію на клінічний перебіг COVID‑19. Сьогодні відомо лише про 1 опубліковане інтервенційне дослідження, яке передбачало додавання магнію пацієнтам із COVID‑19. У когорті з 43 пацієнтів (віком >50 років) 17 хворих отримували комбінацію вітаміну D, магнію та вітаміну B12 із самого початку госпіталізації. Група втручання продемонструвала значне зниження частки пацієнтів із клінічним погіршенням. Захисний ефект добавки зберігався після поправки на вік і гіпертензію [37].
Гіпокаліємія в пацієнтів із COVID‑19
Вірус SARS-CoV‑2 інфікує клітини через взаємодію з рецептором ACE2, який знаходиться здебільшого на поверхні серця, печінки, нирок і легень. Зв’язування ACE2 вірусом посилює деградацію рецептора, що зменшує інгібування класичної осі ренін-ангіотензин-альдостеронової системи та спричиняє підвищення рівня альдостерону. Останній сприяє виведенню калію із сечею [38].
До інших можливих причин розвитку гіпокаліємії у пацієнтів із COVID-19 слід віднести шлунково-кишкові втрати, ураження тубулярного апарату нирок, зокрема через прямий цитотоксичний ефект вірусу SARS-CoV-2, прийом лікарських засобів [39, 40].
Гіпокаліємія є потенційно небезпечним розладом, який може підвищувати ризик порушень серцевого ритму, а також зумовлювати дихальну дисфункцію [6]. Також відомо, що гіпокаліємія асоціюється з тяжчим перебігом COVID‑19. Зокрема, в одному з досліджень виявлено, що гіпокаліємія під час госпіталізації була пов’язана зі зростанням частоти проведення інвазивної механічної вентиляції легень [41]. За даними інших дослідників, низький рівень калію спостерігається у 85% пацієнтів із тяжкою коронавірусною інфекцією [42].
Ретроспективне обсерваційне дослідження, проведене за участю 320 некритично хворих пацієнтів, продемонструвало, що особи з гіпокаліємією потребували значно тривалішої госпіталізації [43].
Отже, раннє виявлення та лікування порушень гіпокаліємії є життєво важливим і може покращити результат лікування пацієнтів із COVID‑19.
Слід зазначити, що гіпокаліємія досить складно піддається корекції на тлі супутньої гіпомагніємії, тому рекомендується призначати препарати калію та магнію одночасно [25].
ДОВІДКА «ЗУ»
Добре відомим на українському ринку препаратом, який поєднує у своєму складі калієву та магнієву солі аспарагінової кислоти, є Панангін Форте.
Цей препарат характеризується такими властивостями:
• швидко відновлює рівні калію та магнію в організмі;
• не має кумулятивного ефекту;
• покращує метаболічні процеси, зокрема в міокарді;
• чинить антиаритмічну дію;
• знижує ризик розвитку тромботичних ускладнень;
• може застосовуватися із профілактичною метою та у відновлювальному періоді.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 10 (527), 2022 р.