9 листопада, 2022
Місцево-рецидивуючий нерезектабельний або метастатичний потрійний негативний рак грудної залози: ефективність пембролізумабу у комбінації з хіміотерапією у раніше не лікованих пацієнток
За оновленими результатами рандомізованого плацебо-контрольованого дослідження III фази KEYNOTE-355
Потрійний негативний рак грудної залози (РГЗ) – найагресивніший підтип РГЗ, який характеризується відсутністю експресії рецепторів до естрогену (ER-), прогестерону (РR-) та ампліфікації людського епідермального фактора росту (HER2-), що обмежує можливість застосування ендокринних і таргетних анти-HER2 препаратів у цих хворих. Стандартом лікування при ньому вважається цитотоксична терапія. У проміжному аналізі даних рандомізованого плацебо-контрольованого дослідження III фази KEYNOTE-355 додавання пембролізумабу до хіміотерапії асоціювалося зі збільшенням частоти загальної виживаності порівняно з застосуванням лише хіміотерапії у пацієнток із метастатичним потрійним негативним РГЗ.
Монотерапія анти-PD-1 моноклональним антитілом пембролізумабом забезпечувала тривалу протипухлинну активність у першій лінії лікування потрійного негативного PD-L1 позитивного метастатичного РГЗ. При цьому ефективність пембролізумабу зростала у разі підвищення експресії PD-L1. Результати проміжного аналізу даних, отриманих у дослідженні III фази KEYNOTE-355, свідчать, що поєднання пембролізумабу з ХТ у першій лінії терапії демонструє значну клінічну перевагу порівняно з лише ХТ у пацієнток із метастатичним потрійним негативним РГЗ та експресією PD-L1 (комбінований позитивний бал – CPS ≥10). Нижче представлені результати остаточного аналізу даних дослідження KEYNOTE-355 із оцінкою загальної виживаності (ЗВ) пацієнток, які отримували пембролізумаб (Кітруда®, компанія «МСД») + ХТ проти плацебо + ХТ.
Методи
У рамках цього етапу дослідження 847 пацієнток були рандомізовані у співвідношенні 2:1 у групи пембролізумаб (200 мг через кожні 3 тижні) + ХТ (однин із трьох варіантів: наб-паклітаксел 100 мг/м2 площі поверхні тіла у 1-й, 8, 15-й дні 28-денного циклу; паклітаксел 90 мг/м2 у 1-й, 8, 15-й дні 28-денного циклу; гемцитабін 1000 мг/м2 + карбоплатин у 1-й та 8-й дні 21-денного циклу) та плацебо + ХТ. Факторами стратифікації були тип ХТ під час дослідження (таксан або гемцитабін-карбоплатин), початкова експресія PD-L1 (CPS ≥1 чи CPS <1) та наявність або відсутність попереднього лікування хіміопрепаратом того самого класу в неоад’ювантному чи ад’ювантному режимі.
Первинною кінцевою точкою була виживаність без прогресування (ВБП) за RECIST 1.1 та ЗВ у пацієнток із CPS ≥10, ≥1 та ІТТ-популяції. Вторинними кінцевими точками були частота об’єктивної відповіді, тривалість відповіді та рівень контролю захворювання (повна відповідь + часткова відповідь + стабілізація впродовж ≥24 тижнів) за RECIST 1.1, а також оцінка профілю безпеки. Безпеку аналізували серед усіх пацієнтів, які отримали щонайменше одну дозу пембролізумабу, плацебо або ХТ. Побічні явища (ПЯ) оцінювали впродовж усього дослідження та протягом 30 днів після припинення лікування (90 днів у разі тяжких ПЯ).
Результати
847 пацієнток із 209 медичних центрів 29 країн із січня 2017-го по червень 2018 року були рандомізовані у групи лікування пембролізумаб + ХТ (n=566) або плацебо + ХТ (n=281). Початкові характеристики учасниць були зіставними в обох групах, а у підгрупах CPS ≥1 (636 пацієнток; 75,1%) та CPS ≥10 (323 пацієнтки; 38,1%) – подібними до таких у ІТТ-популяції. Медіана спостереження у групі пембролізумаб + ХТ дорівнювала 26,4 міс, у групі плацебо + ХТ – 23,1 міс.
У підгрупі CPS ≥10 медіана ЗВ становила 23,0 міс (95% довірчий інтервал – ДІ – 19,0-26,3) у групі пембролізумаб + ХТ та 16,1 міс (95% ДІ 12,6-18,8) у групі плацебо + ХТ (відношення ризиків – ВР – прогресування або смерті 0,73; 95% ДІ 0,55-0,95; р=0,0185; рис. А). Вісімнадцятимісячна ЗВ у групі пембролізумаб + ХТ дорівнювала 58,3% (95% ДІ 51,4-64,5), у групі плацебо + ХТ – 44,7% (95% ДІ 34,9-53,9).
У підгрупі CPS ≥1 медіана ЗВ становила 17,6 міс (95% ДІ 15,5-19,5) у групі пембролізумаб + ХТ та 16 міс (95% ДІ 12,8-17,4) у групі плацебо + ХТ (ВР 0,86; 95% ДІ 0,72-1,04; р=0,1125; рис. Б). Вісімнадцятимісячна ЗВ у групі пембролізумаб + ХТ сягала 48,4% (95% ДІ 34,5 – 53,0), у групі плацебо + ХТ – 41,4% (95% ДІ 34,7-48,0).
В ІТТ-популяції медіана ЗВ становила 17,2 міс (95% ДІ 15,3-19,0) у групі пембролізумаб + ХТ та 15,5 міс (95% ДІ 13,9-17,2) у групі плацебо + ХТ (ВР 0,89; 95% ДІ 0,76-1,05; рис. В). Вісімнадцятимісячна ЗВ у групі пембролізумаб + ХТ становила 47,8% (95% ДІ 43,6-51,9) проти 41,8% (95% ДІ 36,0-47,5) у групі плацебо + ХТ.
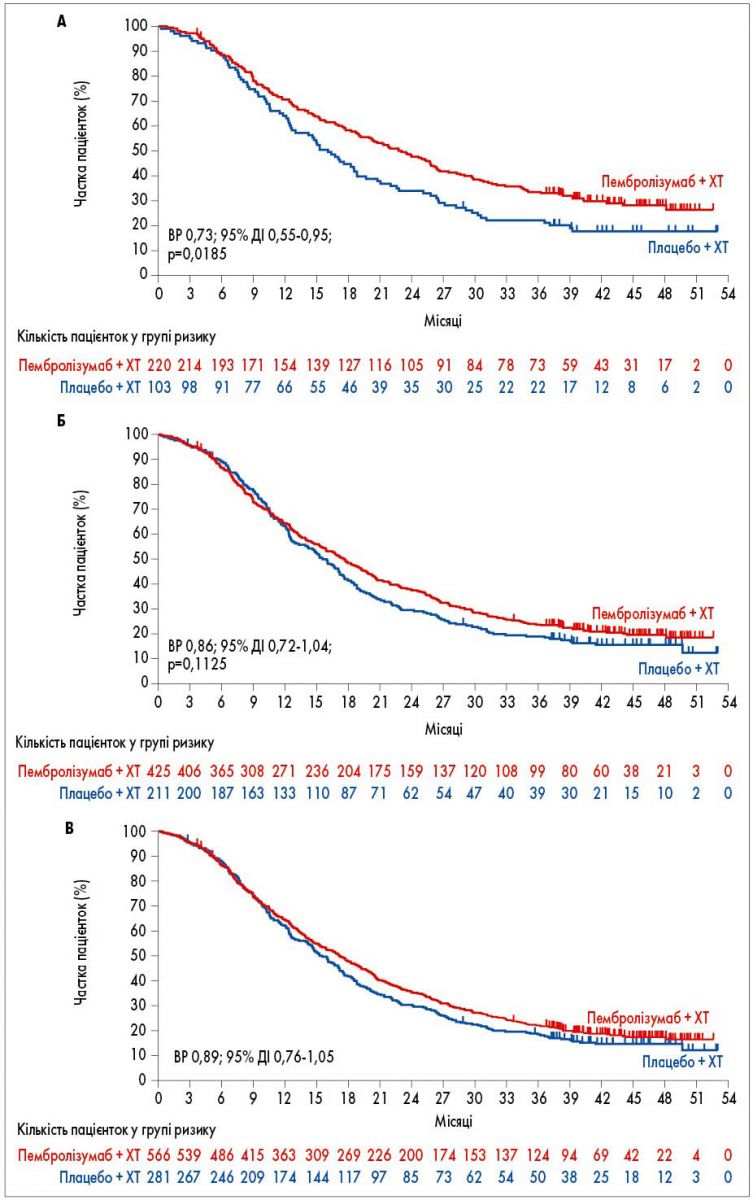 Рис. ЗВ, оцінена методом Каплана – Меєра: А – пацієнтки з CPS ≥10; Б – пацієнтки з CPS ≥1; В – ІТТ-популяція
Рис. ЗВ, оцінена методом Каплана – Меєра: А – пацієнтки з CPS ≥10; Б – пацієнтки з CPS ≥1; В – ІТТ-популяція
Ефективність пембролізумабу залежала від рівня експресії PD-L1: кращі результати лікування демонстрували пацієнтки із вищим рівнем PD-L1. При цьому ЗВ була зіставною у пацієнток із CPS ≥10 та CPS ≥20.
При оцінюванні додаткових порогових значень CPS було встановлено, що ЗВ у групах пембролізумаб + ХТ та плацебо + ХТ є зіставною у пацієнток із CPS ≤1 (ВР 0,97; 95% ДІ 0,72-1,32) та CPS 1-9 (ВР 1,09; 95% ДІ 0,85-1,40). Ефективність додавання пембролізумабу до ХТ була однаковою у пацієнток із CPS 10-19 (ВР 0,71; 95% ДІ 0,46-1,09) та CPS ≥20 (ВР 0,72; 95% ДІ 0,51-1,01).
Результати оцінювання медіани ВБП і частоти об’єктивної відповіді були зіставні з отриманими при другому проміжному аналізі (J. Cortes et al., 2020) та залишалися кращими за додавання пембролізумабу.
Медіана ВБП у підгрупі CPS ≥10 становила 9,7 міс у групі пембролізумаб + ХТ та 5,6 міс у групі плацебо + ХТ (ВР 0,66; 95% ДІ 0,50-0,88), у підгрупі CPS ≥1 – 7,6 та 5,6 міс відповідно (ВР 0,75; 95% ДІ 0,62-0,91), в ІТТ-популяції – 7,5 та 5,6 міс відповідно (ВР 0,82; 95% ДІ 0,69-0,97).
Об’єктивна відповідь у підгрупі CPS ≥10 була досягнута у 116 (52,7%) із 220 пацієнток у групі пембролізумаб + ХТ та у 42 (40,8%) зі 103 учасниць у групі плацебо + ХТ, у підгрупі CPS ≥1 – у 191 (44,9%) із 425 пацієнток та у 82 (38,9%) із 211 хворих відповідно, в ІТТ-популяції – у 231 (40,8%) з 566 пацієнток та у 104 (37,0%) із 281 пацієнтки відповідно.
Додавання пембролізумабу до ХТ сприяло досягненню довшої відповіді на лікування. Зокрема, у підгрупі CPS ≥10 тривалість відповіді склала 12,8 міс у групі пембролізумаб + ХТ проти 7,3 міс у групі плацебо + ХТ.
ПЯ будь-якого ступеня тяжкості, які, на думку авторів дослідження, були пов’язані із призначеним лікуванням, виникли у 96,3% із 562 учасниць групи пембролізумаб + ХТ та у 95,0% з 281 пацієнтки групи плацебо + ХТ. Найпоширенішими ПЯ були анемія (49,1 та 45,9% відповідно), нейтропенія (41,1 та 38,1% відповідно), нудота (39,3 та 41,3% відповідно). ПЯ 3 ступеня тяжкості та вище мали 68,1% пацієнток групи пембролізумаб + ХТ та 66,9% – плацебо + ХТ.
Імунно-опосередковані ПЯ розвинулися у 26,5% пацієнток групи пембролізумаб + ХТ та у 6,4% – плацебо + ХТ. Серед них ПЯ 3-4 ступеня тяжкості були виявлені у 5,3% хворих, які отримували пембролізумаб + ХТ, та не спостерігались у групі плацебо + ХТ. Імунно-опосередковані ПЯ не були причиною смерті жодної пацієнтки у дослідженні. Найпоширенішими імунно-опосередкованими ПЯ були гіпотиреоїдизм, що зустрічався у 15,8% пацієнток групи пембролізумаб + ХТ та у 3,2% – плацебо + ХТ, та гіпертиреоїдизм, частота якого склала 4,3 та 1,1% у групах пембролізумаб + ХТ та плацебо + ХТ відповідно.
Висновки
Результати остаточного аналізу даних дослідження KEYNOTE-355 продемонстрували, що поєднане застосування пембролізумабу з ХТ у першій лінії терапії демонструє значне збільшення ЗВ порівняно з лише ХТ у пацієнток із метастатичним потрійним негативним РГЗ та експресією PD-L1 (CPS ≥10). Профіль безпеки пембролізумабу у поєднанні з ХТ був зіставним із таким у попередніх проміжних аналізах, що свідчить про відсутність кумулятивної токсичності. Безпека досліджуваних режимів відповідала відомим профілям кожного з режимів, і нових несприятливих подій не спостерігалося. Отже, отримані дані свідчать на користь додавання пембролізумабу (Кітруда®, компанія «МСД») до стандартних схем ХТ у першій лінії у пацієнток із місцево-рецидивуючим нерезектабельним або метастатичним потрійним негативним РГЗ.
За матеріалами Cortes J., Rugo H.S., Cescon D.W. et al. Pembrolizumab plus Chemotherapy in Advanced Triple-Negative Breast Cancer. N Engl J Med. 2022; 387: 217-26.
Doi: 10.1056/NEJMoa2202809.
Підготувала Ольга Гуйванюк
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (77) 2022 р.



