10 листопада, 2022
Набута гемофілія типу А: особливості діагностики та лікування
Набута гемофілія типу А (НГА) – це рідкісне порушення гемостазу, що характеризується появою інгібіторів до факторів згортання крові (найчастіше до фактора VIII ). Якщо раніше поширеність НГА становила 1,4 на 1 млн населення на рік (P.W. Collins et al., 2007), то вже у 2017 році вона сягала 6 на 1 млн населення на рік (S. Wahler, A. Tiede, 2017). Однією з причин зростання кількості виявлених випадків НГА може бути підвищення обізнаності клініцистів щодо цієї патології.
НГА може виникати із однаковою частотою у чоловіків і жінок будь-якого віку, проте частіше спостерігається в осіб похилого віку. Так, середній вік на момент встановлення діагнозу становить близько 70 років. При цьому приблизно у 30-50% випадків НГА виникає на тлі аутоімунних розладів або злоякісних новоутворень, а ще у близько 5% пов’язана з вагітністю та зазвичай розвивається після пологів.
Актуальною залишається проблема належної діагностики НГА. Зокрема, за даними Європейського реєстру набутої гемофілії (EACH2), у 10% пацієнтів діагноз було встановлено пізніше ніж через 1 міс після перших проявів хвороби, що, відповідно, збільшувало інтервал між початком кровотечі та стартом гемостатичної терапії й зумовлювало недостатню відповідь на призначене лікування (P. Knoebl et al., 2012; F. Baudo et al., 2012).
Патофізіологія
Причиною розвитку НГА є вироблення нейтралізуючих аутоантитіл проти фактора VIII згортання крові (FVIII). Залишкова активність FVIII становить <1 МО/дл у 50% випадків (<5 МО/дл у 75% та <40 МО/дл у 100%; A. Tiede et al., 2015).
Антитіла при НГА переважно належать до підкласу IgG4, що характерно для понад 90% пацієнтів. Проте можуть також зустрічатися й інші підкласи IgG, IgA та IgМ у різних комбінаціях (A. Tiede et al., 2016). Диференційований вплив окремих ізотипів і підкласів на інгібування FVIII залишається не вивченим. Відомо, що відповідь інгібіторних антитіл проти FVIII є поліклональною та відбувається із залученням різних доменів FVIII (H. Turkantoz et al., 2020). Роль коморбідності у патофізіології анти-FVIII імунної відповіді також остаточно не зрозуміла.
Разючою є відмінність фенотипів кровотеч при НГА та вродженій гемофілії А чи інгібіторній формі гемофілії. Зокрема, типовими для НГА є підшкірні та глибокі м’язові кровотечі, тоді як суглобові кровотечі розвиваються рідко. Підшкірні кровотечі виникають приблизно у 50% пацієнтів з НГА (рис. 1; P.W. Collins et al., 2007; P. Knoebl et al., 2012).
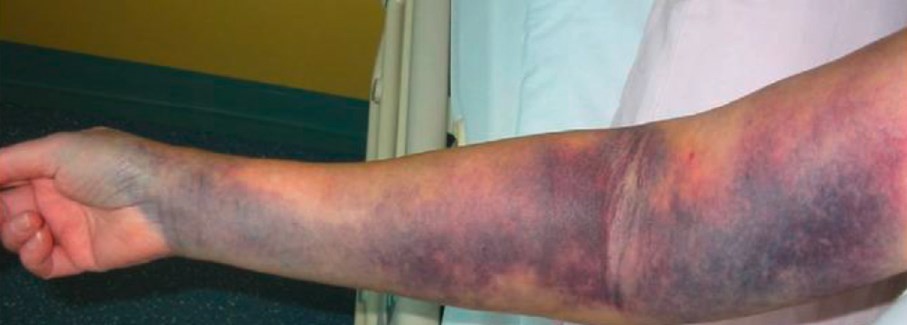 Рис. 1. Підшкірна гематома після венепункції у хворого на НГА
Рис. 1. Підшкірна гематома після венепункції у хворого на НГА
Діагностика
Відмітною ознакою НГА є ізольоване подовження активованого часткового протромбінового часу (АЧТЧ) на тлі незміненого протромбінового часу у пацієнта із кровотечею. І хоча подовження АЧТЧ може виникати з багатьох причин, воно ніколи не має залишатися без пояснення, особливо у пацієнтів із кровотечею або перед проведенням втручань, що характеризуються високим ризиком кровотечі.
Наступним кроком, який дозволить підтвердити, що циркулюючий антикоагулянт спрямований саме проти FVIII, є виявлення зниженої активності FVIII та визначення титру інгібітору FVIII методом Бетезда (БО/мл; рис. 2; A. Tiede et al., 2014). У рутинній практиці з метою швидкого встановлення діагнозу можна використовувати метод змішування плазми, або так званий мікс-тест. Суть цього дослідження полягає у змішуванні еталонної плазми із плазмою крові пацієнта та подальшим повторним оцінюванням АЧТЧ. У разі відсутності в крові хворого інгібітору відбувається корекція АЧТЧ до нормального. Якщо ж інгібітор наявний, то корекції АЧТЧ не відбувається. АЧТЧ рекомендовано досліджувати як відразу (пролонгація в цьому випадку вказує на застосування гепарину або наявність вовчакового антикоагулянту), так і після інкубації при 37 °C протягом 2 год (прогресуюче подовження АЧТЧ свідчить про наявність інгібітору; S. Kitchen et al., 2020).
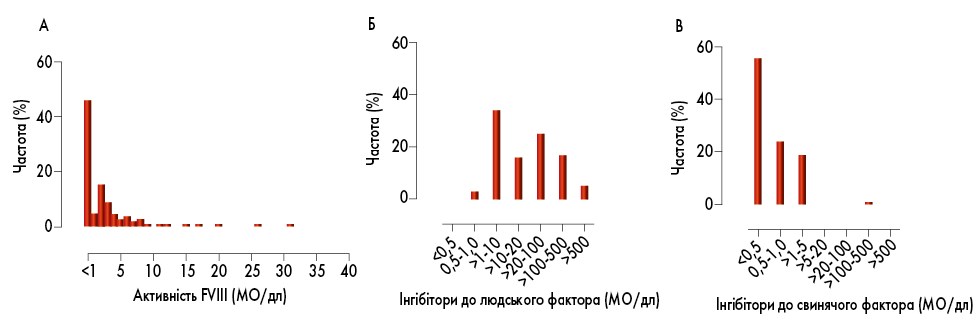 Рис. 2. Лабораторні дані при НГА: частота виявлення активності FVIII (A), титру інгібіторів до людського фактора Бетезда (Б) й інгібіторів до свинячого фактора (сусоктоког альфа), титр перехресної реакції (В)
Рис. 2. Лабораторні дані при НГА: частота виявлення активності FVIII (A), титру інгібіторів до людського фактора Бетезда (Б) й інгібіторів до свинячого фактора (сусоктоког альфа), титр перехресної реакції (В)
Причиною ізольованого подовження АЧТЧ можуть бути дефіцит FVIII (НГА, вроджена гемофілія, інгібіторна форма гемофілії, хвороба або набутий синдром Віллебранда), дефіцит фактора ІХ згортання крові (гемофілія В), дефіцит фактора ХІ (гемофілія С), антифосфоліпідний синдром, дефіцит фактора XII згортання крові, дефіцит прекалікреїну та високомолекулярного кініногену. Окрім цього, подовження АЧТЧ може виникати на тлі застосування гепарину та дабігатрану.
 Іноді можливі труднощі у диференціюванні НГА від антифосфоліпідного синдрому. НГА в такому випадку можна виключити за допомогою аналізів хромогенного субстрату (E. de Maistre et al., 1998), які зазвичай нечутливі до вовчакового антикоагулянту, й імуноаналізу (S. Werwitzke et al., 2016) для виявлення антитіл до FVIII (табл.). Однак варто зауважити, що НГA та антифосфоліпідний синдром є аутоімунними захворюваннями, які можуть відмічатися в одного пацієнта (A. Tripodi et al., 2005).
Іноді можливі труднощі у диференціюванні НГА від антифосфоліпідного синдрому. НГА в такому випадку можна виключити за допомогою аналізів хромогенного субстрату (E. de Maistre et al., 1998), які зазвичай нечутливі до вовчакового антикоагулянту, й імуноаналізу (S. Werwitzke et al., 2016) для виявлення антитіл до FVIII (табл.). Однак варто зауважити, що НГA та антифосфоліпідний синдром є аутоімунними захворюваннями, які можуть відмічатися в одного пацієнта (A. Tripodi et al., 2005).
Що стосується набутого синдрому Віллебранда, то результати мікс-тесту та аналізу Бетезда у цьому випадку будуть негативними, а дефіцит FVIII виявляється лише за одночасного зниження рівня фактора Віллебранда (A. Tiede et al., 2008).
Лікування
Гемостатична терапія
Лікування пацієнтів із НГA здійснюють у спеціалізованих центрах. Якщо терміново направити пацієнта у такий центр неможливо, слід звернутися за консультацією до фахівця.
Хірургічні втручання можуть становити загрозу життю пацієнтів з НГА та мають проводитися тільки після досягнення стабільного гемостазу.
Вибір тактики ведення й оцінка ефективності лікування кровотечі базуються переважно на клінічній оцінці. Для лікування клінічно значущих кровотеч рекомендовані обхідні агенти, такі як рекомбінантний фактор згортання крові VIIa (rFVIIa, ептаког альфа активований), концентрат активованого протромбінового комплексу та рекомбінантний свинячий фактор VIII (рсFVIII, сусоктоког альфа). Концентрати людського FVIII рекомендовано застосовувати лише в тому випадку, коли інші варіанти лікування недоступні. Транексамову кислоту можна використовувати як допоміжний засіб при шкірних кровотечах та кровотечах зі слизових оболонок або як монотерапію при незначних кровотечах.
Під час терапії rpFVIII рекомендовано здійснювати ретельний моніторинг активності FVIII, зокрема, за допомогою одноетапного аналізу, що базується на визначенні АЧТЧ. Такий моніторинг дозволить уникнути передозування та виявити пацієнтів з перехресною реактивністю. Варто зауважити, що інгібітори анти-rpFVIII перехресної реакції виявляють у 44% хворих на НГА. При цьому пацієнти з перехресною реактивністю потребують вищих доз rpFVIII ніж ті, у яких перехресної реактивності немає (E. Fosbury et al., 2017; A. Tiede et al., 2018).
Імуносупресивна терапія
Імуносупресивну терапію призначають з метою елімінації антитіл до FVIII та індукції ремісії НГА. Рекомендовані схеми включають застосування кортикостероїдів, зокрема преднізолону або преднізону у дозі 1 мг/кг маси тіла на добу (R. Kruse-Jarres et al., 2017), ритуксимабу у дозі 375 мг/м2 площі поверхні тіла на тиждень протягом максимум 4 циклів та/або циклофосфаміду у дозі 1,5-2,0 мг/кг на добу.
Особливої обережності слід дотримуватися у разі призначення імуносупресивного лікування ослабленим хворим та особам літнього віку, оскільки відомо, що ризик смерті, пов’язаної з розвитком інфекції на тлі імуносупресивної терапії, перевищує такий фатальної кровотечі у цих групах пацієнтів (A. Tiede et al., 2015; A. Tiede et al., 2016).
Отже, правильна інтерпретація симптомів і лабораторних даних відіграє ключову роль у діагностиці та призначенні належного лікування хворим на НГА. Враховуючи стрімкий розвиток галузі, важливе значення має тісна співпраця між усіма фахівцями, які займаються лікуванням пацієнтів із симптомами кровотечі, у тому числі залучення гематологів.
Реферативний огляд A. Tiede, B. Zieger, T. Lisman (2022). Acquired bleeding disorders. https://onlinelibrary.wiley.com/doi/full/10.1111/hae.14548.
Переклала Ольга Гуйванюк
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (77) 2022 р



