13 грудня, 2022
Карбоцистеїн у лікуванні розладів дихальних шляхів: більше ніж муколітик
Мукоактивні препарати широко використовуються в клінічній практиці вже протягом тривалого часу, а їхня ефективність всебічно вивчається в наукових дослідженнях.
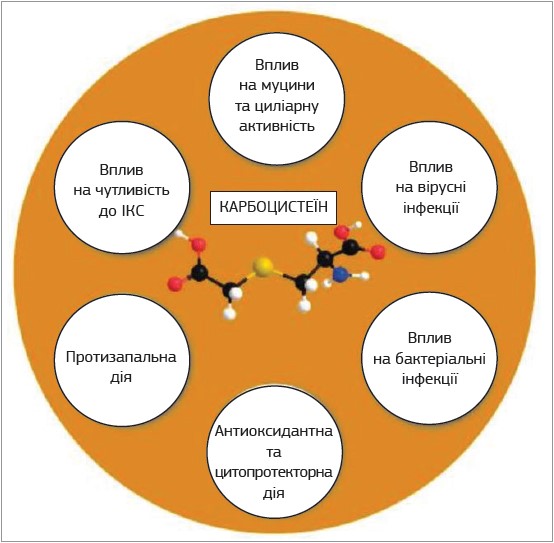
Завдяки багатофакторному механізму дії ці засоби мають широкий терапевтичний потенціал і розглядаються в контексті різних патологій органів дихання. Ефективність та безпека застосування мукоактивних препаратів значною мірою залежать від правильно підібраного засобу із врахуванням індивідуальних особливостей пацієнта та специфіки захворювання. Особливе місце серед мукоактивних препаратів посідає S-карбоксиметил-L-цистеїн (карбоцистеїн), який виявляє мукорегуляторні, муколітичні, протизапальні, антиоксидантні, цитопротекторні та антиінфекційні ефекти (рис. 1).
Рис. 1. Ефекти карбоцистеїну
Карбоцистеїн (2R‑2-аміно‑3-((карбоксиметил)сульфаніл)пропанова кислота) – біологічно активна двохосновна амінокислота; його молекула характеризується наявністю зв’язаної сульфгідрильної групи. Мукорегуляторна дія карбоцистеїну забезпечується його здатністю відновлювати співвідношення сіаломуцинів і фукомуцинів підвищенням концентрації перших і зниженням такої других, а також посилювати транспорт хлоридів до епітелію бронхів.
Вплив карбоцистеїну на муцини та циліарну активність
Полімерні муцини MUC5AC і MUC5B є невід’ємними компонентами слизу дихальних шляхів. Білок MUC5AC міститься в келихоподібних клітинах поверхневого епітелію та в кінцевих секреторних протоках підслизових залоз, а його секреція сприяє скороченню гладкої мускулатури дихальних шляхів і є необхідною складовою розвитку гіперреактивності респіраторного тракту. Крім того, підвищення експресії MUC5AC спостерігається за гострого ураження легень, а також зумовлює посилене надходження нейтрофілів, наростання запалення та гіперсекрецію слизу. Білок MUC5B локалізований у слизових клітинах підслизових залоз; меншою мірою – в секреторних клітинах поверхневого епітелію дихальних шляхів трахеї та бронхів. Він відіграє ключову роль у забезпеченні мукоциліарного кліренсу та захисту дихальних шляхів.
Карбоцистеїн активує рух війок в епітеліальних клітинах респіраторного тракту, покращуючи в такий спосіб мукоциліарний транспорт і сприяючи видаленню шкідливих часток, вірусів, бактерій з поверхні дихальних шляхів.
Карбоцистеїн може запобігати посиленій інфільтрації клітин запалення, зменшувати кількість келихоподібних клітин і рівень секреції білка-муцина MUC5AC, що було продемонстровано під час моделювання ураження дихальних шляхів, індукованого експозицією діоксиду сірки (SO2), в експерименті на щурах. Крім того, було встановлено, що карбоцистеїн має здатність регулювати активність ферментів глікозидази та глікозилтрансферази, пригнічувати надмірну експресію мРНК і білка MUC5AC в епітелії дихальних шляхів щурів, які зазнали впливу SO2. Така регуляторна функція карбоцистеїну зберігається і в експериментальних моделях, у яких порушення в’язкості мокротиння було спричинене фактором некрозу пухлини.
Вплив карбоцистеїну на вірусні інфекції
Карбоцистеїн знижує експресію розчинних форм молекул міжклітинної адгезії (ICAM‑1) у легенях і в такий спосіб пригнічує розвиток риновірусної інфекції, а також знижує титри та кількість РНК риновірусу. Крім того, він нормалізує рівні цитокінів (наприклад, інтерлейкіну (IL)-6, IL‑8, IL‑1), що вивільняються в епітеліальних клітинах трахеї, при інфікуванні респіраторно-синцитіальним вірусом. У дослідженні Yamaya та співавт. було продемонстровано здатність карбоцистеїну знижувати титри та пригнічувати реплікацію РНК вірусу грипу А в епітеліальних клітинах людської трахеї, а також зменшувати рівень IL‑6 й експресію внутрішньоклітинного сигнального білка NF‑κB у ядерних екстрактах клітин. Карбоцистеїн також зменшував експресію сіалової кислоти з a2,6-зв’язком (SAa2,6Gal) – рецептором вірусу грипу людини в клітинах.
З огляду на здатність карбоцистеїну впливати на адгезію і поширення вірусів перспективним є його застосування в схемах комплексної терапії вірусних інфекцій, у т. ч. у пацієнтів із хронічними захворюваннями органів дихання.
Завдяки наявності в молекулах N‑ацетилцистеїну, карбоцистеїну й ердостеїну тіольної групи вони можуть блокувати рецептори ангіотензинперетворювального ферменту‑2, забезпечуючи захист від проникнення вірусу SARS-CoV‑2 до клітини, а також мають широкий спектр антиоксидантних і протизапальних властивостей, які дозволяють зменшити прозапальну відповідь та тяжкість ураження легень, що виникає при інфекції SARS-CoV‑2. Варто зауважити таке: хоча сьогодні надходять нові дані щодо протекторних властивостей окремих тіолів при COVID‑19, для їхнього підтвердження необхідними є рандомізовані контрольовані дослідження за участю значної кількості пацієнтів.
Вплив карбоцистеїну на бактеріальні інфекції
Адгезія мікроорганізмів до епітеліальних клітин глотки є початковим етапом інфекційного процесу. За допомогою низки експериментальних досліджень було продемонстровано, що карбоцистеїн зменшує закріплення M. catarrhalis, H. influenzae та S. рneumoniae на клітинах респіраторного епітелію дихального тракту, а також він здатен індукувати відшарування вже прикріплених до епітеліальних клітин організму хазяїна бактерій.
У дослідженні T. Sumitomo та співавт. застосування карбоцистеїну знижувало рівнень мРНК та експресію білка рецепторів фактора активації тромбоцитів (platelet activating factor receptor), які S. pneumoniae використовує для адгезії до клітин хазяїна, отже, й пригнічувало фіксацію S. pneumoniae в прозапальному мікрооточенні. Крім того, було доведено, що в разі одночасного застосування карбоцистеїну й амоксициліну при загостренні хронічного бронхіту вміст антибіотика в бронхіальному секреті (навіть гнійному) суттєво зростає.
Антиоксидантна та цитопротекторна дія карбоцистеїну
Карбоцистеїн знижує активність запалення, спричиненого активними формами кисню (АФК), що було продемонстровано в експериментальному дослідженні M. L. Garavaglia та співавт. (Garavaglia M. L. et al., 2008). Антиоксидантна дія карбоцистеїну полягала в його здатності збільшувати нейтралізацію АФК і запобігати незворотному зниженню рівнів хлоридів та глутатіону в клітині, що виникає внаслідок дії вільних радикалів. Водночас у дослідженні Guizzardi та співавт. було встановлено, що регулювальна дія карбоцистеїну на концентрацію глутатіону залежить від належної функції трансмембранного регуляторного білка муковісцидозу (ТРБМ). Саме тому ефлюксу глутатіону не спостерігається в разі захворювань, які супроводжуються порушеннями ТРБМ, зокрема при муковісцидозі.
Антиоксидантна активність карбоцистеїну тісно пов’язана з його цитопротекторними та протизапальними властивостями. Карбоцистеїн нормалізує активність a1-антитрипсину, а також зменшує продукцію прозапальних цитокінів, зокрема ІL‑8, збільшуючи нейтралізацію гідроксильних радикалів (•OH) у клітинах.
Сьогодні існує усе більше доказів ушкоджувального впливу екстракту тютюнового диму (ЕТД) на епітеліальні клітини дихальних шляхів. Зокрема, відомо, що ЕТД зумовлює окислювальний стрес клітин і впливає на антиоксидантну систему глутатіону. Здатність ЕТД спричиняти часо- та дозозалежну індукцію апоптозу клітин була продемонстрована в дослідженні Bazzini та співавт., у якому короткотривалий вплив ЕТД підвищував рівень АФК і знижував внутрішньоклітинну концентрацію глутатіону, одночасно підвищуючи експресію глутатіонпероксидаз 2 і 3, глутатіонредуктази, глутамат-цистеїн-лігази. В цьому дослідженні було доведено, що карбоцистеїн протидіє вищезазначеним процесам, а також чинить протекторну дію на клітини, які зазнали впливу ЕТД. Він захищає паренхіму легень від ушкоджувального ефекту ЕТД, запобігає розвитку емфіземи, завдяки антиоксидантній активності забезпечує зниження апоптозу та гальмування легеневих металопротеїназ MMP‑2 і MMP‑9 (Hanaoka, 2010).
Крім того, цитопротекторну дію карбоцистеїну підтверджено в дослідженні Yoshida та співавт., у якому була доведена його здатність активувати фосфорилювання протеїнкінази В, пригнічуючи зумовлену впливом пероксиду водню (Н2О2) активацію каспаз 3 та 9, отже, й зменшувати ушкодження епітеліальних клітин трахеї.
Карбоцистеїн індукує клітинну проліферацію, посилює ядерну експресію сиртуїну‑1 і білка FохO3 (Forkhead box protein O3), а також знижує активність β-галактозидази, уповільнюючи процеси старіння клітин респіраторного тракту, спричинені дією ЕТД (Pace et al., 2016).
Карбоцистеїн і відповідь на терапію кортикоїдами
Як відомо, оксидативний стрес та ЕТД є чинниками, які впливають на розвиток стероїдорезистентності в хворих на хронічне обструктивне захворювання легень (ХОЗЛ) і тяжку бронхіальну астму (Hakim et al., 2013; Barnes P. J. et al., 2014), що відбувається за рахунок зниження активності гістон-деацетилази 2 типу (histone deacetylase 2, HDAC2). HDAC2 – фермент, який деацитилюванням гістонів, що зв’язуються із промоторами генів запалення, обмежує доступ механізму транскрипції до цих генів, знижуючи в такий спосіб рівень їхньої експресії. В експериментальних дослідженнях in vitro й in vivo було продемонстровано, що карбоцистеїн знижує продукцію АФК, стимулює секрецію глутатіону та супероксиддисмутази, підвищує активність HDAC2, а також пригнічує ацетилювання гістону Н4 промотора гена IL‑8, потенціюючи активність дексаметазону, що спостерігалося навіть у тваринних моделях, які зазнали значного впливу оксидативного стресу.
Отже, під дією карбоцистеїну знижується рівень резистентності до дексаметазону при ХОЗЛ, що було показано під час експериментального моделювання ХОЗЛ на щурах. Карбоцистеїн пригнічує хронічне запалення дихальних шляхів, зменшуючи кількість запальних клітин, основних прозапальних цитокінів і запальну клітинну інфільтрацію, а також впливає на ремоделювання дихальних шляхів, зокрема на розвиток фіброзу, товщину епітелію та непосмугованих м’язів респіраторного тракту. Крім того, він зменшує вираженість емфіземи (знижує індекс тяжкості емфіземи D2, активність металопротеїнази MMP‑9 у бронхоальвеолярному лаважі й експресію a1-антитрипсину) та запобігає порушенню функції зовнішнього дихання. На відміну від флутиказону пропіонату карбоцистеїн відновлює дисбаланс у системі «оксиданти – антиоксиданти», а також підвищує рівень HDAC2, що було доведено на експериментальній моделі епітеліальних клітин бронхів. Нові дані свідчать, що ЕТД знижує експресію HDAC3 посиленням процесів ацетилювання в клітинах, що, своєю чергою, підвищує експресію прозапального фактора транскрипції – білка, який зв’язує cAMP‑залежний елемент – р-CREB (cAMP‑response-element-binding), мРНК IL‑1 та хемотаксис нейтрофілів. Під дією карбоцистеїну й беклометазону в клітинах, що зазнали впливу ЕТД, активуються процеси деацетилювання, а HDAC3 пригнічує рівні експресії мРНК p-CREB та IL‑1, а також хемотаксис нейтрофілів.
Протизапальна дія карбоцистеїну
Ключовим компонентом вродженого імунітету є toll-рецептори (TLRs), які переважно експресуються моноцитами/макрофагами та нейтрофілами, а також виявляються в епітеліальних клітинах легень і бронхів. Респіраторний епітелій є першою лінією захисту організму від токсичної дії ЕТД. Продукти, отримані в результаті ушкодження епітеліальних клітин, можуть діяти як ліганди для TLR4 і TLR2, посилюючи в такий спосіб запальні реакції у дихальних шляхах. У зв’язку із цим було продемонстровано, що внаслідок впливу ЕТД респіраторний епітелій може вивільняти підвищені концентрації IL‑8, які підтримують інфлюкс нейтрофілів до дихальних шляхів, запускаючи вроджену імунну відповідь. Як відомо, в хворих на ХОЗЛ переважає саме нейтрофільне запалення. Нейтрофільна еластаза сприяє метаплазії клітин слизової оболонки при хронічному бронхіті та бере активну участь у дисбалансі протеази / антипротеази – процесі, який спричиняє руйнування легеневої тканини та розвиток емфіземи.
В цьому аспекті протизапальну дію карбоцистеїну забезпечує його здатність знижувати експресію TLR4, зменшувати зв’язування ліпополісахаридів, знижувати рівень нейтрофілів, 8-ізопростану, мРНК ІL‑6, ІL‑8, а також пригнічувати опосередковану IL‑1 продукцію ІL‑8 та хемотаксичну активність нейтрофілів (у т. ч. за рахунок пригнічення продукції інозитол 1,4,5-трифосфату й діацилгліцерину)
Ефективність карбоцистеїну в пацієнтів із ХОЗЛ
Доведено, що часті загострення ХОЗЛ пришвидшують прогресування захворювання, погіршують якість життя, пов’язану зі здоров’ям, а також є причиною значного зростання економічних витрат і рівня смертності. Ключові ланки патогенезу ХОЗЛ – запалення дихальних шляхів, окислювальний стрес, бактеріальна колонізація, дисфункція війок і гіперсекреція слизу. В систематичних оглядах, проведених M. Decramer (2010) та I. Cerveri, V. Brusasco (2010), наголошується на ролі хронічної гіперсекреції слизу як найхарактернішого симптому хронічного бронхіту. Незважаючи на те що мукоактивні препарати широко використовуються в клінічній практиці вже давно, їх тривалий прийом залишається спірним питанням у лікуванні хворих на ХОЗЛ.
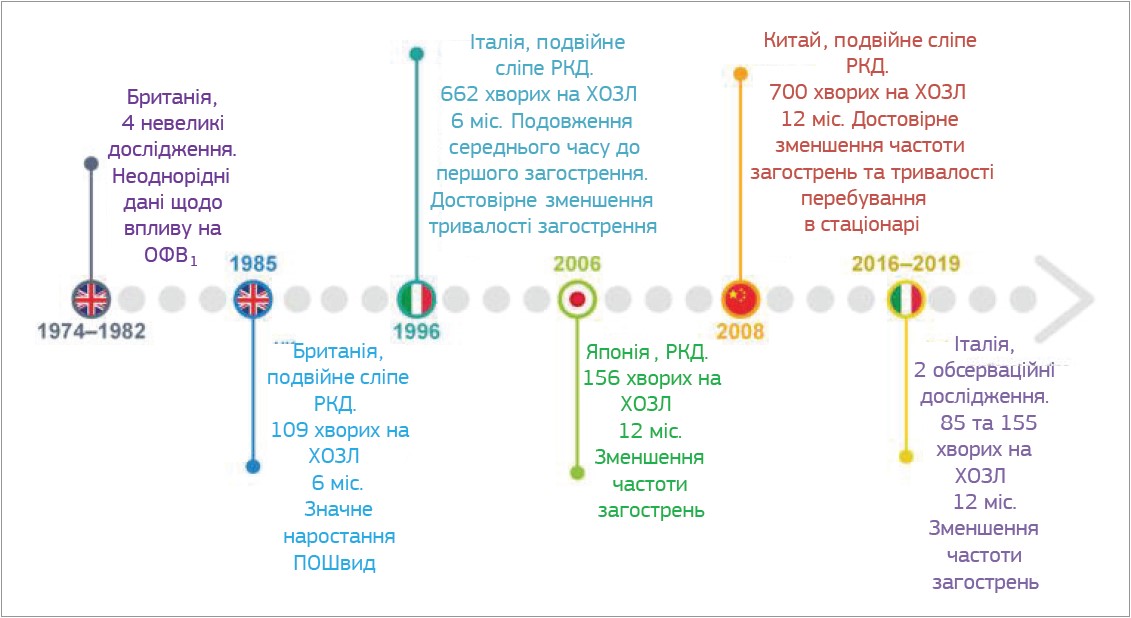
Перші повідомлення про ефективність щоденного прийому карбоцистеїну в дозі 2,25-3 г порівняно із плацебо в пацієнтів із хронічним бронхітом надходили ще до 1990 року з декількох невеликих клінічних випробувань, проведених у Великій Британії. Результати цих досліджень були досить неоднорідними, зокрема щодо впливу карбоцистеїну на такі показники, як ОФВ1 та пікова об’ємна швидкість видиху (ПОШвид); що стосується суб’єктивніших параметрів, як-от кашель, задишка та полегшення відходження мокротиння, то результати були обнадійливими (рис. 2).
Рис. 2. Основні клінічні дослідження ефективності карбоцистеїну в хворих на ХОЗЛ
У британському подвійному сліпому плацебо-контрольованому дослідженні, яке проводилося в паралельних групах, оцінювали ефективність застосування карбоцистеїну в дозі 750 мг 3 р/добу впродовж 6 міс (осінньо-зимовий період) у 109 пацієнтів із хронічним бронхітом. Під час оцінки результатів цього дослідження суттєвих відмінностей у частоті загострень та ПОШвид між групами карбоцистеїну і плацебо не було.
Однак результати японського рандомізованого плацебо-контрольованого дослідження, в якому оцінювали ефективність застосування карбоцистеїну в добовій дозі 1,5 г протягом 12 міс у 156 пацієнтів із ХОЗЛ, свідчили, що призначення карбоцистеїну сприяє статистично значущому зменшенню кількості застудних захворювань та достовірному зниженню частоти загострень у пацієнтів із ХОЗЛ. Варто зауважити, що жоден із залучених до випробування пацієнтів не отримував інгаляційних (ІК) або пероральних кортикоїдів.
Окрім того, згідно з результатами італійського багатоцентрового проспективного подвійного сліпого рандомізованого плацебо-контрольованого дослідження, в якому взяли участь 662 пацієнтів із ХОЗЛ, середній час до першого загострення був достовірно довшим у групі хворих, котрі впродовж 6 міс приймали карбоцистеїн у добовій дозі 2,7 г, порівняно із плацебо.
В масштабнішому багатоцентровому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні щодо вивчення ефективності та безпеки тривалого застосування карбоцистеїну (впродовж року) PEACE, до якого залучили >700 пацієнтів із 22 центрів Китаю, в анамнезі котрих мало бути щонайменше 2 загострення ХОЗЛ за попередні 2 роки, проте протягом останніх 4 тиж клінічний стан таких учасників мав залишатися стабільним, кількість загострень на пацієнта за рік достовірно зменшилася в групі карбоцистеїну проти групи плацебо (стандартне відхилення (СВ) 1,01 (СВ=0,06) проти 1,35 (СВ=0,06) відповідно, коефіцієнт ризику (КР) 0,75; 95% довірчий інтервал (ДІ) 0,62-0,92; p=0,004). Отже, в групі пацієнтів, які впродовж року отримували карбоцистеїн у добовій дозі 1,5 г, частота загострень виявилася на 24% нижчою порівняно із плацебо, при цьому вплив карбоцистеїну на частоту загострень був вираженішим у випадку його застосування впродовж щонайменше 6 міс. Тривалий прийом карбоцистеїну супроводжувався клінічно значущим покращенням якості життя хворих на ХОЗЛ, про що свідчило зростання кількості балів за шкалами «загальна оцінка» та «симптоми» респіраторного опитувальника шпиталю святого Георгія (SGRQ). Профіль безпеки карбоцистеїну був зіставним із плацебо.
Важливим моментом дослідження PEACE є те, що зниження частоти загострень не залежало від застосування ІК. Ці дані відрізняються від дослідження BRONCUS, під час якого застосування муколітика N‑ацетилцистеїну сприяло зниженню частоти загострень лише в пацієнтів, які не отримували терапію ІК.
Нещодавно було проведено обсерваційне проспективне досліджені CAPRI, до якого було залучено 85 пацієнтів із ХОЗЛ, котрі мали щонайменше 1 епізод загострення за попередній рік. Усі учасники дослідження щодня отримували карбоцистеїн у дозі 2,7 г упродовж року. Обстеження пацієнтів проводили кожні 3 міс до кінця дослідження. Первинна кінцева точка (зменшення кількості загострень) була досягнута після 12 міс терапії, тоді як у дослідженні PEACE ті самі результати були отримані через 6 міс. Зниження частоти загострень не залежало від застосування ІК. При оцінці вторинних кінцевих точок спостерігали статично значуще покращення якості життя пацієнтів згідно з даними опитувальника SGRQ. Легенева функція (ОФВ1, ФЖЄЛ, ОФВ1/ФЖЄЛ) суттєво не покращилася, що відповідає результатам інших схожих досліджень. Однак спостерігали значне зниження індексу BODE, який є достовірним предиктором загальної смертності та ризику смерті від респіраторних причин, а також покращення толерантності до фізичних навантажень (згідно з результатами тесту з 6-хвилинною ходьбою, 6MWT).
Результати дослідження CAPRI були підтверджені Paone та співавт. при оцінці 155 хворих на ХОЗЛ. Як і в дослідженні РЕАСЕ, ефективність карбоцистеїну не залежала від терапії ІК.
У систематичному огляді та метааналізі, проведеному в 2019 році Zheng і співавт., спостерігали достовірне зниження загальної кількості загострень на тлі тривалого прийому карбоцистеїну в дозі 1500 мг/добу (-0,43; 95% ДІ -0,57, -0,29; р=0,01). Окрім того, карбоцистеїн сприяв покращенню якості життя та зменшенню кількості пацієнтів зі щонайменше 1 загостренням.
Згідно з рекомендаціями GOLD‑2020, регулярна терапія із застосуванням муколітиків, як-от ердостеїн, карбоцистеїн, N‑ацетилцистеїн, може зменшувати загострення ХОЗЛ в окремих популяціях (рівень доказовості В), а також певною мірою покращувати статус здоров’я хворих на ХОЗЛ, які не отримують ІК.
Отже, незважаючи на те що карбоцистеїн десятиліттями вважався лише мукоактивним препаратом, він демонструє широкий спектр протизапальної та антиоксидантної активності. Карбоцистеїн послаблює міграцію клітин запалення до дихальних шляхів, зменшує ураження ендотелію і кашльову чутливість, а також пригнічує активність вільних радикалів. Ці ефекти паралельно з його мукорегуляторними властивостями відіграють значну роль у терапії запальних захворювань дихальних шляхів. Механізми дії карбоцистеїну є багатофакторними та полягають у його здатності регулювати експресію муцинів і циліарну активність, послаблювати оксидативний стрес, впливати на бактеріальні й вірусні патогени, а також покращувати відповідь на терапію кортикоїдами.
Згідно з рекомендаціями GOLD‑2020, регулярна терапія карбоцистеїном може зменшувати частоту загострень, а також покращувати статус здоров’я хворих на ХОЗЛ, які не отримують ІК.
Серед доступних на фармацевтичному ринку України молекул карбоцистеїну особливої уваги заслуговує препарат Флюдітек («Лабораторія Іннотек Інтернасьйональ», Франція). Флюдітек випускається у вигляді сиропу 5% (для дорослих) та у вигляді сиропу 2% (для дітей). Флюдітек показаний для лікування симптомів порушень бронхіальної секреції та виведення мокротиння, особливо при гострих бронхолегеневих захворюваннях, наприклад при гострому бронхіті; при загостреннях хронічних захворювань дихальної системи.
За матеріалами E. Pace et al., Clinical Efficacy of Carbocysteine in COPD: Beyond the Mucolytic Action, 2022.
ФЛЮДІТЕК (FLUDITEC). Склад: 1 мл сиропу 5% містить 50 мг карбоцистеїну. Фармакотерапевтична група. Засоби, які застосовують при кашлі та застудних захворюваннях. Муколітичні засоби. Карбоцистеїн. Код АТХ R05С В03. Показання. Лікування симптомів порушень бронхіальної секреції та виведення мокротиння, особливо при гострих бронхолегеневих захворюваннях, наприклад при гострому бронхіті; при загостреннях хронічних захворювань дихальної системи у дорослих та дітей віком від 15 років. Протипоказання. Гіперчутливість до активної речовини або до будь-якої з допоміжних речовин (див. розділ «Особливості застосування»). Пептична виразка шлунка та дванадцятипалої кишки у період загострення. Спосіб застосування та дози. ДЛЯ ДОРОСЛИХ ТА ДІТЕЙ ВІКОМ ВІД 15 РОКІВ. Дозувальний стаканчик, наповнений до відмітки 15 мл, містить 750 мг карбоцистеїну. Приймати 1 дозу (15 мл) 3 рази на добу, переважно між прийомами їжі. Тривалість лікування має бути короткою і не повинна перевищувати 5 днів. Побічні реакції. Можливі алергічні шкірні реакції, такі як свербіж, еритематозне висипання, кропив’янка та ангіоневротичний набряк. Було зафіксовано декілька випадків фіксованого висипу. Можливі розлади травлення (біль у шлунку, нудота, блювання, діарея) (див. розділ «Особливості застосування»). Шлунково-кишкова кровотеча (див. розділ «Особливості застосування»). Повідомлялося про поодинокі випадки бульозного дерматиту, такі як синдром Стівенса – Джонсона та мультиформна еритема. Категорія відпуску. Без рецепта. Виробник. Іннотера Шузі, Франція/Innothera Chouzy, France. Реєстраційне посвідчення № UA/8082/01/02. Наказ МОЗ України 01.08.2018 № 1422. Дата останнього перегляду. 08.07.2021. Повна інформація про лікарський засіб Флюдітек викладена в інструкції для медичного застосування. Представництво «Лабораторія Іннотек Інтернасьйональ» в Україні, 01001, м. Київ, вул. Мала Житомирська/Михайлівська, буд. 6/5.
Матеріал для розповсюдження в рамках спеціалізованих семінарів, конференцій, симпозіумів з медичної тематики та у спеціалізованих виданнях, призначених для медичних та фармацевтичних працівників
Підготувала Ольга Гуйванюк
Медична газета «Здоров’я України 21 сторіччя» № 13 (530), 2022 р.