16 листопада, 2025
Керівництво Глобальної стратегії діагностики, лікування та профілактики ХОЗЛ: що нового? Продовження
Частина 1. Частина 2.
За прогнозами науковців, тягар, зумовлений хронічним обструктивним захворюванням легень (ХОЗЛ), упродовж наступних десятиліть збільшуватиметься внаслідок тривалого впливу факторів ризику розвитку захворювання і старіння населення. Продовжуємо знайомити з документом Глобальної стратегії діагностики, лікування та профілактики ХОЗЛ (GOLD), що прагне стати інструментом поліпшення здоров’я людей із ризиком розвитку ХОЗЛ та вже хворих на ХОЗЛ і робить свій внесок у досягнення «Цілей сталого розвитку ООН, пункт 3.4» щодо зменшення частоти передчасної смерті від неінфекційних захворювань, у тому числі ХОЗЛ, на одну третину до 2030 року. У цій частині йдеться про оновлення в розділах профілактики та лікування ХОЗЛ, терапевтичні заходи, які знижують смертність від ХОЗЛ, а також ефективність фармакотерапії при ХОЗЛ.
Розділ 3. Профілактика та лікування ХОЗЛ
Ключові положення
- Усіх осіб, які курять, треба наполегливо заохочувати відмовитися від куріння та підтримувати їх у цьому. Замісна нікотинова терапія та фармакотерапія надійно підвищують рівень довгострокової відмови від куріння. Заборона куріння на законодавчому рівні та консультування з цього приводу, що надається медичними працівниками, поліпшують рівень відмови. Наразі немає доказів, які підтверджують ефективність і безпеку електронних сигарет як засобу для відмови від куріння.
- Основними цілями лікування ХОЗЛ є зменшення симптомів і ризику загострень у майбутньому. Стратегія лікування стабільного ХОЗЛ має базуватися переважно на оцінці симптомів та історії загострень.
- Фармакотерапія може зменшити вираженість симптомів ХОЗЛ, знизити частоту і тяжкість загострень, а також поліпшити загальний стан здоров'я і толерантність до фізичних навантажень. Дані доказової бази свідчать, що фармакотерапія може поліпшувати показники функції легень і знижувати смертність.
- Фармакологічний режим лікування має бути індивідуальним і обиратися залежно від тяжкості симптомів, ризику загострень, можливих побічних ефектів, супутніх захворювань, доступності та вартості ліків, а також відповідати потребам пацієнта, його вподобанням і здатності використовувати різноманітні пристрої доставки ліків у дихальні шляхи.
- Необхідно регулярно оцінювати техніку використання інгаляторів пацієнтами.
- Вакцини проти COVID‑19 є високоефективними щодо SARS-CoV‑2-інфекції, і пацієнти з ХОЗЛ мають вакцинуватися відповідно до національних рекомендацій.
- Вакцинація проти грипу та пневмококової інфекції зменшує частоту інфекцій нижніх дихальних шляхів.
- CDC рекомендує: вакцинацію від кашлюка/правця/дифтерії пацієнтам із ХОЗЛ, які не були щеплені в підлітковому віці; рутинне використання вакцини проти оперізувального герпесу в усіх пацієнтів із ХОЗЛ; нову вакцину проти респіраторно-синцитіального вірусу (RSV) для осіб старше 60 років та/або з хронічними захворюваннями серця або легень.
- Легенева реабілітація з її основними компонентами, у тому числі фізичні вправи в поєднанні з хворобоспецифічними освітніми заходами, поліпшує фізичну форму, симптоми та якість життя при ХОЗЛ будь-якого ступеня тяжкості.
- У пацієнтів із тяжкою хронічною гіпоксемією в стані спокою (PaO2 ≤55 мм рт. ст. або <60 мм рт. ст., за наявності легеневого серця або вторинної поліцитемії) довгострокова киснева терапія покращує виживаність.
- Пацієнтам зі стабільним ХОЗЛ і помірною десатурацією у стані спокою або під час фізичних навантажень не рекомендується рутинно призначати кисневе лікування. Однак при оцінці потреби пацієнта в додатковому кисні необхідно враховувати індивідуальні фактори.
- Пацієнтам із тяжкою хронічною гіперкапнією та госпіталізацією з приводу гострої дихальної недостатності в анамнезі тривала неінвазивна вентиляція може знизити смертність і запобігти повторній госпіталізації.
- В окремих пацієнтів із прогресуючою емфіземою, резистентною до оптимізованого лікування, можуть бути корисними хірургічні або бронхоскопічні інтервенційні методи лікування.
- При прогресуючому ХОЗЛ для контролю симптомів ефективними є паліативні терапевтичні підходи.
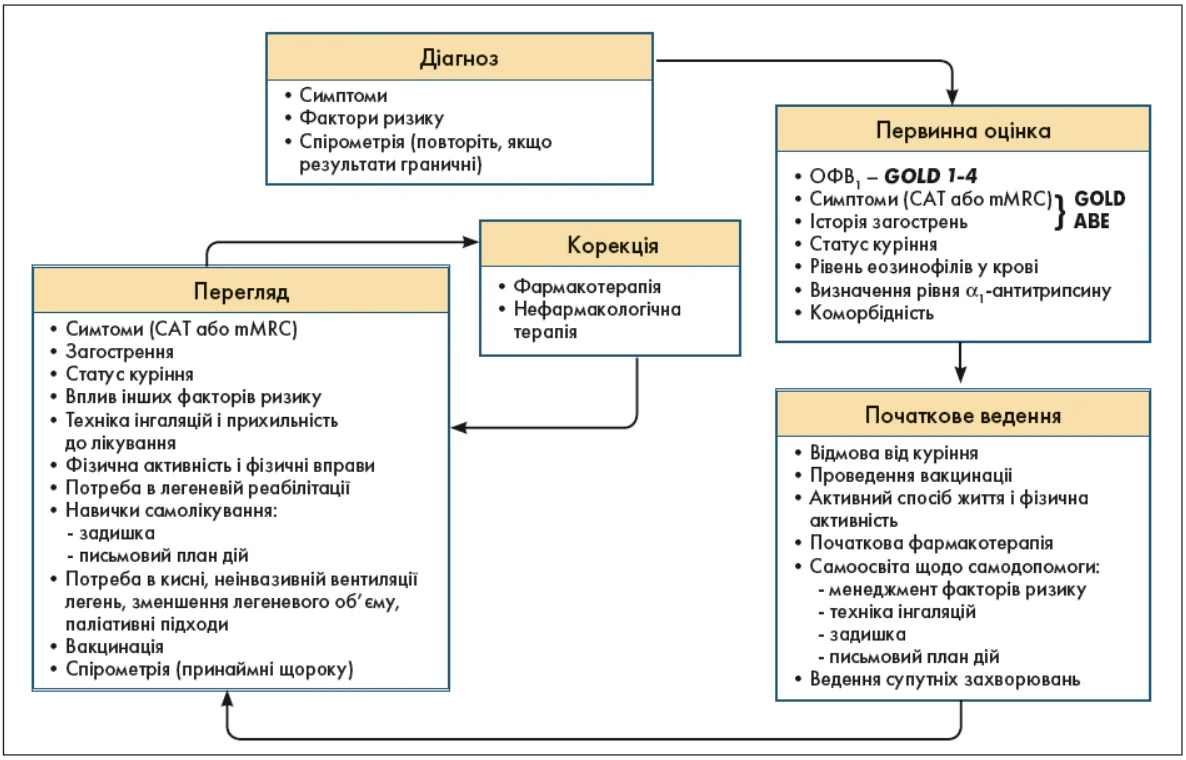
За необхідності фармакологічну і нефармакологічну терапію потрібно коригувати та проводити регулярні огляди пацієнта (рис. 5). Цей розділ містить рекомендації щодо ведення пацієнтів із ХОЗЛ у клінічній практиці та узагальнює дані про ефективність і безпеку стратегій лікування і профілактики ХОЗЛ, на яких засновані ці рекомендації.
Рис. 5. Ведення пацієнтів із ХОЗЛ
Фармакологічне лікування стабільного ХОЗЛ
Алгоритми початкової і подальшої фармакологічної терапії
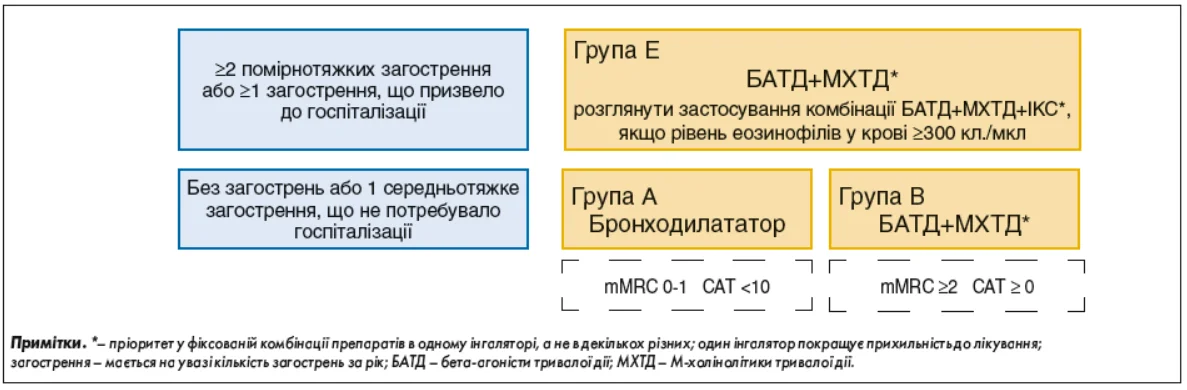
GOLD пропонує індивідуальний підхід до вибору засобів початкового лікування, який базується на вираженості симптомів і ризику загострень. Терапію можна посилювати/зменшувати залежно від наявності домінуючих симптомів – задишки та обмеження фізичної активності, а також з огляду на наявність загострень під час підтримуючої терапії. Початкова фармакотерапія має базуватися на групі GOLD, до якої належить пацієнт (рис. 6). Надалі пацієнтам потрібно надати рекомендації щодо самоконтролю задишки, управління стресом, а також письмовий план дій. Супутні захворювання необхідно лікувати відповідно до конкретних клінічних настанов, незалежно від наявності ХОЗЛ.
Рис. 6. Початкове фармакологічне лікування ХОЗЛ (GOLD 2025)
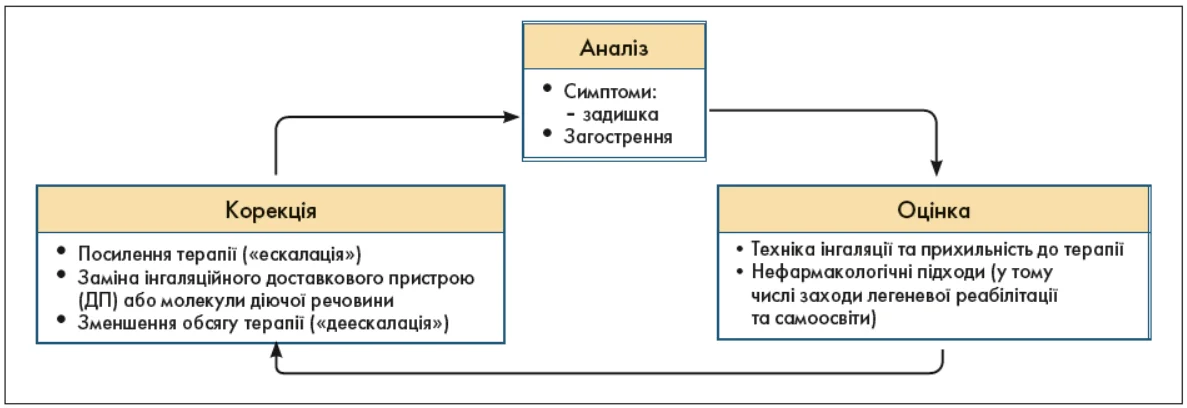
Після впровадження лікування стан пацієнтів необхідно оцінити повторно, аби з’ясувати, чи досягнуті цілі терапії і чи немає будь-яких для неї перешкод (рис. 7). Після початку лікування і повторного огляду пацієнта може знадобитися коригування терапії.
Рис. 7. Цикл ведення пацієнта з ХОЗЛ
Для подальшого лікування передбачено окремий алгоритм. Він базується на двох ключових ознаках, які підлягають терапії, таких як персистування задишки та виникнення загострень (рис. 8) [501, 700-702]. Ці рекомендації щодо подальшого ведення ХОЗЛ призначені для поліпшення лікування пацієнтів, яким уже призначено підтримуючу терапію, як у разі початкового лікування, так і після багатьох років спостереження. Рекомендації засновані на результатах клінічних досліджень і на використанні даних щодо кількості еозинофілів у периферичній крові як біомаркера для визначення доцільності застосування ІКС-терапії з метою профілактики загострень.
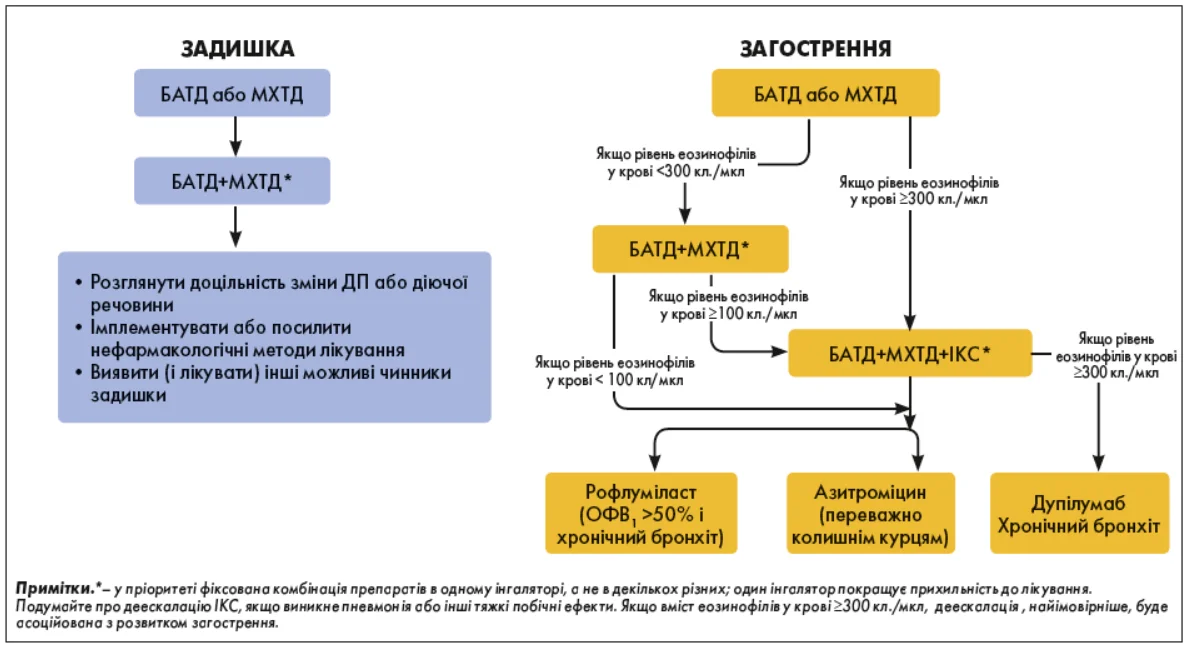
Рис. 8. Схема подальшої фармакотерапії ХОЗЛ (GOLD 2025)
У представленому алгоритмі запропоновано стратегії ескалації та деескалації терапії на основі доступних даних щодо її ефективності та безпеки. Відповідь на ескалацію лікування згодом завжди має бути переглянута. Пацієнти, щодо лікування яких розглядають можливі зміни, зокрема деескалацію, мають перебувати під пильним медичним наглядом.
Терапевтичні заходи, які знижують смертність від ХОЗЛ
ХОЗЛ є третьою провідною причиною смерті у світі (3,23 млн смертей у 2019 р.). З огляду на таргетне лікування підгруп пацієнтів із ХОЗЛ, важливо знати, які модифіковані фактори (ознаки захворювання, що реагують на лікування) асоційовані зі смертністю. Велике клінічне дослідження бази даних пацієнтів із ХОЗЛ первинної ланки медичної допомоги продемонструвало, що найвищий ризик смертності від усіх причин, пов’язаної з ХОЗЛ та ССЗ, був в осіб із підвищеною тяжкістю та частотою загострень ХОЗЛ, груп GOLD B і D, а також в осіб із нижчим показником ОФВ1 (особливо GOLD 3 і 4) [843].
Фахівці досі вивчають механізми, що спричиняють смерть у пацієнтів із ХОЗЛ. Довести переваги в РКД тих чи тих терапевтичних методів щодо запобігання смертності складно, оскільки для цього потрібні великі популяції та/або тривалий період спостереження, та/або ретельно відібрані популяції з високим, але таким, якому можна запобігти, ризиком смерті під час спостереження. У таблиці 3 представлено підсумок фармакологічних і нефармакологічних методів лікування, ефективність яких у зниженні смертності пацієнтів із ХОЗЛ підтверджено доказами.
|
Таблиця 3. Доказові фармакологічні і нефармакологічні методи лікування, які знижують смертність у пацієнтів із ХОЗЛ |
|||
|
Терапія |
РКД* |
Вплив лікування на смертність |
Характеристики пацієнтів |
|
Фармакотерапія |
|||
|
БАТД+МХТД+ІКС1 |
Так |
Трикомпонентна фіксована комбінація в одному інгаляторі в порівнянні з комбінацією двох БДТД, зниження відносного ризику: IMPACT: ВР 0,01 (95% ДІ 0,530,99)1а ETHOS: ВР 0,51 (95% ДІ 0,330,80)1b |
Пацієнти із симптомами з історією частих/тяжких загострень |
|
Нефармакологічні методи терапії |
|||
|
Відмова від куріння2 |
Так |
ВР для звичайної групи досліджуваних у порівнянні з групою втручання (відмова від куріння). ВР 1,18 (95% ДІ1,021,37)2 |
Пацієнти без симптомів або з легкими симптомами |
|
Легенева реабілітація3# |
Так |
Старі дослідження: ВР 0,28 (95% ДІ 0,100,84)3а. Нові дослідження: ВР 0,68 (95% ДІ 0,281,16)3b |
Госпіталізовані з приводу загострень ХОЗЛ (протягом або ≤4 тиж після виписки) |
|
Тривала оксигенотерапія4 |
Так |
NOTT: ≥19 год безперервної подачі кисню проти ≤13 год: зниження на 50%4а. MRC: ≥15 год подачі кисню проти відсутності оксигенотерапії: зниження на 50%4b |
PaO2 ≤55 мм рт. ст. або <60 мм рт. ст. у пацієнтів із легеневим серцем або вторинною поліцитемією |
|
Неінвазивна вентиляція з позитивним тиском5 |
Так |
12% в NPPV(високий рівень IPAP) і 33% у групі контролю. ВР 0,24 (95% ДІ 0,110,49)5 |
Стабільне ХОЗЛ із вираженою гіперкапнією |
|
Хірургічне зменшення об’єму легень (ХЗОЛ)6 |
Так |
0,07 випадку смерті/пацієнтороків (ХЗОЛ) проти 0,15 випадку смерті/пацієнтороків (у групі контролю – звичайної терапії) відносний ризик смерті 0,47 (р=0,005)6 |
Емфізема верхньої частки і низька здатність до фізичного навантаження |
|
Примітки. БДТД – бронходилататори тривалої дії; ІКС – інгаляційні кортикостероїди; ВР – відношення ризиків; ДІ – довірчий інтервал; NPPV (Noninvasive Positive Pressure Ventilation) – неінвазивна вентиляція з позитивним тиском на видиху; IPAP (Inspiratory Positive Airway Pressure) – позитивний тиск під час вдиху; 1a – дослідження IMPACT (Lipson et al., 2020) та 1b – дослідження ETHOS (Martinez et al., 2021); 2 – Lung Health Study (Anthonisen et al., 2005); 3a – Puhan et al., 2011) та 3b – Puhan et al., 2016; 4a – дослідження NOTT (NOTT, 1980) та 4b – дослідження MRC (MRC, 1981); 5 – Kohlein trial (Kohlein et al., 2014); 6 – дослідження NETT (Fishman et al., 2003). |
|||
Фармакологічна терапія
Проведені раніше дослідження – TORCH (TOwards a Revolution in COPD Health) [844] і SUMMIT (Study to Understand Mortality and MorbidITy in COPD) [845] – не підтвердили ефективність комбінації БАТД+ІКС у порівнянні з плацебо щодо зниження смертності (первинний результат) у пацієнтів із ХОЗЛ. У згаданих клінічних дослідженнях не було вимог щодо наявності загострень в анамнезі. У найбільшому дослідженні UPLIFT (Understanding Potential Long-term Impacts on Function with Tiotropium), у рамках якого вивчали ефективність МХТД у порівнянні з плацебо на тлі стандартної терапії, – через 30 днів після завершення періоду дослідження МХТД не продемонстрував зниження смертності (вторинний результат) порівняно з плацебо. Більшість пацієнтів, що брали участь у цьому дослідженні, використовували ІКС.
Результати двох великих РКД, IMPACT (InforMing the PAthway of COPD Treatment) [496] і ETHOS (Efficacy and Safety of Triple Therapy in Obstructive Lung Disease) [699], свідчать про те, що фіксована трикомпонентна комбінація для інгаляційного застосування (БАТД+МХТД+ІКС) сприяє зниженню загальної смертності в порівнянні з двокомпонентною інгаляційною терапією бронходилататорами тривалої дії. У сукупності ці результати свідчать про те, що потрійна фіксована комбінація ефективніше за подвійну (БАТД+МХТД) знижує смертність у пацієнтів із ХОЗЛ, які мають в анамнезі часті та/або тяжкі загострення і які раніше отримували підтримуючу терапію потрійною комбінацією, БАТД+ІКС або монотерапію чи комбінацію двох бронходилататорів тривалої дії. Ці дослідження були розширені за рахунок пацієнтів із симптомами ХОЗЛ (CAT ≥10) з історією частих (≥2 помірних загострення) та/або тяжких загострень (≥1 загострення, що потребувало госпіталізації).
Огляд ефективності: фармакотерапія
Фармакотерапія стабільного ХОЗЛ
Сучасна фармакотерапія ХОЗЛ зосереджена на симптомах і загостреннях. Зниження ОФВ1 вважають сурогатом природного перебігу захворювання. У цьому контексті були проведені дослідження з метою оцінки впливу фармакотерапії на динаміку змін ОФВ1 з часом. Окремі клінічні випробування не надали достатньо переконливих доказів того, що фармакотерапія може уповільнити зниження ОФВ1 [885-889]. Однак систематичний огляд результатів 9 досліджень продемонстрував уповільнення швидкості зниження ОФВ1 на 5,0 мл/рік у групах активного лікування порівняно з групами плацебо [890]. Різниця між групами лікування, що застосовували бронходилататори тривалої дії, та групами плацебо становила 4,9 мл/рік. Різниця між групами лікування, що отримували ІКС, і групами плацебо становила 7,3 мл/рік. Отже, з одного боку, необхідно усвідомлювати потенційну користь фармакотерапії для сповільнення зниження функції легень, з іншого – потрібні подальші дослідження, щоб виокремити категорію пацієнтів, які можуть отримати користь від такого лікування.
Бронходилататори – це препарати, які збільшують ОФВ1 та/або змінюють інші спірометрічні показники (панель 1). Механізм їхньої дії полягає в зміні тонусу гладеньких м’язів дихальних шляхів, а поліпшення видиху відображає радше розширення дихальних шляхів, а не зміну їхньої еластичності. Бронходилататори, як правило, зменшують динамічну гіперінфляцію в стані спокою та під час фізичного навантаження [306, 892] і поліпшують толерантність до нього. Ступінь цих змін, особливо в пацієнтів із тяжким і дуже тяжким ХОЗЛ, важко передбачити на основі поліпшення лише рівня ОФВ1, виміряного у стані спокою [893, 894]. Бронходилататори при ХОЗЛ найчастіше призначають регулярно для профілактики або зменшення симптомів. Рутинне застосування бронходилататорів короткої дії не рекомендується.
Панель 1
Бронходилататори при стабільному ХОЗЛ
- Інгаляційні бронходилататори при ХОЗЛ є ключовими препаратами в лікуванні симптомів захворювання. Їх призначають на регулярній основі для запобігання симптомам і зменшення їх вираженості (Рівень доказовості А).
- Рекомендується призначення інгаляційних бронходилататорів, а не пероральні їх форми (Рівень доказовості А).
- Застосування БАКД і М-холінолітиків короткої дії (МХКД) регулярно та за потреби поліпшує ОФВ1 та симптоми при ХОЗЛ (Рівень доказовості А).
- Терапія комбінацією БАКД та МХКД є ефективнішою щодо поліпшення ОФВ1 і симптомів ХОЗЛ, аніж монотерапія будь-яким із них (Рівень доказовості А).
- Віддають перевагу призначенню БАТД і М-холінолітиків тривалої дії (МХТД) проти короткодіючих бронходилататорів, за винятком пацієнтів лише з епізодами задишки (Рівень доказовості А) і за необхідності швидкого купірування симптомів у пацієнтів, які приймають бронходилататори тривалої дії як підтримуючу терапію.
- БАТД і МХТД значуще поліпшують функцію легень, зменшують задишку, покращують загальний стан здоров’я і знижують частоту загострень (Рівень доказовості А).
- МХТД є ефективнішими щодо зниження частоти загострень у порівнянні з БАТД (Рівень доказовості А) і зменшують частоту госпіталізацій (Рівень доказовості В).
- При призначенні початкового лікування перевагу віддають бронходилататорам тривалої дії, зокрема комбінації БАТД і МХТД. Пацієнтам із персистувальною задишкою, які приймають один бронходилататор тривалої дії, рекомендована ескалація терапії – додавання ще одного (Рівень доказовості А).
- Комбінована терапія із застосуванням БАТД і МХТД підвищує ОФВ1 і зменшує вираженість симптомів у порівнянні з монотерапією кожним із них окремо (Рівень доказовості А).
- Комбінована терапія із застосуванням БАТД і МХТД зменшує частоту загострень у порівнянні з монотерапією (Рівень доказовості В).
- Комбінована терапія бронхолітиками може призначатися як в одному інгаляторі – фіксованою комбінацією, так і в різних. Застосування одного інгалятора є більш прийнятним та ефективним, ніж декількох.
- Енсіфентрин суттєво поліпшує легеневу функцію (Рівень доказовості А), задишку (Рівень доказовості А) і загальний стан здоров’я пацієнтів із ХОЗЛ (Рівень доказовості В).
- Застосування теофілінів демонструє незначний бронходилататорний ефект при стабільному ХОЗЛ (Рівень доказовості А) і асоційоване з помірними перевагами щодо поліпшення симптомів (Рівень доказовості В)
Метилксантини – клінічні ефекти похідних ксантину залишаються предметом суперечок. Вони можуть діяти як неселективні інгібітори фосфодіестерази, але також мають низку небронходилататорних ефектів, значення яких є спірним [936-938]. Даних про тривалість дії звичайних форм ксантину або форм із повільним вивільненням препарату при ХОЗЛ наразі немає.
Дослідження, в якому вивчали ефективність додавання низьких доз теофіліну до ІКС у пацієнтів із ХОЗЛ, що мають підвищений ризик загострення, не виявило різниці щодо кількості загострень ХОЗЛ протягом року в порівнянні з плацебо [944]. Велике плацебо-контрольоване дослідження не виявило впливу перорального теофіліну окремо або в поєднанні з преднізолоном у дозі 5 мг/добу на загострення ХОЗЛ тяжкого перебігу [945].
Комбінована бронходилататорна терапія – поєднання бронходилататорів із різними механізмами дії та з різною її тривалістю може підвищити ступінь бронходилатації з меншим ризиком побічних ефектів у порівнянні зі збільшенням дози одного бронходилататора [946, 947]. Комбінації БАКД з МХКД є ефективнішими за монотерапію кожним із них окремо щодо поліпшення ОФВ1 і симптомів [948]. Лікування формотеролом і тіотропієм в окремих інгаляторах виявляє більший вплив на ОФВ1, ніж терапія кожним із цих компонентів окремо [949]. Існує велика кількість комбінацій БАТД і МХТД в одному інгаляторі, які покращують функцію легень порівняно з плацебо [946]; це покращення є стабільно більшим, ніж ефекти монотерапії бронходилататорами тривалої дії, хоча ступінь такого поліпшення є меншим, ніж повний адитивний ефект, очікуваний на основі відповіді на окремі компоненти [950].
Протизапальні препарати: на сьогодні загострення (наприклад, частота загострень, пацієнти з принаймні одним загостренням, час до настання першого загострення) є основною клінічно значущою кінцевою точкою, що використовується для оцінки ефективності лікарських засобів із протизапальною дією (табл. 4).
|
Таблиця 4. Протизапальна терапія стабільного ХОЗЛ |
|
|
Група препаратів |
Основні положення |
|
ІКС |
• Регулярне лікування за допомогою ІКС підвищує ризик розвитку пневмонії, особливо в пацієнтів із тяжким перебігом ХОЗЛ (Рівень доказовості А). • Комбінація ІКС із БАТД є ефективнішою, ніж монотерапія ними, щодо поліпшення легеневої функції, загального стану здоров’я, зменшення частоти загострень у пацієнтів із загостреннями і середньотяжким і тяжким перебігом ХОЗЛ (Рівень доказовості А). • Не рекомендовано застосовувати комбінацію БАТД+ІКС у пацієнтів із ХОЗЛ. Якщо є показання для призначення ІКС, значно більшу ефективність демонструє трикомпонентна комбінація – БАТД+МХТД+ІКС, тому їй віддають перевагу. • Трикомпонентна комбінована терапія БАТД+МХТД+ІКС поліпшує легеневу функцію, зменшує симптоми захворювання, покращує загальний стан здоров’я, а також зменшує частоту загострень ХОЗЛ у порівнянні з комбінаціями БАТД+ІКС чи БАТД+МХТД або монотерапією МХТД (Рівень доказовості А). Нові дані свідчать про більшу ефективність потрійної інгаляційної терапії в порівнянні з комбінацією БАТД+МХТД щодо смертності в пацієнтів із симптомами ХОЗЛ та історією частих і/або тяжких загострень. • Якщо в пацієнтів із ХОЗЛ є ознаки астми, лікування має обов’язково передбачати застосування ІКС. • Незалежно від використання ІКС існує доказ, що рівень еозинофілів у крові <2% підвищує ризик розвитку пневмонії (Рівень доказовості С). • Комбінація інгаляційних препаратів може бути представлена як у формі фіксованох комбінації в одному інгаляторі, так і в декількох окремих. Перевагу віддають фіксованій комбінації в одному інгаляторі як більш зручній і ефективній формі |
|
Пероральні КС |
Тривале застосування пероральних КС характеризується численними побічними ефектами (Рівень доказовості А) за відсутності доказів переваги від їх використання при ХОЗЛ (Рівень доказовості С) |
|
Інгібітори фосфодіестерази |
• У пацієнтів із хронічним бронхітом, тяжким і дуже тяжким перебігом ХОЗЛ та загостреннями в анамнезі: |
|
Антибіотики |
• Тривала терапія азитроміцином і еритроміцином зменшує частоту загострень протягом року (Рівень доказовості А). • Азитроміцин може бути рекомендований переважно, але не тільки, у колишних курців із загостреннями ХОЗЛ, незважаючи на адекватну терапію (Рівень доказовості В). • Терапія азитроміцином асоційована з підвищеним ризиком розвитку бактеріальної резистентності (Рівень доказовості А) та погіршенням слухових тестів унаслідок ототоксичності (Рівень доказовості В) |
|
Мукорегулятори й антиоксиданти |
• Регулярна терапія муколітиками, такими як ердостеїн, карбоцистеїн і Nацетилцистеїн (NAC), зменшує ризик загострень ХОЗЛ в обраній популяції (Рівень доказовості В). • Муколітикиантиоксиданти рекомендовані лише окремим пацієнтам (Рівень доказовості А) |
|
Імунобіологічна терапія |
• У пацієнтів із середньої тяжкості та тяжким перебігом ХОЗЛ, з історією загострень, хронічним бронхітом і високим рівнем еозинофілів у крові (≥300 кл./мл): - призначення дупілумабу зменшує частоту загострень, покращує легеневу функцію та якість життя (Рівень доказовості А) |
|
Інші протизапальні препарати |
• Терапія статинами з метою запобігання загостренням у пацієнтів із ХОЗЛ не рекомендована (Рівень доказовості А). • Симвастатин не запобігає розвитку загострень ХОЗЛ у пацієнтів із підвищеним ризиком їх виникнення і без показань для статинотерапії (Рівень доказовості А). Однак обсерваційні дослідження показали, що застосування статинів може мати позитивний ефект у деяких пацієнтів із ХОЗЛ, які приймають їх у зв’язку з наявністю в них кардіоваскулярної і метаболічної патології (Рівень доказовості С). • Застосування антагоністів лейкотрієнів у пацієнтів із ХОЗЛ належним чином не вивчали |
ІКС: дані in vitro свідчать про те, що запалення, пов'язане з ХОЗЛ, є обмежено чутливим до КС. Більше того, деякі ліки, у тому числі β2-агоністи, теофілін або макроліди, можуть частково сприяти чутливості до КС при ХОЗЛ [964, 965]. Клінічна значущість цього ефекту ще не встановлена повністю. Дані in vivo свідчать також, що залежність «доза–ефект» і довгострокова (>3 років) безпека застосування ІКС у пацієнтів із ХОЗЛ є не до кінця зрозумілими і потребують подальшого дослідження [962]. Оскільки ефекти ІКС при ХОЗЛ можуть модулюватися супутнім застосуванням бронходилататорів тривалої дії, ці два терапевтичні варіанти розглядають окремо. Як нинішні, так і колишні курці з ХОЗЛ можуть отримувати користь від застосування ІКС з точки зору функції легень і частоти загострень, хоча величина такої ефективності є меншою в затятих курців або нинішніх курців порівняно з колишніми або з тими, хто не курить багато [496, 966].
ІКС в комбінації з БАТД (ІКС+БАТД): у пацієнтів із середньої тяжкості та дуже тяжким перебігом ХОЗЛ і загостреннями комбінація ІКС та БАТД є ефективнішою тактикою лікування, ніж монотерапія цими засобами окремо. Комбінована терапія сприяє поліпшенню функції легень, загального стану здоров’я та зменшенню кількості загострень [971, 972]. Фактори, які треба враховувати, починаючи лікування ІКС у комбінації з одним або двома бронходилататорами тривалої дії, наведено на рисунку 9 [584].
Рис. 9. Важливі фактори перед початком терапії ІКС
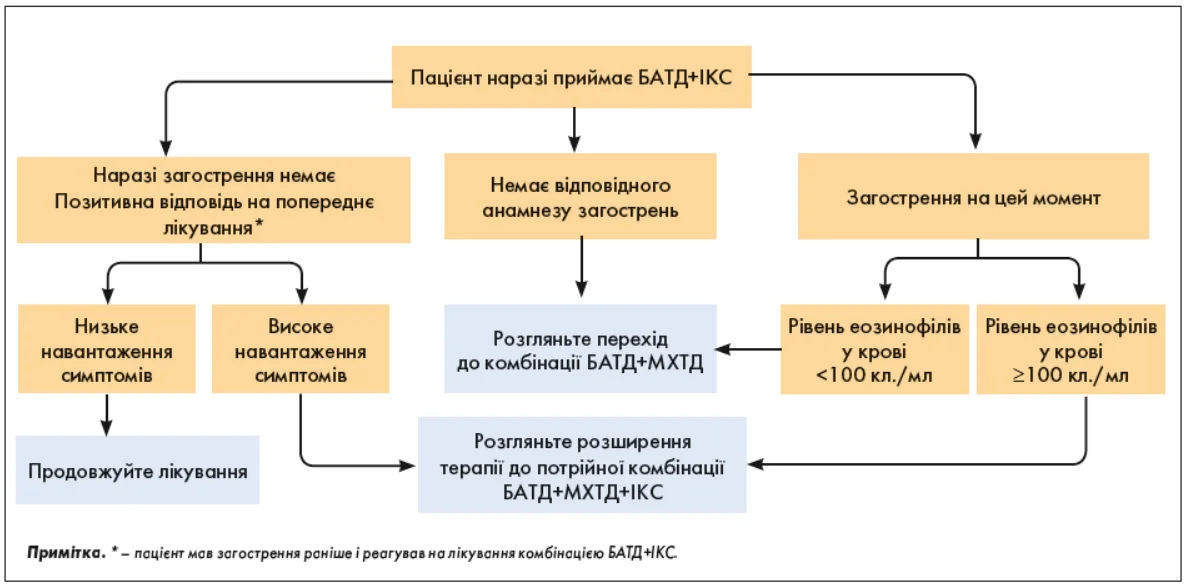
Лікування пацієнтів, які наразі приймають комбінацію БАТД+ІКС: загалом, якщо є показання для застосування ІКС, то фіксована комбінація БАТД+ МХТД+ІКС виявляється ефективнішою, ніж БАТД+ІКС (рис. 10).
Рис. 10. Ведення пацієнтів, які приймають комбінацію БАТД+ІКС
Трикомпонентною комбінацією (БАТД+МХТД+ІКС): крок вище – перехід на потрійну інгаляційну терапію – БАТД+МХТД+ІКС – може відбуватися за допомогою різних підходів [1002] і, як було показано, поліпшує функцію легень, результати лікування, про які повідомляли самі пацієнти, і зменшує кількість загострень у порівнянні з монотерапією БАТД, або комбінаціями БАТД+МХТД чи БАТД+ІКС [493, 495, 496, 1003-1010]. Ретроспективний аналіз одного з РКД, в якому оцінювали ефекти комбінації БАТД+МХТД+ІКС, показав, що потрійна інгаляційна терапія поліпшує клінічні результати в порівнянні з подвійною незалежно від статусу куріння [1011].
Розділ 4. Лікування загострень ХОЗЛ
Ключові положення
- Загострення ХОЗЛ визначають як стан, що характеризується задишкою та/або кашлем і виділенням мокротиння, які погіршуються протягом <14 днів. Загострення ХОЗЛ часто пов'язані з посиленням місцевого і системного запалення, спричиненого інфекцією дихальних шляхів, впливом полютантів або інших негативних факторів на легені.
- Оскільки симптоми загострення ХОЗЛ не є специфічними, потрібно розглянути відповідні диференційні діагнози, зокрема пневмонію, застійну серцеву недостатність і тромбоемболію легеневої артерії.
- Метою лікування загострень ХОЗЛ є мінімізація негативного впливу поточного загострення та запобігання подальшим епізодам.
- Як початкову терапію для лікування загострення ХОЗЛ рекомендують БАКД з короткодіючими антихолінергічними препаратами або без них.
- Підтримуючу терапію бронходілататорами тривалої дії треба розпочати якомога швидше. У пацієнтів із частими загостреннями та підвищеним рівнем еозинофілів у крові необхідно розглянути можливість додавання ІКС до схеми подвійної бронходилатаційної терапії (трикомпонентна інгаляційна терапія).
- У пацієнтів із тяжкими загостреннями системні КС можуть поліпшити функцію легень (ОФВ1), оксигенацію та скоротити час відновлення, у тому числі перебування у стаціонарі. Тривалість такої терапії зазвичай не має перевищувати 5 днів.
- Призначення антибактеріальних препаратів може пришвидшити одужання, зменшити ризик раннього рецидиву загострення, а також неефективності лікування. Тривалість терапії має становити 5 днів.
- Метилксантини не рекомендуються через підвищений профіль побічних ефектів.
- Неінвазивна механічна вентиляція має бути першим режимом вентиляції, що застосовують у пацієнтів із ХОЗЛ та гострою дихальною недостатністю, які не мають абсолютних протипоказань, оскільки такий метод вентиляції поліпшує газообмін, зменшує роботу дихання і необхідність інтубації, скорочує тривалість госпіталізації та поліпшує виживаність.
- Тривалість відновлення після загострення ХОЗЛ варіює від 4 до 6 тиж, при цьому деякі пацієнти не можуть повернутися до функціонального стану, який був до загострення. Після загострення треба вжити відповідних заходів для його профілактики.
Фармакотерапія загострень
Для лікування загострень ХОЗЛ найчастіше використовують три класи препаратів — бронходилататори, КС і антибіотики.
Бронходилататори
Для початкового лікування загострення ХОЗЛ рекомендовано застосування БАКД із МХКД або без них, хоча і немає високоякісних доказів такої тактики відповідно до РКД [1288, 1342]. За результатами систематичного огляду щодо шляхів уведення короткодіючих бронходилататорів не було виявлено суттєвих відмінностей значень ОФВ1 залежно від способу інгаляції препарату – чи то дозовані інгалятори (ДІ) (зі спейсером або без нього), чи небулайзери [592, 1343], хоча останній може бути зручнішим для більш тяжких пацієнтів. Щоб не застосовувати безперервну небулайзерну терапію, рекомендують використовувати ДІ – 1 або 2 вдихи кожну годину (2 або 3 рази), а потім кожні 2-4 год залежно від відповіді пацієнта на терапію.
Хоча клінічних досліджень, в яких би оцінювали застосування інгаляційних бронходилататорів тривалої дії (БАТД, МХТД або їх комбінації) з або без ІКС під час загострення, немає, рекомендовано продовжувати лікування такими комбінаціями під час загострення або розпочати їх застосування якомога швидше перед випискою з лікарні. Внутрішньовенне введення метилксантинів (теофіліну або амінофіліну) не рекомендовано пацієнтам із загостреннями ХОЗЛ через значні побічні ефекти [1344, 1345]. При тяжких загостреннях ХОЗЛ, якщо для доставки бронходилататора обрано небулайзер, перевагу потрібно віддавати таким небулайзерам, які працюють через струмені повітря, а не кисню, щоб уникнути потенційного ризику підвищення PaCO2 [1346].
Кортикостероїди
Результати досліджень (переважно проведених в умовах стаціонару) свідчать, що системні КС при загостренні ХОЗЛ скорочують час відновлення та покращують функцію легень (ОФВ1), оксигенацію [1347-1350], знижують ризик раннього рецидиву загострення, невдачі лікування [1351] і тривалість госпіталізації [1347, 1349, 1352]. Рекомендована доза системних КС становить 40 мг на добу за преднізолоном протягом 5 днів [1353]. Обсерваційне дослідження демонструє, що триваліші курси пероральних КС при загостренні ХОЗЛ пов'язані з підвищеним ризиком пневмонії та смертності [1354]. Пероральне застосування КС є так само ефективним, як і внутрішньовенне введення [1355]. Небулізований будесонід може бути хорошою альтернативою для лікування загострень у деяких пацієнтів [1348, 1356, 1357] і забезпечує переваги, подібні до внутрішньовенного метилпреднізолону, вибір між цими варіантами залежатиме від економічної вартості [1358, 1359]. Навіть короткочасне застосування КС пов'язане з подальшим підвищенням ризику пневмонії, сепсису та смерті [1360], тому їх застосування необхідно обмежувати в пацієнтів із тяжкими загостреннями.
Останні дослідження демонструють, що КС можуть бути менш ефективними в лікуванні загострень ХОЗЛ у пацієнтів із нижчим рівнем еозинофілів у крові [487, 1320, 1323, 1361], і необхідні подальші дослідження стероїд-зберігаючих схем лікування. Подвійне сліпе плацебо-контрольоване РКД STARR2 (Steroids in Acute Exacerbations of Chronic Respiratory Disease, Round 2), в якому оцінювали ефективність короткого курсу преднізолону, спираючися на рівень еозинофілів у крові під час загострення ХОЗЛ, показало, що ця стратегія не поступається стандартному підходу, який передбачає лікування системним преднізолоном (30 мг на добу протягом 14 днів), і дає можливість на 33% зменшити частку пацієнтів, що отримують преднізолон [1362]. Автори дослідження дійшли висновку, що преднізолон можна безпечно призначати за умови врахування рівня еозинофілів у крові і такий підхід дає змогу зменшити системне використання КС у клінічній практиці [1362].
Антибіотики
Інфекційні збудники при загостренні ХОЗЛ можуть бути як вірусними, так і бактеріальними (1311, 1363), однак доцільність застосування антибіотиків при загостренні залишається суперечливою (352, 1364, 1365). Така невизначеність є наслідком того, що в дослідженнях часто не розрізняли бронхіт (гострий або хронічний) і загострення ХОЗЛ. Крім того, дослідження проводили без плацебо-контролю та/або рентгенографії органів грудної клітки, а це не виключало того, що пацієнти могли вже мати супутню пневмонію. Існують дані, які підтверджують доцільність застосування антибіотиків при загостреннях, коли пацієнти мають клінічні ознаки бактеріальної інфекції, наприклад посилення гнійного характеру мокроти [352, 1365]. І насправді, динаміка характеру і кольору мокротиння (білий або прозорий) допомагає коригувати антибіотикотерапію (АБТ) без побічних ефектів. З іншого боку, спостереження за ступенем гнійного характеру мокротиння має чутливість 94,4% і специфічність 52% щодо високого бактеріального навантаження, що вказує на причинно-наслідковий зв'язок (352).
Систематичний огляд плацебо-контрольованих досліджень показав, що призначення АБТ знижує ризик ранньої смертності на 77%, невдач лікування на 53% і гнійного характеру мокроти на 44% (1366). Огляд демонструє докази ефективності лікування антибіотиками пацієнтів із загостренням ХОЗЛ середнього або тяжкого ступеня і посиленням кашлю і гнійного характеру мокроти (1366, 1367). Ці дані підтверджуються більшою кількістю РКД, проведених за участю пацієнтів із ХОЗЛ середньої тяжкості (1368). У РКД додавання доксицикліну до пероральних КС в амбулаторних умовах не збільшувало час до настання наступного загострення (1369). В амбулаторних умовах культуральне дослідження мокроти є недоцільним, оскільки займає щонайменше 2 дні і часто не дає надійних результатів через технічні причини.
Вивчають кілька біомаркерів інфекції дихальних шляхів у разі загострення ХОЗЛ, які мають кращий діагностичний профіль. Раніше дослідження рівня С-реактивного білка (СРБ) давали суперечливі результати (1370, 1371), але в рандомізованому дослідженні у Великій Британії було виявлено значне зменшення кількості призначень антибіотиків на первинній ланці без погіршення результатів лікування в пацієнтів із ХОЗЛ, яким антибіотики призначали на основі рівня СРБ, що визначали на місці звернення (1372). Інше дослідження в пацієнтів, госпіталізованих із приводу загострення ХОЗЛ у Нідерландах, дало подібні результати (зменшення використання антибіотиків без збільшення кількості невдалих випадків лікування). Ці результати потребують підтвердження в інших умовах, перш ніж можна буде рекомендувати загальне застосування цього підходу. Однак отримані дані свідчать, що використання антибіотиків можна безпечно зменшити із 77,4% до 47,7%, якщо рівень СРБ є низьким (1373).
Визначення рівня прокальцитоніну – маркера гострої фази запалення та інфекції – досліджували з метою з’ясування доцільності застосування антибіотиків при загостренні ХОЗЛ (1374). Ефективність цього біомаркера є суперечливою. Кілька досліджень, проведених переважно в амбулаторних умовах, показали, що лікування антибіотиками, доцільність призначення яких заснована на визначенні рівня прокальцитоніну, зменшує ризик побічних ефектів при збереженні клінічної ефективності (1375-1377). Систематичний огляд і метааналіз врахування рівня прокальцитоніну в госпіталізованих пацієнтів із загостренням ХОЗЛ не виявив значного зниження загального впливу антибіотиків (1378).
У пацієнтів із загостренням ХОЗЛ, які лікувалися в умовах інтенсивної терапії, визначення рівня прокальцитоніну для вирішення питання про початок або припинення АБТ було пов'язано з вищим рівнем смертності в порівнянні з пацієнтами, які отримували стандартні схеми АБТ (1379). Такі суперечливі результати не дають підстав рекомендувати визначення прокальцитоніну для прийняття рішення щодо застосування антибіотиків у пацієнтів із загостренням ХОЗЛ; необхідні подальші дослідження з використанням чіткої методології.
Отже, антибіотики треба призначати пацієнтам із загостреннями ХОЗЛ, які мають 3 основні симптоми: посилення задишки, збільшення об'єму мокротиння та його гнійний характер або 2 з основних симптомів, якщо одним із двох симптомів є посилення гнійного характеру мокроти, або потребують штучної вентиляції легень (ШВЛ) (інвазивної або неінвазивної) (1294, 1311). Метааналіз продемонстрував, що лікування антибіотиками протягом ≤5 днів має таку саму клінічну та бактеріологічну ефективність, як і традиційне більш тривале лікування амбулаторних пацієнтів із загостреннями ХОЗЛ. Крім того, коротший термін застосування антибіотиків може зменшити ризик розвитку резистентності до антимікробних препаратів та ускладнень, пов'язаних з АБТ. Рекомендована тривалість АБТ становить 5-7 днів (1380). Для амбулаторного лікування загострень ХОЗЛ – ≤5 днів (1379, 1381).
Вибір конкретного антибіотика має ґрунтуватися на даних щодо місцевої антибіотикорезистентності бактерій. Зазвичай початкове емпіричне лікування – це амінопеніцилін із клавулановою кислотою, макролід, тетрациклін або, в окремих пацієнтів, фторхінолон. У пацієнтів із частими загостреннями, тяжким перебігом ХОЗЛ (1382, 1383) та/або загостреннями, що потребують ШВЛ (1384), треба проводити культуральне дослідження мокроти або інших матеріалів, отриманих із легень, оскільки можуть бути наявні грамнегативні бактерії (наприклад, види Pseudomonas) або резистентні патогени, не чутливі до вищезазначених антибіотиків. Шлях уведення (пероральний або внутрішньовенний) залежить від здатності пацієнта приймати їжу та фармакокінетики антибіотика, хоча перевагу віддають пероральному застосуванню. Зменшення задишки і гнійного характеру мокроти свідчить про клінічний успіх лікування.
Додаткові методи лікування
Залежно від клінічного стану пацієнта необхідно розглянути можливість забезпечення належного балансу рідини, застосування діуретиків за клінічними показаннями, антикоагулянтів, лікування супутніх захворювань і збалансованого харчування. Серед пацієнтів із ХОЗЛ, госпіталізованих із підозрою на загострення, у 5,9% було виявлено тромбоемболію легеневої артерії (1299). Отже, госпіталізовані пацієнти з ХОЗЛ мають підвищений ризик тромбозу глибоких вен і тромбоемболії легеневої артерії (1385, 1386), тому потрібні профілактичні заходи проти цієї категорії ускладнень (1387, 1388). Медичні працівники мають постійно наголошувати на необхідності відмови від куріння.
Профілактика загострень ХОЗЛ
Після загострення ХОЗЛ необхідно вжити відповідних заходів для запобігання подальшим епізодам. У клінічних дослідженнях було продемонстровано значний вплив на ризик/частоту загострень певних методів лікування (табл. 5). Детальнішу інформацію дивіться в розділі 3.
|
Таблиця 5. Методи лікування, що знижують частоту загострення ХОЗЛ |
|
|
Клас засобів |
Представники |
|
Бронходилататори |
БАТД МХТД Комбінація БАТД+МХТД |
|
ІКСумісна терапія |
Комбінація БАТД+ІКС Комбінація БАТД+МХТД+ІКС |
|
Протизапальні засоби (не стероїдні) |
Рофлуміласт Дупілумаб |
|
Антиінфекційні препарати |
Вакцини Тривале застосування макролідів |
|
Мукорегулятори |
Nацетилцистеїн Карбоцистеїн Ердостеїн |
|
Інші варіанти |
Відмова від куріння Легенева реабілітація Редукція легеневого об’єму Вітамін D Захисні заходи (носіння масок, мінімізація соціальних контактів, часте миття рук) |
Список літератури – у редакції.
Реферативний огляд Global Initiative for Chronic Obstructive Lung Disease (2025 REPORT).
Підготувала Анна Артюх
Друкується в скороченому обсязі, повну версію дивіться: https://goldcopd.org/
Тематичний номер «Пульмонологія. Алергологія. Риноларингологія» №3-4 (71-72), 2025 р.