20 січня, 2023
Особливості функціональної патології гастродуоденальної системи у дітей: принципи профілактики і терапії
 29-30 вересня 2022 р. у Дніпрі в онлайн-режимі відбулася Науково-практична конференція з міжнародною участю «ХІV Український гастроентерологічний тиждень». Цей захід об’єднав провідних вчених з усіх куточків України та світу. Однією з обговорюваних у ході пленарних засідань тем стала діагностика, лікування та профілактика захворювань органів травлення у дітей. Із доповіддю «Особливості функціональної патології гастродуоденальної системи у дітей: принципи профілактики і терапії» виступила голова Харківської обласної асоціації дитячих гастроентерологів і нутриціологів України, завідувачка кафедри педіатрії та дитячої гастроентерології Харківської медичної академії післядипломної освіти, доктор медичних наук, професор Ольга Юріївна Бєлоусова.
29-30 вересня 2022 р. у Дніпрі в онлайн-режимі відбулася Науково-практична конференція з міжнародною участю «ХІV Український гастроентерологічний тиждень». Цей захід об’єднав провідних вчених з усіх куточків України та світу. Однією з обговорюваних у ході пленарних засідань тем стала діагностика, лікування та профілактика захворювань органів травлення у дітей. Із доповіддю «Особливості функціональної патології гастродуоденальної системи у дітей: принципи профілактики і терапії» виступила голова Харківської обласної асоціації дитячих гастроентерологів і нутриціологів України, завідувачка кафедри педіатрії та дитячої гастроентерології Харківської медичної академії післядипломної освіти, доктор медичних наук, професор Ольга Юріївна Бєлоусова.
– Захворювання шлунково-кишкового тракту (ШКТ) посідають провідне місце в структурі хронічної патології дитячого віку. Найпоширенішою патологією ШКТ у дітей є функціональні гастродуоденальні порушення, які зустрічаються із частотою 85-90% (S. Mahadeva, K.L. Goh, 2006; С.М. Ткач, 2017). Класичним проявом гастродуоденальної дисфункції у дітей є диспепсія. Тривалий час під терміном «диспепсія» (від грец. dys – порушення, peptein – перетравлювати) розуміли порушення перетравлювання. Значення цього терміну завжди було предметом суперечок та маніпуляцій. Сьогодні відомо, що диспепсія не є специфічним синдромом і може зустрічатися при різноманітних структурних та функціональних видах патології ШКТ, а також виникати на тлі багатьох негастроентерологічних захворювань. Варто зауважити, що у більш ніж 50% випадків диспепсія має функціональний характер та не супроводжується будь-якими органічними змінами; у менш як 50% дітей скарги на диспепсію зумовлені наявністю органічної патології, найчастіше це виразкова або гастроезофагеальна рефлюксна хвороба (ГЕРХ; V. Stanghellini, F.K.L. Chan, 2016).
Часто практикуючим лікарям доводиться проводити диференційну діагностику функціональної диспепсії (ФД) та хронічного гастриту (ХГ). Обидва ці захворювання є самостійними нозологічними формами. На відміну від ХГ, який є органічним процесом, що характеризується наростаючою атрофією залозистого епітелію та секреторною недостатністю, ФД не має морфологічного субстрату, зазвичай не прогресує та має сприятливий перебіг. Поєднання цих двох діагнозів є неприпустимим, оскільки тим самим порушується сам фундамент, на якому базується вчення про функціональні розлади ШКТ, та позбавляється сенсу розмежування функціональної й органічної диспепсії.
Патофізіологія ФД
Патофізіологія ФД є складною, мультифакторіальною та не до кінця вивченою. У результаті проголошення Римського консенсусу IV комітетом експертів, який займається питаннями диспепсії, вперше було акцентовано увагу на тому, що функціональні захворювання ШКТ є групою розладів, які характеризуються порушенням взаємодії центральної нервової системи (ЦНС) та периферичної ланки нервової системи, що забезпечує діяльність органів ШКТ (вісь «головний мозок – кишечник»). У такий спосіб було підкреслено домінуючий внесок ЦНС у розвиток симптомів ФД.
Згідно з Римськими критеріями IV, розрізняють такі клінічні варіанти ФД:
- постпрандіальний дистрес-синдром (ПДС), що характеризується виникненням диспепсичної симптоматики, індукованої прийомом їжі;
- епігастральний больовий синдром (ЕБС), для якого характерним є наявність болю та відчуття печії в ділянці епігастрія, що можуть виникати одразу після прийому їжі, але також можуть і зникати після прийому їжі або відзначатися натщесерце;
- синдром «перехресту» ПДС та ЕБС, або overlap-синдром, для якого характерним є як наявність диспепсичних симптомів, індукованих прийомом їжі, так і епігастрального болю та/або печії.
Важливо, що незалежно від варіанту, постійні симптоми ФД є причиною емоційного дистресу та зниження працездатності, що чинить неабиякий вплив на якість життя дитини (N.G. Talley et al., 2015; D.A. Drossman et al., 2016; V. Stanghellini et al., 2016).
Незважаючи на численні дослідження у цій галузі, сьогодні все ще недостатньо даних про усі патогенетичні ланки, які лежать в основі виникнення ФД (D.A. Drossman et al., 2016). Відомо, що на розвиток ФД впливають такі фактори, як гіперсекреція соляної кислоти, психогенні чинники, порушення моторики, зниження чутливості шлунку до розтягнення, аліментарні чинники та порушення функції підшлункової залози (ПЗ). При цьому нерідко спостерігають поєднання кількох факторів, що значно ускладнює перебіг ФД.
Що стосується клінічного перебігу ФД, то єдиної специфічної скарги у пацієнтів не існує. Натомість у понад 99% пацієнтів зустрічається більше 2 симптомів ФД, а у 80% випадків може виникати 5 та більше проявів ФД одночасно (M.A. Benninga et al., 2016). Тому нерідко в одного пацієнта можна побачити цілу гаму функціональних розладів (рис. 1), серед яких буває складно виділити провідний. 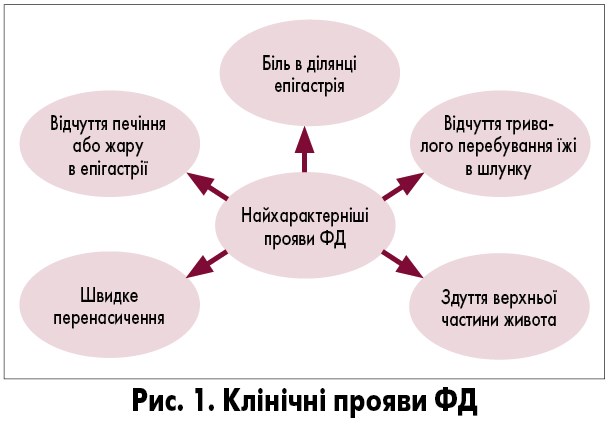
Мінливість клінічної картини, у тому числі у пацієнтів із поєднанням функціональних порушень, зокрема ФД + синдром подразненого кишечнику (СПК), ФД + ГЕРХ або ФД + біліарна дисфункція, вимагає від практикуючого лікаря постійного перегляду та корекції призначеної схеми лікування.
Окрім різноманіття гастроентерологічних та негастроентерологічних скарг, відмінною особливістю ФД є наявність психоневрологічних розладів (M. Kanazava et al., 2004). Зокрема, скарги пацієнтів можуть бути такими, що відповідають проявам різних синдромів нейроциркулярної дистонії, як-от кардіалгічного, респіраторного, астенічного, цефалгічного тощо. Потрібно пам’ятати, що успіх лікування таких пацієнтів, а також досягнення комплаєнтності багато в чому залежить від психоемоційних та соціально-побутових чинників і ситуацій.
Практичний досвід і результати пролонгованих досліджень показують, що тривалий перебіг функціональних гастроінтестинальних розладів та відсутність контролю лікування можуть призводити до розвитку значних порушень у подальшому. Однак діагностика ФД часто викликає значні труднощі, що призводить до призначення великої кількості непотрібних обстежень та є причиною поліпрагмазії. У рекомендаціях Європейського товариства дитячих гастроентерологів, гепатологів і нутриціологів (European Society for Pediatric Gastroenterology, Hepatology and Nutrition; ESPGHAN) наголошується, що ФД, як і усі функціональні порушення, є доброякісним станом, а тому її корекція повинна бути відповідною. З позиції доказової медицини ефективне медикаментозне лікування ФД передбачає призначення прокінетиків, спазмолітиків, антисекреторних препаратів, антацидів, гастропротекторів, седативних засобів та ферментів ПЗ (рис. 2).
Патогенетичне обґрунтування призначення препаратів ферментів ПЗ
Як відомо, гіперсекреція соляної кислоти у шлунку може спричинити відносну недостатність вироблення ферментів ПЗ. Окрім цього, через закислення дванадцятипалої кишки можуть інактивуватися ферменти, які вже надійшли з ПЗ. Іншими причинами недостатності ферментів ПЗ є розведення їх концентрації у просвіті кишки, швидкий транзит хімусу через ШКТ або порушення процесів змішування ферментів із хімусом у результаті дискінезії шлунку та дванадцятипалої кишки. Тому наявність відносної недостатності ПЗ у пацієнтів із ФД є показанням до призначення препаратів ферментів ПЗ.
Жирна та надмірно оброблена їжа, часте переїдання, перекуси, хронічний стрес та висока калорійність раціону мають значний вплив на розвиток функціональних розладів ШКТ у дитячому віці. Як боротися з порушеннями харчової поведінки? Перш за все необхідно оптимізувати харчовий раціон дитини. Проте в умовах уже існуючої хвороби та наявності зовнішньосекреторної недостатності ПЗ доцільним є призначення ферментних препаратів.
Раніше при відносній недостатності екзокринної функції ПЗ рекомендували дотримання дієти з обмеженням жирів. Як наслідок, мальнутриція прогресувала (D. de la Iglesia-Garcia et al., 2017). Переломним моментом стала поява ферментних препаратів з кишково-розчинною оболонкою, які стали основою менеджменту екзокринної недостатності ПЗ. Зокрема, згідно з міжнародними рекомендаціями, при лікуванні таких пацієнтів основним завданням є усунення стеатореї не за рахунок обмеження прийому жирів, які необхідні для забезпечення всмоктування жиророзчинних вітамінів, а за допомогою призначення ферментної замісної терапії (S. Sankararaman et al., 2019). Це дозволило наблизити засвоєння жирів до нормального рівня (S. Pongprasobchai et al., 2013).
Отож, ферментотерапія екзокринної недостатності ПЗ дозволяє запобігти нутритивному, вітамінному та мінеральному дефіциту. При цьому вибір ферментного препарату повинен базуватися на можливості максимально наблизити процеси перетравлення до фізіологічного рівня. Ферменти препарату повинні мати здатність добре перемішуватися з їжею і потрапляти у дванадцятипалу кишку одночасно з хімусом. Найточніше цим вимогам відповідають ферментні препарати, гастрорезистентні капсули яких містять мінімікротаблетки діаметром до 2 мм (J.M. Lohr et al., 2009; J.E. Dominguez-Munoz et al., 2011). Особливе місце серед цих препаратів посідає лікарський засіб Мезим® капсули. Завдяки можливості розкриття капсули, препарат зручно дозується, а його застосування є безпечним у дітей усіх вікових груп. Згідно з інструкцією, для немовлят або дітей, яким важко ковтати капсулу, її можна відкрити та змішати необхідну кількість мікрочастинок (мінімікротаблеток препарату Мезим® капсули) з невеликою кількістю їжі (грудного молока, фруктового пюре тощо) та давати дитині з ложки безпосередньо перед годуванням. Особливістю сучасних ферментних препаратів є їх активація у тонкій кишці та, відповідно, відсутність впливу на функціональну активність ПЗ. Тривала терапія сучасними ферментними препаратами не пригнічує продукцію власних ферментів ПЗ, про що свідчить сталий рівень еластази-1 на тлі прийому препарату Мезим® капсули.
Застосування ферментних препаратів при функціональних гастроінтестинальних порушеннях сприяє нормалізації травлення та покращує моторику кишечнику.
Лікувальна доза препарату Мезим® капсули підбирається індивідуально, а добова залежить від тяжкості екзокринної недостатності ПЗ. Рекомендованою дозою для дітей віком до 4 років є 1000 ОД ліпази на 1 кг маси тіла на добу. Для дітей старше 4 років – 500 ОД ліпази на 1 г жирів у добовому обсязі їжі. Рекомендована доза препарату Мезим® капсули для дітей шкільного віку та підлітків становить 10 000-25 000 ОД на прийом їжі (E. de Madaria et al., 2013; J. Toouli et al., 2010).
Підготувала Ольга Гуйванюк
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3(65)-4(66) 2022 р.




