24 січня, 2023
Надлишкова вага та ожиріння в умовах стресу: ігнорувати чи реагувати?
Актуальність проблеми зайвої ваги та ожиріння важко переоцінити. Починаючи з 1980 року їх поширеність у світі зросла вдвічі і тепер охоплює приблизно третину населення планети. Рівень ожиріння різко виріс в обох статей і в усіх вікових групах, особливо серед осіб молодого віку і жінок.  На жаль, Україна не стала винятком, що пов’язано, зокрема, з пандемією COVID‑19, яка негативно позначилася на рівні фізичної активності популяції. Війна та вплив хронічного стресу також внесли свій вклад у поширеність ожиріння та супутніх проблем зі здоров’ям.
На жаль, Україна не стала винятком, що пов’язано, зокрема, з пандемією COVID‑19, яка негативно позначилася на рівні фізичної активності популяції. Війна та вплив хронічного стресу також внесли свій вклад у поширеність ожиріння та супутніх проблем зі здоров’ям.
Надлишкова вага та ожиріння в умовах хронічного стресу стали темою доповіді старшої наукової співробітниці, керівниці відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), докторки медичних наук Любові Костянтинівни Соколової і завідувачки кафедри акушерства та гінекології № 2 Вінницького національного медичного університету ім. М.І. Пирогова, професорки, докторки медичних наук Ольги Василівни Булавенко. Доповідь прозвучала на черговому засіданні освітнього проєкту «Школа ендокринолога».
Для формування правильного підходу до ведення пацієнтів із надлишковою вагою та ожирінням необхідно насамперед розуміти, що собою являє жирова тканина (ЖТ) в людському організмі та які функції вона виконує.
В анатомії органи визначаються як макроскопічно розрізнені структури, які мікроскопічно складаються щонайменше з двох різних тканин, що взаємодіють для загальних функціональних цілей. Жировий орган відповідає цьому визначенню, оскільки він анатомічно відокремлений і складається з двох ЖТ: білої і бурої. Біла ЖТ розподіляється підшкірно і вісцерально, утворюючи жирові депо, i превалює в організмі дорослої людини, становлячи 15-40% від загальної маси тіла. Своєю чергою, бура ЖТ здебільшого локалізується в шийних, надключичних, паравертебральних, пахових ділянках і заочеревинному просторі, на неї припадає лише 0,1-0,5% маси тіла. ЖТ в організмі людини виконує низку важливих функцій, забезпечуючи термоізоляцію, механічний захист і зберігання енергії. Але однією з найважливіших і найцікавіших, із клінічної точки зору, є її ендокринна функція (Cypess A.M., 2022).
Білі та бурi адипоцити виділяють багато пептидних гормонів (адипокінів), біоактивних ліпідів (ліпокінiв) i молекул PHK з локальним (паракринним) і системним (ендокринним) впливом на мозок, β-клітини підшлункової залози, печінку, скелетні м’язи і серцево-судинну систему. Продукція та секреція адипокінів і ліпокінiв залежить від енергетичного статусу ЖТ. Завдяки ендокринній дії ці фактори сприяють системному енергетичному метаболізму, регулюючи апетит, термогенез, метаболізм глюкози і ліпідний обмін.
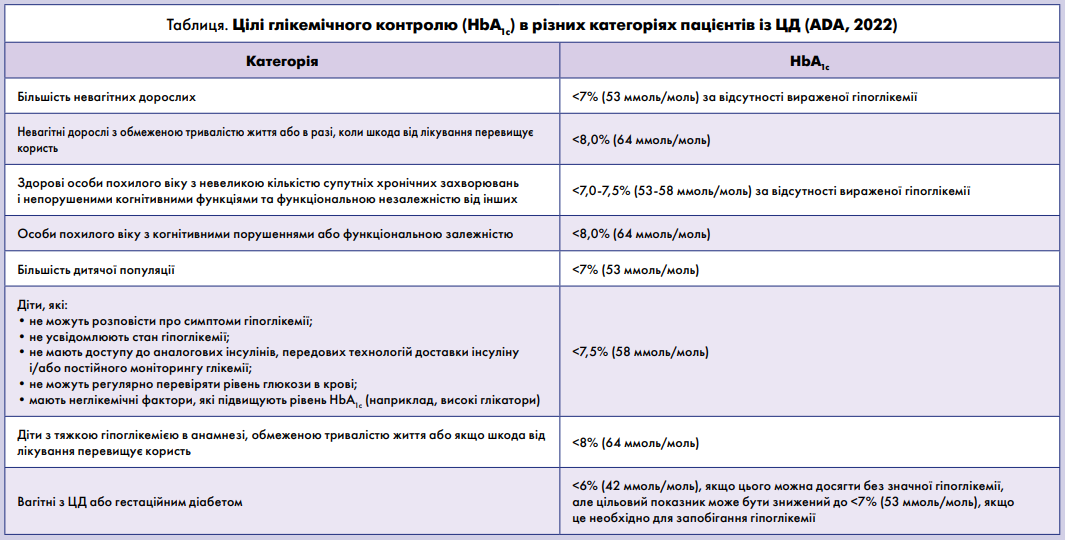
Ендокринні фактори, що їх у здоровому стані виділяють біла і бура ЖТ, підтримують функції органів і метаболічний гомеостаз (Scheja L. et al., 2019). При цьому клінічно значущий вплив ЖТ на організм зумовлений центральними гормонами ЖТ, до яких належать лептин, адипонектин. Регуляція передачі сигналів і реалізація біологічної функції гормонів ЖТ відбувається на різних рівнях, у тому числі і на рівні екзосомальної мікроРНК і ліпокінів, що в подальшому впливає на епігенетику. Саме тому варто говорити про прогностично негативний вплив ожиріння на функціонування деяких органів і систем у майбутньому. Детальніше функція та біологічний вплив кожного з гормонів, що секретує ЖТ, наведені в таблиці 1.
При ожирінні гіпертрофічні адипоцити й імунні клітини, які містяться в ЖТ, прискорюють формування хронічного прозапального профілю зі зміненою секрецією адипокінів і ліпокінів, що супроводжується метаболічним дисбалансом (Scheja L. et al., 2019).
Надлишок ЖТ супроводжується порушенням апетиту, гомеостазу глюкози, секреції інсуліну, функції β-клітин підшлункової залози з підвищенням ризику розвитку цукрового діабету (ЦД) 2 типу. Усе це відбувається на тлі неспецифічного запалення, що спричинює ремоделювання судин, впливає на серцево-судинний ризик і призводить до розвитку метаболічної жирової хвороби печінки. Саме тому лікар будь-якої спеціальності має ставитися до ожиріння як до системного хронічного захворювання, яке потребує обов’язкового лікування, а не як до косметично-естетичної проблеми.
Ожиріння – це не лише медико-соціальна, але й демографічна проблема, адже адипокіни – важливі регулятори репродуктивної функції у відповідь на зміни енергетичного балансу.
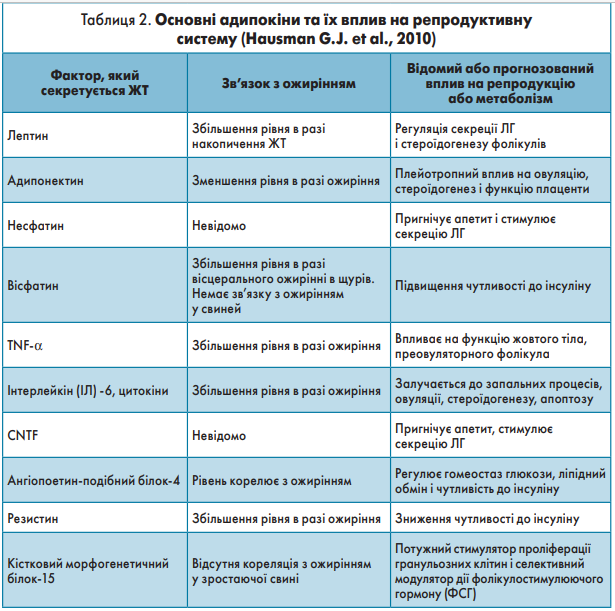
Так, лептин, ціліарний нейротрофічний фактор (CNTF) і несфатин посилюють секрецію лютеїнізуючого гормону (ЛГ) i пригнічують апетит. Крім того, лептин підвищує тонус симпатичної системи і тим самим регулює функцію адипоцитів. Лептин, адипонектин і фактор некрозу пухлини-α (TNF-α) безпосередньо впливають на функцію яєчників, тоді як ангіопоетин-подібний білок‑4, резистин i вiсфатин регулюють чутливість до інсуліну, гомеостаз глюкози і ліпідний обмін. Основні адипокіни та їх вплив на репродуктивну систему відображені в таблиці 2.
Таким чином, ЖТ є ендокринним органом, який впливає на репродуктивну вісь шляхом (Татарчук Т.Ф., 2021):
- ароматизації андрогенів в естрогени (з підтриманням ароматазних ферментів);
- метаболізму естрогенів у 17-гідроксильованих формах (високоактивні метаболіти) з підтриманням ферментів 17-гідроксистероїддегідрогенази;
- накопичення стероїдних гормонів;
- зниження синтезу секс-стероїд-зв’язувального глобуліну (СССГ) в печінці, тим самим підвищуючи рівень вільно циркулюючих андрогенів і естрогенів.
Ожиріння негативно впливає на жіночу фертильність і призводить до порушення менструального циклу, нерегулярної овуляції та тривалої відсутності зачаття. Пацієнткам із цією патологією важче завагітніти, навіть застосовуючи допоміжні репродуктивні технології. Так, жінки з ожирінням, які проходять через процедуру екстракорпорального запліднення, мають менші ооцити і нижчу ймовірність нормального запліднення. Метаболічний дисбаланс, спричинений надлишком ЖТ, впливає і на перебіг вагітності та пологів: у жінок з ожирінням класу III (індекс маси тіла (IMT) >40 кг/м2) ймовірність народження живої дитини на 50% нижча, ніж у жінок із нормальним ІМТ (Marquard et al., 2011; Shah et al., 2011).
Репродуктивна дисфункція при ожирінні зумовлена складним багатофакторним патогенезом, що призводить до формування замкненого кола. Однією з його складових є метаболічний дисбаланс, який спричиняє підвищення утворення активних форм кисню і розвитку оксидативного стресу. Останній стає причиною апоптозу гранульозних клітин, зниження рівня естрадіолу, росту і розвитку ооцитів, що безпосередньо впливає на якість ооцитів і призводить до негативних репродуктивних наслідків (Agromo Prasad S. et al., 2016).
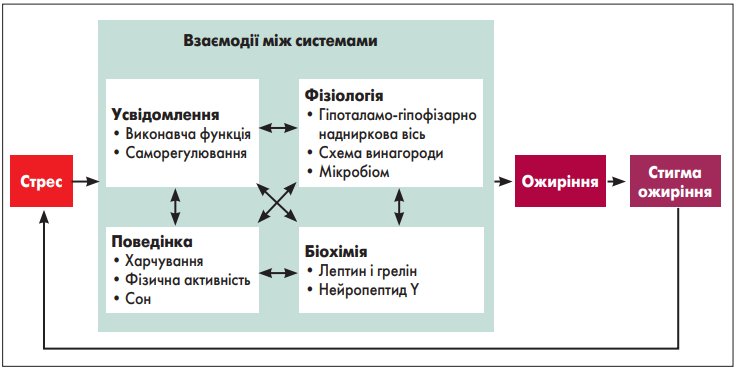
Іншою важливою складовою патогенезу зазначеного стану є стрес, зумовлений як впливом зовнішніх факторів (зміни довкілля, психоемоційний тиск, вимоги, пандемія, війна), так і власне стигмою ожиріння, яка супроводжується гіперкортизолемією, порушенням поведінкових реакцій, пов’язаних із харчуванням, і ще більше поглиблює метаболічний дисбаланс. Модель взаємозв’язку стресу й ожиріння відображена на рисунку 1.
Рис. 1. Стрес та ожиріння: модель взаємозв’язку (Tomiyama A.J., 2019).
Говорячи про взаємозв’язок стресу й ожиріння, не можна не згадати про посттравматичний стресовий розлад (ПТСР), який є гострою проблемою в умовах воєнного часу.
Відомо, що ПТСР призводить до центрального ожиріння, змін у мозку та, імовірно, змін рівнів гормонів апетиту (лептину, нейропептиду Y, грелiну, адипонектину, PP). Зміни в мозку, а також зміни рівнів гормонів апетиту можуть пояснювати зв’язок між ПТСР і центральним ожирінням. Своєю чергою, центральне ожиріння призводить до підвищення кров’яного тиску, рівнів маркерiв запалення і розвитку таких супутніх захворювань, як метаболічний синдром, ЦД, серцево-судинні захворювання та порушення репродуктивної функції (Farr O.M. et al., 2014).
Факторами, що погіршують перебіг ПТСР, є дієта, сімейний анамнез, стать, раса, прийом антипсихотиків і наявність супутньої психіатричної патології (депресія та ін.).
Дослідження харчової поведінки людей в умовах стресу показали, що особи, які початково мають надлишкову вагу або масу тіла на верхній межі норми, зазвичай більш схильні до збільшення ваги під час стресу, тоді як особи з нормальною або недостатньою вагою – ні. Так, 70% учасників проспективних досліджень повідомили про збільшення споживання їжі під час стресу, тоді як зниження апетиту спостерігали лише у 30% спостережуваних (Herhaus et al., 2020).
Під час стресу, незалежно від того, чи збільшується загальне споживання калорій, відбувається зміщення харчової поведінки в бік споживання «комфортної їжі», до якої належать солодощі, випічка, пікантні закуски. Це легко пояснюється, адже швидке всмоктування глюкози з цих продуктів супроводжується викидом ендорфінів і сприймається тілом як задоволення (Dallman M.F., 2010).
Ще одним фактором, що зумовлює прогресування ожиріння в умовах стресу, є хронічний дефіцит нічного сну (<6 год), який збільшує схильність до підвищення маси тіла й адипозопатії з більшим умістом вісцерального жиру. Підраховано, що на кожну втрачену годину сну підвищення IMT може становити 1,22 кг/м2.
Порушення сну супроводжується такими патогенетичними процесами (Kessler C., 2021):
- підвищенням рівня кортизолу;
- зміною центральних і периферичних сигнальних шляхів гормонів голоду;
- стимуляцією адипоцитами синтезу прозапальних цитокінів, оскільки зниження рівня мелатоніну автоматично призводить до гіперінсулінемії та зменшення чутливості тканин до інсуліну;
- зниженням рівнів гормонів насичення (лептину), тиреотропного гормону (ТТГ) й адипонектину – потужного протизапального гормону, який утворюється з жирів.
Реалізація негативного впливу стресу на організм відбувається через вісь гіпоталамус-гіпофіз-наднирники. Ця жорстко регульована система являє собою один із механізмів реагування організму на гострий і хронічний стрес. Тривалий стрес і/або неадекватна регуляція системи стресу можуть призвести до хронічного гіперкортицизму або, у деяких випадках, притуплення реакції кортизолу на стрес, що сприяє інсулінорезистентності, прогресуванню ожиріння та ЦД 2 типу (Gianotti I., 2021).
Ба більше, гострий і хронічний стрес через вісь гіпоталамус-гіпофіз-наднирники та ЦНС може посилити метаболічні порушення, підтримуючи запальний процес. ЖТ і запалення тісно взаємопов’язані, а хронічне запалення ЖТ призводить до інсулінорезистентності, коли надмірне збільшення вісцеральної білої ЖТ спричинює каскад біологічних процесів, зокрема мітохондріальну дисфункцiю, гіпоксію та загибель адипоцитів, які, як вважають, сприяють запаленню (Gianotti I., 2021).
Хронічні стресові ситуації, порушення сну та гіперстимуляція надниркових залоз або гіпоталамо-гіпофізарно-наднирникової системи призводять до підвищення рівня циркулюючого кортизолу. А це – головний чинник серед адипогенних ушкоджувальних факторів. Порушена (або згладжена) циркадна варіабельність рівня кортизолу прямо корелює з розподілом жиру у верхній частині тіла. Аномальні добові ритми кортизолу в разі нерегулярного графіка харчування підвищують ризик гіпертрофії вісцеральних адипоцитів (Kessler C., 2021).
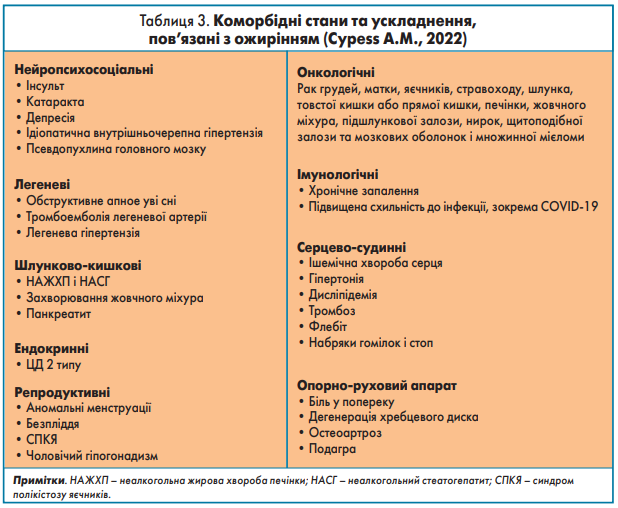
Усі ці патогенетичні процеси негативно відображаються на здоров’ї організму як системи і призводять до розвитку численних ускладнень і супутніх захворювань, пов’язаних з ожирінням (табл. 3).
З огляду на це, стає зрозуміло, що ожиріння – це хронічне комплексне багатофакторне прогресуюче рецидивне захворювання, яке потребує обов’язкового моніторингу і лікування. Лікар кожної спеціальності має виносити це захворювання в діагноз, тим самим наголошуючи на його впливі на здоров’я загалом.
Своєю чергою, зниження і контроль маси тіла при ожирінні супроводжується низкою позитивних наслідків для здоров’я та репродуктивної функції зокрема, а саме (Gill L. et al., 2021):
- покращенням фертильності;
- зниженням рівнів андрогенів;
- покращенням якості життя, пов’язаної зі станом здоров’я;
- підвищенням чутливості до інсуліну;
- профілактикою або досягненням ремiсiї ЦД 2 типу;
- зменшенням рівня глiкованого гемоглобіну;
- зниженням артеріального тиску;
- покращенням ліпідного профілю крові;
- зниженням ризику смерті від кардiоваскулярних причин;
- зменшенням тяжкості апное уві сні;
- зниженням ризику розвитку раку грудей;
- покращенням стану при НАЖХП;
- профілактикою або покращенням перебігу СПКЯ;
- зменшенням ризику розвитку онкогінекологічних захворювань;
- нормалізацією овуляції;
- зменшенням стресового нетримання сечі;
- зниженням ризику дисменореї;
- покращенням стану суглобів і зниженням ризику остеоартрозу.
У жінок з ожирінням для покращення перебігу СПКЯ рекомендується досягнення зниження маси тіла на 5-15%, при лікуванні безпліддя – зниження ваги на ≥10% спрямоване на збільшення ймовірності зачаття та живонародження (Garvey W. et al., 2016).
При цьому обов’язковою умовою успішного лікування ожиріння є комплексний підхід, що передбачає лікувальне харчування, фізичні вправи, поведінкову терапію, фармакотерапію, і, у крайньому разі, – баріартричну хірургію.
Однією з основних перешкод, що знижує прихильність пацієнтів до лікування ожиріння, є повторний набір втрачених кілограмів. Так, спостереження за пацієнтами, які втратили вагу за допомогою обмеження калоражу раціону і поведінкової психотерапії, виявило, що через 5 років вага поверталася до вихідних показників, незважаючи на обрану тактику модифікації життя (Wadden et al., 1993). При цьому повторне лікування ожиріння цими методами буде вже менш ефективним через адаптивні механізми.
Маса тіла суворо регулюється складною гомеостатичною системою, і потужні нейроендокринні механізми захищають організм від втрати ваги, унаслідок чого пояснюється понад 95% рецидивів (повторного набору ваги), які зазвичай пов’язані з поведінковою терапією ожиріння. Те саме спостерігають, коли відміняють фармакологічне лікування або виконують оборотну баріатричну операцію (Ogunleye M. et al., 2015; Karmall S. et al., 2013).
При цьому втрата ваги через обмеження калорій може спричинити реакцію організму у вигляді сповільнення метаболізму і зміни рівнів гормонів, що регулюють апетит (Jam Y.V. et al., 2016; Sumithran P. et al., 2011).
Саме тому лікар має сприяти припиненню фізіологічного «перетягування канату» між втратою і відновленням ваги за допомогою фармакотерапії. Згідно з міжнародними рекомендаціями щодо лікування надмірної ваги та ожиріння в дорослих, одночасна модифікація способу життя і фармакотерапія для довготривалого контролю ваги показана пацієнтам:
- з ІМТ ≥27 кг/м2 і такими коморбідними станами, як предіабет, ЦД, артеріальна гіпертензія (АГ), СПКЯ, обструктивне апное уві сні;
- з ІМТ ≥30 кг/м2.
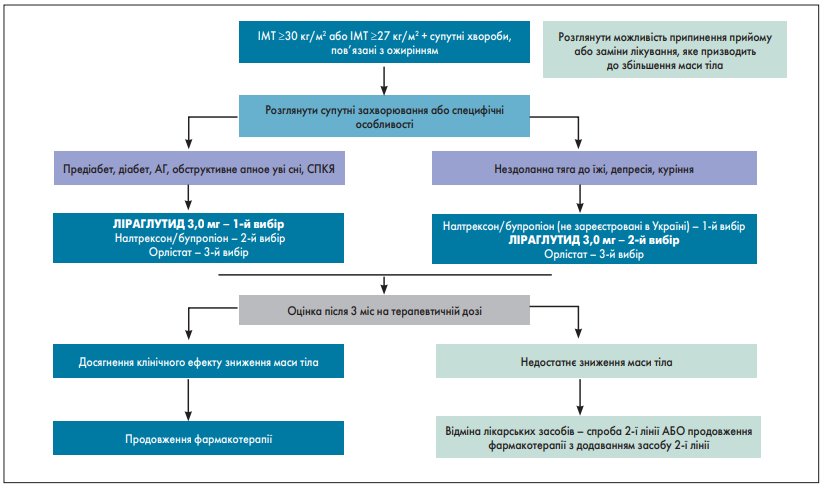
Ці показання відображені в рекомендаціях із лікування ожиріння в дорослих Американської асоціації клінічної ендокринології (AACE) / Американської колегії ендокринологів (ACE) і Канадських клінічних гайдлайнів із лікування ожиріння (рис. 2).
Рис. 2. Алгоритм фармакотерапії ожиріння згідно з рекомендаціями Канадських клінічних гайдлайнів із лікування ожиріння в дорослих
Поки налтрексон/бупропіон не зареєстрований в Україні, тому ключовим препаратом для лікування ожиріння, ефективним і безпечним, що підтверджено низкою клінічних рандомізованих досліджень, є ліраглутид у терапевтичній дозі 3,0 мг/добу. Препарат маркетується на ринку України фармацевтичною компанією Novo Nordisk під торговою назвою Саксенда®.
У дослідженні з ефективності та безпеки препарату Саксенда® SCALE MAINTENANCE взяли участь 422 пацієнти з ожирінням. Протягом 12-тижневого вступного періоду пацієнти мали втратити ≥5% початкової маси тіла за рахунок низькокалорійної дієти (від 1200 да 1400 ккал на день) і збільшення фізичних навантажень. Після цього учасники до низькокалорійної дієти та фізичних вправ додатково отримували або препарат Саксенда® 3,0 мг/добу, або плацебо (контроль) протягом року.
У результаті було встановлено, що застосування ліраглутиду (Саксенда®) в дозі 3,0 мг/добу сприяє додатковій втраті ваги на 6,2%, порівняно з 0,2% у групі плацебо, та утриманню результату зниження маси тіла, досягнутому при застосуванні дієти і фізичних вправ. 81% осіб з ожирінням, рандомізованих у групу застосування препарату Саксенда® + дієта і фізичні вправи, зберегли втрату ваги на рівні ≥5% порівняно з 49% осіб у групі плацебо + дієта і фізичні вправи (Wadden T.A. et al., 2013).
Ще одним об’єктивним параметром, що свідчить про клінічну ефективність препарату Саксенда® в дозі 3,0 мг підшкірно 1 раз на добу, є зменшення окружності талії в середньому на 8,2 см на 56-му тиж лікування (дослідження SCALE Obesity and Prediabetes, Pi-Sunyer X. et al., 2015). Це підтверджує, що зниження маси тіла при застосуванні ліраглутиду відбувається саме завдяки втраті переважно вісцерального жиру порівняно з підшкірним (Sunyer X. et al., 2015).
Під час терапії ожиріння ліраглутидом варто пам’ятати таке:
- Лікування потрібно починати з дози 0,6 мг, повільно збільшуючи її щотижня на 0,6 мг до досягнення підтримувальної добової дози – 3,0 мг.
- Відповідь на лікування ліраглутидом у терапевтичній дозі потрібно оцінювати не раніше ніж через 3 міс, тобто в середньому через 4,5 міс після початку прийому Саксенда® (1,5 міс – період титрації дози). При цьому втрата 5% від вихідної маси тіла уже є показником достатньої ефективності лікування.
- За необхідності перед початком лікування варто провести УЗД черевної порожнини з акцентом на жовчний міхур і жовчовивідні шляхи, оскільки і втрата ваги, і застосування ліраглутиду призводять до згущення жовчі і підвищують ризик розвитку жовчнокам’яної хвороби (ЖКХ). Потрібно розглянути можливість проведення планового оперативного втручання в пацієнтів із ЖКХ перед початком прийому ліраглутиду, для мінімізації ризиків, пов’язаних із лікуванням.
- Якщо пацієнт незадовільно переносить підвищення дози, можна тимчасово повернутися до попередньої дози, яка добре переносилась, і знову спробувати підвищити дозу через кілька днів або через тиждень залежно від переносимості, або ж відкласти збiльшення дози на тиждень. Також можна змінити час введення препарату, наприклад увечері перед сном.
- Порадити пацієнтам пристосувати їхні харчові звички з метою запобігання побічним ефектам, зокрема їсти часто, але малими порціями, добре пережовувати їжу, обмежувати об’єм напоїв під час прийому їжі, уникати різких запахів і жирних продуктів.
- Нагадати пацієнту, що більшість побічних ефектів iз боку шлунково-кишкового тракту мають зазвичай тимчасовий характер і легкий або помірний ступінь , зникають з часом і не потребують припинення лікування.
- Якщо лікування препаратом Саксенда® було перервано з будь-яких причин й при відновленні застосування його необхідно розпочинати з дози 0,6 мг/добу і проводити повільну титрацію, навіть якщо попередньо пацієнт добре переносив дозу 3,0 мг/добу.
Таким чином, ЖТ – це метаболічно динамічний орган, який є основним місцем зберігання надлишку енергії, але також служить і ендокринним органом, здатним синтезувати низку біологічно активних сполук, які регулюють метаболічний гомеостаз.
Пептидні гормони (адипокіни), біоактивні ліпіди (ліпокіни) та мікроPHK, якi секретуються адипоцитами, чинять множинний вплив на інші органи і системи. Ці біологічно активні сполуки відіграють важливу роль у підтриманні здоров’я, але також залучені в розвиток патологічних станів, пов’язаних з ожирінням. Надмірне відкладення жиру спричинює порушення регуляції цих сполук, що негативно впливає на здоров’я та призводить до численних супутніх захворювань, спричинених ожирінням.
Ожиріння – це складне прогресуюче рецидивне хронічне захворювання, яке характеризується патологічним або надмірним умістом жиру в організмі і погіршує здоров’я. Хронічний перебіг ожиріння, як і метаболічна адаптація, спричинена втратою маси тіла, потребує боротьби впродовж усього життя людини, а розуміння складного патогенезу ожиріння та його наслідків допоможе вибрати кращу стратегію лікування.
Фармакотерапія ожиріння має застосовуватися в пацієнтів з IMT ≥ 30 кг/м2 або IMT ≥27 кг/м2 за наявності супутніх хвороб, пов’язаних з ожирінням (предіабет, ЦД, АГ, обструктивне апное уві сні, СПКЯ).
Препаратом 1-ї лінії при лікуванні ожиріння є ліраглутид (Саксенда®) в дозі 3 мг/добу, підшкірно. Результати клінічних досліджень і досвід застосування препарату в умовах реальної клінічної практики показують, що ліраглутид може застосовуватися для зниження маси тіла, утримання результату втрати ваги, а також для запобігання відновленню набору маси тіла. Окрім того цей препарат сприяє покращенню загального здоров’я і самопочуття, зменшенню ризику розвитку ускладнень і прогресування супутньої патології, відповідно покращуючи загальний прогноз, якість і тривалість життя пацієнтів, що і є метою кожного лікаря.
Список літератури – у редакції.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (60) 2022 р.