11 лютого, 2023
Сучасна концепція менеджменту чоловічого гіпогонадизму: ефективність замісної терапії тестостероном та контроль безпеки як головні пріоритети
У статті представлено актуальні дані міжнародних клінічних керівництв і рекомендацій щодо замісної терапії тестостероном при чоловічому гіпогонадизмі. Особливу увагу приділено трансдермальним системам доставки тестостерону, які забезпечують оптимальне співвідношення користі й ризику, вирізняються простотою та зручністю застосування. Обґрунтовано необхідність тривалого використання замісної терапії тестостероном у пацієнтів із віковим андрогенним дефіцитом.
Ключові слова: чоловічий гіпогонадизм, дефіцит тестостерону, замісна терапія тестостероном, трансдермальний гель, еректильна дисфункція, тестостерон-індукована поліцитемія.
Експерти Європейської асоціації урології (EAU) визначають чоловічий гіпогонадизм як клінічний синдром, що супроводжується зниженням вироблення андрогенів і/або порушенням сперматогенезу й розвивається внаслідок дисфункції яєчок або їх неадекватної стимуляції гіпоталамо-гіпофізарною системою. Гіпогонадизм негативно впливає на функції багатьох органів і, як наслідок, на якість життя пацієнтів, тому своєчасна діагностика й адекватне лікування мають вкрай важливе значення для підтримання чоловічого здоров’я (Salonia A. et al., 2022).
Доведено, що поширеність гіпогонадизму збільшується з віком: основними причинами є центральне ожиріння, супутні захворювання (наприклад, цукровий діабет) і загальне погіршення стану здоров’я (Wu F.C. et al., 2010).
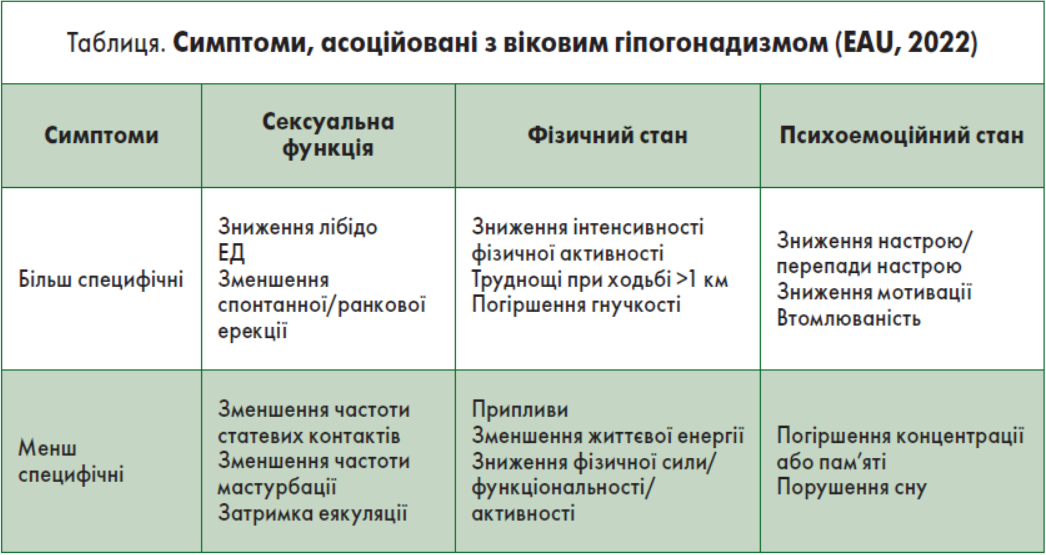
Діагноз гіпогонадизму встановлюється на основі стійких клінічних симптомів і біохімічних ознак дефіциту тестостерону (Salonia A. et al., 2022). Складнощі діагностування чоловічого гіпогонадизму зумовлені головним чином відсутністю специфічних симптомів. Перші клінічні ознаки дефіциту тестостерону, зокрема тривале почуття втоми, апатія, підвищена дратівливість і зниження статевого потягу, лікарі часто пов’язують із наслідками хронічного стресу, тому ранні прояви гіпогонадизму тривалий час залишаються поза увагою (таблиця).
Європейське дослідження старіння чоловіків EMAS продемонструвало, що тріада сексуальних симптомів – зниження лібідо, еректильна дисфункція (ЕД) та зменшення частоти спонтанних ранкових ерекцій – є найбільш специфічними ознаками, асоційованими з віковим зниженням рівня тестостерону (Wu F. C. et al., 2010).
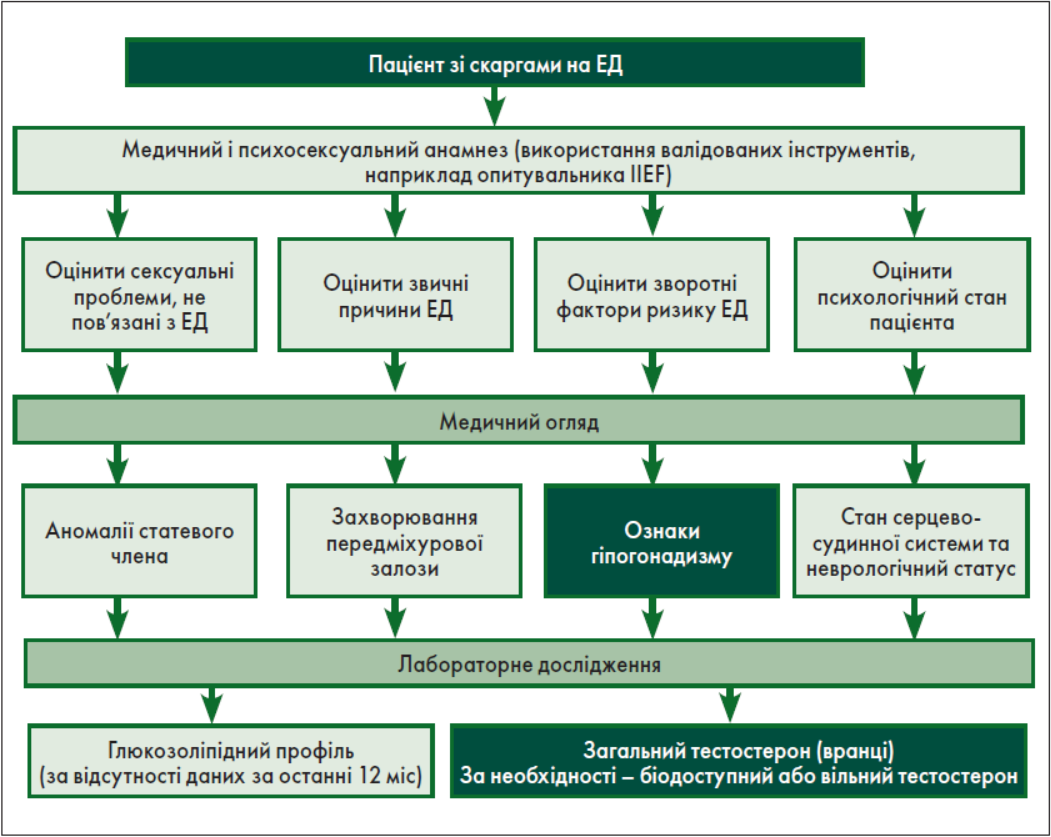
Варто зазначити, що у чоловіків з ЕД, яка характеризується багатофакторною етіологією, супутній дефіцит тестостерону визначається у 30% випадків, тобто в кожного третього чоловіка (Dohle G.R. et al., 2019). Отже, симптоми сексуальної дисфункції є найбільш прогнозованою визначальною ознакою потенційного чоловічого гіпогонадизму. Саме проблеми у сексуальній сфері є найпоширенішою причиною скарг серед дорослих чоловіків. Це вимагає від лікаря не лише глибокого розуміння причинно-наслідкового зв’язку між віковим гіпогонадизмом та ЕД, а й чіткої прихильності до алгоритмів обстеження пацієнтів із такою патологією (рисунок).
Рис. Мінімальний обсяг діагностичного обстеження пацієнта з ЕД (EAU, 2022)
Пацієнти із симптомним гіпогонадизмом (рівень загального тестостерону <12 нмоль/л) без специфічних протипоказань є кандидатами для отримання замісної терапії тестостероном (ЗТТ). Однак, перш ніж розпочинати терапію тестостероном, доцільно виявити й усунути потенційно оборотні причини гіпогонадизму (Grober E.D. et al., 2021), а саме:
- гострі захворювання;
- ожиріння;
- вживання препаратів (опіоїди, глюкокортикоїди);
- крайній ступінь дефіциту поживних речовин, анорексія;
- надмірні фізичні навантаження;
- апное сну;
- гіперпролактинемія;
- гемохроматоз;
- гіпоталамічні розлади (хірургічні втручання, травми, випромінювання тощо).
Відповідно до рекомендацій EAU щодо сексуального й репродуктивного здоров’я, метою ЗТТ у чоловіків із гіпогонадизмом є відновлення фізіологічних рівнів тестостерону у плазмі крові, що відповідає середньо-нормальним значенням у молодих осіб (Salonia A. et al., 2022). Проте невизначеність точних порогових значень загального й/або вільного тестостерону, що можуть бути застосовані як цільові показники у процесі лікування, зумовлює деякі складнощі у клінічній практиці при призначенні ЗТТ. Так, твердження «більше не означає краще» стосовно ЗТТ є особливо актуальним. Незважаючи на те що уніфікованого міжнародного консенсусу з питання цільових показників вільного тестостерону ще не досягнуто, відповідні рекомендації авторитетних урологічних товариств США й Канади можуть представляти певний інтерес для лікарів. Міжнародні експерти встановили, що при проведенні терапії тестостероном у чоловіків із віковим гіпогонадизмом слід підтримувати рівень вільного тестостерону в діапазоні від 14,0 до 20,8 нмоль/л.
Серед доступних трансдермальних форм тестостерону найбільш часто використовуваною є гель як найбільш фізіологічний, простий і практичний спосіб доставки тестостерону. На користь гелю свідчить і можливість швидко припинити його дію у разі побічних ефектів, таких як надмірне підвищення гематокриту або рівня простат-специфічного антигена (Lunenfeld B. et al., 2009). При ініціюванні терапії тестостероном експерти рекомендують використовувати його у формі гелю замість введення препаратів тестостерону пролонгованої дії, щоб терапія могла бути скоригована або призупинена у разі настання побічних ефектів (Salonia A. et al., 2022).
Гель швидко поглинається роговим шаром шкіри, утворюючи резервуар у прилеглих тканинах, звідки тестостерон безперервно вивільняється й надходить у кровотік протягом 24 год після одноразового щоденного застосування. Доведено, що тестостерон у формі трансдермального гелю ефективно нормалізує рівень гормона у сироватці крові, маючи відмінний профіль безпеки (Salonia A. et al., 2022).
Першу оцінку стану пацієнта рекомендовано проводити через 3 міс після призначення ЗТТ у формі трансдермального гелю. Подальше обстеження може бути проведене через 6 або 12 міс, залежно від особливостей пацієнта, вираженості симптомів, а також результатів біохімічного дослідження.
Взяття зразків крові слід здійснювати через 2-4 год після нанесення гелю, щоб використовувати піковий рівень тестостерону як орієнтир для адекватних терапевтичних доз (Salonia A. et al., 2022). Слід зауважити, що рівень тестостерону після нанесення гелю може змінюватися, тому, вірогідно, знадобиться ще одне вимірювання.
В Україні офіційно затверджений препарат для ЗТТ у формі трансдермального гелю зареєстровано під торговою назвою Андрожель. Препарат представлений у вигляді флакону з помпою-дозатором; 1 г гелю містить 16,2 мг тестостерону. Клінічне дослідження III фази продемонструвало, що Андрожель 16,2 мг/г швидко відновлює нормальний фізіологічний рівень тестостерону у плазмі: після 6 міс щоденного використання 2,5 г гелю середній рівень загального тестостерону зберігався в межах цільового діапазону (14,4-21,35 нмоль/л [415-615 нг/дл]) (Kaufman J. et al., 2011).
Нова форма гелю Андрожель 16,2 мг/г із помпою-дозатором розроблена для заміни раніше представленої форми Андрожель 1% у вигляді пакетиків-саше. Андрожель 16,2 мг/г містить ті самі інгредієнти, що й саше Андрожель 1%, однак гель у флаконі з помпою-дозатором є більш концентрованим. З огляду на це пропорція окремих компонентів дещо відрізняється. Кожне натискання помпи Андрожель 16,2 мг/г забезпечує дозу 1,25 г гелю, що містить 20,25 мг тестостерону. Рекомендована доза становить 2,5 г гелю 1 раз на добу, що відповідає двом натисканням помпи (40,5 мг тестостерону). Андрожель 16,2 мг/г слід наносити вранці, в один і той самий час, легкими рухами на чисту суху неушкоджену шкіру передпліч і плечей.
Незважаючи на те що прямі порівняльні дослідження двох препаратів не проводилися, наявні фармакокінетичні дані свідчать про те, що при використанні двох натискань на помпу-дозатор гелю (40,5 мг тестостерону) 1 раз на добу середній рівень тестостерону у плазмі крові, який досягається протягом 24 год, є зіставним із таким, що досягається при при застосуванні одного саше Андрожель 1%. Доведено, що при нанесенні трансдермального гелю стабільний рівень тестостерону у крові зазвичай досягається на 2‑й день лікування.
гідно з результатами одного з найбільших плацебо-контрольованих досліджень ЗТТ The Sexual Function Trial of the Testosterone Trials (TTrials) (Snyder P.J. et al., 2016, 2018), застосування тестостерону у формі гелю купірувало сексуальні розлади, зокрема покращувало сексуальну активність, статевий потяг та еректильну функцію, уже через 3 міс після ініціації терапії. У ході досліджень було доведено поліпшення 10 із 12 ознак сексуальної активності (від флірту до статевого акту) у чоловіків із гіпогонадизмом старше 65 років. Ефективність ЗТТ була особливо відзначена при оцінюванні частоти статевих актів, мастурбації та нічних ерекцій відповідно до даних психосексуальної щоденної анкети. Учені довели, що відповідно до даних психосексуальної щоденної анкети PDQ-Q4, ступінь покращення симптомів корелює зі збільшенням рівнів загального й вільного тестостерону та естрадіолу у сироватці крові, однак чітко визначити пороговий рівень тестостерону наразі неможливо. Дослідження за участю 220 чоловіків із метаболічним синдромом і з/без ЦД 2 типу продемонструвало, що застосування тестостерону у формі трансдермального гелю покращувало сексуальну функцію в осіб, які повідомляли про її розлади. Чоловіки відзначали збільшення лібідо й сексуального задоволення, що впливало на поліпшення показників опитувальника Міжнародного індексу еректильної функції (IIEF) (Jones T.H. et al., 2011).
Контроль безпеки тестостерон-замісної терапії
Найбільш вагомим аргументом на користь використання тестостерону у формі трансдермального гелю на початкових етапах ЗТТ є здатність контролювати потенційні ризики, які головним чином пов’язані із впливом тестостерону на показники кровотворення. Рекомендації EAU (2022) наголошують на тому, що перед прийняттям спільного з лікарем рішення про призначення терапії тестостероном пацієнти мають бути повною мірою поінформовані про очікувані переваги такого лікування та можливі несприятливі наслідки використання різних форм препаратів тестостерону.
Дані клінічних випробувань свідчать про те, що найпоширенішим побічним ефектом застосування препаратів тестостерону є збільшення рівня гематокриту, яке зазвичай проявляється через 3-12 міс від початку терапії. Поліцитемія може розвиватися після збільшення дози тестостерону, переходу від трансдермального введення до парентерального, а також за супутньої патології, яка впливає на показник гематокриту. Наявні дані свідчать про те, що ризик розвитку поліцитемії визначається у сукупності складом препарату, його дозуванням і фармакокінетикою.
Доведено, що застосування препаратів, які забезпечують стабільні концентрації тестостерону у сироватці крові (без виражених піків і падінь), пов’язано з низьким ризиком поліцитемії, частота виникнення якої варіює від 13% при застосуванні трансдермального гелю до 67% при призначенні розчинів для внутрішньом’язових ін’єкцій (Pastuszak A.W. et al., 2015). S. Ohlander et al. (2018) дійшли висновку, що короткодіючий ін’єкційний тестостерон асоціюється з вищим ризиком еритроцитозу порівняно з іншими лікарськими формами.
Рівень гематокриту >54% вимагає припинення ЗТТ, зниження дози або заміни форми препарату залежно від клінічної ситуації задля уникнення будь-яких потенційних ускладнень із боку серцево-судинної системи.
Підвищення рівня гематокриту до >54%, яке було попередньо визначене як підстава для припинення ЗТТ або зниження дози тестостерону, відмічалося у 22% (106/491) учасників нещодавно опублікованого рандомізованого плацебо-контрольованого дослідження III фази T4DM при застосуванні ін’єкцій тестостерону ундеканоату тривалої дії (Wittert G. et al., 2021).
Тестостерон-індукована поліцитемія: як запобігти розвитку кардіоваскулярних ускладнень
Достеменно відомо, що збільшення в’язкості крові пов’язане з підвищеним ризиком венозної тромбоемболії (ВТЕ), інфаркту міокарда й інсульту (Ohlander S. et al., 2018). Однак взаємозв’язок між тестостерон-індукованою поліцитемією та можливим ризиком серцево-судинних ускладнень ніколи раніше не вивчався. Навіть рекомендації EAU (2022) містять інформацію про порогові значення гематокриту (<54%), які екстраполюються на загальну популяцію.
Наразі опубліковані результати першого дослідження (Ory J. et al., 2022), метою якого було визначити, чи призводить вторинна поліцитемія, асоційована із ЗТТ, до підвищення ризику серйозних кардіоваскулярних подій (СКВП) і ВТЕ. СКВП було визначено як комбінацію смерті від будь-якої причини, інфаркту міокарда й інсульту; ВТЕ – як тромбоз глибоких вен і легеневу емболію. Використовуючи базу даних 74 млн пацієнтів, автори виділили дві когорти чоловіків із низьким рівнем загального тестостерону (<350 нг/дл [12,15 нмоль/л]), які отримували терапію тестостероном: тих, у кого розвинулася поліцитемія (n=5887), і тих, у кого не розвинулася (n=42 784). Поліцитемія при цьому визначалася як рівень гематокриту ≥52%.
Результати дослідження продемонстрували, що у перший рік після ініціювання терапії тестостероном ризик виникнення СКВП й ВТЕ становив 5,2% у чоловіків із поліцитемією та 3,9% – у пацієнтів із нормальним рівнем гематокриту (відношення шансів [ВШ] 1,35; 95% довірчий інтервал [ДІ] 1,13-1,61). Ймовірність виживання (ймовірність 1 року без СКВП/ВТЕ) була значно нижчою у групі пацієнтів із поліцитемією (95% проти 97%, p<0,0001; ВШ 1,22; 95% ДІ 1,04-1,43). Підвищений ризик розвитку гострого інфаркту міокарда (ВШ 1,81; 95% ДІ 1,2-2,7) і ВТЕ (ВШ 1,51; 95% ДІ 1,17-1,94) спостерігався у чоловіків із тестостерон-індукованою поліцитемією. Автори дослідження встановили, що розвиток вторинної поліцитемії на фоні терапії тестостероном може підвищувати ризик СКВП і ВТЕ протягом першого року лікування, тільки якщо рівень гематокриту >52%. Водночас безпосередньо терапія тестостероном (за відсутності поліцитемії) не підвищувала ризик СКВП/ВТЕ у чоловіків із гіпогонадизмом (Ory J. et al., 2022).
- Згідно з новими рекомендаціями EAU, для менеджменту можливих побічних ефектів ЗTT слід починати саме з тестостерону у формі гелю.
- Ризик ВТЕ та СКВП пов’язаний із поліцитемією (гематокрит ≥52%), спричиненою тестостероном.
- Цей ризик зберігається протягом перших 12 місяців після початку ЗТТ.
- Проведення ЗТТ як Андрожелем, так і Nebido призводить до збільшення рівня гематокриту, але цей ефект є значно більш вираженим у чоловіків, які отримують Nebido (p<0,001)*.
- Видається клінічно значущим не тільки починати терапію з Андрожелю, а й продовжувати її щонайменше 1 рік після ініціації, щоб мінімізувати можливі ризики.
Висновки численних масштабних досліджень і світовий досвід мають важливе практичне значення для ведення пацієнтів із віковим андрогенним дефіцитом. Наявні дані вказують на необхідність розпочинати лікування з трансдермального гелю тестостерону та дотримуватися цього підходу як мінімум протягом першого року після старту ЗТТ. Простий і фізіологічний спосіб відновлення нормального рівня тестостерону за допомогою гелю Андрожель 16,2 мг/г дозволяє покращити сексуальні симптоми, нормалізувати психологічний стан і значно підвищити якість життя чоловіків.
* Michael Zitzmann, Jann F. Cremers, Claudia Krallmann & Sabine Kliesch (2022) The HEAT-Registry (HEmatopoietic Affection by Testosterone): comparison of a transdermal gel vs long-acting intramuscular testosterone undecanoate in hypogonadal men, The Aging Male, 25:1, 134-144, DOI: 10.1080/13685538.2022.2063830
Підготувала Дарина Чернікова