27 лютого, 2023
Особливості патогенетичної терапії у хворих з неспецифічним виразковим колітом із застосуванням пробіотичних засобів на основі бактерій роду Bacillus
 Запальні захворювання кишечнику – неспецифічний виразковий коліт (НВК) і хвороба Крона – належать до актуальних проблем сучасної охорони здоров’я. Впродовж останніх десятиліть спостерігається стрімке зростання захворюваності на ці патології. З огляду на тяжкість перебігу, частоту серйозних ускладнень та інвалідизації ці хвороби, безумовно, також є важливою соціальною проблемою [1-3].
Запальні захворювання кишечнику – неспецифічний виразковий коліт (НВК) і хвороба Крона – належать до актуальних проблем сучасної охорони здоров’я. Впродовж останніх десятиліть спостерігається стрімке зростання захворюваності на ці патології. З огляду на тяжкість перебігу, частоту серйозних ускладнень та інвалідизації ці хвороби, безумовно, також є важливою соціальною проблемою [1-3].
Підтвердженням цього факту можна вважати те, що останні 10-15 років світова фармацевтична індустрія інвестує шалені кошти на створення принципово нових засобів патогенетичної терапії. Основа лікування запальних захворювань кишечнику загалом і НВК зокрема – застосування засобів біологічної терапії (моноклональні антитіла) та малих молекул (аміносаліцилати, інгібітори Янус-кінази, тіопурини). Основним завданням патогенетичної терапії є досягнення стійкої ремісії (щонайменше клінічної, в ідеальному випадку – ендоскопічної та гістологічної) [2].
НВК – хронічне запальне захворювання товстої кишки, за якого ушкоджується насамперед слизова оболонка прямої кишки з подальшим поширенням процесу в проксимальному напрямку. Поширеність НВК у популяції становить від 21 до 268 випадків на 100 тис. осіб [1-3].
Застосування сучасних високотехнологічних засобів патогенетичного впливу дозволяє значно частіше досягти ремісії порівняно зі схемами лікування 10-20-річної давності. Однак навіть одночасне чи послідовне використання таких препаратів часто не забезпечує відновлення самопочуття пацієнта із НВК і усунення патологічних змін слизового бар’єра [3-5].
Скринінговим маркером патологічних змін слизової кишечнику є синдром надлишкового бактеріального росту, для виявлення якого рекомендовано використовувати дихальні тести з лактулозою або глюкозою. Цікаво, що в пацієнтів із функціональними захворюваннями кишечнику та НВК показники цього тесту практично однакові, що підтверджує винятково важливу і патогенетично схожу роль кишкової мікрофлори за цих захворювань [6].
Механізм розвитку змін кишкового мікробіому є надзвичайно багатогранним, але остаточно не вивченим. Важливу роль відіграють стан місцевого та системного імунітету, особливості харчування, а також наявність хронічних захворювань. У хворих на НВК було виявлено тенденцію до зниження колонізації Firmicutes та Bacteroides (насамперед за рахунок збільшення популяції прото- й актинобактерій). Також при НВК відзначалося зниження рівня біфідобактерій, меншою мірою – лактобактерій. Загальною особливістю змін у мікробіомі було суттєве зменшення розмаїття кишкової мікрофлори, яке корелювало з тяжкістю перебігу хвороби, а застосування пробіотичних препаратів сприяло суттєвому полегшенню симптомів НВК, що підтверджено низкою досліджень і Кокрейнівськими оглядами [7, 8].
Саме тому важливий напрям впливу на слизовий бар’єр кишечнику – пошук саме тих бактерій, які здатні відновити нормальну взаємодію між компонентами мікробіому. На сьогодні серед перспективних варіантів такого пошуку є Faecalibacterium prausnitzii, Bacillus subtilis, Bifidobacterium infantis, оскільки ці мікроорганізми сприяють активній регенерації мукозального бар’єра за рахунок відновлення мукозального імунітету, стимуляції синтезу бутирату тощо. Вплив на рівень бутирату важливий, оскільки ця сполука має протизапальні властивості, нормалізує стан слизового бар’єра кишечнику, а на клітинному рівні пригнічує синтез прозапальних цитокінів, зокрема фактора некрозу пухлини та інтерлейкінів 1 і 6.
Необхідні компоненти, властиві сучасним пробіотичним штамам:
- відсутність передачі резистентності потенційно небезпечній флорі;
- здатність до виживання під час транзиту через шлунково-кишковий тракт, у т. ч. стійкість до дії соляної кислоти і жовчі;
- визначена чутливість до антибіотиків;
- підвищення резистентності до патогенної кишкової мікрофлори.
Рід Bacillus налічує >200 видів і об’єднує численну групу аеробних або факультативно анаеробних мікроорганізмів. Одним із найперспективніших представників є B. subtilis (Ehremberg) Cohn 1872, 174. Бактерії роду Bacillus характеризуються стійкістю до несприятливих умов зовнішнього середовища, в т. ч. до дії соляної кислоти та жовчі, тому мають перевагу над мікроорганізмами інших таксономічних груп при використанні їх у медицині [9]. В процесі еволюції приматів Bacillus вступали в складні симбіотичні зв’язки з організмом людини й інших ссавців, тому вони виконують низку корисних для макроорганізму функцій, найважливішою з яких є здатність елімінувати з кишечнику патогени. Представники Bacillus постійно потрапляють до шлунково-кишкового тракту людей з навколишнього середовища, в більшій кількості – в результаті вживання ферментованих продуктів харчування. На слизових оболонках спори цих бактерій активізуються і переходять до вегетативного росту. Тривалість їхнього перебування в організмі людини здебільшого визначається генетичними особливостями штамів, роботою мукозального імунітету, наявністю хронічних захворювань організму господаря (насамперед органів травлення) [10].
Хоча більшість сучасних пробіотиків створена на основі бактерій Lactobacillus і Bifidobacterium, спороутворювальні бацили мають низку суттєвих переваг. Експериментально доведена їхня нешкідливість, а також вища конкурентна протимікробна і ферментативна активність.
Вони позитивно впливають на роботу як системного, так і мукозального імунітету, сприяють нормалізації ліпідного балансу, є стійкими до впливу соляної кислоти та жовчі, стабільними при зберіганні [9, 10]. Впродовж останніх двох десятиліть накопичилися наукові дані, які демонструють високу профілактичну й терапевтичну ефективність представників роду Bacillus у разі захворювань органів травлення, порушень імунного статусу й обміну речовин. Однією з основних корисних властивостей спороутворювальних бактерій роду Bacillus є висока антагоністична активність щодо значного низки патогенних і умовно-патогенних мікроорганізмів. Антагонізм бацил безпосередньо пов’язаний зі здатністю представників різних видів синтезувати речовини із протимікробним впливом [9].
На сьогодні відомо ≈1000 антибактеріальних сполук, які продукуються бактеріями цього роду. Всі вони відрізняються за своєю структурою та спектром мікроорганізмів, на які згубно діють, при цьому більшість таких сполук, утворених бактеріями роду Bacillus, є поліпептидами.
Основні компоненти цих антибіотиків характеризуються плейотропною біологічною активністю, низькою токсичністю і мають потенціал для застосування в медицині як противірусні, антибактерійні, метаболічні засоби [11]. Бактерії роду Bacillus є також продуцентами амінокислот, ферментів, полісахаридів, вітамінів тощо [12].
Завдяки синтезу ферментів бактерії роду Bacillus можуть брати участь у регулюванні моторики та травлення, мають протиалергенну й антитоксичну дії. Серед гідролітичних ферментів, які продукуються ними, слід звернути увагу на протеази, що відіграють надзвичайно важливу роль у підтримці мукозального бар’єра і мукозального імунітету [13]
Ще однією важливою для організму групою біологічно активних речовин, синтезованих бацилами, є екзополісахариди. Давно відомо, що позаклітинні полісахариди можуть підвищувати опір організму до бактерійних і вірусних інфекцій, стимулювати фагоцитоз, продукцію лізоциму, проявляти протипухлинну, протизапальну активність, що надає широкі можливості для їхнього застосування в медицині [12, 13].
На сьогодні в світі для застосування в медицині як пробіотиків найдослідженішими є штами бацил кількох видів – B. subtilis, B. cereus, B. licheniformis, B. megaterium, B. pumilus, B. clausii, B. coagulans, B. amyloliquefaciens. На їхній основі створені препарати для профілактики та лікування порушень мікрофлори кишечнику, кишкових інфекцій, антибіотикоасоційованої діареї, синдрому подразненого кишечнику, корекції імунного статусу [13].
Одним із нових пробіотичних продуктів із метаболічною активністю є дієтична добавка Ремедіум (сировина Chrisal NV, Бельгія), що містить 5 видів полірезистентних до антибіотиків штамів Bacillus (спори B. subtilis, B. licheniformis, B. amyloliquefaciens, B. megaterium, B. pumilus), безпечність яких підтверджена висновками Управління з контролю за якістю продуктів харчування та лікарських засобів США (FDA). Одна доза дієтичної добавки містить 1,7×109 КУО живих мікробних клітин.
На базі НДІ «Інститут мікробіології і вірусології ім. Д. К. Заболотного НАН України» (м. Київ) проведено дослідження антагоністичної активності деяких пробіотичних штамів бацил та їхніх композицій щодо представників різних родів умовно-патогенних мікроорганізмів (метод відтермінованого антагонізму). Найвища протимікробна активність дослідженої композиції виявлена до бактерій роду Staphylococcus, Proteus і грибів роду Candida [13].
Отже, було підтверджено, що спороутворювальні бактерії роду Bacillus є безпечними для макроорганізму (за винятком B. anthracis і B. cereus), а також являють собою продуценти комплексу біологічно активних речовин, корисних для макроорганізму, крім того, вони мають імуномодулювальні властивості.
Саме тому метою нашого дослідження стало вивчення можливості використання Ремедіуму в комплексному лікуванні хворих на НВК, з’ясувавши його ефективність і безпечність.
Матеріали та методи
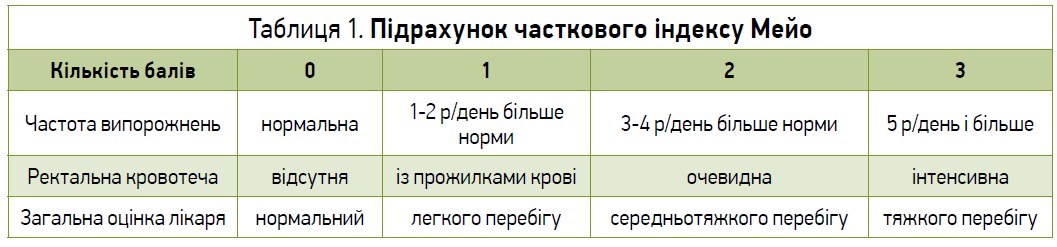
Всього було обстежено 39 хворих на НВК середньої тяжкості у фазі неповної ремісії. Неповну ремісію визначали як слабку активність хвороби, котру встановлювали за підрахунком часткового індексу Мейо [14, 15], що в таких пацієнтів дорівнював від 2 до 4.
Частковий індекс Мейо підраховується як сума балів (табл. 1) [16].
Пацієнтів було рандомізовано на 2 групи (комп’ютерним методом). 20 хворих 1-ї групи продовжували отримувати патогенетичні засоби базисної терапії без зміни дози впродовж 1 міс. Пацієнти 2-ї групи протягом цього самого часу додатково отримували Ремедіум по 1 флакону оральної суспензії 1 р/день упродовж 30 днів. Дози засобів базисної терапії не змінювалися протягом цього місяця спостереження. Обидві групи були зіставними за віком, статтю і тяжкістю клінічних проявів на початку спостереження.
До огляду і через 1 міс лікування всім хворим проводили клінічне та лабораторне обстеження: загальний аналіз крові, С‑реактивний білок, копрограма, кальпротектин калу, комплексне імунологічне обстеження.
Результати та обговорення
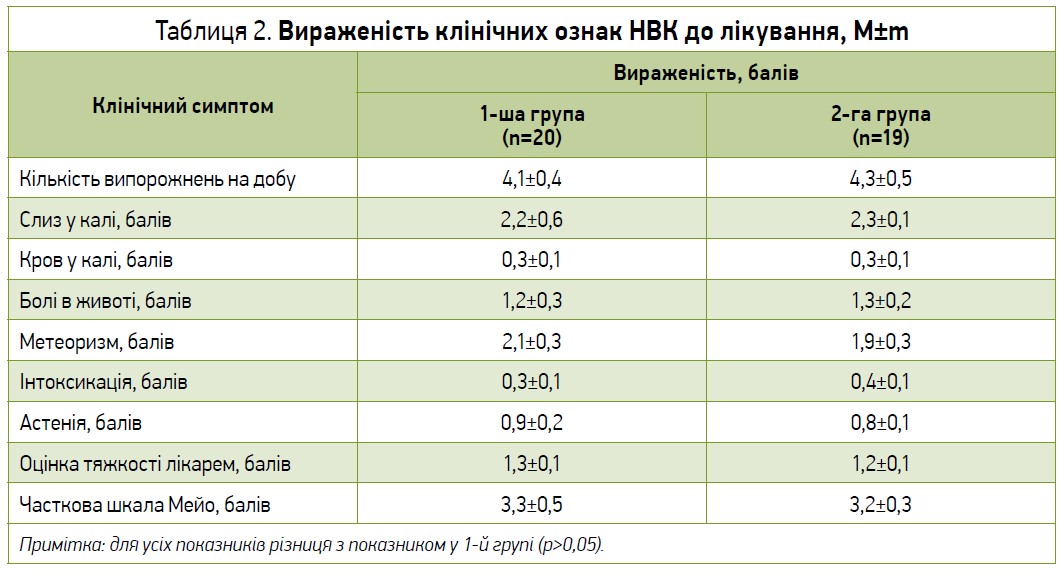
Пацієнти обох груп були зіставними за тяжкістю перебігу та вираженістю клінічних проявів до лікування (табл. 2). Вираженість і тяжкість клінічних симптомів оцінювали методом анкетування за 3-бальною шкалою (0 – прояви відсутні, 1 – слабко виражені, 2 – помірно виражені, 3 – сильно виражені).
На підставі аналізу вираженості клінічних проявів в обох групах чітко видно, що більшість пацієнтів перебувала в стані неповної ремісії.
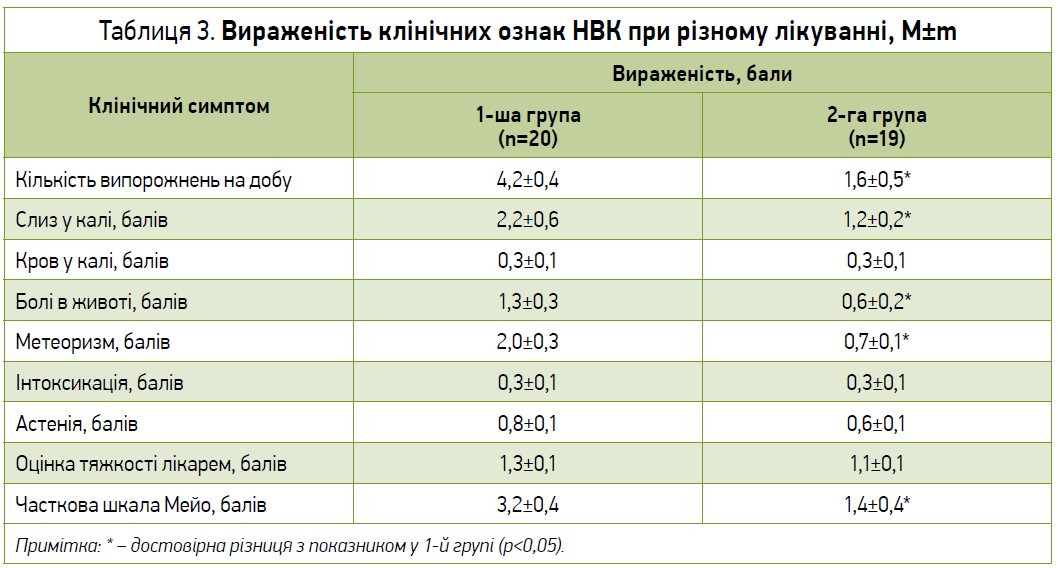
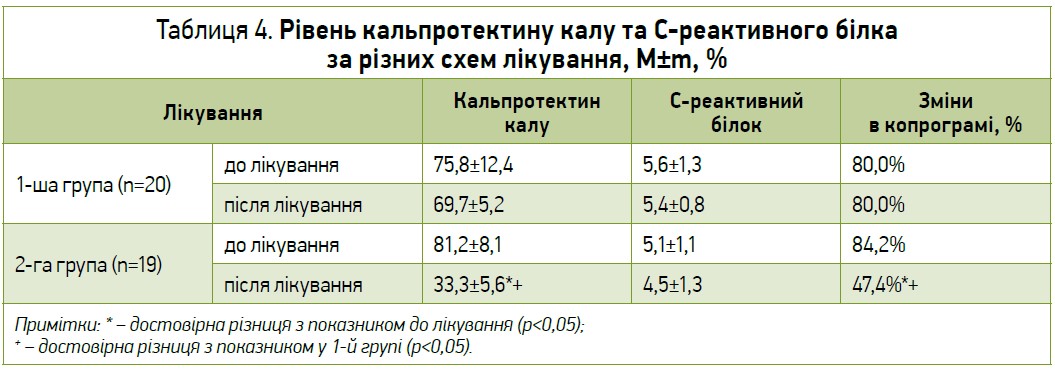
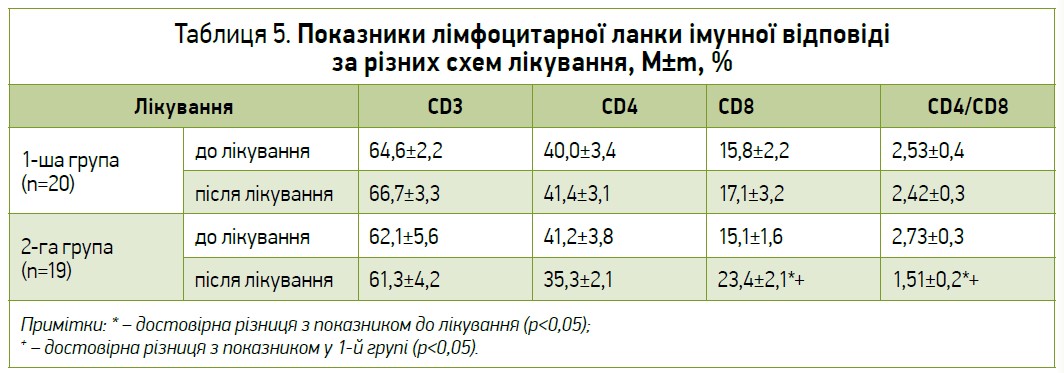
Зазвичай збільшення доз засобів патогенетичної терапії чи перехід на медикаменти наступної сходинки в таких випадках не надає суттєвого лікувального ефекту, але часто призводить до збільшення небажаних побічних ефектів [17]. Додаткове призначення Ремедіуму пацієнтам із НВК сприяло достовірному зменшенню вираженості таких симптомів хвороби, як частота дефекації, наявність слизу в калі, метеоризму, болів у животі (p<0,05) (табл. 3). Відзначалася також тенденція до покращення стану щодо інтенсивності таких проявів хвороби, як наявність астенії, а також оцінка тяжкості стану пацієнта лікарем (p>0,05). У результаті спостерігалося достовірне зниження часткового індексу Мейо (p<0,05), що дозволило трактувати стан більшості пацієнтів як досягнення клінічної ремісії [16, 17]. При оцінці лабораторних показників відзначалося достовірне зниження рівня кальпротектину в калі та відсотка пацієнтів, у яких виявлялися запальні зміни в копрограмі (p<0,05) (табл. 4). Також спостерігалася тенденція до зниження рівня С‑реактивного білка в крові (p>0,05). У групі пацієнтів, які отримували Ремедіум, виявлено тенденцію до зниження рівня CD4-лімфоцитів (p>0,05) при одночасному наростанні вмісту CD8-лімфоцитів, що сприяло зниженню CD4/CD8-коефіцієнта (табл. 5). Це свідчить про зниження інтенсивності запального процесу з автоімунним механізмом [18].
У жодного з 19 хворих, котрі приймали Ремедіум, не відзначено алергічних реакцій чи інших побічних ефектів.
Висновки
1. Використання дієтичної добавки Ремедіум у хворих на НВК як додаткового пробіотичного засобу до лікування аміносаліцилатами дозволило достовірно покращити самопочуття пацієнтів, суттєво зменшивши вираженість таких проявів захворювання, як частота дефекації, наявність слизу в калі, метеоризм, болі в животі, а також забезпечило зниження часткового індексу Мейо (p<0,05).
2. Застосування пробіотичного засобу Ремедіум сприяло зниженню рівня фекального кальпротектину, зменшенню запальних змін у копрограмі й інтенсивності запального процесу за показниками імунограми.
3. Призначення пробіотичного засобу Ремедіум було безпечним у пацієнтів із НВК, воно не зумовило розвитку небажаних явищ у жодного із пролікованих хворих.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 3 (539), 2023 р.