28 лютого, 2023
Глобальна стратегія з лікування і профілактики бронхіальної астми
Стисле резюме змін GINA‑2022
 За підрахунками на бронхіальну астму (БА) страждає приблизно 300 млн людей в усьому світі. Це серйозна глобальна проблема охорони здоров’я, що є актуальною для всіх вікових груп. Поширеність БА в багатьох країнах, що розвиваються, зростає. Збільшуються також витрати на лікування, що загалом становить значний тягар для пацієнтів і громади. Отже, незважаючи на значний прогрес у лікуванні астми, вона являє собою значну проблему для системи охорони здоров’я і суспільства через втрату дієздатності, а також тяжкі випробування для родин пацієнтів, особливо коли це стосується педіатричної астми. До того ж БА лишається причиною великої кількості смертей в усьому світі, у тому числі серед молоді. Майже 96% смертей від астми припадає на країни з низьким і середнім доходом.
За підрахунками на бронхіальну астму (БА) страждає приблизно 300 млн людей в усьому світі. Це серйозна глобальна проблема охорони здоров’я, що є актуальною для всіх вікових груп. Поширеність БА в багатьох країнах, що розвиваються, зростає. Збільшуються також витрати на лікування, що загалом становить значний тягар для пацієнтів і громади. Отже, незважаючи на значний прогрес у лікуванні астми, вона являє собою значну проблему для системи охорони здоров’я і суспільства через втрату дієздатності, а також тяжкі випробування для родин пацієнтів, особливо коли це стосується педіатричної астми. До того ж БА лишається причиною великої кількості смертей в усьому світі, у тому числі серед молоді. Майже 96% смертей від астми припадає на країни з низьким і середнім доходом.
БА – це гетерогенне захворювання, що зазвичай характеризується хронічним запаленням дихальних шляхів. Діагностується за наявності в анамнезі респіраторних симптомів, таких як свистячі хрипи, задишка, стиснення в грудях і кашель, які змінюються з часом та за інтенсивністю, а також нестійкого обмеження повітряного потоку на видиху. Обмеження повітряного потоку згодом може стати персистувальним.БА зазвичай асоційована з гіперреактивністю і запаленням дихальних шляхів, однак для встановлення діагнозу цих характеристик недостатньо або їх наявність не є обов’язковою.
Є розпізнавальні кластери відповідно до демографічних, клінічних і/або патофізіологічних характеристик захворювання, що їх називають «фенотипи астми», однак вони незначно корелюють зі специфічним патологічним процесом або відповіддю на лікування.
Рекомендації щодо БА і COVID‑19
Сучасні дослідження підтверджують, що в пацієнтів із добре контрольованою БА легкого і помірного ступеня тяжкості ризик розвитку тяжкого COVID‑19 не є підвищеним, однак він зростає, коли йдеться про пацієнтів, які для контролювання симптомів астми потребують застосування пероральних кортикостероїдів (ПКС), а також в ушпиталених пацієнтів із тяжким перебігом захворювання. Було оновлено поради щодо процедур / діагностичних і лікувальних заходів, які сприяють утворенню аерозолю:
- як і раніше, рекомендують уникати застосування небулайзерів, оскільки вони збільшують ризик поширення вірусу: під час небулізації респіраторні вірусні часточки можуть передаватися на відстані не менше 1 м;
- у разі тяжких загострень астми найкращим вибором для інгаляційної доставки лікарських засобів є дозувальний інгалятор під тиском (pMDI) зі спейсером із використанням мундштука або щільно прилягаючої лицьової маски, якщо потрібно;
- рекомендовано уникати проведення спірометрії в пацієнтів із БА з підозрою на COVID‑19 або підтвердженим діагнозом. Хоча використання вбудованого фільтра мінімізує ризик передачі вірусу під час спірометрії, запобіжні заходи все ж потрібні, оскільки багато пацієнтів кашляють після проведення спірометрії.
Вакцинація пацієнтів із БА від COVID‑19
Наразі вивчено та використовують велику кількість вакцин від COVID‑19. Постійно накопичуються нові докази щодо застосування протиковідних вакцин, у тому числі в пацієнтів з астмою. Загалом алергічні реакції на вакцини спостерігають досить рідко. Пацієнти, в анамнезі яких задокументована серйозна алергічна реакція на інгредієнт вакцини проти COVID‑19 (наприклад, поліетиленгліколь у Pfizer/BioNTech або Moderna або полісорбат 80 у вакцині AstraZeneca або J&J/Janssen), мають отримати іншу вакцину проти COVID‑19. Однак люди, в анамнезі яких є анафілаксія на харчові продукти, отруту комах або інші ліки, можуть безпечно отримувати вакцини проти COVID‑19. Будь-які занепокоєння щодо вакцинації пацієнти мають обговорити зі своїм лікарем.
На сьогодні, аналізуючи всі переваги й ризики, ураховуючи вищезазначену обережність, GINA рекомендує особам з астмою вакцинацію проти COVID‑19, у тому числі бустерні дози, якщо вони є в наявності.
Для пацієнтів із тяжкою астмою GINA пропонує, якщо це можливо, не вводити першу дозу імунобіологічної терапії та вакцину проти COVID‑19 у той самий день, щоб у разі необхідності легше розрізнити побічні ефекти від їх застосування.
Діагностика БА
Дані, наведені на рисунку 1, було переглянуто, аби підкреслити, що діагностичний підхід відрізняється залежно від того, чи пацієнт вже перебуває на контролювальній терапії, а також для уточнення цілей діагностики (рис. 1).
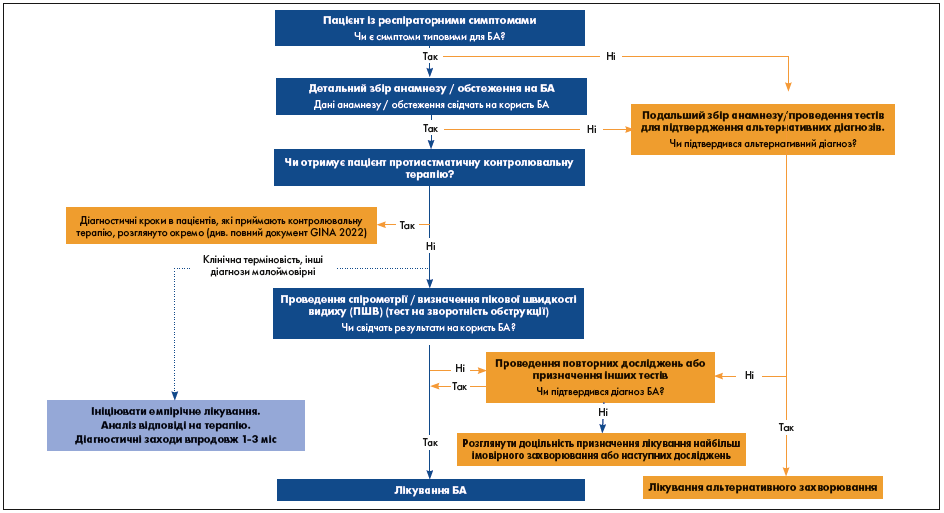 Рис. 1. Діагностична блок-схема при БА
Рис. 1. Діагностична блок-схема при БА
Оцінка контролю симптомів БА
Так склалося, що частоту застосування β2-агоністів короткої дії (БАКД) (<2 або ≥2 днів/тиждень) враховували під час загальної оцінки контролю симптомів БА. Такий підхід базувався на припущенні, що якщо БАКД використовують більш як 2 дні на тиждень, то пацієнту необхідно розпочинати контролювальну терапію або збільшувати її дозу. Крім того, використання БАКД протягом року з частотою, вищою за середню, асоціювалося з вищим ризиком тяжких загострень [70, 71], а в короткостроковій перспективі – збільшення використання БАКД за потреби асоціювалося з підвищеною ймовірністю тяжкого загострення астми в наступні дні або тижні [72].
Однак, якщо пацієнт, якому для купірування симптомів, тобто як препарат «за потреби», призначено фіксовану комбінацію ІКС з формотеролом і пацієнт використовує препарат у середньому понад 2 дні/тиждень, це вже забезпечує додаткову контролювальну терапію БА, тому подальше збільшення дози може бути не потрібне. Збільшення використання фіксованої комбінації ІКС-формотерол за потреби пов’язане зі значно нижчим ризиком розвитку тяжких загострень у наступні дні або тижні порівняно із застосуванням за потреби лише БАКД [73, 74] або з монотерапією БАКД [75].
З цих причин такий показник контролю БА, як використання фіксованої комбінації ІКС-формотерол за потреби, чітко розділене на ≤2 і >2 днів/тиждень, не враховують під час комплексної оцінки контролю симптомів астми. Однак слід оцінювати середню частоту застосування ІКС-формотеролу за потреби за останні 4 тиж і брати її до уваги, переглядаючи дози контролювальної терапії.
Визначення легкої БА
Розділ про визначення тяжкості астми після розширеного обговорення було доопрацьовано. Сучасне визначення тяжкості астми ґрунтується на концепції «difficulty to treat asthma» (складна в лікуванні астма). Визначення «тяжка астма» широко визнане та актуальне для використання в клінічній практиці. Однак різниця між поняттями корисність і актуальність щодо відповідного визначення легкої астми набагато менш чітка. Пацієнти і клініцисти часто припускають, що «легка астма» означає відсутність будь-якого ризику і потреби в контролювальній терапії, але до 30% смертей від астми припадає саме на людей із нечастими симптоми захворювання. GINA пропонує провести обговорення проблеми із зацікавленими сторонами, щоб дійти згоди щодо того, чи є необхідним і як має бути сформульоване та використовуватися поняття «легкої астм». Тим часом GINA пропонує уникати терміну «легка астма» в клінічній практиці всюди, де це є можливим, а якщо він і використовується, то з обов’язковим нагадуванням про ризики тяжких загострень БА і необхідність обов’язкового застосування ІКС.
Рекомендації GINA щодо лікування БА в дорослих і підлітків
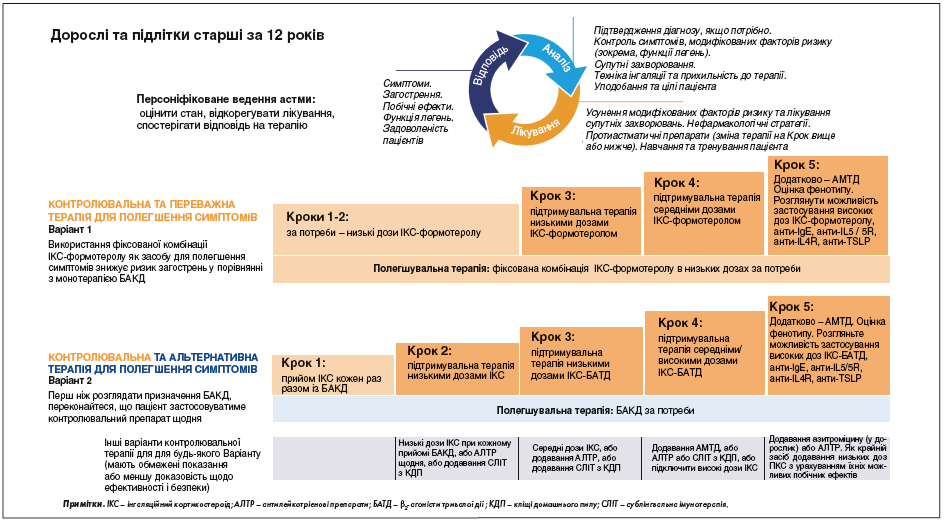
Покрокова терапія БА наведена на рисунку 2, а саме 2 варіанти (треки) покрокового лікування астми, обґрунтування яких було підсилено оновленою доказовою базою:
- Варіант 1. Контролювальна та переважна терапія для полегшення симптомів (CONTROLLER and PREFERRED RELIEVER) – застосування фіксованої комбінації ІКС-формотерол як засобу для полегшення симптомів на всіх кроках лікування є переважним, з огляду на докази щодо нижчого ризику загострень астми і кращого або такого самого контролю симптомів порівняно із застосуванням БАКД.
- Варіант 2. Контролювальний та альтернативний препарат для полегшення симптомів (CONTROLLER and ALTERNATIVE RELIEVER): перш ніж розглянути режим лікування із застосуванням БАКД для полегшення симптомів, необхідно перевірити, чи пацієнт використовує щоденно свій контролювальний препарат.
Рис. 2. Персоналізована терапія БА в дорослих і підлітків для контролю захворювання і мінімізації майбутніх ризиків
Також було оновлено кроки лікування і додано новий імунобіологічний препарат (тезепелумаб) – антитіла до тимусного стромального лімфопоетину (anti-thymic stromal lymphopoietin, anti-TSLP) – як новий засіб лікування тяжкої астми на Кроці 5.
«Інші варіанти контролювальної терапії» наводяться як такі, що мають або певні специфічні показання, або меншу доказову базу щодо безпеки і/або ефективності, ніж лікування в рамках 1-го або 2-го варіантів.
Кроки 1-2: низькі дози фіксованої комбінації ІКС-формотерол за потреби
Додано додаткові докази, у тому числі результати систематичного огляду [188, 190], які демонструють значне зменшення кількості візитів і ушпиталень у відділення невідкладної допомоги за умови застосування фіксованої комбінації ІКС-формотерол за потреби порівняно з простою комбінацією щоденного ІКС + БАКД за потреби. Також застосування фіксованої комбінації ІКС-формотерол за потреби забезпечує суттєвіше зменшення частоти тяжких загострень астми в дорослих і підлітків, які раніше застосовували ІКС + БАКД за потреби окремо [190, 221]. Подібні висновки продемонстровано і щодо безпеки застосування фіксованої комбінації і ІКС + БАКД окремо.
Кромони
Застосування кромонів (недокроміл натрію і кромоглікат натрію) в дозованих інгаляторах під тиском (pMDI) було припинено в усьому світі. Препарати цієї групи мають хороший профіль безпеки, але низьку ефективність (Рівень доказовості A) [247-249], а власне доставкові пристрої, що містять діючу речовину, потребують копіткого щоденного промивання, щоб уникнути забруднення.
Мускарінові антагоністи
Мускаринові антагоністи тривалої дії (МАТД) при астмі не мають застосовуватися у вигляді монотерапії, без комбінації з ІКС. Монотерапія МАТД при астмі є небезпечною через зростаючий ризик тяжких загострень БА [230].
Додавання MAТД до комбінації ІКС + β2-агоніст тривалої дії (БАТД) на Кроці 5
Результати метааналізу досліджень ефективності додавання MAТД до комбінації ІКС-БАТД підтвердили помірне підвищення функції легень [211, 274-277, 252] (Рівень доказовості А) і помірне загальне зниження частоти тяжких загострень [211, 274, 275, 278, 279], однак без клінічно значущих переваг щодо симптомів або якості життя. Доказова база не підтверджує ефективність додавання МАТД пацієнтам із персистувальною задишкою. Пацієнти із загостреннями БА, незважаючи на застосування комбінації ІКС-БАТД, мають отримувати щонайменше середню дозу такої комбінації, перш ніж розглядати додавання таким пацієнтам МАТД.
Підвищений уміст еозинофілів у крові
Перш ніж розглядати призначення імунобіологічної терапії у пацієнтів із тяжкою астмою («difficulty to treat») та еозинофілією крові (≥300/мкл), рекомендовано дослідити причини еозинофілії, які можуть бути не пов’язані з астмою: обстежити на наявність паразитозів, у тому числі стронгілоїдозу (серологічне або копрологічне дослідження), оскільки вони часто є причиною еозинофілії крові. Стронгілоїдоз часто має асимптомний перебіг [566]. Важливо проводити зазначений діагностичний пошук, оскільки призначення ПКС або імунобіологічної терапії може спричинити дисемінацію паразитарного захворювання.
У пацієнтів з еозинофілією крові (наприклад, ≥1500/мкл) потрібно розглянути такі причини, як еозинофільний гранулематоз із поліангіїтом* (Eosinophilic granulomatosis with polyangiitis, EGPA) і уникати призначення анти-IL4R, оскільки вони були виключені з досліджень Фази III.
Застосування анти-TSLP у дорослих і підлітків
Препарат тезепелумаб – гуманізовані моноклональні антитіла до тимусного стромального лімфопоетину (anti-thymic stromal lymphopoietin, anti-TSLP). Препарат є засобом додаткової терапії, що рекомендована для дорослих і дітей ≥12 років із тяжкою БА. Призначення тезепелумабу асоційоване з кращою ефективністю щодо тяжких загострень астми в пацієнтів із підвищеним умістом еозинофілів у крові або високим рівнем FeNO. Препарат призначається в дозі 210 мг підшкірно кожні 4 тижні. У рамках дослідження анти-TSLP було додано до варіантів лікування пацієнтів ≥12 років, в яких не було підтверджене запалення типу 2 під час повторного дослідження, але застосування препарату не має достатньо доказів у пацієнтів, які приймають ПКС.
Результати застосування анти-TSLP [305, 593]: за даними РКД, застосування тезепелумабу в пацієнтів із тяжкою астмою і тяжкими загостреннями впродовж останнього року призвело до зменшення частоти загострень на 30-70%, а також до покращення якості життя, функції легень і контролю симптомів, незалежно від алергічного статусу. Існувала чітка кореляція між вищим базовим рівнем еозинофілів у крові або FeNO і кращими клінічними результатами лікування тезепелумабом. У пацієнтів, які приймали ПКС, застосування анти-TSLP не сприяло зниженню дози ПКС порівняно з плацебо.
Потенційні предиктори хорошої відповіді на призначення анти-TSLP:
- вищий рівень еозинофілів у крові (сильний предиктор);
- вищі рівні FeNO (сильний предиктор).
Антагоністи рецепторів інтерлейкіну‑4 (анти-IL4R)
Додавання до терапії тяжкої астми анти-IL4R (дупілумаб) рекомендовано в дорослих і підлітків ≥12 років без ознак запалення Типу 2 під час повторного дослідження, які потребують застосування ПКС (Рівень доказовості A) [297, 303, 304].
Схвалено додавання дупілумабу до терапії тяжкої БА в дітей ≥6 років із тяжкою еозинофільною БА/БА 2-го типу [302]. Препарат вводять підшкірно.
Результати застосування анти-IL4R: за даними РКД, застосування дупілумабу в пацієнтів із неконтрольованою тяжкою астмою (ACQ‑5 ≥1,5) і принаймні одним загостренням за минулий рік сприяло зниженню частоти тяжких загострень на 56%, значному покращанню якості життя, контролю симптомів і легеневої функції [297], проте різниця не була клінічно значущою. У ретроспективному (post hoc) аналізі клінічні результати в пацієнтів з алергічним і неалергічним фенотипом на початку дослідження були подібними [589]. У пацієнтів зі стероїд-залежною тяжкою астмою призначення анти-IL4R сприяло зниженню середньої дози ПКС на ~30% порівняно з плацебо [590].
У дітей віком 6-11 років з еозинофільною астмою / астмою 2-го типу застосування дупілумабу дало можливість знизити частоту тяжких загострень на 41% і покращити функцію легень на 5,2 відсоткового пункту. Діти, які отримували ПКС, були виключені з дослідження [302]. Дупілумаб також показаний для лікування помірної тяжкості і тяжкого атопічного дерматиту [591]. У пацієнтів із хронічним риносинуситом із назальними поліпами застосування дупілумабу забезпечувало зменшення розміру носових поліпів, полегшення назальних симптомів і зменшення потреби в ПКС або операції на приносових пазухах [500, 592].
Потенційні предиктори хорошої відповіді на дупілумаб:
- вищий рівень еозинофілів у крові (сильний предиктор) [303];
- вищий уміст FeNO (сильний предиктор) [303].
Анти-IgE під час вагітності
Доказових даних щодо лікування тяжкої астми під час вагітності доволі мало, а ризики від застосування імунобіологічної терапії (зокрема, анти-IgE, омалізумабу) під час вагітності мають бути зіставлені з ризиками для матері і дитини від неконтрольованої БА. Дослідження реєстру не виявило підвищеного ризику вроджених вад розвитку в дитини в разі застосування омалізумабу під час вагітності [527].
Результати застосування анти-IgE: за даними РКД, застосування омалізумабу при тяжкій алергічній БА супроводжується зниженням частоти тяжких загострень на 44% і покращанням якості життя [297]. У метааналізі обсерваційних досліджень у пацієнтів із тяжкою алергічною астмою спостерігали зниження частоти загострень на 59%, зниження частки пацієнтів, які отримували підтримувальне лікування ПКС, на 41% і значне поліпшення контролю симптомів [574]. У пацієнтів із назальними поліпами застосування омалізумабу поліпшувало суб’єктивні й об’єктивні результати лікування [497].
Потенційні предиктори хорошої відповіді на призначення омалізумабу:
- високий базовий рівень IgE не є предиктором імовірної відповіді [575];
- в одному обсерваційному дослідженні спостерігали суттєвіше зниження частоти загострень БА (проти плацебо) при рівні еозинофілів крові ≥260/мкл [576, 577] або вмісті FeNO ≥20 ppb (част./млрд) [576] (критерії демонструють середнє значення в цьому дослідженні), але у двох великих обсерваційних дослідженнях частота загострень зменшувалася як при низькому, так і при високому рівні еозинофілів у крові [578-580] або з низьким чи високим вмістом FeNO [580];
- виникнення астми в дитинстві;
- клінічний анамнез, який свідчить про симптоми, індуковані алергенами.
Системні КС
Розглядати застосування ПКС потрібно як крайній засіб лікування астми у будь-яких вікових категоріях через ризик виникнення серйозних довгострокових несприятливих наслідків, коли прийом інших засобів лікування максимально оптимізований і ніякої доступної альтернативи немає.
Письмовий план дії при БА
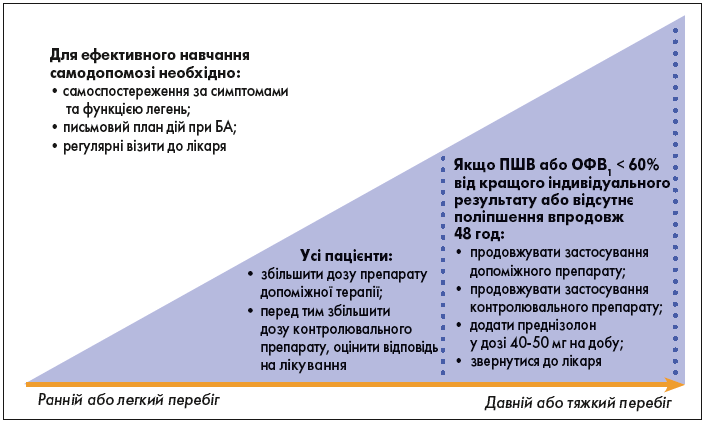
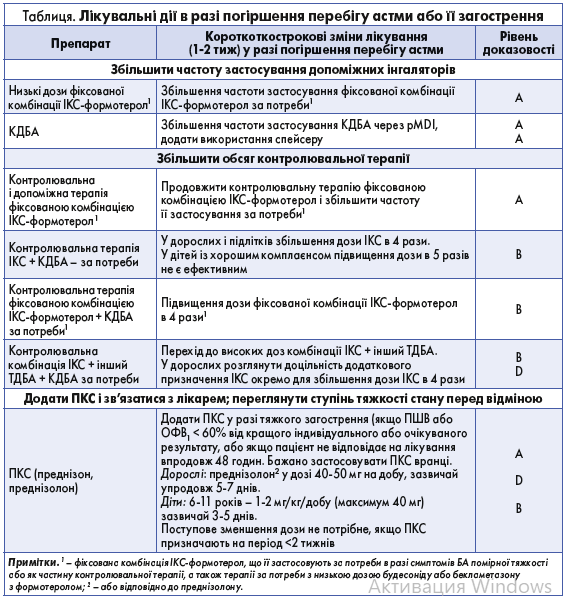
Термін «письмовий» було уточнено і до нього було додано інші формати, а саме – друковані, цифрові чи графічні. Необхідно надати пацієнтові інструкції щодо того, до яких змін треба удатися щодо кратності прийому препаратів за потреби і контролювальної терапії, якщо контроль БА погіршився, а також, коли саме необхідно звертатися по медичну допомогу, а не лише за усними вказівками (рис. 3, табл.).
Рис. 3. Самодопомога відповідно до письмового плану дій
Інші зміни
- Використання електронних сигарет пов’язане з підвищеним ризиком респіраторних симптомів і загострень астми.
- Повітряні фільтри можуть зменшити вплив різноманітних дрібних часточок у повітрі, але це не впливає на результати лікування БА [404, 405].
- Були оновлені дані щодо зв’язку між забрудненням повітря і невідкладним зверненням по медичну допомогу при астмі. Так, метааналіз епідеміологічних досліджень продемонстрував значний зв’язок між контактом із такими забруднювачами повітря, як озон, оксиди азоту, аерозолі кислот і дрібні тверді часточки, і симптомами або загостреннями астми, у тому числі невідкладними станами, що потребують відвідування відділень невідкладної допомоги і госпіталізації [107]. Близькість житлових будинків і шкіл до головних доріг асоційована з більшою захворюваністю на астму [411]. Певні погодні й атмосферні умови, як-от гроза [412, 413], можуть стати тригером загострення астми внаслідок різних механізмів, зокрема пилу і забруднення шляхом підвищення рівня респірабельних алергенів і змінам температури і/або вологості.
- У розділі, присвяченому винаходам, що здатні покращувати прихильність пацієнтів до лікування БА, зазначено, що електронні інгалятори, які завчасно нагадують про час застосування або пропущені дози, покращують прихильність до лікування [437-440] і сприяють зниженню частоти загострень і потреби в застосуванні ПКС. Своєю чергою, моніторинг даних електронного інгалятора може виявити погану прихильність до лікування в пацієнтів із тяжкою астмою.
- У пацієнтів із неконтрольованими симптомами БА, незважаючи на лікування середніми або високими дозами ІКС, підвищення рівня еозинофілів крові і вищий рівень FeNO асоційовані з більшим ризиком тяжких загострень [569].
- Нагадування пацієнтам, що були госпіталізовані із загостренням астми, про те, що вони мають продовжувати застосування ІКС-умісної терапії, або, якщо така не була призначена, має бути призначена надалі.
Реферативний огляд Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2022.
Підготувала Анна Артюх
Повну версію дивіться: https://ginasthma.org
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (61) 2022 р.