29 березня, 2023
Роль ранньої профілактики у запобіганні розвитку кровотеч у немовлят з гемофілією А

 Гемофілія – спадкове X-зчеплене захворювання, яке характеризується порушенням згортання крові через дефіцит фактора VIII (FVIII; гемофілія A) чи фактора IX (FIX; гемофілія B), що супроводжується частими крововиливами в суглоби, м’язи та внутрішні органи й призводить до інвалідизації пацієнтів. Тому з метою запобігання розвитку ускладнень кровотеч, які погіршують якість життя хворих, важливо забезпечити їм належну профілактику, що дозволить брати активну участь у різних сферах діяльності суспільства на рівні зі здоровими особами. Раніше профілактичне лікування пацієнтів з гемофілією передбачало введення дефіцитного концентрату фактора згортання з частотою 3 рази на тиждень, що не завжди зручно. Проте сьогодні в Україні є можливість застосування нефакторних препаратів, представником яких є біоспецифічне моноклональне антитіло еміцизумаб (Roche). Його перевагами є тривалість дії, що дозволяє вводити препарат 1 раз на 28 днів, та більш зручний спосіб введення (підшкірний) порівняно з профілактичним внутрішньовенним введенням концентрату фактора згортання.
Гемофілія – спадкове X-зчеплене захворювання, яке характеризується порушенням згортання крові через дефіцит фактора VIII (FVIII; гемофілія A) чи фактора IX (FIX; гемофілія B), що супроводжується частими крововиливами в суглоби, м’язи та внутрішні органи й призводить до інвалідизації пацієнтів. Тому з метою запобігання розвитку ускладнень кровотеч, які погіршують якість життя хворих, важливо забезпечити їм належну профілактику, що дозволить брати активну участь у різних сферах діяльності суспільства на рівні зі здоровими особами. Раніше профілактичне лікування пацієнтів з гемофілією передбачало введення дефіцитного концентрату фактора згортання з частотою 3 рази на тиждень, що не завжди зручно. Проте сьогодні в Україні є можливість застосування нефакторних препаратів, представником яких є біоспецифічне моноклональне антитіло еміцизумаб (Roche). Його перевагами є тривалість дії, що дозволяє вводити препарат 1 раз на 28 днів, та більш зручний спосіб введення (підшкірний) порівняно з профілактичним внутрішньовенним введенням концентрату фактора згортання.
Тема профілактики та лікування ускладнень гематологічних захворювань активно висвітлювалася провідними гематологами у рамках науково-практичної конференції «Діагностика та лікування гематологічних захворювань: підведення підсумків 2022 року», яка пройшла 20-21 грудня. Зокрема, про оновлені дані щодо ролі ранньої профілактики у наймолодших пацієнтів з гемофілією А, оприлюднені на конгресі Американського товариства гематологів (American Society of Hematology, ASH) 2022 року розповіла завідувачка центру патології гемостазу Національної дитячої спеціалізованої лікарні «ОХМАТДИТ» МОЗ України, кандидат медичних наук Катерина Вікторівна Вільчевська.
– Гемофілія – орфанне захворювання, яке діагностується у ранньому дитячому віці та супроводжується інвалідизацією пацієнтів. Одним із головних завдань ведення хворих цієї групи є запобігання виникненню кровотеч шляхом призначення ранньої профілактики. Немовлята від народження до 12 місяців з гемофілією A часто не отримують профілактичного лікування, що зумовлює зростання ризику розвитку кровотеч та їх ускладнень, таких як внутрішньочерепні крововиливи й ураження суглобів. Це супроводжується підвищенням рівня інвалідизації і смертності та може мати руйнівний вплив на життя дитини (J.A. Mason et al., 2021; N.J. Anderson et al., 2017).
Частота внутрішньочерепних крововиливів незалежно від віку є вищою серед осіб з гемофілією порівняно з загальною популяцією (2,30 проти 0,25 на 1000 людино-років; A.F. Zwagemaker et al., 2021). При цьому новонароджені з гемофілією мають найвищий ризик розвитку внутрішньочерепних крововиливів, він в 11,2 раза вищий, ніж у немовлят з гемофілією віком 1-12 місяців (A.F. Zwagemaker et al., 2021; N.J. Anderson et al., 2020). Після періоду новонародженості ризик внутрішньочерепних крововиливів у хворих на гемофілію є найвищим у дітей раннього віку (A.F. Zwagemaker et al., 2021). У когортному дослідженні у Великій Британії середній вік дітей з гемофілією, у яких уперше стався внутрішньочерепний крововилив, становив 5 місяців, з них тільки 6% попередньо отримували профілактичну терапію (E.A. Chalmers et al., 2018). Тобто частота внутрішньочерепних крововиливів при гемофілії А вища у новонароджених, ніж у немовлят старшого віку, що свідчить про їх незахищеність від кровотеч за умови невчасного початку профілактичного лікування. Відсутність належної профілактики кровотеч при гемофілії A у немовлят створює ризик розвитку тривалих проблем зі здоров’ям суглобів, оскільки дво- чи триразова кровотеча в один і той же суглоб може призвести до його незворотного ушкодження, що врешті знижує якість життя (J.A. Mason et al., 2021).
З метою запобігання виникненню ускладнень у хворих на гемофілію Всесвітня федерація гемофілії розробила рекомендації. У цьому документі зазначено, що педіатричним пацієнтам із тяжкою формою гемофілії A чи B необхідно розпочинати ранню профілактику концентратами факторів згортання крові або іншими гемостатичними агентами до початку захворювання суглобів, оптимально – до 3-річного віку, щоб запобігти спонтанним і проривним кровотечам, включаючи гемартрози, які можуть призвести до уражень суглобів (A. Srivastava et al., 2020).
За даними M.E. Mancuso та співавт. (2021), регулярна профілактична терапія знижує ризик розвитку внутрішньочерепних крововиливів більше ніж на 50%, автори рекомендують починати профілактику якнайшвидше після встановлення діагнозу гемофілії А для запобігання внутрішньочерепним крововиливам. Зокрема, в осіб з гемофілією А у сімейному анамнезі профілактику слід починати з народження. Довгострокові спостереження свідчать, що навіть внутрішньосуглобові кровотечі легкого ступеня, які повторюються після народження дитини до початку профілактики, можуть призвести до гемофільної артропатії й інвалідизації. І навпаки – початок профілактики гемофілії A на ранньому етапі життя забезпечував найкращі віддалені результати (M.J. Manco-Jonson et al., 2007; J. Oldenburg et al., 2015).
При проведенні профілактики концентратом FVIII у немовлят з гемофілією A можуть виникнути окремі труднощі. Зокрема, встановлення катетера для внутрішньовенного введення препарату є болючою травматичною процедурою, яка може супроводжуватися зростанням ризику розвитку кровотечі, інфекції та тромбозу (у рідкісних випадках; B.B. Warren et al., 2020). Труднощі профілактики концентратами факторів згортання можуть бути пов’язані також зі зростанням імовірності розвитку інгібіторів до FVIII, що найчастіше спостерігається протягом перших 50 днів введення препарату (H.M. van den Berg et al., 2019). У дітей відмічається швидше виведення концентрату FVIII, ніж у дорослих, тому дітям потрібні частіші ін’єкції концентрату FVIII (3-4 рази на тиждень). Тобто профілактика ускладнень гемофілії шляхом введення концентрату FVIII у немовлят утруднена через необхідність частих внутрішньовенних інфузій і ризик розвитку інгібіторів до концентратів факторів згортання крові (N.J. Anderson et al., 2017).
В Україні у пацієнтів з гемофілією сьогодні є можливість застосовувати нефакторні препарати. У 3-му виданні рекомендацій Всесвітньої федерації гемофілії зазначено, що схваленим препаратом для профілактики у всіх хворих на тяжку форму гемофілії A, включаючи немовлят, незалежно від віку та статусу інгібіторів FVIII, є еміцизумаб. У цьому ж документі вказано, що підшкірний шлях введення еміцизумабу спрощує початок профілактичного лікування дітей у дуже ранньому віці без необхідності встановлення катетера. Для пацієнтів, у яких венозний доступ є проблематичним, слід розглянути нефакторну замінну терапію, яку можна вводити підшкірно. У рекомендаціях Медичної та наукової консультативної ради (NHF’s Medical and Scientific Advisory Council) зазначено, що у немовлят варто розглянути можливість профілактики еміцизумабом у будь-який час після народження, враховуючи підвищений ризик розвитку внутрішньочерепних крововиливів до початку профілактики концентратом FVIII.
Досвід застосування нефакторного препарату сьогодні відповідає незадоволеним потребам популяції. Підшкірне введення еміцизумабу надає можливість проведення ранньої профілактики у немовлят з гемофілією A від народження, при цьому зростає масив доказів щодо ефективності й безпеки лікарського засобу. Рішення про початок прийому еміцизумабу слід приймати в кожному конкретному випадку окремо шляхом його обговорення між медичними працівниками, батьками чи опікуном.
Довгострокові спостереження є виправданими для вивчення ефективності використання еміцизумабу від народження у немовлят з гемофілією A. Зокрема, у дослідженні HAVEN 7 протягом 8 років проводили збір та обмін даними щодо безпеки та здоров’я суглобів з метою обґрунтування ранньої профілактики еміцизумабом у немовлят із гемофілією A від народження (G. Young et al., 2021; S. W. Pipe et al., 2022; A. Srivastava et al., 2020; M.E. Mancuso et al., 2021).
У рамках форуму ASH-2022 було представлено проміжні результати багатоцентрового відкритого дослідження IIIb фази HAVEN 7. Його метою було оцінювання ефективності, безпеки, фармакокінетики та фармакодинаміки еміцизумабу у немовлят віком до 12 місяців із тяжкою гемофілією A без інгібіторів до FVIII, а також збір довгострокових даних щодо ефективності та безпеки препарату у плані запобігання розвитку внутрішньосуглобових крововиливів протягом 8 років для подальшого розуміння впливу профілактики еміцизумабом від народження до раннього дитинства. На початку дослідження пацієнтам призначали еміцизумаб у насичувальній дозі 3 мг/кг маси тіла протягом 4 тижнів з подальшим введенням у підтримувальній дозі протягом 48 тижнів і розподілом у групи отримання препарату у дозі 1,5 мг/кг на тиждень чи 3 мг/кг на 2 тижні, чи 6 мг/кг на 4 тижні протягом наступних 7 років. На початку дослідження середній вік хворих становив 5,1 місяця, 74,1% із них у мали родичів з гемофілією. Серед учасників дослідження 44,4% раніше не отримували лікування, а у 66,7% хворих спостерігалася щонайменше одна кровотеча до отримання першої дози еміцизумабу. Тобто у дослідження включали попередньо не лікованих або частково лікованих новонароджених віком до 12 місяців із тяжкою формою гемофілії A без інгібіторів до FVIII та без внутрішньочерепних крововиливів.
На момент проміжного аналізу 54 учасники отримали мінімум одну дозу еміцизумабу. Середня тривалість лікування складала 42,1 тижня. Після навантажувальної дози середня мінімальна концентрація становила 63,2 мкг/мл (95% довірчий інтервал – ДІ – 59,5-66,8). Мінімальні рівноважні концентрації складали 60-65 мкг/мл та були вищими, ніж повідомлялося у попередніх дослідженнях HAVEN, і підтримувалися протягом усього дослідження. При цьому середні рівноважні мінімальні концентрації дещо збільшувалися з віком і досягали плато на рівні 65 мкг/мл через 6 місяців. Лікування еміцизумабом не вплинуло на середні концентрації факторів IX та X, при цьому відмічалася нормалізація активованого часткового тромбопластинового часу до 3 тижнів у більшості учасників дослідження.
У цьому клінічному дослідженні жодне небажане явище не призвело до відміни препарату, потреби у модифікації дози або переривання його прийому. Усі небажані явища, які виникли під час лікування, не були пов’язані з використанням еміцизумабу. При вивченні імуногенності препарату у 48 пацієнтів у жодного з них не виявлено нейтралізуючих антитіл до еміцизумабу. У процесі аналізу проміжних результатів дослідження відмічалася ефективність препарату щодо кінцевих точок дослідження.
Під час проміжного аналізу даних пацієнтів, середній вік яких дорівнював 16 місяців, середня річна частота кровотеч (РЧК) на основі моделі (95% ДІ) становила 0,4 (95% ДІ 0,23-0,65) для всіх випадків пролікованих кровотеч, 1,9 (95% ДІ 1,35-2,68) – для всіх випадків кровотеч і 0 (95% ДІ 0,00-0,20) – для пролікованих м’язових кровотеч. РЧК для лікованих спонтанних кровотеч не оцінювали (рис. 1). У 77,8% (n=42) учасників не відмічалися кровотечі після лікування, тоді як у 42,6% (n=23) дітей не було жодного випадку кровотеч. Жоден пацієнт не потребував лікування спонтанних кровотеч, а 98,1% учасників – м’язових кровотеч (рис. 2). Усі проліковані кровотечі у досліджені вважалися травматичними.
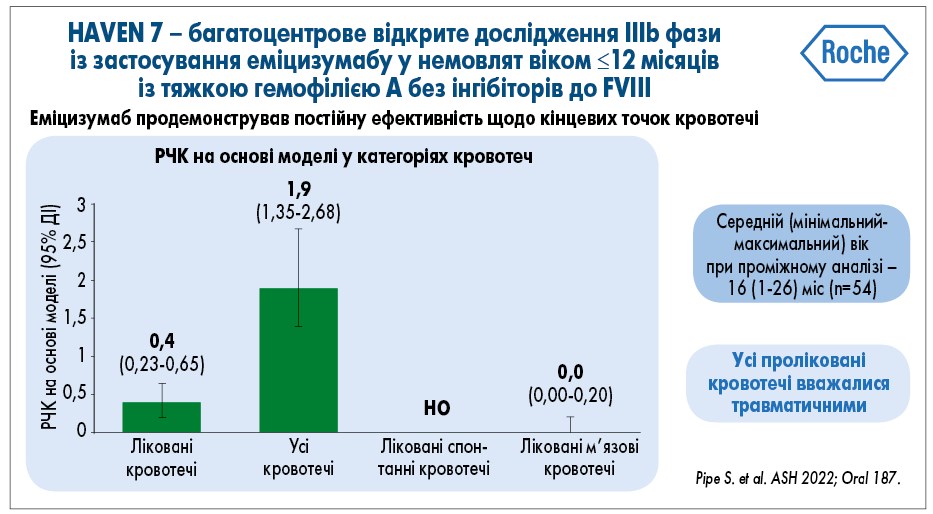 Рис. 1. Річна частота кровотеч на основі моделі
Рис. 1. Річна частота кровотеч на основі моделі
РЧК – річна частота кровотеч; НО – не оцінено.
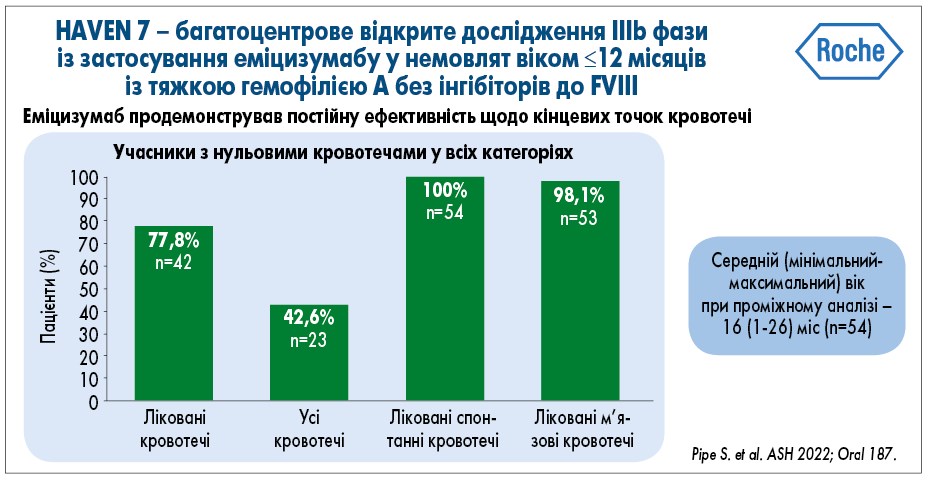 Рис. 2. Частка пацієнтів без кровотеч усіх категорій
Рис. 2. Частка пацієнтів без кровотеч усіх категорій
Отже, результати проміжного аналізу свідчать, що учасники мали низьку РЧК, при цьому в усіх пацієнтів не було спонтанних кровотеч під час лікування. Фармакокінетичний аналіз підтверджував дані про те, що у немовлят з гемофілією ефективні концентрації в плазмі крові були досягнуті та підтримувалися. Профілактика еміцизумабом добре переносилася, у жодного немовляти не виникло внутрішньочерепного крововиливу та не отримано позитивного результату на нейтралізуючі антитіла.
Дослідження HAVEN 7 триває, його метою є збір та обмін довгостроковими даними про безпеку профілактики еміцизумабом від народження до раннього дитячого віку протягом 8 років для подальшого розуміння значення препарату у збереженні здоров’я суглобів упродовж тривалого часу (S.W. Pipe et al., 2022).
Згідно з матеріалами конгресу Міжнародного товариства з тромбозу та гемостазу (International Society of Thrombosis and Haemostasis, ISTH, 2020), при порівнянні ефективності профілактики еміцизумабом у рамках програми HAVEN у пацієнтів з/без інгібіторів до FVIII молодших і старших 12 років відмічалося збільшення частки осіб без кровотеч. Це свідчить про перехід гемофілії з тяжкої форми у легку та появу нових перспектив у лікуванні захворювання (рис. 3).
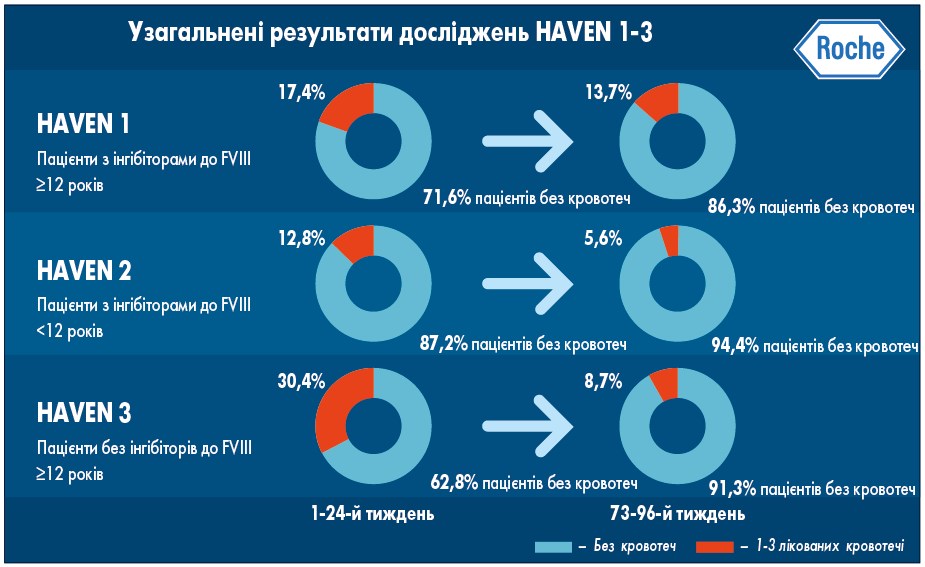 Рис. 3. Ефективність профілактики еміцизумабом за результатами аналізу програми досліджень HAVEN (за матеріалами конгресу ISTH 2020 р.)
Рис. 3. Ефективність профілактики еміцизумабом за результатами аналізу програми досліджень HAVEN (за матеріалами конгресу ISTH 2020 р.)
Сьогодні також вивчається і застосування еміцизумабу у немовлят із гемофілією A в умовах клінічної практики, однак все ще існує потреба в додаткових клінічних даних щодо його ефективності та безпеки у профілактиці ускладнень гемофілії A (M. Shima et al., 2019; M. Mancuso et al., 2021; A. Srivastava et al., 2020).
Таким чином, за даними проміжного дослідження IIIb фази HAVEN 7, еміцизумаб відіграє важливу роль у ранній профілактиці тяжкої гемофілії A у немовлят віком до 12 місяців щодо запобігання розвитку ускладнень кровотеч, таких як внутрішньочерепні крововиливи та ураження суглобів, що призводять до інвалідизації пацієнтів і погіршення якості їхнього життя.
Підготувала Ірина Пікалюк
Матеріал підготовлено за підтримки ТОВ «Рош Україна». Для розміщення у спеціалізованих виданнях, призначених для медичних закладів або спеціалістів охорони здоров’я. Інформація для професійної діяльності медичних і фармацевтичних працівників. Деякі схеми лікування можуть включати лікарські засоби, застосовані за межами їхніх показань та/або не зареєстровані в Україні. Запит медичної інформації про продукти ТОВ «Рош Україна» ви можете надіслати на електронну адресу: ukraine.medinfo@roche.com. ТОВ «Рош Україна», м. Київ, 03150, вул. Велика Васильківська, 139. Тел.: +380 (44) 298-88-33, факс: +380 (44) 298-88-33. Тел. тільки для України: 0800-501-50. www.roche.ua. Багатомовна глобальна гаряча лінія для медичних працівників та пацієнтів за тел.: +36 146-182-58. WhatsApp/SMS: +36 707-177-394; e-mail: patientcare@roche.com. Повідомити про побічні явища під час лікування препаратом ТОВ «Рош Україна» або поскаржитись на якість препарату ви можете за контактними реквізитами офісу або на електронну адресу: ukraine.safety@roche.com.
Препарат еміцизумаб, реєстраційне посвідчення UA/16914/01/01/, UA/16914/01/02.
M-UA-00000742
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 6 (79) 2022 р.



