29 березня, 2023
Ефективність помалідоміду в лікуванні множинної мієломи: погляд через призму міжнародних досліджень
 Множинна мієлома (ММ) – злоякісна В-клітинна лімфоїдна пухлина, що виникає унаслідок неконтрольованої проліферації неопластичних плазматичних клітин, які продукують імуноглобулін. ММ визнана другою за частотою онкогематологічною патологією, на частку якої припадає близько 10% пухлин системи крові та 1,0-1,8% усіх онкологічних захворювань.
Множинна мієлома (ММ) – злоякісна В-клітинна лімфоїдна пухлина, що виникає унаслідок неконтрольованої проліферації неопластичних плазматичних клітин, які продукують імуноглобулін. ММ визнана другою за частотою онкогематологічною патологією, на частку якої припадає близько 10% пухлин системи крові та 1,0-1,8% усіх онкологічних захворювань.
17-18 листопада 2022 року відбулася XIV науково-практична конференція з міжнародною участю «Сучасні підходи до діагностики та лікування лімфопроліферативних захворювань», у рамках якої професор Ягеллонського університету (м. Краків, Польща) Артур Юрчишин поділився сучасними аспектами терапії ММ.
– Тривалий час ММ належала до захворювань, які не піддаються лікуванню. Проте за останні десятиліття зроблено значний прорив у цьому напрямі, пов’язаний із впровадженням нових підходів до лікування. Зокрема, прогрес у терапії ММ спостерігається з початку 2000-х років, що зумовлено безпрецедентною кількістю (понад 25) інноваційних препаратів, їх впровадження дозволило значно збільшити загальну виживаність (ЗВ) хворих. Так, застосування нових препаратів, у тому числі інгібіторів протеасом (бортезоміб, карфілзоміб, іксазоміб), імуномодулювальних препаратів (талідомід, леналідомід, помалідомід) і моноклональних антитіл (елотузумаб, даратумумаб, ізатуксимаб) дозволило покращити виживаність хворих за рахунок розширення терапевтичних можливостей. Це вкрай актуально, оскільки ММ характеризується ремісіями та рецидивами, що чергуються.
Згідно з сучасними гайдлайнами, новітні стратегії лікування ММ передбачають використання потрійної комбінації препаратів та пролонговане лікування. Потрійна комбінація включає один імуномодулювальний препарат та один препарат групи інгібіторів протеасом для індукційної терапії. У 2021 р. були опубліковані рекомендації Європейського товариства медичної онкології (ESMO), за якими стандартом лікування вперше діагностованої ММ у хворих, які можуть бути кандидатами на трансплантацію стовбурових клітин, є режим VRd (бортезоміб + леналідомід + дексаметазон) або DaraVTD (даратумумаб + бортезоміб + талідомід + дексаметазон). Якщо режим VRd або DaraVTD недоступний, можливе призначення VTd (бортезоміб + талідомід + дексаметазон) або VCd (бортезоміб + циклофосфамід + дексаметазон) [1]. Підтримувальна терапія показана після аутологічної трансплантації стовбурових клітин. З цією метою рекомендовано використовувати леналідомід, що дозволяє істотно покращити безрецидивну та загальну виживаність.
Практично у всіх пацієнтів із ММ з часом виникає рецидив/рефрактерність. Результати попередніх досліджень свідчать, що до впровадження нових препаратів для лікування ММ медіана виживаності без прогресування (ВБП) і ЗВ у разі рефрактерності до леналідоміду та бортезомібу була дуже низькою. Сьогодні в арсеналі клініцистів наявна значна кількість новітніх препаратів, рекомендованих до застосування у другій та подальших лініях терапії. І ключовим завданням для лікаря є вибір такої терапії, яка буде мати найвищу ефективність. K. Yong та співавт. (2016) продемонстрували, що кожна нова лінія терапії супроводжується зменшенням прихильності хворих до лікування. Так, отримані у дослідженні дані засвідчили, що кожен наступний перехід з однієї лінії терапії на іншу супроводжується втратою 15-30% пацієнтів [2]. Саме тому критично важливим є застосування найефективніших схем лікування [3]. Одним з ефективних препаратів для терапії ММ є помалідомід – імуномодулювальний препарат III покоління.
У 2013 р. були оприлюднені результати багатоцентрового рандомізованого відкритого дослідження III фази MM-003, основною вимогою для включення пацієнтів у яке була наявність рефрактерної/рецидивуючої ММ (РРММ) після терапії бортезомібом і леналідомідом [4]. Загалом до дослідження було включено 455 хворих з РРММ, яких рандомізували на дві групи у співвідношенні 2:1. У 1-й групі (n=302) застосовували помалідомід (4 мг/добу перорально у 1-21-й день 28-денного циклу) + низькі дози дексаметазону (40 мг/добу перорально у 1-й, 8, 15 та 22-й дні). Учасники 2-ї групи (n=153) отримували високодозовий режим гормональної терапії: дексаметазон по 40 мг/добу перорально у 1-4-й, 9-12-й та 17-20-й дні. Результати дослідження продемонстрували, що у групі помалідоміду виживаність хворих була істотно вищою: ЗВ склала 12,7 міс, ВБП – 4 міс, тоді як у групі високодозової гормональної терапії ці ж показники становили 8,1 та 1,9 міс.
STRATUS (MM-010) на сьогодні є найбільшим дослідженням, у якому оцінювалася ефективність і безпека режиму помалідомід + низькі дози дексаметазону у пацієнтів із РРММ і несприятливим прогнозом [5]. Критеріями включення, як і в дослідженні MM-003, були наявність РРММ та попереднє лікування бортезомібом і леналідомідом. Медіана спостереження склала 16,8 міс. Загалом у дослідження було включено 682 пацієнти. Медіана ВБП і ЗВ у пацієнтів досягла 4,6 та 11,9 міс, загальний рівень відповіді – 32,6%, тривалість відповіді – 7,4 міс. Отримані дані підтверджують, що режим помалідомід + низькі дози дексаметазону забезпечує клінічно значущі переваги та добре переноситься пацієнтами.
Роль помалідоміду в лікуванні РРММ продемонстрована також у рандомізованому клінічному дослідженні ІІІ фази ICARIA-MM. У ньому оцінювали ефективність трикомпонентної схеми ізатуксимаб + помалідомід + дексаметазон порівняно з комбінацією помалідомід + дексаметазон у 307 пацієнтів, які раніше отримували у середньому 3 лінії терапії [6]. Констатовано збільшення частоти об’єктивної відповіді (ЧОВ; 60 проти 35%) та ВБП (12 проти 7 міс; рис. 1).
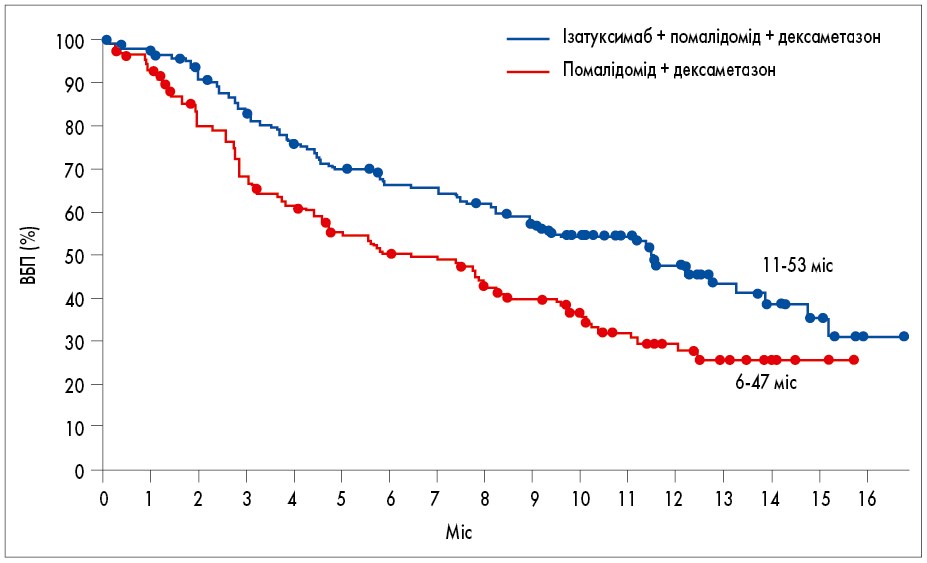 Рис. 1. Результати дослідження ICARIA-MM
Рис. 1. Результати дослідження ICARIA-MM
У рандомізованому контрольованому дослідженні APOLLO (n=304), в якому порівнювали комбінацію даратумумаб + помалідомід + низькі дози дексаметазону з помалідомід + низькі дози дексаметазону, переваги трикомпонентної схеми підтверджені ВБП (12 проти 7 місяців) та ЧОВ (69 проти 46%; рис. 2) [7].
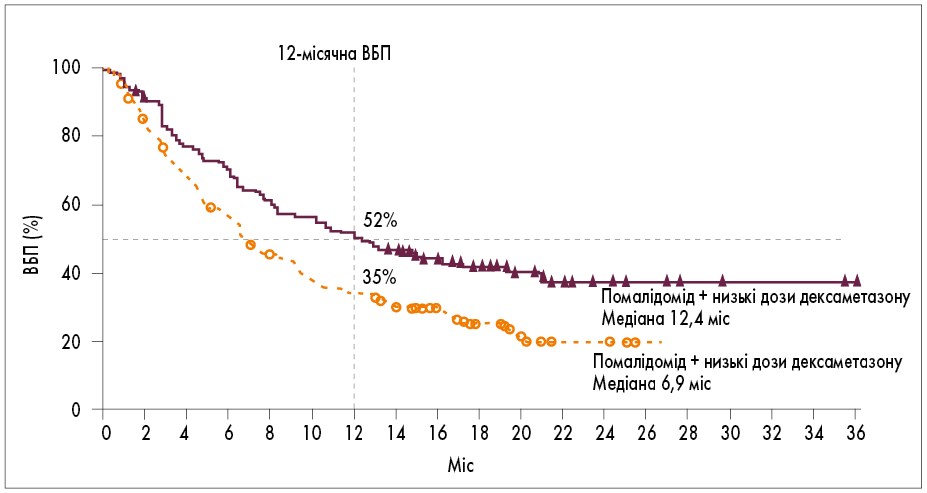
Рис. 2. Результати дослідження APOLLO
У 2019 р. було презентовано результати дослідження OPTIMISMM. Це єдине дослідження III фази, результати якого продемонстрували покращення ВБП на 70% у пацієнтів з ранньою стадією РРММ, котрі мали рефрактерність до леналідоміду [7]. Загалом до дослідження було включено 559 пацієнтів зі 133 лікарень і дослідницьких центрів 21 країни. Попередньо пацієнти отримали щонайменше 2 курси терапії леналідомідом, у 71% хворих до нього реєструвалася рефрактерність. Всіх пацієнтів рандомізували на дві групи: 1-ша група (n=281) отримувала потрійну терапію (помалідомід 4 г/добу у 1-14-й день + бортезоміб 1,3 мг/м2 площі поверхні тіла у 1-й, 4, 8 і 11-й дні 1-8-го циклу + дексаметазон 20 мг/добу), 2-га група (n=278) – подвійну терапію (бортезоміб 1,3 мг/м2 + дексаметазон 20 мг/добу). Результати цього дослідження продемонстрували, що у групі помалідоміду ВБП була істотно вищою, ніж у пацієнтів, які отримували бортезоміб + дексаметазон (11,2 міс; 95% ДІ 9,66-13,73 та 7,1 міс; 95% ДІ 5,88-8,48 відповідно).
Отже, результати сучасних досліджень свідчать, що застосування помалідоміду разом з дексаметазоном у низьким дозах є ефективною та безпечною терапією ММ після другого рецидиву. ВБП при застосуванні помалідоміду складає від 6 міс. Комбінована терапія із включенням помалідоміду (з дексаметазоном або бортезомібом) забезпечує вищу виживаність хворих, ніж схема бортезоміб + дексаметазон і леналідомід, особливо в другій лінії. Наявні дані також свідчать, що трикомпонентна схема помалідомід + бортезоміб + дексаметазон ефективна при РРММ у хворих групи високого ризику.
Список літератури знаходиться в редакції.
Підготувала Анна Хиць
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 6 (79) 2022 р.



