6 квітня, 2023
Зниження рівня холестерину ліпопротеїнів низької щільності в пацієнтів після гострого коронарного синдрому на тлі гіполіпідемічної терапії
Пацієнти, які перенесли гострий коронарний синдром (ГКС), мають високий ризик повторних ішемічних серцево-судинних (СС) подій, особливо впродовж першого року після виписки з лікарні. На основі підтвердженої причинної ролі холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) у розвитку атеросклерозу продемонстровано чіткий зв’язок між зниженням рівня ХС ЛПНЩ завдяки фармакотерапії і зменшенням кількості СС-ускладнень на тлі ГКС. У сучасних європейських рекомендаціях йдеться про важливість контролю рівня ХС ЛПНЩ, покрокового початку й ескалації гіполіпідемічної терапії (ГЛТ) на ранній стадії після ГКС. Асоціація невідкладної серцево-судинної допомоги (ACVC) у співпраці з Європейською асоціацією превентивної кардіології (EAPC) і Європейським товариством кардіологів (ESC) розробили клінічну консенсусну заяву, у якій зосереджено увагу на обґрунтуванні наявних доказів, їх упровадженні у клінічну практику, а також проблемах, із якими стикаються лікарі, та шляхах їх розв’язання для надання якісної допомоги пацієнтам після ГКС. Пропонуємо до вашої уваги ключові положення цього документа.
У настанові ESC і Європейського товариства з атеросклерозу (EAS, 2019) щодо лікування дисліпідемії та рекомендаціях ESC (2020) із ведення хворих на ГКС без елевації сегмента ST ідеться про необхідність поетапного підходу під час проведення ГЛТ із повторним оцінюванням цільових рівнів ХС ЛПНЩ через 4‑6 тиж. (Collet et al., 2021; Mach et al., 2020). Високоінтенсивну статинотерапію слід розпочинати в усіх осіб із ГКС, при цьому цільовий рівень ХС ЛПНЩ становить <55 мг/дл (<1,4 ммоль/л) зниження щонайменше на 50% проти вихідного, незалежно від показника, який був на початку. Якщо цільових значень ХС ЛПНЩ не вдається досягти, до лікування доцільно додати езетиміб. У разі, якщо така стратегія теж є недостатньо ефективною, слід розглянути ад’ювантну терапію інгібітором пропротеїнконвертази субтилізин / кексин типу 9 (PCSK9).
У рекомендаціях ESC2021 р. щодо профілактики серцево-судинних захворювань (ССЗ) у клінічній практиці зазначено важливість покрокового лікувального підходу до встановлення цільових показників рівня ХС ЛПНЩ. Так, у пацієнтів із діагностованим атеросклеротичним ССЗ початковий цільовий рівень ХС ЛПНЩ становить <70 мг/дл (<1,8 ммоль/л), наступний <55 мг/дл (<1,4 ммоль/л) (Visseren et al., 2021).
За даними досліджень, після виписки зі стаціонару багатьом пацієнтам із ГКС не вдається досягти цільового рівня ХС ЛПНЩ через неефективну ГЛТ і неналежне коригування доз препаратів (Cannon et al., 2021; Kotseva et al., 2019).
У хворих, які перенесли інфаркт міокарда (ІМ), загальна частота повторного ІМ, інсульту або смерті від ССЗ протягом перших трьох місяців становить 10% (Jernberg et al., 2015).
Тож різке і швидке зниження рівня ХС ЛПНЩ (концепція «що нижче, то краще») за допомогою ранньої та інтенсивної комбінованої ГЛТ у популяції пацієнтів після ГКС є розумним підходом (Raber et al., 2022; Nicholls et al., 2022).
Обґрунтування і біологічна основа зниження рівня ХС ЛПНЩ у пацієнтів із ГКС
Тромбоцити, моноцити і ліпіди, а також ендотеліальна дисфункція лежать в основі атерогенезу, який спричиняє розвиток атеросклеротичного ураження коронарних артерій (Libby, 2021).
Основними механізмами, що призводять до гострих СС-наслідків, є:
- розрив бляшок;
- поверхнева ерозія;
- утворення тромбів.
На сьогодні вважають, що причиною близько третини випадків ГКС є поверхнева ерозія, механізм виникнення якої до кінця не вивчений. Як відомо, важливу роль відіграє взаємодія матриксних металопротеаз, компонентів вродженої імунної системи й нейтрофілів разом з активованими тромбоцитами (Heger et al., 2019).
За останніми даними, ХС ЛПНЩ асоційований із кількістю і прозапальною активністю циркулюючих моноцитів, що підтверджує зв’язок між високим рівнем ХС ЛПНЩ і прогресуванням атеросклерозу (Stiekema et al., 2021). Моноцити пацієнтів із сімейною гіперхолестеринемією (СГ) мають підвищену експресією ключового рецептора, необхідного для екстравазації в атеросклеротичні бляшки. Своєю чергою, на тлі лікування інгібіторами PCSK9 відбувається зменшення вмісту ХС у моноцитах, зниження їхньої прозапальної активності та міграційного потенціалу. Це підтверджує кореляцію між підвищеним рівнем циркулюючого ХС, активацією запалення та прогресуванням атеросклеротичного захворювання (Bernelot Moens et al., 2017).
C.P. Cannon et al. (2004) продемонстрували чіткий зв’язок між інтенсивною ГЛТ та кращими результатами в пацієнтів після ГКС. Нещодавно описано зменшення кількості СС-наслідків, коли зниження рівня ХС ЛПНЩ перевищувало визначені цільові показники, підтверджуючи ефективність концепції «що нижче, то краще» як терапевтичної стратегії для осіб із ГКС (Giugliano et al., 2017).
У двох невеликих рандомізованих клінічних дослідженнях оцінювали вплив дуже раннього додавання інгібіторів PCSK9 алірокумабу або еволокумабу до стандартної ГЛТ у пацієнтів із ГКС без виразного атеросклеротичного ураження судин, які перенесли черезшкірне коронарне втручання (ЧКВ) (Raber et al., 2022; Nicholls et al., 2022). За отриманими даними, на тлі лікування спостерігали значне поліпшення стану хворих на початковому етапі. Більшість пацієнтів, які отримували стандартну ГЛТ, не досягли цільових рівнів ХС ЛПНЩ. Тобто раннє інгібування PCSK9 в осіб із ГКС є дієвим і безпечним, забезпечує стабілізаційний ефект, що запобігає розриву бляшки й розвитку повторного ГКС.
Фармакодинамічний профіль, ефективність і безпека гіполіпідемічних препаратів
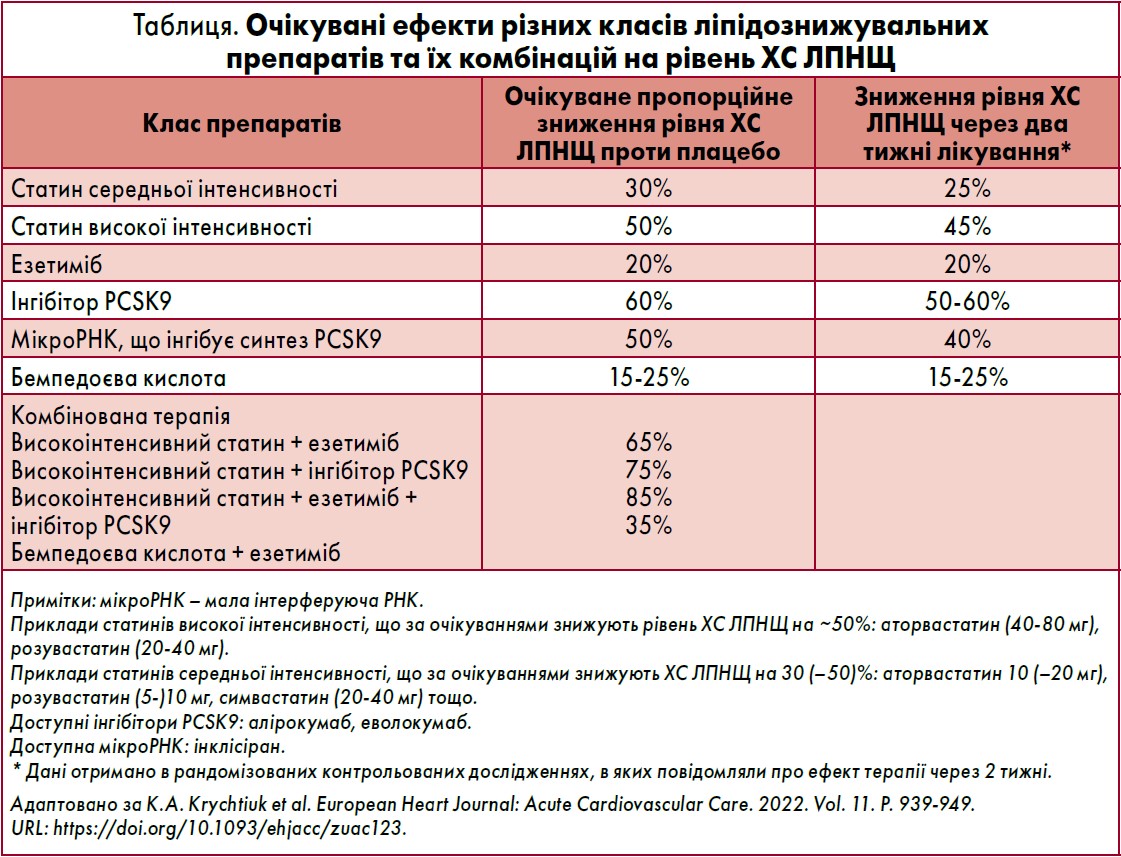
У більшості попередніх досліджень увагу зосереджували на величині зменшення рівня ХС ЛПНЩ, а не швидкості зниження вмісту ліпідів. Однак у пацієнтів після ГКС спостерігали підвищений ризик рецидивів, тому швидкість зниження ХС ЛПНЩ стала новим напрямом вивчення для науковців (Li et al., 2019; Schupke et al., 2019). Зокрема, у таблиці узагальнено дані щодо величини зниження рівня ХС ЛПНЩ, досягнутого на тлі застосування різних препаратів через два тижні після початку терапії (Trankle et al., 2019; Kereiakes et al., 2015).
Як відомо, високоінтенсивне лікування статинами сприяє зменшенню вмісту ХС ЛПНЩ на 50%, а комбінована терапія з езетимібом – на 65% проти вихідного рівня. Наявні дані щодо ефективності й безпеки терапії інгібіторами PCSK9, націленої на зниження рівня ХС ЛПНЩ в осіб після ГКС у гострій фазі. У дослідженні EVACS (n=57) значне зниження рівня ХС ЛПНЩ було очевидним через 24 год після застосування еволокумабу в пацієнтів на дуже ранній стадії після ГКС, причому дві третини з них досягли рекомендованих рівнів ХС ЛПНЩ <55 мг/дл (<1,4 ммоль/л) на момент виписки з лікарні (Leucker et al., 2020). Результати дослідження EVOPACS (n=308) підтвердили 90% досягнення цільового рівня ХС ЛПНЩ через вісім тижнів після ГКС у разі початку терапії еволокумабом порівняно з 11% у групі стандартного лікування (Koskinas et al., 2019).
У дослідженні VCU-AlirocRT (n=20) із застосуванням алірокумабу протягом 24 год після розвитку ГКС без підйому сегмента ST фіксували значне зменшення вмісту ХС ЛПНЩ уже на 3-й день терапії, а також різке зниження зазначеного показника до 28 мг/дл (0,72 ммоль/л) через 14 днів після початку лікування (Trankle et al., 2019).
Щодо безпеки ГЛТ, то є припущення, що агресивне зниження ХС ЛПНЩ може спричиняти розвиток геморагічного інсульту (Amarenco et al., 2006).
Однак аналіз дослідження ODYSSEY OUTCOMES продемонстрував, що частота геморагічного інсульту після ГКС виявилася незначною і не підвищувалася на тлі лікування інгібітором PCSK9 алірокумабом порівняно з плацебо (Jukema et al., 2019).
Також виконано метааналіз, що охопив 11 досліджень за участю понад 20 тис. пацієнтів, для порівняння менш і більш інтенсивного зниження рівня ХС ЛПНЩ у хворих після ішемічного інсульту. За отриманими даними, інтенсивніше зменшення рівня ХС ЛПНЩ асоціювалося з підвищеним ризиком геморагічного інсульту, тоді як частота повторного інсульту і серйозних СС-подій знижувалась (Lee et al., 2022).
Автори дійшли висновку, що переваги й ризики інтенсивнішого зниження рівня ХС ЛПНЩ загалом є сприятливішими, особливо в осіб з атеросклеротичним захворюванням (Mach et al., 2018).
Докази і досвід зниження рівня ХС ЛПНЩ у пацієнтів із ГКС на тлі лікування
Значне зниження рівня ХС ЛПНЩ після ГКС
У дослідженні MIRACL, яке тривало чотири місяці, отримано переконливі докази того, що у хворих після ГКС застосування аторвастатину (80 мг/добу) порівняно з плацебо асоціювалося зі значним зменшенням рівня ХС ЛПНЩ. Це лікування було пов’язане зі зниженням ризику великих СС-подій (MACE) на 16% (Schwartz et al., 2001).
Зокрема, у випробуванні PROVE-IT із середньою тривалістю два роки порівнювали використання аторвастатину (80 мг/добу) і правастатину (40 мг/добу). Таке застосування аторвастатину корелювало зі значно рідшими випадками MACE (зниження ризику на 16%), причому клінічна користь стала очевидною вже через чотири місяці після рандомізації (Cannon et al., 2004).
Варто зауважити, що нещодавно також отримано дані стосовно зменшення ризику СС-подій після ГКС завдяки додаванню до статинів нестатинової ГЛТ. Так, у випробуванні IMPROVE-IT порівнювали езетиміб (10 мг) і плацебо, кожен із яких додавали до симвастатину в дозуванні 40‑80 мг/добу, протягом 10 днів після ГКС, де отримано такі результати:
- Переваги езетимібу виявляли вже після року лікування.
- Зафіксовано значуще зниження відносного ризику MACE на 6% через шість років (Cannon et al., 2015).
У дослідженні ODYSSEY OUTCOMES порівнювали застосування інгібітора PCSK9 алірокумабу і плацебо в пацієнтів через 1‑12 міс. після ГКС із рівнем ХС ЛПНЩ >70 мг/дл (>1,8 ммоль/л) на тлі стабільної високоінтенсивної статинотерапії. Алірокумаб знижував ризик MACE на 15%, при цьому ефективність була очевидною орієнтовно через рік (Schwartz et al., 2018).
За даними дослідження FOURIER, лікування еволокумабом у пацієнтів з ІМ упродовж 12 міс. після рандомізації (n=5711), які мали високу частоту СС-ускладнень, було пов’язане із суттєвішим зниженням первинної комбінованої кінцевої точки на 19% проти 8% в осіб із віддаленим ІМ (n=16 609) (Gencer et al., 2020). У межах відкритого розширеного випробування FOURIER із середнім періодом спостереження п’ять років понад 3 тис. хворих, які спочатку отримували плацебо, були переведені на еволокумаб і порівнювалися з аналогічною за розміром групою учасників, що продовжували приймати цей препарат. За отриманими даними, остання група мала на 20% нижчий рівень смертності від ССЗ, ІМ або інсульту, що свідчить про важливість раннього ефективного лікування (O’Donoghue et al., 2022).
Різке / раннє зниження рівня ХС ЛПНЩ після ГКС
Сьогодні доступні дані широкомасштабних досліджень, які підтверджують значне зниження рівня ХС ЛПНЩ на тлі ефективної ГЛТ після ГКС, але докази стосовно переваг різкого зменшення рівня ХС ЛПНЩ поки що обмежені. Так, у контрольованому плацебо дослідженні SECURE-PCI не продемонстровано клінічної користі застосування двох навантажувальних доз аторвастатину по 80 мг у хворих на ГКС із запланованим інвазивним лікуванням. Однак у підгрупі пацієнтів, які перенесли ЧКВ (65%), частота МАСЕ значуще знизилась (на 28%), тоді як у групі без ЧКВ спостерігали тенденцію до зростання цього показника (Berwanger et al., 2018).
За даними національного реєстру США, що охоплюють 300 тис. пацієнтів, призначення статинів упродовж 24 год після ГКС пов’язане із суттєвим зниженням госпітальної летальності (Fonarow et al., 2005).
До того ж раннє застосування статинів асоційоване з меншою кількістю випадків таких небезпечних станів, як:
- кардіогенний шок;
- аритмії;
- зупинка та розрив серця.
Наприклад, обсерваційні дані підтверджують, що призначення статинів протягом 24 год після госпіталізації з приводу ГКС корелює зі зниженням частоти MACE на 22% упродовж майже чотирьох років спостереження (Kimet al., 2019).
Отже, дуже раннє ініціювання статинотерапії високої інтенсивності перед ЧКВ може бути корисним. Зокрема, початок приймання інгібіторів PCSK9 у стаціонарі забезпечує досягнення цільового рівня ХС ЛПНЩ у більшості пацієнтів після ГКС у ранній і вразливій фазах. Проте необхідні додаткові дослідження, щоб визначити, чи спостерігатиметься надалі зменшення кількості СС-подій на тлі досягнутого зниження рівня ХС ЛПНЩ за допомогою інгібіторів PCSK9 на дуже ранній стадії після ГКС.
У великому обсерваційному дослідженні за участю 40 607 пацієнтів із нещодавно перенесеним ГКС оцінювали зв’язок між змінами рівня ХС ЛПНЩ під час зазначеної події та амбулаторного візиту через 6‑10 тижнів і ризиком СС-наслідків.
Середній час спостереження становив 3,78 року. У пацієнтів, які після виписки з лікарні отримували високоінтенсивну статинотерапію і досягли >50% зниження рівня ХС ЛПНЩ, фіксували нижчу частоту всіх СС-подій порівняно з тими, хто приймав статини в нижчих дозах. Автори дійшли висновку, що суттєвіше раннє зменшення вмісту ХС ЛПНЩ та інтенсивніше лікування статинами після ІМ асоціювалося зі зниженим ризиком усіх СС-наслідків (Schubert et al., 2021).
В іншому дослідженні вивчали прихильність до статинотерапії та досягнення цільового рівня ХС ЛПНЩ у популяції хворих із високим СС-ризиком. Переважна більшість пацієнтів мали раніше серйозні СС-події (99,9%). За отриманими даними, дотримання режиму лікування через 3 і 6 міс. становило 61 і 55,14% відповідно. Висока прихильність до ГЛТ корелювала з майже втричі вищою ймовірністю досягнення цільового рівня ХС ЛПНЩ (Guglielmi et al., 2017).
Такі висновки свідчать про важливість початку високоінтенсивної ГЛТ до виписки зі стаціонару для досягнення рекомендованих рівнів ХС ЛПНЩ.
Недосягнення цільових показників ліпідного профілю у клінічній практиці: перешкоди і шляхи розв’язання
У дослідженні EUROASPIRE V лише половині хворих було призначено високоінтенсивну ГЛТ (De Backer et al., 2019).
Як зазначають дослідники, у нещодавньому випробуванні DA VINCI частка пацієнтів зі встановленим атеросклеротичним ССЗ і дуже високим СС-ризиком, які отримували високоінтенсивну терапію статинами в комбінації з езетимібом або інгібіторами PCSK9, становила 36,7; 9 і 1,2% відповідно (Ray et al., 2021).
Недосягнення цільових показників рівня ХС ЛПНШ у пацієнтів після перенесеного ГКС може бути пов’язане з такими чинниками:
- призначення неадекватного лікування;
- терапевтична інерція;
- недотримання рекомендацій.
Адаптація ГЛТ відповідно до структурованого протоколу з урахуванням індивідуального СС-ризику є важливою. Крім того, після виписки зі стаціонару обмежений доступ до програм кардіореабілітації і/або брак структурованого подальшого спостереження можуть спричинити затримку повторного оцінювання ліпідного профілю чи втрату отриманих раніше результатів, що обмежує можливості для досягнення оптимальної стратегії вторинної профілактики ГКС. Адже зниження ризику рецидивів у хворих після ГКС протягом усього життя значною мірою залежить від дотримання режиму лікування.
Отже, необхідне впровадження освітніх заходів, орієнтованих на лікарів та осіб, які доглядають пацієнтів після ГКС, із фокусом на доказових даних, рекомендаціях і ефективних стратегіях підвищення комплаєнсу лікування цих хворих. Клініцисти мають сприяти навчанню пацієнтів під час госпіталізації та подальшому спостереженню за їхнім станом завдяки ефективній комунікації та відповідним освітнім матеріалам (Bond et al., 2021).
Стратегії ефективного зниження рівня ліпідів у пацієнтів із ГКС
Адаптація ГЛТ після ГКС у гострій фазі
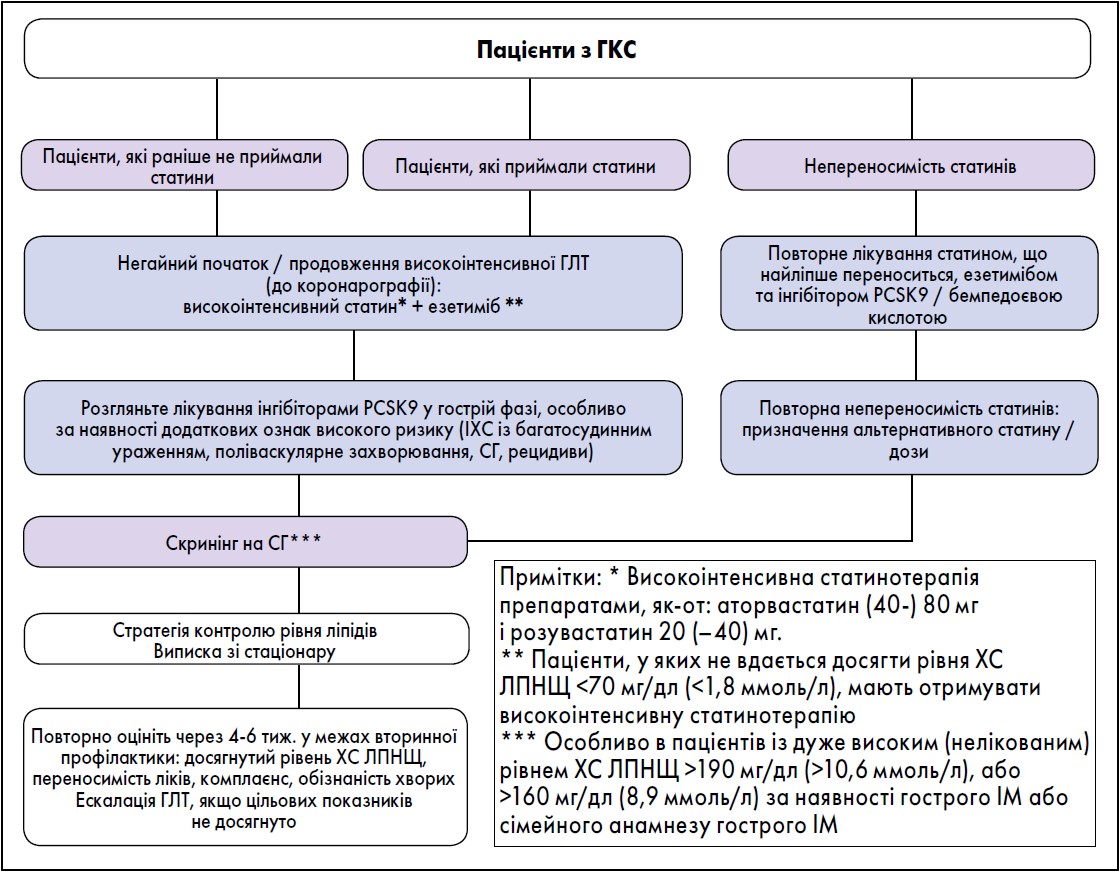
Усі пацієнти з ГКС мають застосовувати високоінтенсивну статинотерапію, яку бажано розпочинати до проведення коронарографії та отримання результатів ліпідної панелі (рисунок). Пацієнтам, які вже приймають статини, важливо продовжувати лікування безперервно або перейти на статини високої інтенсивності.
Рисунок. Алгоритм зниження рівня ХС ЛПНЩ у пацієнтів після перенесеного ГКС
Адаптовано за K.A. Krychtiuk et al. European Heart Journal: Acute Cardiovascular Care. 2022. Vol. 11. P. 939‑949. URL: https://doi.org/10.1093/ehjacc/zuac123.
На додаток до високоінтенсивного лікування статинами доцільним є додавання езетимібу на ранній стадії ГКС незалежно від рівня ХС ЛПНЩ. Підтверджено хорошу переносимість і клінічну користь цього препарату в осіб після щойно перенесеного ГКС, зокрема зниження рівня ХС ЛПНЩ (Cannon et al., 2015). Тож після виписки зі стаціонару пацієнтів після ГКС подальше застосування комбінації високоінтенсивної статинотерапії та езетимібу є доцільним (Ray et al., 2022). Власне, найбільшу користь такого раннього лікування отримують хворі з вихідним рівнем ХС ЛПНЩ >100 мг/дл (>5,6 ммоль/л), адже очікується, що використання лише статинів високої інтенсивності буде недостатньо для досягнення цільового рівня ЛПНЩ <55 мг/дл (<3 ммоль/л).
Також варто зазначити, що початок лікування інгібіторами PCSK9 після перенесеного ГКС може бути корисним і безпечним. Зокрема, у разі застосування цього терапевтичного підходу виявлено високий показник досягнення цільового рівня ХС ЛПНЩ, особливо в ранній фазі після ГКС. Потенційними кандидатами для лікування інгібіторами PCSK9 є пацієнти з додатковими чинниками ризику, як-от:
- Ішемічна хвороба серця (ІХС) із багатосудинним ураженням.
- Поліваскулярне захворювання.
- СГ і значне підвищення рівня ХС ЛПНЩ (Jukema et al., 2019; Sabatine et al., 2018).
У цій популяції досягти цільових показників лише за допомогою традиційної терапії малоймовірно. Крім того, усі хворим на ГКС, особливо з підвищеним рівнем ХС ЛПНЩ і сімейним анамнезом гострого ІМ, необхідно виконати скринінг на потенційну СГ.
Отже, у пацієнтів із високою ймовірністю СГ і рівнем ХС ЛПНЩ >190 мг/дл (>10,6 ммоль/л) слід розглянути призначення потрійної терапії статином високої інтенсивності, езетимібом та інгібітором PCSK9 (Tokgozoglu et al., 2021; Alings et al., 2020).
Непереносимість статинів
Оптимальний підхід до лікування пацієнтів після ГКС, особливо в гострій фазі, у разі підозри на непереносимість статинів ще не визначено (Stroes et al., 2015). Наявні дані досліджень, що в деяких випадках м’язові симптоми, які спостерігали в хворих, виявилися ефектом ноцебо, і багато хто згодом відновив приймання статинів (Wood et al., 2020; Kristiansen et al., 2021).
У клінічній практиці для забезпечення ефективного зниження рівня ліпідів у критичній фазі доцільно розпочати лікування інгібітором PCSK9 у комбінації з езетимібом і паралельним повторним застосуванням статину.
Слід зауважити, що попередня комбінована терапія езетимібом і бемпедоєвою кислотою, призначення статинів і повторне оцінювання через 4‑6 тиж. можуть бути доцільним лікувальним підходом за особливого клінічного сценарію. Зокрема, у дослідженні CLEAR OUTCOMES, що наразі триває, за участю 14 тис. пацієнтів із ССЗ або високим ризиком їх розвитку, які не переносять статини, вивчають вплив бемпедоєвої кислоти на серйозні СС-події. Тож для такої категорії хворих оптимальним варіантом може бути комбінована терапія (езетимібом, бемпедоєвою кислотою та інгібітором PCSK9). У пацієнтів, які не досягають цільових показників ХС ЛПНЩ на тлі подвійної ГЛТ статином високої інтенсивності та езетимібом, раціональним є додавання бемпедоєвої кислоти, якщо інгібітори PCSK9 недоступні (Rubino et al., 2021).
Висновки
Пацієнти з ГКС мають підвищений ризик рецидивів, особливо на дуже ранній стадії. Упродовж останніх десятиліть описано чіткий зв’язок досягнутих рівнів ХС ЛПНЩ і СС-наслідків у ранній фазі після ГКС. Навіть якщо оцінювання рівня ХС ЛПНЩ та ескалацію терапії виконувати що 4‑6 тиж., пацієнтові може знадобитися до трьох місяців для досягнення цільових показників, що збігається з періодом найвищого ризику повторних СС-подій.
Отже, в усіх пацієнтів із ГКС доцільно розглянути стратегію раннього та інтенсивного зниження рівня ХС ЛПНЩ на тлі лікування статинами і подвійну терапію статином і езетимібом за замовчуванням. Використання інгібіторів PCSK‑9 є новим дієвим підходом, особливо у хворих з ознаками високого ризику. У фокусі уваги систем охорони здоров’я мають бути виявлені перешкоди у щоденній клінічній практиці при веденні осіб із ГКС і лікувальних стратегій для забезпечення якісного подальшого догляду пацієнтів групи високого ризику.
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті
www.escardio.org