26 червня, 2023
П’ятнадцятирічні результати активного спостереження, хірургічного лікування або променевої терапії раку передміхурової залози
Резюме дослідження та коментар фахівця
Попри нещодавні досягнення у ранньому виявленні та лікуванні локалізованого раку передміхурової залози, тактика ведення таких хворих залишається суперечливою. Хоча мультипараметрична магнітно-резонансна томографія та прицільна біопсія оптимізують діагностику повільно прогресуючих пухлин, складні аспекти стратифікації ризику все одно призводять як до надмірного, так і до недостатнього лікування. До вашої уваги коротке резюме результатів 15‑річного дослідження англійських науковців Ф. С. Хамді та співавт. (2023) Prostate Testing for Cancer and Treatment (ProtecT) та коментар фахівця Медичної школи Тулейна, Новий Орлеан (США) О. Сартора.
Ключові слова: простат-специфічний антиген, локалізований рак передміхурової залози, активне спостереження, простатектомія, променева терапія.
Клінічна проблема
Відносна ефективність стратегій лікування локалізованого раку передміхурової залози (РПЗ) залишається невизначеною, навіть при ранньому виявленні захворювання за допомогою тестування на рівень простат-специфічного антигена (ПСА).
Клінічне дослідження
Дизайн: рандомізоване дослідження Prostate Testing for Cancer and Treatment (ProtecT) проведене у Великобританії, у якому порівнювали результати трьох стратегій лікування локалізованого РПЗ, виявленого за результатами тестування на рівень ПСА:
- активне спостереження;
- простатектомія;
- променева терапія.
Втручання: 1643 чоловіки віком від 50 до 69 років були розподілені в одну із трьох груп упродовж 1999-2009 років. Медіана спостереження становила 15 років. Первинним результатом була смерть від РПЗ.
Результати
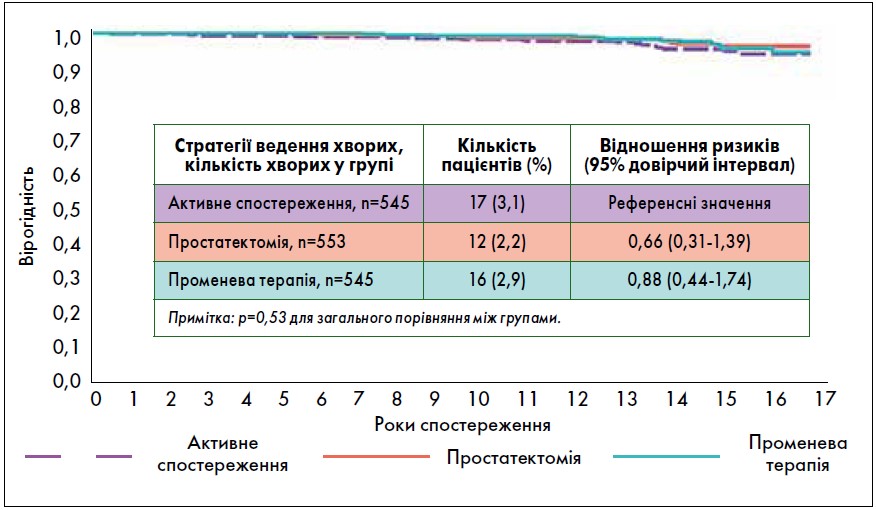
Ефективність: рівень смертності від РПЗ був низьким і подібним у всіх трьох групах (рис. 1).
Рис. 1. Смертність від РПЗ
Вторинні результати: у групі активного спостереження було діагностовано більше випадків метастазування РПЗ порівняно із двома іншими групами (рис. 2). Крім того, більшість пацієнтів у групі активного спостереження отримували довготривалу андроген-деприваційну терапію або в них діагностували місцеве прогресування захворювання. Однак у цілому виживаність не зазнала негативного впливу через відтермінування специфічного лікування, і майже чверті чоловіків, які перебували під активним спостереженням, не знадобилося лікування від РПЗ.
Рис. 2. Вторинні результати
Обмеження та питання, що залишаються
- Гістологічний аналіз показав, що більша кількість пацієнтів мали проміжну стадію раку, ніж вважалося на той момент, коли вони були включені у дослідження.
- Діагностичні методи візуалізації та підходи активного спостереження зазнали змін від початку дослідження у 1999 році.
- Нові системні методи лікування прогресуючого захворювання стають все доступнішими, і саме це, ймовірно, сприяло подовженню виживаності у чоловіків із метастазами в даному дослідженні.
Висновки
Чоловіки з локалізованим РПЗ, виявленим за результатами ПСА, які були рандомізовані для активного спостереження, простатектомії або променевої терапії, мали однаково низький рівень смертності від цього захворювання протягом 15 років спостереження.
Коментар фахівця: локалізований рак передміхурової залози – тоді і зараз
О. Сартор, кафедра медицини та урології, відділення гематології та медичної онкології, Медична школа при Університеті Тулейн, Новий Орлеан (США)
Із 1999 по 2009 рік у Великобританії в рамках дослідження Prostate Testing for Cancer and Treatment (ProtecT) 82 429 чоловікам віком від 50 до 69 років було проведено тестування на рівень ПСА. Після 15 років, упродовж яких тривало дослідження, можна підбити підсумки цієї грандіозної роботи. З усіх чоловіків, які вперше взяли участь у дослідженні, 2664 (3,2%) особам було встановлено діагноз локалізованого РПЗ. Загалом, 1643 (61,7%) пацієнти були рандомізовані у групи активного спостереження, проведення простатектомії або променевого лікування, а також короткого курсу (від 3 до 6 міс) андроген-деприваційної терапії. Початково лікування було стратифіковано відповідно до віку, суми балів за шкалою Глісона (<7, 7 або від 8 до 10) та рівня ПСА.
Через 15 років були доступні дані спостереження щодо 98% учасників дослідження. Частота смерті була низькою і зіставною у трьох групах. Загалом, 21,7% чоловіків померли з причини, не пов’язаної із РПЗ, а 2,7% – від РПЗ. Частота метастазування становила 9,4% у групі активного спостереження і приблизно вдвічі менше – у групах простатектомії та променевої терапії. Частота клінічного прогресування також була вищою у групі активного спостереження, ніж в інших двох групах, але ця кінцева точка була досить гетерогенною і представляла собою дещо розмитий показник результату.
Автори дійшли висновку, що вибір методу ведення пацієнтів із локалізованим РПЗ передбачає певний компроміс між користю та шкодою лікування – можливо, не той висновок, на який сподівалися прихильники лікування, враховуючи тривалість і масштаб дослідження. Побічні ефекти радикальної простатектомії та променевої терапії добре описані, і відомо, що багато чоловіків мають значні сексуальні розлади або проблеми з боку сечової системи після проведеного місцевого лікування. Сьогодні як ніколи очевидно, що потрібні менш інтенсивні підходи до лікування РПЗ.
На момент початку дослідження ProtecT загальноприйнятим методом обстеження чоловіків на РПЗ було визначення рівня ПСА з наступним проведенням біопсії у разі його підвищення, а потім – лікування раку. Цей спрощений підхід кардинально змінився по мірі того, як з’являлися нові докази. Тестування на ПСА більше не є нормою. У багатьох клініках визначення рівня ПСА взагалі не проводять, а настанови тепер передбачають прийняття інформованого рішення, орієнтованого на пацієнта. На жаль, такий підхід не є ідеальним, враховуючи, що лікарі первинної ланки в силу великої завантаженості мають обмежений час для детального обговорення та пояснення можливих наслідків прийнятого рішення.
На сьогодні при виявленні у пацієнта підвищеного рівня ПСА лікар може призначити мультипараметричну магнітно-резонансну томографію (МРТ) для вибіркової біопсії лише у чоловіків з оцінкою від 3 до 5 балів за шкалою Prostate Imaging Reporting and Data System (PI-RADS), де вищі бали вказують на вищу підозру на рак. Прицільна біопсія виявляється достатньою для діагностики пухлин у пацієнтів з оцінкою від 3 до 5 балів за системою PI-RADS.
Також доступні додаткові методи стратифікації ризику, які не обмежуються клінічною стадією, рівнем ПСА та сумою балів за шкалою Глісона. Транскриптомні аналізи (також відомі як геномні класифікатори) можуть надати важливу прогностичну інформацію та сприяти у прийнятті рішення щодо лікування. Геномні оцінки зародкової лінії також схвалені експертами у пацієнтів із пухлинами більш високих ступенів злоякісності або в окремих випадках спадкового РПЗ. Натепер схвалено проведення позитронно-емісійної томографії (ПЕТ) простат-специфічного мембранного антигена (ПСМА) для кращого стадіювання РПЗ у пацієнтів із несприятливим проміжним або локалізованим раком високого ризику. За певних обставин ПЕТ-сканування ПСМА також може бути корисним для визначення доцільності проведення біопсії. Після завершення стратифікації ризику РПЗ лікар може вжити відповідні заходи, враховуючи додаткові фактори, такі як вік, сімейний анамнез, супутні захворювання і (можливо, найважливіше) побажання пацієнта.
Незважаючи на масштабний характер дослідження ProtecT і довготривале спостереження, певні питання потребують подальшого вивчення. Середній рівень ПСА серед рандомізованих пацієнтів був досить низьким – 4,6 нг/мл. Серед 1643 пацієнтів 1268 (77,2%) осіб склали групу І ступеня (6 балів за шкалою Глісона), і лише у 169 (10,3%) чоловіків рівень ПСА був ≥10 нг/мл. Хоча підкласифікація пацієнтів проміжного ризику не проводилася, лише 99 (6,0%) осіб мали захворювання ІІІ ступеня (7 балів за шкалою Глісона [4+3]) або вище. Переважна більшість досліджуваних мали низький ризик або сприятливий проміжний ризик і сьогодні вважалися б прийнятними кандидатами для активного спостереження. Кількість пацієнтів, віднесених до групи з несприятливим проміжним або високим ризиком, є недостатньою для формулювання певних висновків за результатами дослідження ProtecT.
Активний моніторинг таким чином, як він проводився в дослідженні ProtecT, не повинен використовуватися сьогодні. Можна значно покращити тактику ведення пацієнтів, призначивши мультипараметричну МРТ. Підвищена частота метастазування, яка була відзначена у групі активного спостереження в дослідженні ProtecT, ймовірно, буде зменшена при дотриманні протоколів активного спостереження, які використовуються сьогодні. Тактика активного спостереження у пацієнтів із РПЗ низького ризику сьогодні є більш прийнятною, ніж у 1999 році, хоча іноді пацієнти занепокоєні тим, що захворювання залишається нелікованим. Однак терапія тривожності шляхом видалення передміхурової залози часто створює ще більші проблеми. Дедалі частіше застосовуються різні форми фокальної терапії, особливо тепер, коли сучасні технологічні досягнення дозволяють краще візуалізувати і навіть таргетувати пухлину. Загалом, лікування локалізованого РПЗ зазнало значних змін із 1999 року, коли було розпочато дослідження ProtecT. Незважаючи на це його результати надали цінні дані для прийняття рішень щодо великої когорти пацієнтів із РПЗ низького або проміжного ризику.
Реферативний огляд підготувала Марія Ареф’єва
За матеріалами: Hamdy F. C. et al., ProtecT Study Group. Fifteen-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Prostate Cancer. N Engl J Med. 2023 Apr 27;388(17):1547–1558. https://www.nejm.org/doi/full/10.1056/NEJMoa2214122; https://www.nejm.org/doi/full/10.1056/NEJMe2300807?query=TOC&cid=NEJM%20eToc,%20March%2016,%202023%20DM2140114_NEJM_Non_Subscriber&bid=1465833406
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1-2 (28-29), 2023 р.