30 червня, 2023
Невидимий літній ворог: ефективний спосіб подолання грибкових інфекцій шкіри
Здавна помічено, що інфекційна захворюваність має сезонний характер. Такі сезонні коливання визначав ще Гіппократ, який у книзі «Афоризми» писав, що «кожна хвороба виникає у будь-яку пору року, але деякі з них частіше розвиваються та мають більшу тяжкість у певний сезон». Гіппократ пояснював такий факт впливом факторів навколишнього середовища, в т. ч. сезонними змінами пори року. Думку засновника європейської медицини підтверджено сучасними епідеміологічними даними, які демонструють зростання захворюваності на грибкові інфекції шкіри (ГІШ) влітку (Sharma B. et al., 2021).
Літо та ГІШ
Ріст ГІШ улітку пояснюють високою вологістю та оптимальною температурою, які створюють умови для кращого виживання грибів та їхніх спор (Shenoy M. et al., 2022). Деякі автори, підкреслюючи надзвичайну поширеність грибкових інфекцій у спекотні місяці, називають їх «літо-асоційованим дерматитом» (Rajesh G. et al., 2019). Доведено, що навіть підвищення рівня ультрафіолетового випромінювання влітку не чинить шкідливого впливу на гриби через наявність у них меланіну, який захищає гриби та дозволяє їм існувати в умовах підвищеної електромагнітної радіації (Campana R. et al., 2022). Серед інших факторів, що можуть сприяти розповсюдженню ГІШ і проростанню грибкових спор улітку, виокремлюють дисфункцію епідермального бар’єра, збільшення контактного шляху передачі збудників унаслідок зростання частоти прямих фізичних контактів, потіння, нехтування належною особистою гігієною, носіння мокрого чи вологого одягу (Shenoy M. et al., 2022). Додатковими факторами ризику ГІШ є часте та неналежне використання місцевих стероїдів (Das A. et al., 2022), неконтрольоване застосування антибіотиків, наявність супутнього цукрового діабету (Aragón-Sánchez J. et al., 2023).
Сучасні статистичні дані
ГІШ – надзвичайно поширена дерматологічна патологія: у 2017 р. у 195 країнах світу від ГІШ, волосся та нігтів страждали майже 1 млрд осіб; рівень глобальної поширеності склав 10,09% і вже тоді внесок дерматомікозів (0,17%) у загальну кількість DALY (роки життя, скориговані на непрацездатність), спричинених захворюваннями шкіри (1,76%), визнано статистично достовірним (Bongomin F. et al., 2017). Під час проведення цієї багатомасштабної роботи підтверджено зростання поширеності та захворюваності на дерматомікози в теплому, вологому кліматі та в регіонах із низьким рівнем соціально-економічного розвитку через скупченість населення, близьке сусідство із тваринами, погану особисту гігієну (Bongomin F. et al., 2017). ГІШ асоційовані зі значним фінансовим тягарем: у 2017 р. у США на частку дерматофітних інфекцій припала майже половина всіх амбулаторних візитів до лікаря, які супроводжувалися загальними витратами в розмірі 802 млн дол. США (Benedict K. et al., 2019).
Сучасні епідеміологічні дослідження, проведені в 27 країнах Європи (n=44 689), свідчать, що майже 94 млн європейців скаржаться на свербіж / печіння / сухість шкіри, найрозповсюдженішою причиною яких є ГІШ (8,9%), тоді як поширеність акне, атопічного дерматиту чи екземи складає лише 5,4 та 5,5% відповідно (Richard M. et al., 2022). Згідно з даними іншого багатомасштабного епідеміологічного випробування, в 17 країнах Європи фіксують зростання клінічної та/або мікологічно підтвердженої толерантності до антифунгальних засобів (Saunte D. et al., 2021); автори дослідження висловили обґрунтовані побоювання щодо ймовірного розвитку епідемії грибкових захворювань в Європі. Цей прогноз може здійснитися: вже зараз у Швеції поширеність поверхневих ГІШ складає 14,3% (Özenci V. et al., 2019).
Патофізіологічні особливості ГІШ
Розрізняють 2 основні типи ГІШ: поверхневі (за яких патологічний процес локалізується в епідермісі) та глибокі (дерма, гіподерма) мікози. Більшість грибів, що локалізуються на шкірі, волоссі, нігтях, руйнують кератин (поверхневий структурний білок, який відповідає за підтримання структурної стабільності, цілісності шкіри) та використовують його як джерело необхідних поживних речовин (Mijaljica D. et al., 2022). Під час потрапляння на поверхню шкіри, зокрема на верхній ороговілий шар епідермісу, грибкова клітина продукує фермент кератиназу (рис. 1), що руйнує навколишні тканини та спричиняє запалення шкіри, що часто супроводжується свербінням (Mijaljica D. et al., 2022). Поверхневі ураження шкіри називають кератинофільними дерматофітами; їх переважно зумовлюють представники родів Epidermophyton, Microsporum і Trichophyton. Ці збудники здатні спровокувати такі поширені влітку ГІШ, як дерматофітія тулуба (локалізований або поодинокий кільцеподібний висип на тілі), епідермофітія стоп (грибкова інфекція між пальцями ніг), дерматофітний оніхомікоз (ураження нігтів на пальцях рук і ніг), дерматомікоз у пахвовій ділянці, мікоз шкіри чи волосистої частини голови (Mijaljica D. et al., 2022).
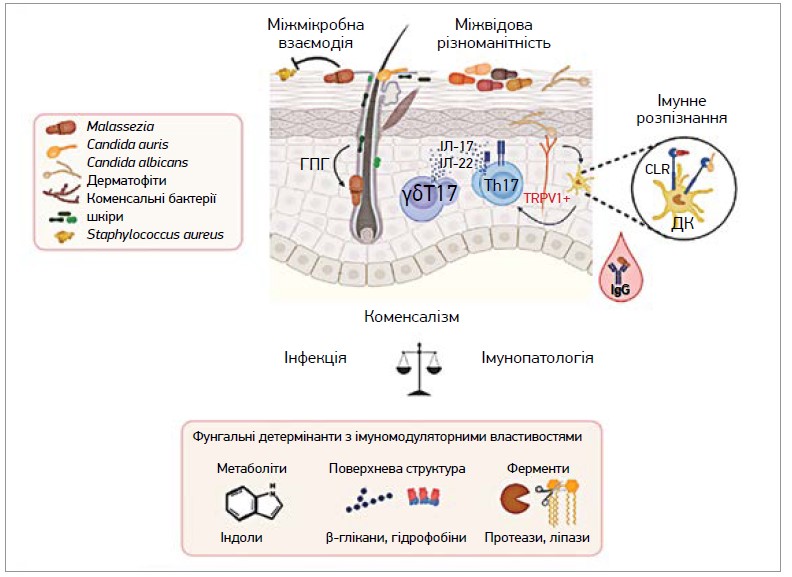
Рис. 1. Грибки шкірні в нормі та за патології (Ruchti F. et al., 2023)
Примітки: ГПГ – горизонтальне перенесення генів; ДК – дендритна клітина;
ІЛ – інтерлейкін; CLR – лектинові рецептори С-типу; TRPV1+ – підвид нейронів;
Th – Т-хелпери; γδT17 – ІЛ-17A-продукувальні γδ-лімфоцити.
Грибки шкіри співіснують з організмом людини як коменсали чи патогени. Гриби-коменсали розпізнаються дендритними клітинами переважно за допомогою лектинових рецепторів С-типу або TRPV1+-нейронів, які сприяють рекрутингу інтерлейкін (ІЛ)-17A-продукувальних γδ-лімфоцитів (γδT17) й активують грибок-специфічний адаптивний імунітет, включаючи синтез IgG, активацію локальних та системних Т-хелперів 17 (Th17). γδT17 і Th17 забезпечують контроль популяції грибів-коменсалів шляхом секреції IЛ-17A, IЛ-22. Мікробіота шкіри взаємодіє із грибами завдяки декільком механізмам, включаючи горизонтальне перенесення генів або Malassezia-асоційоване інгібування утворення біоплівки Staphylococcus aureus. Порушення епітеліального бар’єра чи утворення ранового каналу сприяє проникненню грибів до глибоких шарів дерми, обумовлюючи активацію ІЛ-17-опосередкованого запалення та посилення подальшого ушкодження дерми. Зміна активності імунної системи, особливо тих ланок, що беруть участь в індукції IЛ-17, зумовлює втрату контролю над популяцією грибів. Наслідками цього є надмірний ріст грибків і виникнення хронічного запального процесу в дермі. Метаболіти та ферменти грибів також погіршують стан шкіри, порушуючи бар’єрну функцію або діючи як додаткові подразнювальні агенти.
Діагностика та принципи лікування
Здебільшого діагностика ГІШ ґрунтується на аналізі анамнезу та досить типовій клінічній картині, але будь-які сумніви щодо етіології ураження дозволяють вирішити такі лабораторно-інструментальні методи, як дерматоскопія, культуральне дослідження, полімеразна ланцюгова реакція, генетичний аналіз (Moskaluk A. et al., 2022). Рання діагностика ГІШ із подальшим своєчасним призначенням терапії здатна запобігти виникненню тяжкого ураження шкіри та швидкому поширенню захворювання в контактних осіб, особливо в літній період.
Згідно з американськими (2014), британськими (2014), німецькими (2020) рекомендаціями, лікування поверхневої ГІШ передбачає застосування топічних та пероральних антифунгальних препаратів, стероїдів, комбінацій фунгальних і стероїдних засобів; в актуальніших настановах цей перелік доповнено топічними інгібіторами кальциневрину (Georgescu S. et al., 2022). Як лікарські засоби вибору пропонується призначати топічний антифунгальний препарат, похідний імідазолу (Woo T. et al., 2019). Протягом тривалого часу із цією метою використовували тербінафін, але згодом було накопичено широку доказову базу, яка доводить переваги застосування сертаконазолу 2% крему (Залаїн, Egis) у лікуванні ГІШ.
Сертаконазол: від особливостей хімічної будови до клінічних переваг
Як і всі імідазоли, сертаконазол має азолове кільце, але на відміну від традиційних представників імідазолів містить додаткову сполуку – бензотіофен. Введення до хімічної структури нового компонента бензотіофену мало на меті подолати стійкість патогенних грибів до азольних сполук. Бензотіофен – високоліпофільна сполука, що легко вбудовується в клітинну мембрану грибів, порушує її проникність, провокуючи розрив плазматичної мембрани грибкової клітини та подальшу її загибель. Завдяки таким властивостям бензотіофен чинить фунгіцидну дію та полегшує реалізацію фунгістатичного впливу азолового кільця на компоненти мембрани грибкової клітини. Комбінована хімічна структура сертаконазолу забезпечує подвійну фунгіцидну та фунгістатичну активність, інгібує трансформацію грибів із нешкідливої сапрофітної форми в потенційно патогенну, інвазійну. Зазначені особливості забезпечують потужний протигрибковий ефект сертаконазолу, а також мінімізують ризик виникнення рецидивів на тлі його застосування.
Спектр протимікробної дії сертаконазолу є надзвичайно широким: він перекриває активність значної кількості дерматофітів (Trichophyton, Microsporum, Epidermophiton), патогенних дріжджових грибів (Candida, Torulopsis, Trichosporon, Malassezia), грибів-опортуністів (Scopulariopsis, Altermania, Acremonium, Aspergillus, Fusarium), а також ефективно пригнічує ріст окремих грамнегативних і грампозитивних бактерій.
Сертаконазол: доказова база
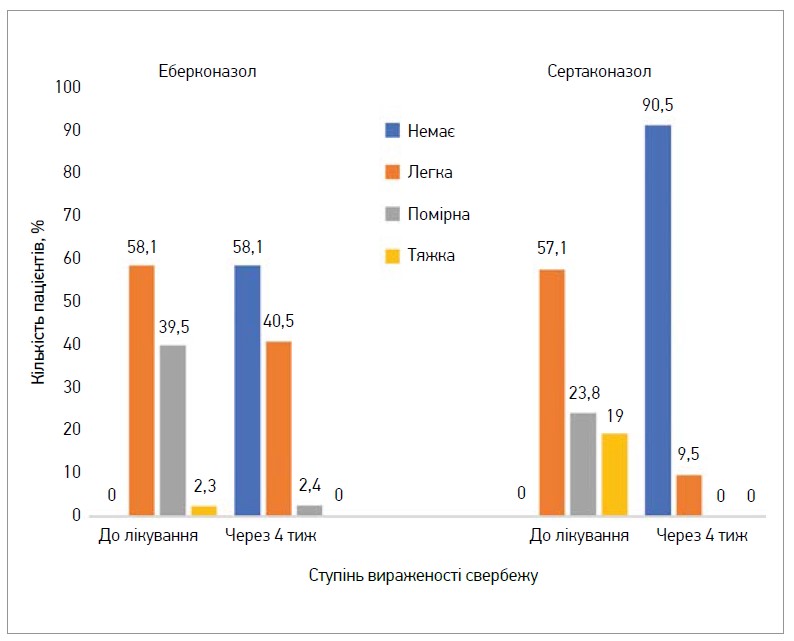
Доведено, що використання сертаконазолу асоційовано зі швидким настанням клініко-мікологічного одужання та хорошою переносимістю (Gupta A. et al., 2017). Згідно з даними рандомізованого контрольованого дослідження (РКД), у якому взяли участь хворі на дерматофітію тулуба та трихофітію промежини (n=85), ефективність 4-тижневої терапії сертаконазолом перевершує таку еберконазолу (рис. 2). Обидва препарати однаково зменшують свербіж, еритему, почервоніння, лущення та сприяють мікологічному одужанню порівняно з початковими даними (р<0,001), але сертаконазол краще нівелює клінічні прояви захворювання, особливо свербіж і лущення (р<0,001) (Ravichandran M. et al., 2021).
Рис. 2. Порівняння протисвербіжної активності еберконазолу та сертаконазолу
Сертаконазол перевершує клотримазол у лікуванні дерматофітії тулуба: 3-тижнева терапія сертаконазолом асоціюється зі швидким зменшенням еритеми (p<0,02), свербежу, лущення, розміру, країв ушкоджень (в усіх випадках p<0001), поліпшенням результатів КОН-тесту порівняно із клотримазолом (Shivamurthy R. et al., 2014). Порівняння ефективності та переносимості сертаконазолу з тербінафіном у терапії локальної дерматофітії дозволило авторам РКД підтвердити зіставність зазначених антимікотиків (Chatterjee D. et al., 2016).
В іншому РКД, де оцінювали результативність 2% крему сертаконазолу й аморолфіну в лікуванні дерматофітії, доведено кращу мікологічну ефективність (р=0,01) сертаконазолу, а також швидше зменшення інтенсивності симптомів, кількості уражень шкіри (р=0,002 через 12 тиж), покращення якості життя (р<0,001) у групі сертаконазолу (Das A. et al., 2019). Застосування сертаконазолу дозволяє інгібувати ріст різноманітних видів грибів та їхніх спор, здатних персистувати в тканинах і протистояти дії інших антимікотиків (Fink S. et al., 2022).
Метааналіз 8 контрольованих клінічних досліджень довів ефективність 2% крему сертаконазолу в лікуванні Malassezia-асоційованого дерматиту порівняно з кетоконазолом, клотримазолом, метронідазолом, пімекролімусом, такролімусом (відношення шансів складало 1,95) (Georgescu S. et al., 2022). На відміну від тербінафіну, здатного пригнічувати ріст дерматофітів, але який не може вплинути на T. indotineae, сертаконазол інгібує активність дерматофітів, дріжджових грибів і плісняви. Крім того, сертаконазол має високу спороцидну активність щодо спор грибів і дріжджів на відміну від тербінафіну (Georgescu S. et al., 2022).
Висновки
Літний період супроводжується підвищенням показників захворюваності на ГІШ, що потребує особливої пильності до стану шкіри. Рання діагностика та застосування оптимальних антимікотиків є запорукою ефективного лікування ГІШ. Особливості механізму дії сертаконазолу, притаманний йому широкий спектр мікробіологічної активності, висока клінічна ефективність, мінімальна ймовірність виникнення рецидивів і розвитку резистентних мікроорганізмів, хороша переносимість, профіль безпеки та зручність застосування дозволяють розглядати сертаконазол 2% крем (Залаїн) як засіб першої лінії емпіричної терапії різноманітних ГІШ, зумовлених дерматофітами, дріжджоподібними, пліснявими грибами.
Медична газета «Здоров’я України 21 сторіччя» № 10 (546), 2023 р.