12 вересня, 2023
Ведення пацієнтів із цукровим діабетом і серцевою недостатністю: консенсусна заява Корейської діабетичної асоціації і Корейського товариства серцевої недостатності
Цукровий діабет (ЦД) є основним чинником ризику розвитку серцевої недостатності (СН). Прогноз у разі СН у пацієнтів із ЦД гірший, ніж без захворювання ендокринної системи. Раннє діагностування та лікування СН в осіб із ЦД є важливими. Пропонуємо до вашої уваги огляд статті Kyu-Sun Lee et al. «Evaluation and Management of Patients with Diabetes and Heart Failure: A Korean Diabetes Association and Korean Society of Heart Failure Consensus Statement» видання Diabetes Metab J (2023; 47:10‑26), присвяченої сучасним критеріям діагностики та скринінгу СН, фармакологічним методам лікування пацієнтів із СН, а також впливу антидіабетичних препаратів на СН.
Серцева недостатність (СН) – це складний клінічний синдром з основними симптомами (задишка, набряк гомілковостопних суглобів і втома) та/або ознаками (підвищений яремний венозний тиск, застійні явища в легенях, легеневі хрипи та периферичні набряки), спричиненими структурними або функціональними порушеннями серця, які призводять до зниження серцевого викиду та/або підвищення внутрішньосерцевого тиску. У світі поширеність СН та ЦД зростає зі старінням населення (McDonagh et al., 2021; Heidenreich et al., 2022; Bozkurt et al., 2021; Park et al., 2020). За даними Інформаційного бюлетеня про діабет, опублікованого Корейською діабетичною асоціацією 2020 р., серед дорослих корейців віком ≥30 років 16,7% (19,2% у чоловіків і 14,3% у жінок) мали ЦД (Bae et al., 2022).
Відомо, що поширеність СН серед дорослого населення промислово розвинених країн коливається від 1до 3% (Savarese et al., 2022). Наприклад, у Кореї поширеність СН постійно зростає: 0,77% – 2002-го до 2,24% – 2018-го (Park et al., 2021). Така тенденція упродовж 2002‑2018 рр. зберігається також за віком та статтю.
Ожиріння та ЦД були визначені як важливі чинники ризику розвитку та несприятливого прогнозу СН (Jung et al., 2022).
В огляді представлено сучасні критерії діагностики та скринінгу СН, а також рекомендовані на сьогодні фармакологічні втручання у пацієнтів із СН. Крім того, проаналізовано вплив антидіабетичних препаратів на СН та лікування ЦД 2-го типу в пацієнтів із СН.
Епідеміологія і прогноз
Поширеність СН у пацієнтів із ЦД
СН є поширеним супутнім захворюванням і фатальним ускладненням ЦД. Власне, поширеність СН коливається від 19 до 26% серед пацієнтів із ЦД (Ryden et al., 2000; Shindler et al., Kostis et al., 1996; Thrainsdottir et al., 2005).
За даними Корейської національної служби медичного страхування – Національної вибіркової когорти за 2006‑2015 рр., частота госпіталізації з приводу СН у корейській популяції із ЦД зросла із 72 до 146 і зі 124 до 161 на 10 тис. чоловіків і жінок відповідно (Park et al., 2021).
Результати Фремінгемського дослідження серця продемонстрували підвищений ризик розвитку СН у пацієнтів із ЦД, удвічі вищу частоту СН у чоловіків і вп’ятеро вищу – у жінок із ЦД, ніж у відповідної за віком групи без діабету (Kannel et al., 1979).
У спостережних дослідженнях збільшення рівня глікованого гемоглобіну (HbA1c) на 1% у хворих на ЦД 1-го типу пов’язане зі збільшенням ризику розвитку СН на 30%, а у хворих на ЦД 2-го типу – на 8%, незалежно від інших чинників ризику, як-от ожиріння, куріння, артеріальна гіпертензія (АГ), дисліпідемія та ішемічна хвороба серця (ІХС) (Lind et al., 2011; Stratton et al, 2000). Ці результати свідчать, що хронічна гіперглікемія є одним з основних чинників, що погіршує перебіг СН у пацієнтів із ЦД як 1-го, так і 2-го типу.
Поширеність ЦД у пацієнтів із СН
Хоча через різні досліджувані популяції та різні джерела даних між епідеміологічними дослідженнями, присвяченими СН, нє неоднорідність, поширеність ЦД серед пацієнтів із СН у Кореї становила від 20 до 36% (Park et al., 2020).
Поширеність коморбідного ЦД у пацієнтів із СН в Кореї протягом 2002‑2018 рр. постійно зростала (Park et al., 2021).
За даними досліджень у західних країнах та реєстрів, пов’язаних із СН, поширеність ЦД коливається від 25 до 45% (Yusuf et al., 1991; Zannad et al., 2011; McMurray et al., 2014; McMurray et al., 2019; Adams et al., 2005; Nieminen et al., 2006; Greenberg et al., 2007; MacDonald et al., 2008.
Діабетична кардіоміопатія
S. Rubler et al. (1972) припустили наявність у хворих на ЦД унікального типу кардіоміопатії, так званої діабетичної кардіоміопатії. Такі пацієнти мали застійну СН без ІХС, АГ, клапанних вад серця або алкоголізму. Цю концепцію було підтверджено в межах Фремінгемського дослідження серця, у якому зазначено, що за наявності ЦД СН виявляють частіше у 5 разів в жінок і в 2,4 раза – у чоловіків, незалежно від інших чинників ризику, як-от вік, ІХС та АГ(Rubler et al., 1972).
Багато епідеміологічних досліджень також підтвердили значно більшу поширеність шлуночкової дисфункції у пацієнтів із ЦД, незалежно від впливу відповідних змінних. За даними цих досліджень, Фонд Американського коледжу кардіології (ACC) та Європейське товариство кардіологів (ESC) описали діабетичну кардіоміопатію як клінічний стан серцевої дисфункції без атеросклеротичного ураження коронарних судин та АГ у пацієнтів із ЦД (Thrainsdottir et al., 2005; Kannel et al., 1979; Rubler et al., 1972; Yancy et al., 2013; Ryden et al., 2013).
Патофізіологія діабетичної кардіоміопатії є складна і не зовсім зрозумілою. Для пояснення розвитку діабетичної кардіоміопатії було запропоновано кілька механізмів:
- Зміни мітохондріального окиснення жирних кислот.
- Порушення мітохондріальної обробки Са2+.
- Серцева інсулінорезистентність, яка спричиняє порушення сигналізації субстрату інсулінового рецептора, фосфатидилінозитол‑3-кінази (PI3K) / протеїнкінази B (Akt) та наступних шляхів.
- Активація ренін-ангіотензин-альдостеронової системи (РААС).
- Кардіальна автономна нейропатія.
- Мікросудинна дисфункція.
- Запальні шляхи, що призводять до фіброзу, жорсткості та гіпертрофії міокарда (Murtaza et al., 2019; Lee et al., 2021).
Клінічні ознаки діабетичної кардіоміопатії прогресують від безсимптомної діастолічної дисфункції до систолічної дисфункції та симптоматичної СН. Для впливу на патофізіологію діабетичної кардіоміопатії розробляють багато нових потенційних методів лікування, зокрема застосування антиоксидантів, коензиму Q10, гамма-інгібіторів PI3K, терапію на основі міРНК та лікування стовбуровими клітинами (Kenny et al., 2019).
Прогноз щодо ЦД у пацієнтів із СН
Порівняно з особами без діабету пацієнти із СН і ЦД мають гірші клінічні результати (смертність, госпіталізація та якість життя) (Dunlay et al., 2019; Fujita et al., 2012; Yap et al., 2019).
Часто ЦД у пацієнтів із СН асоціюється з більшим у 1,6‑2 рази відносним ризиком серцево-судинної (СС) смерті або госпіталізації з приводу СН, порівняно з тими, хто не має діабету, незалежно від фракції викиду лівого шлуночка (ФВЛШ) (Kristensen et al., 2017; MacDonald et al., 2008).
Оцінювання і діагностування серцевої недостатності
Скринінг і діагностика СН
У пацієнтів із ЦД часто СН виявляється першою серцево-судинною подією (Birkeland et al., 2020). Тому важливо оцінювати СН у симптоматичних пацієнтів із ЦД. Найпоширенішими типовими симптомами є задишка з ортопное, втома та набряки ніг або кісточок.
Для оцінювання СН у симптоматичних пацієнтів із ЦД необхідний детальний аналіз даних анамнезу та фізикального обстеження. Однак симптоми та ознаки не є достатньо точними для встановлення діагнозу СН (Oudejans et al., 2011; Kelder et al., 2011).
Крім симптомів і клінічних ознак, важливим етапом діагностування СН є виконання електрокардіограми (ЕКГ) у 12 відведеннях, рентгенографії органів грудної клітки та початкових лабораторних тестів. ЕКГ надає важливу інформацію щодо аритмії, серцевого ритму, морфології та тривалості комплексу QRS та ішемічних ознак, як-от підйом або зниження сегмента ST.
Завдяки рентгенографії органів грудної клітки отримують інформацію про кардіомегалію, застій у легенях та інші легеневі захворювання, які можуть спричинити утруднене дихання.
Первинні лабораторні тести передбачають загальний аналіз крові (ЗАК), сечі, визначення вмісту в крові електролітів, креатиніну, глюкози, ліпідного профілю натще, функції печінки, профілю заліза та функції щитоподібної залози. До цих лабораторних тестів слід додати визначення тропоніну-І, оскільки воно є корисним для виявлення гострого коронарного синдрому.
Визначення рівнів натрійуретичних пептидів (NP); натріуретичного пептиду типу В (BNP) або N-термінального натрійуретичного пептиду типу проВ (NT-proBNP) рекомендовано як початковий діагностичний тест у пацієнтів із симптомами, що вказують на СН, якщо такі доступні.
Підвищення концентрації NP у плазмі (хронічна СН: BNP≥35 пг/мл або NT-proBNP ≥125 пг/мл; гостра СН: BNP≥100 пг/мл, NT-proBNP ≥300 пг/мл) підтверджує діагноз СН. Трансторакальну ехокардіографію (ТТЕхоКГ) рекомендовано як початковий діагностичний тест для оцінювання структури та функції серця після збору повного анамнезу хвороби, фізикального обстеження та лабораторних тестів, зокрема визначення рівнів NP. Вимірювання ФВЛШ є фундаментальним кроком у класифікації СН та виборі фармакологічної та апаратної терапії на підставі доказів (табл. 1).
|
Таблиця 1. Класифікація СН |
|||
|
Діагностичні |
СНЗФВ |
СНПЗФВ |
СННФВ |
|
1 |
Симптоми ± ознакиa |
Симптоми ± ознакиa |
Симптоми ± ознакиa |
|
2 |
ФВЛШ ≤40% |
ФВЛШ |
ФВЛШ ≥50%
|
|
3 |
|
|
Підвищення рівня NP Об’єктивні ознаки структурних та/або функціональних порушень серця, що відповідають наявності діастолічної дисфункції ЛШ/або підвищеному тиску наповнення ЛШ |
|
Примітки: СГЗФВ – серцева недостатність зі зниженою фракцією викиду; СНПЗФВ – серцева недостатність із помірно зниженою фракцією викиду; СННФВ – серцева недостатність із нормальною фракцією викиду. a Ознак СН на ранній стадії може не бути та/або бути неспецифічними (особливо в разі СННФВ) і/або в пацієнтів, які приймали оптимальне медикаментозне лікування, зокрема діуретики. |
|||
Для встановлення діагнозу СН, окрім ФВЛШ, потрібні докази, які можуть свідчити про підвищене наповнення ЛШ (наприклад, визначення гемодинаміки за допомогою інвазивного тесту або дослідження діастолічної функції за допомогою візуалізаційних методів, визначення рівнів NP за допомогою неінвазивного тесту).
СН є імовірнішою у пацієнтів з інфарктом міокарда (ІМ) в анамнезі, АГ, ІХС, фібриляцією передсердь, у разі зловживання алкоголем, наявності хронічних захворювань нирок, проведення кардіотоксичної хіміотерапії, а також у тих, у кого в сімейному анамнезі є випадки кардіоміопатії або раптової смерті (McDonagh et al., 2021).
У таблиці 2 узагальнено початкові діагностичні тести, рекомендовані для обстеження пацієнтів із підозрою на СН.
|
Таблиця 2. Початкові тести для скринінгу та діагностики СН |
|
|
Діагностичне дослідження |
Рекомендації |
|
BNP або NT-proBNP |
Рекомендовано як початковий діагностичний тест у пацієнтів із симптомами та ознаками, що наводять на думку про СН, щоб виключити діагноз СН. Граничне значення: BNP ≥35 (пг/мл) або NT-proBNP ≥125 пг/мла |
|
ЕКГ |
Може виявити такі аномалії, як підйом сегмента ST, депресія ST, фібриляція передсердь, зміни зубця Q, гіпертрофія ЛШ, і розширений комплекс QRS (наприклад, блокада лівої ніжки пучка Гіса), що підвищує ймовірність діагнозу СН |
|
Рентгенографія органів грудної клітки |
Рекомендовано для оцінювання наявності чи відсутності легеневого застою та кардіомегалії у пацієнтів із підозрою на СН |
|
ЕхоКГ |
Визначення ФВЛШ, розмірів камери, товщини стінки, місцевих порушень руху стінки, функції клапанів, функції ПШ,виявлення легеневої гіпертензії та встановлення параметрів діастолічної функції |
|
Стандартні аналізи крові |
ЗАК, сироватковий рівень сечовини, електроліти, креатинін, тести на функцію щитоподібної залози та печінки, рівень глюкози натще, HbA1c, ліпіди та залізо,стани (TSAT і феритин) |
|
Примітки: ПШ – правий шлуночок; ЗАК – загальний аналіз крові; TSAT – насичення трансферину. aГраничні значення можуть мати нижчу специфічність, особливо в літніх пацієнтів або із фібриляцією передсердь (ФП) або хронічною хворобою нирок (ХХН). Як правило, для діагностування СН у цих пацієнтів рекомендовано вищі граничні значення. |
|
Найчастішою причиною і чинником, пов’язаним із розвитком СН у пацієнтів із ЦД, є ІХС (Lee et al., 2022). Крім того, ЦД належить доо чинників ризику розвитку ІХС. Однак хворі на ЦД частіше скаржаться на атиповий біль у грудях або можуть не мати симптомів, навіть за обширної ІХС (так звана «тиха ішемія»).
Тому в пацієнтів із ЦД і типовими, атиповими серцевими симптомами або порушеннями на ЕКГ у стані спокою навіть без симптомів для оцінювання ішемії міокарда слід розглянути доцільність виконання коронарної комп’ютерної томографії-ангіографії або функціональних навантажувальних тестів (ЕКГ із фізичним навантаженням, стрес-ехокардіографії, однофотонної емісійної комп’ютерної томографії (КТ) та позитронно-емісійної томографії). Крім того, інвазивну коронарну ангіографію рекомендовано пацієнтам зі стенокардією або із СН зі зниженою фракцією викиду (СНЗФВ) і з проміжною та високою дотестовою ймовірністю ІХС та наявністю ішемії за результатами неінвазивних стресових тестів (McDonagh et al., 2021; Knuuti et al., 2020; Sharma et al., 2019).
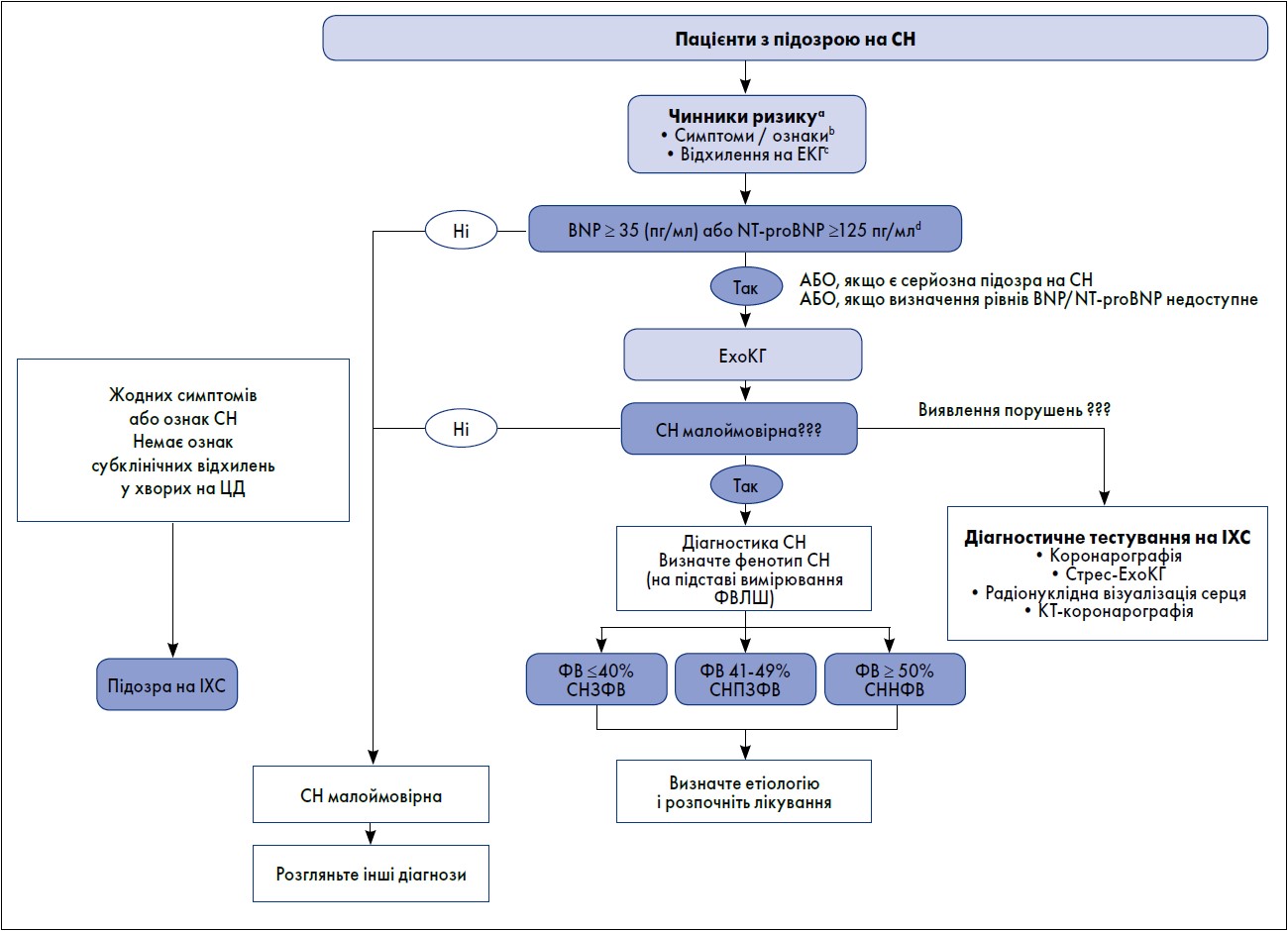
Діагностичний алгоритм для пацієнтів із наявністю симптомів у разі підозри на СН і ЦД наведено на рис. 1 (Korean Society of Heart Failure, 2022).
Рис. 1. Діагностичний алгоритм для пацієнтів із підозрою на хронічну СН
Примітки: aЧинниками ризику СН є ІХС, ЦД, дисліпідемія, АГ, опромінення грудної клітки, кардіотоксичні препарати, інфекції, надмірне споживання алкоголю, ожиріння та куріння;
bТиповими симптомами СН є ортопное, пароксизмальна нічна задишка, знижена толерантність до фізичного навантаження, втома, виснаженість та набряк кісточок; cВідхилення на ЕКГ охоплюють ФП, Q-хвилі, гіпертрофію ЛШ та розширений QRS-комплекс, що збільшує ймовірність діагнозу СН та може також вказувати на необхідну терапію;dЗначення для діагностики гострої СН (BNP ≥100 пг/мл, NT-proBNP ≥300 пг/мл) та значення NT-proBNP для підтвердження діагнозу гострої СН (залежно від віку поріг; >450 пг/мл у віці <55 років, >900 пг/мл у віці від 55 до 75 років і >1,800 пг/мл у віці >75 років).
Адаптовано за Korean Society of Heart Failure, 2022.
Пацієнти із ЦД у групі ризику розвитку СН або пре-СН
Патофізіологічні чинники, пов’язані із ЦД, як-от інсулінорезистентність, оксидативний стрес і запалення, можуть провокувати розвиток структурних захворювань серця та СН через системні міокардіальні та клітинні механізми (Marwick et al., 2018).
Навіть якщо пацієнти із ЦД наразі не мають симптомів, пов’язаних із СН, важливо розпізнати тих осіб із ЦД, у яких імовірний ризик розвитку СН; терапевтичні стратегії профілактики СН у них також є важливими. У клінічних настановах щодо СН виокремлюють групу ризику розвитку СН (стадія А) та пре-СН (стадія В) (Heidenreich et al., 2022). За нещодавно прийнятою консенсусною заявою щодо універсального визначення та класифікації СН, пацієнти із ЦД належать до стадії А (Bozkurt et al., 2021). Власне, навіть якщо пацієнти із ЦД не мають симптомів або ознак СН, вони належать до стадії В за наявності будь-яких ознак субклінічних порушень.
Алгоритми лікування СН у пацієнтів із ЦД, із фокусом на лікування за клінічними практичними настановами
Пацієнти з ризиком розвитку СН
Основною метою лікування пацієнтів із ризиком розвитку СН є запобігання розвитку порушення структури та функції серця. За нещодавніми настановами, для первинної профілактики СН рекомендовано:
- У пацієнтів з АГ артеріальний тиск (АТ) (<130/80 мм рт. ст.) контролювати за допомогою медичної терапії згідно з рекомендаціями для запобігання симптоматичній СН (GDMT).
- У пацієнтів із ЦД 2-го типу та наявною СС-хворобою або високим СС-ризиком використовувати інгібітори натрій-залежного котранспортера глюкози 2-го типу (іНЗКТГ‑2) для запобігання госпіталізації через СН (Yap et al., 2019; Kristensen et al., 2017; Birkeland et al., 2020; Oudejans et al., 2011; Kelder et al., 2011; Wettersten, 2021; Lee, 2022; American Diabetes Association Professional Practice Committee. Diabetes Care, 2022; Knuuti et al., 2019; ESC, 2020; Sharma et al., 2019; Marwick et al., 2018; Zinman et al., 2015; Neal et al., 2017).
- Здоровий спосіб життя – регулярна фізична активність, підтримання ваги у межах норми, здоровий харчовий режим та уникнення куріння, що є корисним для зниження ризику розвитку СН у майбутньому (Heidenreich et al., 2022).
Пацієнти із СНЗФВ
Загальні принципи фармакотерапії
У недавніх рекомендаціях із лікування СН наведено класи медикаментів згідно з рекомендаціями GDMT, зокрема інгібітори РААС (інгібітори рецепторів ангіотензину-неприлізину (ІРАН), інгібітор ангіотензинперетворювального ферменту (іАПФ) або блокатор рецептора ангіотензину II (БРА), бета-блокатори (ББ), антагоніст мінералокортикостероїдного рецептора (АМКР) та іНЗКТГ‑2 як перша лінія терапії для зниження кардіоваскулярної смертності та госпіталізації у пацієнтів із СНЗФВ та симптомами II‑III класів за класифікацією Нью-Йоркського серцевого товариства (NYHA) (McDonagh et al., 2021; Heidenreich et al., 2022).
Чотирикомпонентна терапія за допомогою ІРАН, ББ на підставі доказів, МКР та іНЗКТГ‑2 може знизити ризик смерті на 73% упродовж 2 років (Greene et al., 2021). Однак досягнення цільових доз кожного класу препаратів перед початком лікування наступним засобом може тривати >6 міс. Крім того, як зазначають дослідники, кожен із цих основних препаратів зменшує захворюваність і смертність протягом 30 днів після початку лікування (Lam et al., 2020).
Для отримання ранньої клінічної користі кожної окремої терапії запропоновано стратегії для початку та титрування комплексної хворобомодифікувальної терапії (Neal et al., 2017; McMurray et al., 2021). За даними рандомізованих контрольованих досліджень (РКД), відсоток пацієнтів із ЦД варіює від 20% до майже 50% (Shaw et al., 2020; Packer et al., 2020). Проте користь GDMT у пацієнтів із СНЗФВ спостерігали як у пацієнтів із ЦД, так і без діабету.
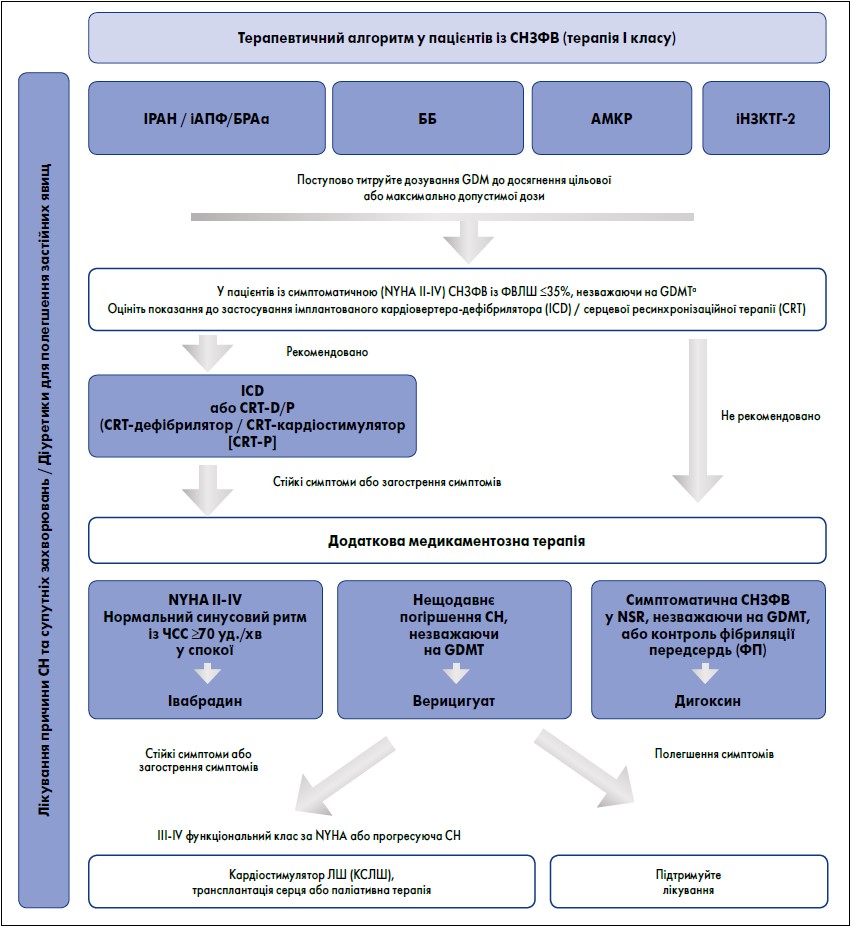
Алгоритм стратегії лікування, зокрема рекомендована лікарська терапія та прилади для застосування в пацієнтів із СНЗФВ, наведено на рисунку 2.
Рис. 2. Терапевтичний алгоритм для пацієнтів із СНЗФВ
Примітки: GDM – рекомендований настановою препарат; NYHA – Нью-Йоркська кардіологічна асоціація; GDMT – медикаментозне лікування згідно з рекомендаціями. aБРА рекомендовано як замінник, якщо пацієнти не переносять іAПФ або ІРАН.
Адаптовано за Korean Society of Heart Failure, 2022.
Рекомендовані дози засобів, що модифікують захворювання, а також протипоказання або обережний підхід до призначення цих препаратів у пацієнтів із СНЗФВ узагальнено в таблиці 3.
|
Таблиця 3. Доказові дози препаратів, що модифікують захворювання, у пацієнтів із СНЗФВ |
||
|
Препарат |
Початкове дозування |
Цільове дозування |
|
ІАПФ |
||
|
Каптоприл |
6,25 мг тричі на добу |
50 мг тричі на добу |
|
Еналаприл |
2,5 мг двічі на добу |
10–20 мг двічі на добу |
|
Лізиноприл |
2,5–5 мг раз на добу |
20-35 мг раз на добу |
|
Раміприл |
2,5 мг двічі на добу |
5 мг двічі на добу |
|
Трандолаприл |
0,5 мг раз на добу |
4 мг раз на добу |
|
ІРАНa |
||
|
Сакубітрил/Валсартан |
49/51 мг двічі на добу |
97/103 мг двічі на добу |
|
ББ |
||
|
Бісопролол |
1,25 мг раз на добу |
10 мг раз на добу |
|
Карведилол |
3,125 мг двічі на добу |
25 мг двічі на добу |
|
Метопролол |
12,5-25 мг раз на добу |
200 мг раз на добу |
|
Небіволол |
1,25 мг раз на добу |
10 мг раз на добу |
|
АMКР |
||
|
Еплеренон |
25 мг раз на добу |
50 мг раз на добу |
|
Спіронолактон - б |
25 мг раз на добу |
50 мг раз на добу |
|
іНЗКТГ-2 |
||
|
Дапагліфлозин |
10 мг раз на добу |
10 мг раз на добу |
|
Емпагліфлозин |
10 мг раз на добу |
10 мг раз на добу |
|
БРА |
||
|
Кандесартан |
4 мг раз на добу |
32 мг раз на добу |
|
Лозартан |
50 мг раз на добу |
150 мг раз на добу |
|
Валсартан |
40 мг двічі на добу |
160 мг двічі на добу |
|
Інші молекули |
||
|
Івабрадин |
5 мг двічі на добу |
7,5 мг двічі на добу |
|
Верицигуат |
2,5 мг раз на добу |
10 мг раз на добу |
|
Дигоксин |
62,5 мкг раз на добу |
250 мкг раз на добу |
|
Примітки: aСакубітрил / валсартан можна призначати в нижчій початковій дозі 24/26 мг двічі на добу в пацієнтів з історією симптоматичної гіпотензії, bСпіронолактон призначають у початковій дозі 12,5 мг пацієнтам із порушенням ниркової функції або гіперкаліємією. |
||
ІРАН
Сакубітрил / валсартан значно знижує частоту госпіталізації через загострення СН, СС-смерті та рівень загальної смертності в пацієнтів із СНЗФВ порівняно з еналаприлом (McMurray et al., 2014).
ІРАН також зменшує частоту СС-смерті або госпіталізацію через загострення СН у госпіталізованих пацієнтів із гострою декомпенсованою СН або із СНЗФВ, які раніше не отримували іАПФ (Velazquez et al., 2019; Wachter et al., 2019).
Останні дані свідчать, що ІРАН може зменшити потребу в діуретиках у пацієнтів із СНЗФВ і сприяє зворотному ремоделюванню серця та поліпшенню результатів лікування (Kerr et al., 2021; Park et al., 2022).
Згідно з цими результатами рекомендовано застосовувати ІРАН у симптоматичних пацієнтів із СНЗФВ для зниження ризику госпіталізації через загострення СН та смерті. Також ІРАН рекомендовано як заміну іАПФ або БРА в пацієнтів із СНЗФВ для зниження ризику госпіталізації через загострення СН та смерті (якщо пацієнти не переносять іАПФ або БРА).
ІАПФ / БРА
ІАПФ рекомендовано всім пацієнтам із СНЗФВ, якщо немає протипоказань або непереносимості, для зниження ризику госпіталізації та смерті від СН. Для поліпшення клінічних результатів дозу іАПФ слід підвищувати до рекомендованої максимально переносимої.
БРА рекомендовано як заміну іАПФ або ІРАН у пацієнтів із СНЗФВ для зниження ризику госпіталізації та смерті від СН (якщо пацієнти не переносять іАПФ або ІРАН).
Як зазначають дослідники, лише три БРА (валсартан, кандесартан та лозартан) продемонстрували користь щодо зниження частоти госпіталізації через загострення СН або смерті у великих РКД (Cohn et al., 2001; Pfeffer et al., 2003; Granger et al., 2003; Konstam et al., 2009).
Бета-блокатори
ББ рекомендовано всім пацієнтам із СНЗФВ для зниження ризику госпіталізації через загострення СН, редукції симптомів і запобігання смерті.
Приймання ББ необхідно починати за стабільного клінічного стану пацієнта із низької дози, поступово підвищуючи її до максимально переносимої. Зокрема, доведено користь трьох ББ (бісопролол, карведилол і метопролол-сукцинат із контрольованим / пролонгованим вивільненням) щодо зниження частоти госпіталізації через загострення СН та смертності в пацієнтів із СНЗФВ (CIBIS-II, 1999; Packer et al., 2001; Hjalmarson et al., 2000).
АМКР
АМКР рекомендовано всім пацієнтам із СНЗФВ для зниження ризику госпіталізації та смерті від СН (Pitt et al., 2022).
Для поліпшення клінічних результатів, дозування АМКР слід підвищувати до максимально переносимого рекомендованого. Пацієнтам із ризиком розвитку порушення функції нирок або гіперкаліємії під час лікування АМКР необхідно ретельно контролювати рівень калію та функцію нирок.
ІНЗКТГ‑2
Дапагліфлозин та емпагліфлозин зменшують ризик СС-смерті або госпіталізації через загострення СН приблизно на 26 і 25% відповідно у пацієнтів із симптоматичною стабільною СНЗФВ (McMurray et al., 2019; Packer et al., 2020; Braunwald et al., 2022).
Крім того, емпагліфлозин може знижувати потребу в діуретиках у пацієнтів з амбулаторною СН (Kim et al., 2022).
Для отримання користі іНЗКТГ‑2 для серцево-судинної системи, дапагліфлозин та емпагліфлозин рекомендовано пацієнтам із СНЗФВ із метою зниження ризику госпіталізації через загострення СН та смерті, незалежно від наявності ЦД.
Пацієнти із поліпшеною ФВ
Попри обмежену кількість даних щодо ведення пацієнтів із СН із поліпшеною ФВ (попередня ФВЛШ ≤40%, збільшення ФВЛШ на 10 пунктів проти базового рівня і під час другого визначення ФВЛШ >40%), дослідження щодо скасування терапії у пацієнтів із дилатаційною кардіоміопатією, у яких відновилася функція ЛШ, продемонструвало високий ризик рецидиву СН (44%) упродовж 6 міс. (Halliday et al., 2019). Щоб запобігти рецидиву СН і дисфункції ЛШ, рекомендовано продовжувати GDMT (навіть у пацієнтів без симптомів).
Пацієнти із СНПЗФВ і СННФВ
Попри велику кількість досліджень у пацієнтів із СННФВ та СНПЗФВ, зокрема значної кількості пацієнтів із ЦД, немає прямих доказів, що поточна терапія знижує СС-показники, окрім іНЗКТГ‑2. Два масштабні дослідження, EMPEROR-preserved і DELIVER, вивчали вплив іНЗКТГ‑2 на серцево-судинні показники в пацієнтів із СННФВ і СНПЗФВ. Результати цих досліджень засвідчили, що іНЗКТГ‑2 (емпагліфлозин, дапагліфлозин) значно знижують ризик СС-смерті або госпіталізації через загострення СН незалежно від наявності ЦД (Anker et al., 2021; Solomon et al., 2022).
За даними попередніх метааналізів кількох клінічних випробувань із використанням іНЗКТГ‑2 підтверджено їхній значний вплив на зниження ризику СС-смерті та госпіталізації через загострення СН незалежно від ФВЛШ (Jhund et al., 2022; Vaduganathan et al., 2022).
Отже, іНЗКТГ‑2 стануть основою терапії для зниження серцево-судинної смерті та частоти госпіталізації через загострення СН у широкому колі пацієнтів із СН, незалежно від наявності ЦД або ФВЛШ.
Крім того, для зниження симптомів застою в цих пацієнтів рекомендовано діуретики. Зниження маси тіла в пацієнтів з ожирінням та збільшення фізичної активності можуть додатково поліпшити стан здоров’я та фізичну працездатність, тож мають бути розглянуті у цій популяції. Важливо вчасно виявляти та звертати увагу під час лікування на основні чинники ризику, причину та супутні хвороби, як-от АГ, ІХС та анемія, якщо вони є. Зважаючи на постійний розвиток медичної науки та клінічних досліджень, рекомендації щодо лікування СН із часом можуть змінюватись. Рекомендовано консультуватися з кваліфікованим кардіологом або лікарем для отримання актуальної інформації та індивідуального підходу до лікування.
Нагляд та контроль
Пацієнти із хронічною СН, навіть якщо їхні симптоми добре контрольовані і стабільні, потребують постійного нагляду для забезпечення продовження оптимальної терапії та виявлення безсимптомного прогресування СН. Рекомендовано виконувати контрольне обстеження не рідше ніж через 6 міс. для оцінювання симптомів, частоти і ритму серцевих скорочень, АТ, ЗАК, рівня електролітів та функції нирок. Рекомендовано виконувати ТТЕхоКГ через 3‑6 міс. після оптимізації загальної лікувальної програми в пацієнтів із СНЗФВ, щоб визначити потребу в призначенні нових фармакологічних засобів та імплантації пристроїв.
Крім того, ТЕхоКГ слід повторити в пацієнтів із загостренням СН. Хоча визначення рівнів BNP або NT-proBNP надає прогностичну інформацію, рутинний моніторинг цих показників для коригування загальної лікувальної програми в пацієнтів із СН не рекомендовано (McDonagh et al., 2021; Heidenreich et al., 2022).
Коли звертатися до кардіолога в разі СН
Своєчасне і належне скерування до кардіолога окремих пацієнтів із СН є дуже важливим для оцінювання вперше виявленої СН та оптимізації стратегій лікування для запобігання її прогресуванню.
Фармакотерапія ЦД у пацієнтів із СН
ІНЗКТГ‑2
ІНЗКТГ‑2 знижують рівень глюкози в крові завдяки інгібуванню резорбції глюкози в проксимальних канальцях нирок у пацієнтів із ЦД 2-го типу.
Клінічні дослідження, що оцінювали СС-результати використання іНЗКТГ‑2, підтвердили, що ці препарати знижують ризик госпіталізації через СН у пацієнтів із ЦД 2-го типу (Marwick et al., 2018; Zinman et al., 2015; Wiviott et al., 2019). За даними останніх досліджень, іНЗКТГ‑2 мають корисні ефекти на СН у пацієнтів без діабету.
У дослідженні DAPA-HF (Study to Evaluate the Effect of Dapagliflozin on the Incidence of Worsening Heart Failure or Cardiovascular Death in Patients With Chronic Heart Failure) вивчали вплив дапагліфлозину на ризик загострення СН або смерті від СС-причин у пацієнтів із СН II‑IV класу за NYHA та ФВ ≤40% (McMurray et al., 2019).
Після медіанного періоду (18,2 міс.), лікування дапагліфлозином знижувало ризик госпіталізації через СН або СС-смерть на 26% (відношення ризику [HR] 0,74; 95% довірчий інтервал [CI] 0,65‑0,85).
Корисні ефекти дапагліфлозину були подібними як у пацієнтів із ЦД, так і без. Ці результати підтверджено у дослідженні EMPEROR-Reduced (EMPAgliflozin outcomE tRial in Patients With chrOnic heaRt Failure With Reduced Ejection Fraction) (Packer et al., 2020). Упродовж медіанного періоду спостереження 16 міс. первинні показники, як-от смерть від СС-причин та госпіталізація через СН, зменшилися на 25% у групі, що отримувала емпагліфлозин (HR0,75; 95% CI 0,65‑0,86).
Ці ефекти фіксували незалежно від наявності ЦД. У ретроспективному спостережному дослідженні з використанням бази даних Національного страхового сервісу в Кореї було встановлено, що призначення іНЗКТГ‑2 пов’язане з меншим ризиком розвитку СН, порівняно з призначенням інгібіторів дипептидилпептидази‑4 (іДПП‑4) або сульфонілсечовини як засобів додаткової терапії до метформіну в пацієнтів із ЦД 2-го типу в Кореї (Jeon et al., 2021). За цими результатами, іНЗКТГ‑2 рекомендовано як препарати першої лінії для зниження рівня глюкози в крові у пацієнтів із ЦД 2-го типу із СН, незалежно від рівня HbA1c. ІНЗКТГ‑2 спричиняють осмотичний діурез, збільшуючи виділення глюкози із сечею та зумовлюючи підвищену схильність пацієнтів до втрати рідини та постуральної гіпотензії, особливо у літніх пацієнтів або тих, хто приймає діуретики. Втрата рідини, спричинена іНЗКТГ‑2, може призвести до порушення функції нирок. У клінічних випадках повідомляли про гостре ураження нирок у пацієнтів, які отримують іНЗКТГ‑2. Слід оцінювати ступінь гідратації, а також під час лікування іНЗКТГ‑2 забезпечити достатнє вживання води. ІНЗКТГ‑2 збільшують ризик розвитку інфекцій сечовивідних шляхів та генітальних інфекцій, особливо у жінок. Тому необхідно вчасно виявляти ознаки та симптоми цих інфекцій та лікувати.
Зокрема, описано кетоацидоз з еуглікемією або помірно підвищеним рівнем глюкози в крові (<250 мг/дл) у пацієнтів, які отримували іНЗКТГ‑2 (Donnan et al., 2019). За тривалого голодування через гостре захворювання або перед запланованою хірургічною операцією лікування іНЗКТГ=2 слід припинити для уникнення можливого ризику розвитку діабетичного кетоацидозу.
Метформін
Хоча метформін раніше вважали протипоказаним пацієнтам із СН через потенційний ризик розвитку лактацидозу, останні аналізи свідчать, що метформін має корисні ефекти в пацієнтів із ЦД і СН, поліпшуючи чутливість до інсуліну. У метааналізі дев’яти когортних досліджень терапія метформіном була пов’язана зі зниженням загальної смертності порівняно з будь-якою іншою антидіабетичною терапією: 23% проти 37% (відношення шансів [OR] 0,80; 95% довірчий інтервал [CI] 0,73‑0,88) у пацієнтів із ЦД і СН (Eurich et al., 2013).
У дослідженні метформін не асоціювався зі збільшеним ризиком розвитку метаболічного ацидозу. Більшість доказів підтверджує безпеку метформіну в пацієнтів із ЦД і СН. Однак слід припинити його застосування у пацієнтів із гострою декомпенсованою СН, сепсисом або гіпоперфузією для уникнення розвитку лактоацидозу.
Агоністи рецепторів глюкагоноподібного пептиду‑1
Агоністи рецепторів глюкагоноподібного пептиду‑1 (АРГПП‑1) є ефективними для контролю глікемії та зниження ваги. У дослідженнях із вивчення СС-результатів при застосуванні АР ГПП‑1 деякі з них демонстрували користь щодо СН у пацієнтів із ЦД 2-го типу. Дослідження LEADER (Liraglutide Effect and Action in Diabetes: Evaluation of Cardiovascular Outcome Results) продемонструвало значне зниження комбінованого показника смерті від СС-причин, нефатального інфаркту міокарда або нефатального інсульту в пацієнтів із ЦД 2-го типу з підвищеним СС-ризиком (Marso et al., 2016). У дослідженні SUSTAIN‑6 (Trial to Evaluate Cardiovascular and Other Long-term Outcomes With Semaglutide in Subjects With Type 2 Diabetes) застосування семаглутиду знизило ризик виникнення серйозних серцево-судинних подій на 24% (Marso et al., 2016).
У дослідженні REWIND (Researching Cardiovascular Events With a Weekly Incretin in Diabetes) дулаглутид також пов’язували зі зниженням ризику СС-подій на 12% (Gerstein et al., 2019).
Однак ризик госпіталізації з приводу СН, який оцінювали як вторинний показник у цих дослідженнях, не вирізнився між групами лікування та контролю. У метааналізі восьми РКД АРГПП‑1 знизив ризик госпіталізації з приводу СН на 10% (HR0,90; 95% CI 0,83‑0,98) (Giugliano et al., 2021).
Ба більше, у дослідженні FIGHT (Functional Impact of GLP‑1 for Heart Failure Treatment) за участю 300 осіббб із СН (III‑IV класи за NYHA) із ЦД 2-го типу, ліраглутід не мав впливу на клінічну стабільність після госпіталізації або на частоту повторної госпіталізації з приводу СН (Margulies et al., 2016).
Отже, АРГПП‑1 можуть бути безпечними для застосування у пацієнтів із СН, хоча не демонструють позитивного ефекту.
Похідні сульфонілсечовини
Хоча деякі спостережні дослідження, у яких порівнювали похідні сульфонілсечовини з іншими антидіабетичними препаратами, вказують на слабкий зв’язок між прийманням зазначених препаратів і ризиком серцево-судинних подій, результати РКД свідчать про нейтральний їх вплив на ризик СС-подій. Так, у дослідженні CARMELINA (Cardiovascular and Renal Microvascular Outcome Study With Linagliptin in Patients With Type 2 Diabetes Mellitus) лінагліптин не погіршив безпеку з боку серцево-судинної системи порівняно з плацебо в пацієнтів із СС-захворюваннями (UKPDS Group, 1998).
У дослідженні SOLID (Sulfonylurea Compared to Insulin for Glycemic Control in Type 2 Diabetes) глібенкламід не був пов’язаний зі збільшенням ризику СС-подій порівняно з інсуліном (Rados et al., 2016).
Проте необхідно брати до уваги, що похідні сульфонілсечовини можуть призводити до гіпоглікемії, особливо в пацієнтів зі зниженою нирковою функцією, і це може бути небезпечним для осіб із СС-захворюваннями. Загалом під час вибору антидіабетичного препарату в осіб із СС-захворюваннями важливо враховувати індивідуальні особливості, клінічний стан та поточне лікування. Призначення лікарських засобів має здійснювати лікар, зважаючи на вказані чинники та забезпечуючи безпеку й ефективність такого втручання.
Тіазолідиндіони
Тіазолідиндіони (ТЗД) можуть спричиняти затримку рідини та збільшення ваги, а також підвищувати ризик розвитку СН.
У дослідженні RECORD (Rosiglitazone Evaluated for Cardiac Outcomes and Regulation of Glycaemia in Diabetes) виявлено підвищений ризик смерті або госпіталізації з приводу СН у зв’язку з розиглітазоном (HR2,10; 95% CI 1,35‑3,27) (Komajda et al., 2010).
Тоді як у дослідженні DREAM (Diabetes Reduction Assessment with ramipril and rosiglitazone Medication) розиглітазон зменшував ризик розвитку ЦД та хвороби нирок, але підвищував ризик розвитку СН (HR7,03; 95% CI 1,60‑30,9) у пацієнтів із предіабетом (Gerstein et al., 2006).
У дослідженні PROACTIVE (PROspective pioglitAzone Clinical Trial In macroVascular Events) піоглітазон хоча й знизив на 16% ризик розвитку вторинної кінцевої точки – смертності від усіх причин, нефатального інфаркту міокарда та інсульту (HR0,84; 95% CI 0,72‑0,98), ризик розвитку СН порівняно з плацебо збільшився (HR1,41; 95% CI 1,10‑1,80) (Dormandy et al., 2005). Застосування ТЗД протипоказане в пацієнтів із СН II‑IV функціональних класів за NYHA та має здійснюватися з обережністю в осіб з ознаками або симптомами СН або високим ризиком її розвитку.
Цільовий рівень глікемії в пацієнтів із СН
Попри те, що було проведено кілька РКД, у яких вивчали ефективність інтенсивного глікемічного контролю щодо СС-показників, оптимальні цільові рівні глікемії в пацієнтів із СН та ЦД ще не оцінювали (Shen et al., 2021).
Поточні рекомендації Корейського товариства з діабету вказують на рівень HbA1c менш ніж 6,5% для більшості дорослих пацієнтів із ЦД 2-го типу, але наголошують на індивідуалізації підходу залежно від характеристик пацієнта та супутніх захворювань (Hur et al., 2021).
Консенсусна декларація
1. Загалом оцінювання та лікування СН у пацієнтів із ЦД та без діабету подібні. Пацієнти із ЦД мають вищий ризик розвитку СН та гірший прогноз. Тому в цій популяції хворих необхідний більш комплексний підхід до лікування СН.
2. Рекомендовано визначати рівні BNP або NT-proBNP для діагностування або виключення СН у пацієнтів із ЦД, які мають симптоми (задишка, неприємні відчуття або типовий біль у грудях) та/або ознаки (застійні явища в легенях або периферичний набряк).
3. Необхідно розглянути можливість виконання функціональних стрес-тестів або коронарографії для оцінювання ішемії міокарда та визначення ІХС як причини СН у пацієнтів із ЦД, які мають симптоми (утруднене дихання, неприємні відчуття або типовий біль у грудях) та/або ішемічні ознаки на ЕКГ (відхилення сегмента ST, інверсія зубця T або Q-хвилі).
4. У пацієнтів із підозрою на СН або високими рівнями BNP (≥35 пг/мл, ≥100 пг/мл; для хронічної і гострої СН, відповідно) або NT-proBNP (≥125 пг/мл, ≥300 пг/мл; для хронічної і гострої СН відповідно), необхідно виконати TTEхоКГ для оцінювання структури та функції серця.
5. Рекомендовано застосовувати інгібітори ренін-ангіотензин-альдостерону (ІРАА), зокрема ІРАН, іАПФ або БРА, ББ, АМКР та іНЗКТГ‑2 як засоби першої лінії терапії для зменшення серцево-судинної смертності та госпіталізації в пацієнтів із СНЗФВ і симптомами II‑III функціональних класів за NYHA.
6. Рекомендовано іНЗКТГ‑2 застосовувати у пацієнтів із СННФВ та СНПЗФВ із виразною симптоматикою і/або госпіталізаціями з приводу СН, а також із ЦД і СН, незалежно від ФВ, для зменшення СС-подій та поліпшення прогнозу.
7. У пацієнтів із ЦД та СН рекомендовано використовувати стандартні лікувальні підходи до контролю глікемії, як-от дієта, фізична активність, оральні гіпоглікемічні засоби та/або інсулін, з урахуванням індивідуальних характеристик пацієнта та супутніх захворювань.
8. У разі використання антиглікемічних препаратів у пацієнтів із ЦД та СН необхідно уникати препаратів, які можуть погіршувати симптоми СН або підвищувати ризик СС-подій.
9. Цільові рівні глікемії в пацієнтів із ЦД та СН мають бути індивідуалізовані, зважаючи на загальний стан пацієнта, супутні захворювання та прогностичні чинники.
Підготував Денис Соколовський
Оригінальний текст документа читайте на сайті www.ncbi.nlm.nih.gov