4 березня, 2024
Сучасні можливості корекції мітохондріальної дисфункції: у фокусі – біорегуляційні енерготропи
Протягом останніх років лікарі різноманітних спеціальностей приділяють багато уваги мітохондріям – ключовим органелам людської клітини, які відповідають за продукування клітинної енергії. Нині панує думка, що порушення функції мітохондрій може спричинити розвиток різноманітних захворювань (як генетичної, так і хронічної патології), а також деяких патологічних станів.
Саме дисфункція мітохондрій визнана однією з характерних ознак старіння [8] і різноманітних хронічних захворювань, у т. ч. нейродегенеративної патології (хвороби Альцгеймера, Паркінсона, Гантінгтона, бічний аміотрофічний склероз) [6], ендотеліальної дисфункції [12] та різноманітних серцево-судинних захворювань – атеросклерозу, ішемічної хвороби серця, інфаркту міокарда [3, 4], фібриляції передсердь [2, 10], метаболічного синдрому, захворювання печінки, асоційованого з метаболічними розладами [16]. Виникнення цукрового діабету [15], ожиріння, недостатності яєчників [8], остеопорозу [7], порушення антиоксидантного захисту, розвиток неопластичної патології [15] також пов’язують з мітохондріальною дисфункцією. Навіть нейроповедінкові та психіатричні захворювання (розлади аутистичного спектра, шизофренія, біполярні й афективні розлади), в т. ч. синдром хронічної втоми, синдром війни в Перській затоці визнані асоційованими з дисфункцією мітохондрій [11]. Згідно з домінувальним ставленням ефективність лікування всіх вищезазначених захворювань може бути поліпшена завдяки покращенню функціональної активності мітохондрій [6, 8-10].
Молекулярні основи мітохондріальної дисфункції: стисло про сучасні погляди
Завдяки електронній мікроскопії стало відомо, що мітохондрії надходять до клітини завдяки транспорту через клітинну мембрану, а після проходження крізь цитоскелет вони фіксуються в окремих місцях: найбільшу щільність мітохондрій спостерігають перинуклеарно та поблизу ендоплазматичного ретикулуму [5]. Мітохондрії включено до складу спеціалізованих структурних доменів, відомих як мітохондрія – асоційовані мембрани. Фактично зазначені структурні домени забезпечують фізичний контакт між різноманітними клітинними органелами (ядро, лізосоми, ендоплазматичний ретикулум, апарат Гольджі), які беруть участь у регуляції синтезу аденозин‑5’-трифосфату (АТФ) (рис. 1).
Рис. 1. Функції мітохондрій [5]
Нині вважають, що мітохондріальна дисфункція виникає через декілька причин:
- недостатня кількість мітохондрій;
- нездатність організму забезпечити мітохондрії необхідними субстратами для синтезу АТФ;
- дисфункція власних мітохондріальних механізмів щодо забезпечення транспорту електронів і синтезу АТФ [5, 11].
Кількість та функціональна активність мітохондрій у клітині може змінюватися:
- при руйнуванні та деградації мітохондрій, активність яких уже значно знизилася під впливом різноманітних факторів зовнішнього середовища;
- за злиття компонентів мітохондрій із частково зниженою активністю з неушкодженими компонентами задля покращення загальної функції енергетичних станцій клітини;
- під час утворення абсолютно нових мітохондрій [11].
Недостатня кількість вихідних субстратів значно обмежує здатність мітохондрій синтезувати такі високоенергетичні молекули, як АТФ: нестача метаболітів зумовлює неможливість відновлення нікотинамідаденіндинуклеотиду та унеможливлює його подальшу трансформацію, фосфорилювання аденозиндифосфату в АТФ [5, 11]. Внаслідок зазначених причин мітохондріальна дисфункція супроводжується зниженням ефективності внутрішньоклітинного транспорту електронів і спричиняє зниження синтезу високоенергетичних молекул, у т. ч. АТФ [11].
Крім забезпечення внутрішньоклітинного синтезу АТФ, установлені т. зв. позаклітинні ефекти мітохондріального функціонування, завдяки яким мітохондрії здатні впливати на активність центральної нервової системи, кишкової мікробіоти, метаболічні процеси, імунної системи [5]. Доведено, що мітохондрії беруть участь у різноманітних метаболічних процесах: гомеостаз заліза, кальцію, глюкози, лактату, ліпідів, антиоксидантний захист. Саме тому наслідки мітохондріальної дисфункції проявляються на різноманітних рівнях і мають різні клінічні прояви (гастроінтестинальні, серцево-судинні, неврологічні, психіатричні, ендокринологічні, пухлинні тощо) та навіть провокують прискорення старіння [2-12].
Сучасні можливості біорегуляційної корекції мітохондріальної дисфункції
З метою відновлення функціональної активності мітохондрій нині застосовують різноманітні нефармакологічні та фармакологічні підходи, в т. ч. природні засоби – енерготропи [5]. Енерготропи – метаболічно активні засоби, які впливають на процеси енергетичного обміну, пов’язані з внутрішньоклітинними окислювальними механізмами анаеробного й аеробного окислення [17]. Дія енерготропних препаратів здійснюється здебільшого на рівні мітохондрій: вони сприяють окисленню пірувату до ацетил-КоА з подальшим окисленням останнього до вуглекислого газу, реокисленню відновленого коензиму Q ферментами електронно-транспортного ланцюга внутрішньої мітохондріальної мембрани, а також окисному дезамінуванню амінокислот з їхнім подальшим надходженням до циклу Кребса [17]. Доцільність застосування лікарських засобів для нівелювання мітохондріальної дисфункції та поліпшення перебігу різноманітних хронічних захворювань підтримує значна кількість вчених, вважаючи, що покращення функції мітохондрій сприятиме швидшому одужанню та/або покращенню стану хворих [6, 8-10].
Безперечно, з огляду на вищезазначені молекулярні реакції можна запропонувати значну кількість енерготропних препаратів, але найчастіше в клінічній практиці використовуються такі препарати, як вітаміни, мінерали, антиоксиданти, метаболіти, інгібітори та кофактори ферментів, мембранні фосфоліпіди. Біорегуляційні препарати можуть бути ідеальними енерготропами, адже вони містять значну кількість активних інгредієнтів; саме тому біорегуляційні засоби часто називають енерготропами (тобто дещо звужуючи вищенаведене поняття), а їхнє практичне застосування – енерготропною терапією.
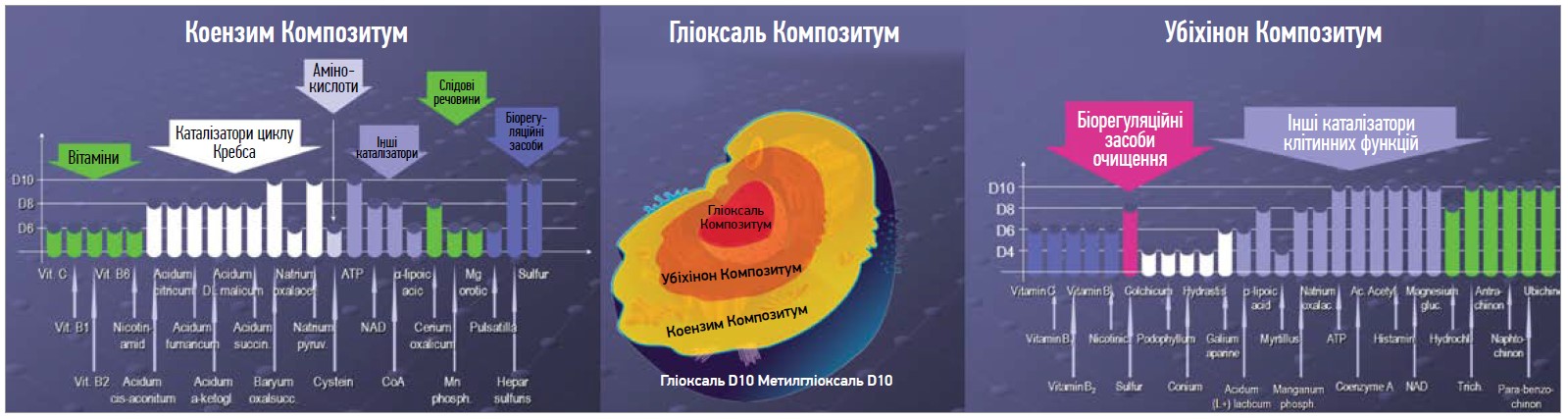
Найвідомішими біорегуляційними енерготропами є комплексні засоби, які презентує у нашій країні компанія Heel під торговими назвами Гліоксаль Композитум, Коензим Композитум, Убіхінон Композитум. Кожен вищезазначений препарат призначений для парентерального застосування та має ампульну форму випуску. Так, ампула Гліоксаль Композитум містить 22 мг гліоксалю D10 та 22 мг метилгліоксалю D10 [18]. Впливаючи на глутамінну трансаміназу щавлевої кислоти, Гліоксаль Композитум забезпечує активацію ферментів клітинного дихання та відновлення синтезу АТФ, сприяє виведенню токсинів із внутрішньоклітинного простору завдяки відновленню роботи ферментних систем [18]. Багатокомпонентий засіб Коензим Композитум містить декілька активних інгредієнтів, основними з яких є каталізатори циклу Кребса, коензим А, АТФ і вітаміни (рис. 2). Завдяки комбінованому мінеральному, рослинному складу Коензим Композитум забезпечує активацію ферментних систем циклу Кребса, усуває гіпоксію тканин і сприяє виникненню метаболічного, антиоксидантного, дезінтоксикаційного ефектів [19]. До складу іншого багатокомпонентного енерготропа Убіхінон Композитум входять речовини, необхідні для відновлення активності різноманітних ферментних систем і клітинного дихання, в т. ч. убіхінон, коензим А, кислота аскорбінова, вітамін В6, нікотинамід [20]. Отже, комбіноване застосування біорегуляційних енерготропів у нівелюванні мітохондріальної дисфункції можна вважати патогенетично обґрунтованим. Усі зазначені препарати вводять парентерально 1-3 р/тиж у вигляді внутрішньом’язових, підшкірних, внутрішньошкірних ін’єкцій [18-20].
Рис. 2. Комбінована біорегуляційна енерготропна терапія та її складові [13]
Ефективність та безпечність комбінованого і послідовного застосування енерготропів вивчалися в різноманітних експериментальних й клінічних дослідженнях. Призначення Убіхінону Композитум і Коензиму Композитум лабораторним тваринам сприяло покращенню мітохондріальної активності сперматозоїдів [1]. Введення великій рогатій худобі Убіхінону Композитум і Коензиму Композитум забезпечувало підвищення фертильності биків завдяки поліпшенню рухової активності сперматозоїдів без негативного впливу на їхню життєздатність, цілісність акросом, структуру хроматину [1].
Прикладом успішного застосування послідовної комплексної терапії енерготропами може бути клінічне дослідження, дизайн якого передбачав два етапи: на першому етапі, проведеному в умовах in vitro, досліджували вплив Коензиму Композитум, Убіхінону Композитум, Гліоксалю Композитум, Траумелю на функціональну активність натуральних кілерів у здорових добровольців [14]; під час другого етапу, виконаного in vivo, зазначені препарати протягом 3 міс вводили хворим на прогресувальний рак різноманітних локалізацій з подальшим дослідженням функції натуральних кілерів. Черговість застосування енерготропів була такою: спочатку пацієнти отримували Убіхінон Композитум, згодом – Гліоксаль Композитум, Траумель, а завершували лікування за допомогою Коензиму Композитум. Комбінована терапія зазначеними біорегуляційними енерготропами сприяла достовірному (р<0,05) та значному підвищенню цитотоксичної активності натуральних кілерів як у здорових добровольців, так і в ракових хворих, що, на думку дослідників, стало результатом відновлення енергетичних запасів у цих клітинах [14].
Висновки
Мітохондріальна дисфункція супроводжує перебіг різноманітних захворювань та патофізіологічних станів. Комбіноване і послідовне застосування трьох біорегуляційних енерготропних засобів (Гліоксаль Композитум, Коензим Композитум, Убіхінон Композитум) сприяє відновленню енергетичних запасів клітини, нівелюванню мітохондріальної дисфункції та поліпшенню стану хворих із різноманітною патологією [18-20].
Гліоксаль Композитум рекомендується призначати як підтримувальну терапію при захворюваннях, перебіг яких асоційований з мітохондріальною дисфункцією (стенокардія, розсіяний склероз, склеродермія, м’язова дистрофія, онкологічні захворювання) [18]. Коензим Композитум доцільно вводити до складу комплексної терапії різноманітних гострих і хронічних захворювань, реконвалесценції після інфекційних захворювань, при фізичному та психічному виснаженні, порушенні засвоєння вітамінів [19], як і Убіхінон Композитум, котрий слід додавати до схем лікування з метою відновлення заблокованих ферментних систем та за порушення їхнього функціонування з метою стимуляції захисних механізмів [20]. Послідовне застосування зазначених біорегуляційних енерготропних засобів відповідає основним принципам біорегуляційної терапії та дозволяє вплинути на клітинну фазу патологічного процесу, відновивши внутрішньоклітинні запаси енергії та сприяючи швидшому відновленню клітинних функцій.
Список літературизнаходиться в редакції.



![Рис. 1. Функції мітохондрій [5]](/multimedia/userfiles/images/2024/ZU_4_2024/ZU_4_2024_Energotropi_pic_1.jpg)