23 травня, 2021
Сучасні можливості застосування валсартану в лікуванні пацієнтів з артеріальною гіпертензією
 Згідно з сучасними статистичними даними, захворювання серцево-судинної (СС) системи є провідною причиною смерті в Україні. Близько 67% летальних випадків у структурі загальної смертності в нашій країні стаються через СС-патологію. Артеріальна гіпертензія (АГ) – одна з найактуальніших медико-соціальних проблем зважаючи на її поширеність та частоту розвитку СС-ускладнень. Розглянемо основні принципи лікування пацієнтів з АГ відповідно до сучасних рекомендацій Європейського товариства кардіологів (ESC), зокрема питання можливості використання валсартану в терапії хворих на АГ.
Згідно з сучасними статистичними даними, захворювання серцево-судинної (СС) системи є провідною причиною смерті в Україні. Близько 67% летальних випадків у структурі загальної смертності в нашій країні стаються через СС-патологію. Артеріальна гіпертензія (АГ) – одна з найактуальніших медико-соціальних проблем зважаючи на її поширеність та частоту розвитку СС-ускладнень. Розглянемо основні принципи лікування пацієнтів з АГ відповідно до сучасних рекомендацій Європейського товариства кардіологів (ESC), зокрема питання можливості використання валсартану в терапії хворих на АГ.
В Україні зареєстровано понад 11 млн хворих на АГ, а частота мозкового інсульту та смертності від нього є найвищими в Європі. Це зумовлено малоефективним контролем артеріального тиску (АТ), вагомий вклад у який вносить низька прихильність до призначеної терапії [1].
Для кардіологів та лікарів первинної ланки була вельми важливою розробка 2018 року нових європейських рекомендацій із діагностики та лікування АГ сумісно ESC та Європейським товариством з гіпертензії (ESH). Порівняно з попередньою версією документ має низку відмінностей та нововведень як із точки зору діагностики, класифікації, стратифікації ризику, так і з позицій підходу до медикаментозного контролю АТ. Необхідно підкреслити важливість дотримання основних положень рекомендацій у реальній клінічній практиці для підвищення ефективності лікування та поліпшення комплаєнсу пацієнтів. Відповідно до оновленої настанови, основною тактикою є призначення комбінованої антигіпертензивної терапії (АГТ) у вигляді фіксованих комбінацій (ФК) для більшості пацієнтів вже на початку лікування (стратегія однієї таблетки) [2].
Двома важливими положеннями нових рекомендацій з АГ є цільові діапазони та нижні рівні АТ на тлі застосування АГТ залежно від віку пацієнта, коморбідної патології, а також суттєвий акцент на прихильності хворого до призначеного лікування [3]. Безумовно, найактуальнішим із позиції практичної медицини є питання терапії АГ: початок медикаментозної АГТ, цільові рівні АТ та алгоритм вибору антигіпертензивного препарату (АГП).
Згідно з європейськими рекомендаціями (2018), ініціювати фармакологічну АГТ необхідно у всіх хворих на АГ 2‑3-го ст. незалежно від ризику та у пацієнтів з АГ 1-го ст. за умови високого / дуже високого ризику розвитку СС-ускладнень і наявності СС-патологій, хронічної хвороби нирок (ХХН) та/або ознак ураження органів, зумовленого АГ. В осіб з АГ 1-го ст. та низьким або помірним ризиком АГТ необхідно починати у разі неефективності заходів із модифікації способу життя у зниженні АТ протягом 3‑6 місяців. Окремо наведені критерії початку АГТ у пацієнтів старших вікових груп. Так, приймання АГП та корекція способу життя показані усім літнім хворим (навіть у віковій категорії «80+») при систолічному АТ (САТ) ≥160 мм рт. ст., а також особам віком 65‑79 років при АГ 1-го ст. та за умови сприятливої переносимості лікування [2, 3].
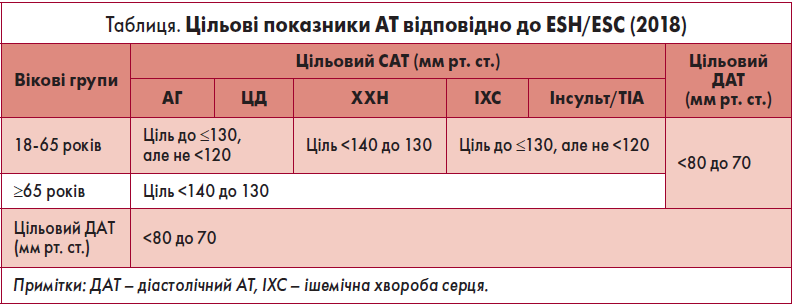
При обговоренні питання цільових рівнів АТ необхідно зазначити, що у настанові вказаний нижній рівень безпечного зниження АТ, а також наведені менші значення цільового АТ для старших вікових груп. Так, для пацієнтів віком 18‑64 роки як при неускладненій АГ, так і за наявності цукрового діабету (ЦД), та/або СС-патології, та/або інсульту / транзиторної ішемічної атаки (ТІА) в анамнезі доцільно застосовувати ступінчастий підхід до зниження АТ: першою метою є рівень АТ <140/90 мм рт. ст., та за умови хорошої переносимості його слід знижувати до ≥130/80 мм рт. ст., але не <120/70 мм рт. ст. У хворих на ХХН цільовий АТ має бути в діапазоні 130‑139/70‑79 мм рт. ст. Такі самі цільові показники АТ (130‑139/70‑79 мм рт. ст.) рекомендовані для усіх хворих вікової категорії «65+» із можливістю змінення тактики АГТ та її цілей в ослаблених пацієнтів та осіб, які потребують сторонньої допомоги (таблиця) [2, 3].
В європейських рекомендаціях з АГ ключовою стратегією медикаментозного контролю АТ, як вже було зазначено, є використання комбінованої АГТ вже на старті лікування у більшості пацієнтів, причому у вигляді ФК (стратегія однієї таблетки). Монотерапію можна застосовувати в осіб з АГ 1-го ст. із низьким ризиком та САТ <150 мм рт. ст. або хворим із високим нормальним АТ за наявності помірного ризику СС-ускладнень, а також ослабленим особам похилого віку (рисунок) [2, 3].
Призначення саме ФК АГП зумовлене перевагами над їх вільними комбінаціями. З одного боку, на тлі застосування ФК значно зростає прихильність пацієнтів до лікування, оскільки зменшується кількість таблеток, які необхідно прийняти. З іншого – ФК сприяють найефективнішому досягненню та контролю показників АТ (при переході на терапію ФК приблизно вдвічі зростає частка пацієнтів, у яких АТ контролюється), забезпечують кращу органопротекцію і, таким чином, дають змогу значно знизити ризик СС-ускладнень [1, 3].
У рекомендаціях ESH/ESC (2018) кращою початковою схемою комбінованої АГТ у більшості хворих (за умови відсутності особливих клінічних ситуацій) є призначення блокатора ренін-ангіотензин-альдостеронової системи – інгібітора ангіотензинперетворювального ферменту (іАПФ) або блокатора рецепторів ангіотензину II (БРА) – у поєднанні з антагоністом кальцію (АК) або діуретиком [2, 3].
Переваги даного алгоритму комбінованої АГТ можуть бути розглянуті на прикладі валсартану – одного з еталонних представників класу БРА.
Насамперед слід звернути увагу на те, що в патогенезі підвищення АТ, ремоделювання міокарда й судинного русла ключову роль відіграють РААС та ангіотензин II як її головний медіатор, що безпосередньо взаємодіє із СС-системою і реалізує свої негативні ефекти. Механізм дії іАПФ полягає у пригніченні активності ангіотензинперетворювального ферменту, який сприяє перетворенню ангіотензину I в ангіотензин II. Але в організмі останній синтезується й іншими способами, наприклад, у тканинах він утворюється під впливом ферментів хімази. Такі шляхи вислизають з-під контролю іАПФ, унаслідок чого пригнічення РААС цією групою АГП може бути недостатньо ефективним. На відміну від іАПФ, мішенню БРА є рецептори ангіотензину II 1-го типу, тож у результаті їх блокування повністю припиняється прямий негативний вплив ангіотензину II на СС-систему [3].
У 2015 р. були опубліковані результати великого метааналізу (68 клінічних досліджень, 195 267 пацієнтів), присвяченого порівняльній оцінці впливу різних класів АГП на прогноз. Зіставлення даних, отриманих у цих дослідженнях, показало, що за впливом на загальну смертність іАПФ не мають жодних переваг над БРА. При цьому БРА продемонстрували тенденцію до навіть суттєвішого зниження ризику інсульту та серцевої недостатності (СН), а також комбінованої кінцевої точки, що включала інсульт + ІХС + СН, порівняно з іншими АГП [4].
Крім того, БРА мають важливу перевагу над іншими класами АГП – хорошу переносимість, яка сприяє формуванню високої прихильності пацієнтів до лікування.
Класифікація БРА [5]
За хімічною структурою (тропність до рецепторів)
- біфенілтетразоли (ірбесартан, кандесартан, лозартан, олмесартан)
- біфенілові нететразоли (азілсартан, телмісартан)
- небіфенілові нететразоли (епросартан)
- негетероциклічні БРА (валсартан)
За характером метаболізму
- проліки, для яких необхідна метаболічна трансформація і виділення активних метаболітів (азілсартан, кандесартан, лозартан, олмесартан)
- ліки (валсартан, епросартан, ірбесартан, телмісартан), які безпосередньо містять активні метаболіти і не потребують певної метаболічної трансформації
За даними G. Mancia et al., прихильність хворих на АГ до лікування БРА перевищує таку до інших класів АГП. Позитивний комплаєнс зберігається також за призначення ФК БРА з іншими препаратами. Наприклад, у дослідженні J. Jackson et al. показано, що дотримання режиму терапії ФК БРА із гідрохлортіазидом (ГХТЗ) мало місце у 54% пацієнтів, тоді як за приймання вільної комбінації даних ліків показник знижувався до 19%. Це ще раз підкреслює важливість призначення фіксованих антигіпертензивних комбінацій хворим на АГ, які потребують терапії 2‑3 лікарськими засобами [4].
БРА мають схожу молекулярну будову, яка зумовлює ефекти класу. Проте не всі сартани клінічно та фармакологічно еквівалентні, що пояснюється наявністю у структурі фрагменту, який є специфічним для кожної діючої речовини і формує ефекти молекули [6].
Ефекти класу пов’язані зі здатністю сартанів блокувати рецептори ангіотензину ІІ, звідки й походить їх назва (SARTAN – Short for Angiotensin-RecepTor-ANtagonist) [7]. Проте слід пам’ятати, що є декілька типів рецепторів ангіотензину ІІ, і стимуляція кожного з них зумовлює різні ефекти [8]. СС-ефекти ангіотензину ІІ реалізуються через рецептори 1-го та 2-го типів, причому їх стимуляція призводить до протилежних ефектів.
Так, стимуляція рецепторів 1-го типу спричиняє артеріальний вазоспазм, підвищення тиску в гломерулярному апараті нирок зі зниженням ниркового кровотоку, стимуляцію мезангіального апарату, збільшення реабсорбції натрію, секреції альдостерону та вазопресину, вивільнення ендотеліїну 1, підвищення активності симпатичної нервової системи, ремоделювання судин та міокарда. Стимуляція рецепторів 2-го типу, навпаки, зумовлює сприятливі ефекти: вазодилатацію, яка, зокрема, виникає внаслідок збільшення продукції оксиду азоту (NO), пригнічення клітинного поділу (гладких міоцитів судинної стінки, фібробластів тощо), гальмування гіпертрофії кардіоміоцитів [8].
Тому важлива не лише здатність до блокування рецепторів ангіотензину ІІ, але також його селективність. У валсартану ця селективність є найбільш вираженою з усіх БРА: його спорідненість до рецепторів 1-го типу в 20 тис. разів більша, ніж до рецепторів 2-го типу [6, 9]. Тобто препарат надійно блокує негативні ефекти ангіотензину ІІ, опосередковані рецепторами 1-го типу, і майже не впливає на ефекти, опосередковані рецепторами 2-го типу.
Проте сартани різняться не тільки за селективністю блокування рецепторів ангіотензину ІІ 1-го типу, але й за силою цього блокування. Валсартан, наприклад, викликає неконкурентний антагонізм на відміну від більшості БРА [6, 7, 9, 10]. Неконкурентний зв’язок є кращим, адже у цьому випадку рецептор залишається неактивним навіть при підвищенні концентрації ангіотензину ІІ у крові [6, 7].
Відмінності у фармакокінетиці сартанів пов’язані з особливостями молекули: два препарати (лозартан та кандесартан) є проліками, активність яких забезпечується метаболітами. Валсартан та інші препарати являють собою активні ліки, які не потребують попереднього присистемного метаболізму [11].
Важливе практичне значення серед параметрів фармакокінетики сартанів має виразність метаболізму в печінці та шляхи елімінації [12, 13]. Метаболізм препаратів та печінкова елімінація залежать від стану і наявності захворювань печінки у пацієнтів, що може впливати на появу медикаментозних взаємодій. Для сартанів характерні печінковий метаболізм (із різним ступенем виразності) та біліарний шлях елімінації. Переважна печінкова елімінація дає змогу застосовувати їх при порушенні функції нирок, що особливо важливо для хворих із уже наявною патологією нирок. При захворюваннях печінки, які супроводжуються зниженням активності печінкових ферментів та метаболізму, клінічно значущі зміни концентрації та кліренсу характерні для лозартану, що потребує зниження дози препарату вдвічі. Корекція дози валсартану при патології печінки не потрібна [11].
Найбільшу афінність до CYP2C9 серед сартанів має лозартан, меншою мірою – ірбесартан та кандесартан, практично не має – валсартан. При цьому CYP2C9 схильний до індукції або інгібування іншими лікарськими засобами та характеризується різноманітним генетичним поліморфізмом, який змінює активність ферменту. Роль генетичного поліморфізму CYP2C9 вивчали для лозартану. У носіїв «повільного» алелю (CYP2C9*3) визначені суттєві зміни фармакокінетики лозартану – уповільнення швидкості утворення і концентрації активного метаболіту EXP3174 [14]. Фармакологічні взаємодії при використанні валсартану не виникають [11].
Продемонстровано, що валсартан ефективно знижує АТ у пацієнтів з АГ різного ступеня тяжкості. Про це свідчать результати дослідження G. Calhoun et al., присвяченого оцінці залежності антигіпертензивної дії валсартану від початкового рівня АТ. Через чотири тижні від ініціювання терапії валсартаном або комбінацією валсартан + ГХТЗ у пацієнтів із початковим рівнем САТ 140‑149 мм рт. ст. його зниження становило 12,1 і 15,9 мм рт. ст., а при САТ 180‑189 мм рт. ст. – 31,5 і 38,9 мм рт. ст. відповідно [4].
Схожі дані були отримані співробітниками кафедри внутрішньої медицини 3 ДЗ «Дніпропетровська медична академія МОЗ України» при лікуванні хворих на АГ препаратом Тіара Дуо (комбінація валсартану та ГХТЗ) фармацевтичної фірми «Дарниця». На тлі застосування Тіари Дуо рівень САТ знижувався з 148 до 129 мм рт. ст., а діастолічного АТ – з 92 до 80 мм рт. ст., причому цільового рівня АТ через три місяці терапії досягли 85% хворих [1].
Висока антигіпертензивна ефективність валсартану в багатьох випадках визначає його сприятливу дію у лікуванні пацієнтів з АГ та різними супутніми станами, які підвищують СС-ризик. Перелік успішних масштабних рандомізованих клінічних досліджень із застосуванням валсартану в лікуванні пацієнтів з АГ та різноманітними СС-патологіями вражає. У дослідженнях Jikei Heart Study та VALUE продемонстровано здатність валсартану забезпечувати надійний і стабільний контроль АТ та покращувати прогноз у хворих на АГ групи високого СС-ризику [15]. У випробуванні MARVAL валсартан знижував частоту розвитку мікроальбумінурії у пацієнтів із ЦД 2-го типу, а в NAVIGATOR – ризик виникнення ЦД в осіб із порушеннями вуглеводного обміну [4, 16].
Застосування валсартану вивчали також у пацієнтів із фібриляцією передсердь (GISSI-AF), СН (Val-HeFT), поєднанням АГ та ЦД / порушенням толерантності до глюкози (NAGOYA HEART Study), а також у хворих, які перенесли інфаркт міокарда (ІМ) (VALLIANT) [4, 17, 18]. Валсартан офіційно рекомендований для терапії пацієнтів після ІМ та був першим серед БРА, зареєстрованим для лікування хронічної СН (ХСН) (Val-HeFT) [19, 20].
Крім кардіо- та нефропротекторних ефектів, валсартан чинить ще один, не менш важливий, – вплив на жорсткість судин. Відомо, що підвищена жорсткість артерій є важливим предиктором розвитку ускладнень АГ – гіпертрофії лівого шлуночка, ІМ, інсульту [21]. Аортальна жорсткість, яку оцінюють за швидкістю розповсюдженості пульсової хвилі упродовж аорти на ділянці від сонних до стегнових артерій, є незалежним предиктором розвитку СС-подій. Це продемонстровано у 12 дослідженнях (~13 тис. осіб), як у загальній популяції, так і в пацієнтів з АГ, ЦД, метаболічним синдромом, хворих похилого віку [22, 23]. У роботах A. Mahmud та I. Feely встановлено, що валсартан (як у моно- так і в комбінованій терапії) знижує швидкість розповсюдженості пульсової хвилі та індекс аугментації, який характеризує виразність відбитої хвилі та її внесок у збільшення пульсового АТ [4].
P. Boutouyrie et al. показали, що комбінація валсартану й амлодипіну ефективно знижувала не тільки периферичний, але й центральний САТ, рівень якого залежить від еластичних властивостей крупних артерій, а також структурно-функціонального стану артерій середнього калібру та мікроциркуляторного русла. Отже, рівень центрального АТ є показником, який опосередковано відображає стан всього СС-русла. Той факт, що валсартан може ефективно впливати на цей важливий показник, був продемонстрований у дослідженні VICTORY [24].
Обговорюючи питання щодо впливу АГТ на якість життя хворих, слід враховувати, що важливим фактором, який визначає якість життя чоловіків, є наявність еректильної дисфункції (ЕД). Про поширеність цієї патології дають змогу судити результати роботи H. Feldman et al., які обстежили 1290 пацієнтів чоловічої статі віком 40‑70 років. ЕД було діагностовано у 52% чоловіків (у 17% – мінімальну, у 25% – помірну, у 10% – виразну).
Поширеність ЕД серед чоловіків з АГ може коливатися від 19% (M. Martin-Morales et al.) до 74% (L. Shiri et al.). При цьому наявність ЕД асоційована з підвищенням рівня загальної (р=0,0001) та серцево-судинної (р=0,0006) смерті, а також частоти ІМ (р=0,046). Лікування АГ може посилювати ЕД, оскільки в осіб від 60 років зниження системного АТ сприяє зменшенню кровонаповнення статевого члена. Раніше на великій популяції пацієнтів (n=3502, середній вік – 55,8 років, ЕД у 75%) було показано, що валсартан здатний поліпшувати сексуальну функцію у чоловіків з АГ [4].
Повертаючись до алгоритмів застосування АГП, представлених в рекомендаціях ESH/ESC (2018), слід окремо відзначити, що за неефективності двокомпонентної ФК (варто переконатися, що її призначено в оптимальних дозуваннях обох компонентів) експерти вказують на необхідність переведення пацієнта на трикомпонентну схему. Було вперше наголошено, що за умови відсутності особливих клінічних ситуацій найбільш раціональним варіантом такої схеми є поєднання блокатора РААС з АК та діуретиком у вигляді ФК. Трикомпонентна терапія має також передбачати титрування доз усіх компонентів до максимальної, перш ніж переходити на наступну сходинку АГТ – чотирикомпонентну [2, 3].
У нашій країні однією з таких потрійних комбінацій є препарат Тіара Тріо® (валсартан + амлодипін + ГХТ) фармацевтичної фірми «Дарниця». У дослідженні Г.В. Дзяка та співавт. було показано високу антигіпертензивну ефективність Тіари Тріо у пацієнтів з АГ 2‑3-го ст. О.С. Сичов та О.О. Ханюков зі співавт. у своїй роботі продемонстрували додатковий антиаритмічний ефект цього препарату в лікуванні хворих на АГ із супутніми порушеннями ритму серця, які отримували специфічну антиаритмічну терапію. Слід також зазначити, що така ФК – єдина потрійна комбінація, зареєстрована на фармринку України, яку схвалено для застосування Управлінням із контролю за якістю харчових продуктів та медикаментів США (FDA) [1].
Необхідно зауважити, що, незважаючи на пріоритетність призначення комбінованої АГТ на початку лікування у більшості пацієнтів з АГ, в оновлених рекомендаціях є вказівка щодо доцільності застосування монотерапії в окремих категорій пацієнтів – це особи старечого віку (˃80 років) та/або хворі від 65 років із синдромом старечої астенії. Крім того, призначення одного АГП можливе для пацієнтів з АГ 1-го ст., якщо рівень САТ становить <150 мм рт. ст., а також осіб із високим нормальним АТ за умови дуже високого ризику розвитку СС-ускладнень [2, 3]. У цьому контексті доцільно наголосити, що в нашій країні фармацевтична фірма «Дарниця» нещодавно зареєструвала та випустила на фармацевтичний ринок моноформи валсартану, зокрема препарат Тіара Соло у двох варіантах дозування – 80 та 160 мг.
Обґрунтування призначення валсартану для лікування пацієнтів з АГ та супутньою патологією
- Найбільша доказова база щодо впливу на прогноз пацієнта із СС-патологією
- Найширші показання для застосування (АГ, ІМ, ХСН)
- Має фармакологічну активність (не потребує попереднього метаболізму в печінці)
- Ефективне зниження АТ протягом 24 год при одноразовому прийманні
- Антигіпертензивний ефект не залежить від часу застосування
- Метаболізм без участі цитохрому Р450, низький ризик медикаментозної взаємодії
Як вже було зазначено раніше, в європейських рекомендаціях із ведення хворих на АГ (2018) особливий акцент був зроблений на комплаєнсі пацієнтів. У документі підкреслюється, що низька прихильність хворого до АГТ на додаток до бездіяльності лікаря в ситуації, коли цільового рівня АТ не досягнуто, є найчастішою причиною відсутності належного контролю АТ. На жаль, нині експерти констатують, що як за даними досліджень зразків сечі на наявність метаболітів АГП, так і за результатами епідеміологічних робіт, що базувалися на аналізі повторної виписки рецептів пацієнтам з АГ, прихильність до АГТ залишається низькою – менш ніж 50%. Своєю чергою доведено, що погане дотримання режиму АГТ тісно корелює з підвищенням СС-ризику.
Є різні тактики для поліпшення комплаєнсу пацієнтів, одна з них – на рівні алгоритмів призначення АГП – стосується зменшення кількості застосовуваних таблеток. Так, за необхідності приймання однієї таблетки неприхильність до терапії спостерігається приблизно у 10% випадків, двох – 20%, трьох – до 40%, а часткова чи повна відсутність прихильності має місце в ситуації, коли пацієнт отримує п’ять таблеток і більше. Саме тому створення подвійних та потрійних ФК АГП (стратегія однієї таблетки) є ефективним методом підвищення комплаєнсу хворих при АГТ, сприяє досягненню цільових рівнів АТ та поліпшенню його контролю, а також дає змогу знизити ризик розвитку СС-ускладнень, зокрема ІМ, інсультів та показники смертності населення [3].
Отже, БРА можна широко застосовувати в лікуванні АГ як препарати першого вибору для лікування різних категорій пацієнтів з АГ та високим ризиком розвитку СС-ускладнень і супутньою патологією – ІМ в анамнезі, ЦД, метаболічним синдромом, нефропатією, ХСН. Валсартан – препарат, який має доведену доказову базу в терапії зазначених категорій хворих. Вибір лікаря на користь БРА на першому етапі лікування пацієнтів з АГ є кроком, спрямованим на формування високої прихильності до довготривалої терапії та зниження ризику відмови від лікування внаслідок низької ефективності або поганої переносимості.
Список літератури знаходиться в редакції