26 жовтня, 2022
Вибір антигіпертензивної стратегії: про що слід пам’ятати лікарю-практику
Динамічний розвиток медичної науки та результати нових досліджень у різних галузях медицини стають підґрунтям для швидких та ефективних змін щодо підходів до терапії різних патологій. Як відомо, одним із найпоширеніших захворювань у світі є саме артеріальна гіпертензія (АГ). Понад половина дорослого населення має підвищений АТ, при цьому частина з них, навіть не знають про своє захворювання, що лише збільшує тягар важких серцево-судинних (СС) ускладнень серед популяції в майбутньому.
Про зміни стратегій лікування АГ впродовж останніх десятиліть та сучасні міжнародні підходи у своїй доповіді під час конференції «Асоціації превентивної та антиейджинг медицини» розповіла докторка медичних наук, професорка Катерина Миколаївна Амосова.
Чи варто змінювати сталу практику?
Одне з перших досліджень щодо активної стратегії зниження систолічного артеріального тиску (САТ) нижче 135–140 мм рт. ст. під назвою «The ACCORD» (2010) було проведено серед пацієнтів із супутнім цукровим діабетом (ЦД) 2-го типу з високим ризиком СС подій. Науковці вивчали, чи терапія спрямована на досягнення в учасників норми рівня систолічного тиску (120 мм рт. ст.) зменшуватиме кількість серйозних СС подій. За висновками дослідників, інтенсивна антигіпертензивна терапія (АГТ) не мала суттєвих клінічних переваг щодо зниження первинних СС подій або рівня смертності з будь-якої причини, проте асоціювалася з більшою кількістю небажаних ускладнень. Інше рандомізоване дослідження переваг інтенсивного або стандартного контролю АТ The SPRINT (2015) у пацієнтів (n=9362) без ЦД в анамнезі засвідчило, що серед осіб старше 50 років з АГ зниження САТ до цільового значення <120 мм рт. ст. порівняно зі стандартним цільовим значенням <140 мм рт. ст. призводило до значно нижчих показників первинних СС подій і смертності з будь-якої причини. Ці результати стали підґрунтям для оновлення 2017 року спільних рекомендацій Американського коледжу кардіологів (АСС) з Американським товариством серця (AHA). Зокрема, новим критерієм діагнозу АГ було визначено САТ >130 мм рт. ст. і ДАТ >80 мм рт. ст. Упродовж наступних років усі міжнародні настанови змінювали свої рекомендації відповідно до оновлених даних досліджень:
Рекомендації АСС/АНА (2017) визначають цільовий рівень АТ для пацієнтів з АГ та СС ризиком <130/80 мм рт. ст.; для пацієнтів із неускладненою АГ та низьким СС ризиком <140/90 мм рт. ст.
За рекомендаціями Європейського товариства кардіологів (ESC) у настанові «Артеріальна гіпертензія» (2018) цільовий рівень АТ для загальної популяції має бути <130/80 мм рт. ст.; для осіб віком до 65 років <120‑129/80 мм рт. ст. і старше 65 років <130‑139/<90 мм рт. ст.
У настанові Міжнародного товариства гіпертензії (ISH, 2020) визначено першим кроком – рівень АТ протягом перших трьох місяців захворювання <140/90 мм рт. ст.; наступним кроком, після трьох місяців від початку захворювання, <130/80 мм рт. ст. Для осіб віком старше 65 років цільовим АТ зазначено <140/90 мм рт. ст.
Послідовні кроки у протоколі ESC-Профілактика (2021) рекомендують на першому етапі для всіх пацієнтів утримувати САТ <140 мм рт. ст.; при задовільній переносимості терапії надалі визначати цільовий рівень САТ <130 мм рт. ст. Для осіб віком старше 70 років САТ слід підтримувати на рівні <140 мм рт. ст.
Як розпочинати медикаментозне лікування пацієнтів з АГ?
Важливим інструментом у роботі лікаря та визначення тактики медикаментозної терапії є шкали SCORE та ASCVD для оцінювання ризику виникнення несприятливих СС подій. Додаткові інструменти визначення СС ризиків допомагають лікарю сформулювати оптимальну мету зниження АТ та швидкість її досягнення. Рекомендації щодо початку терапії, зазначені у сучасних настановах, включають: АСС/АНА (2017) – розпочинати лікування одразу після встановлення діагнозу АГ І ступеня у пацієнтів із високим СС ризиком або через 6 міс. після корекції способу життя у пацієнтів із низьким ризиком; ESC-АГ (2018) – необхідність початку терапії у пацієнтів із високим нормальним АТ (130‑139/85‑89 мм рт. ст.) та дуже високим ризиком несприятливих СС подій; ISH (2020) – терапію розпочинати одразу при АГ І ступеня у пацієнтів із супутніми СС захворюваннями та через 6 міс. від початку захворювання в осіб без ускладнень. Остання міжнародна настанова ESC-Профілактика (2021) рекомендує розпочинати терапію одразу з поєднання двох препаратів. Для вищої комплаєнтності пацієнта важливо, щоб така комбінація була в одному лікарському засобі, дозування препаратів — залежно від ступеня АГ. Основою цієї комбінації має бути інгібітор ангіотензинперетворювального ферменту (іАПФ) або блокатор рецепторів ангіотензину ІІ (БРА) у поєднанні з блокатором кальцієвих каналів (БКК) або тіазидним діуретиком (ТД).
Як зробити оптимальний вибір серед блокаторів ренін-ангіотензинової системи?
Останнім часом серед науковців точилися активні дискусії щодо визначення переваг іАПФ або БРА. У декількох метааналізах із порівнянням окремо іАПФ з плацебо (контрольна група) частота виникнення інфаркту міокарда (ІМ) була нижчою у групах іАПФ. Водночас в інших метааналізах із порівнянням БРА з плацебо частота ІМ у групі БРА була вищою, що може ускладнити вибір лікаря. Однак чітку відповідь можуть дати лише прямі порівняння іАПФ та сартанів у дослідженнях.
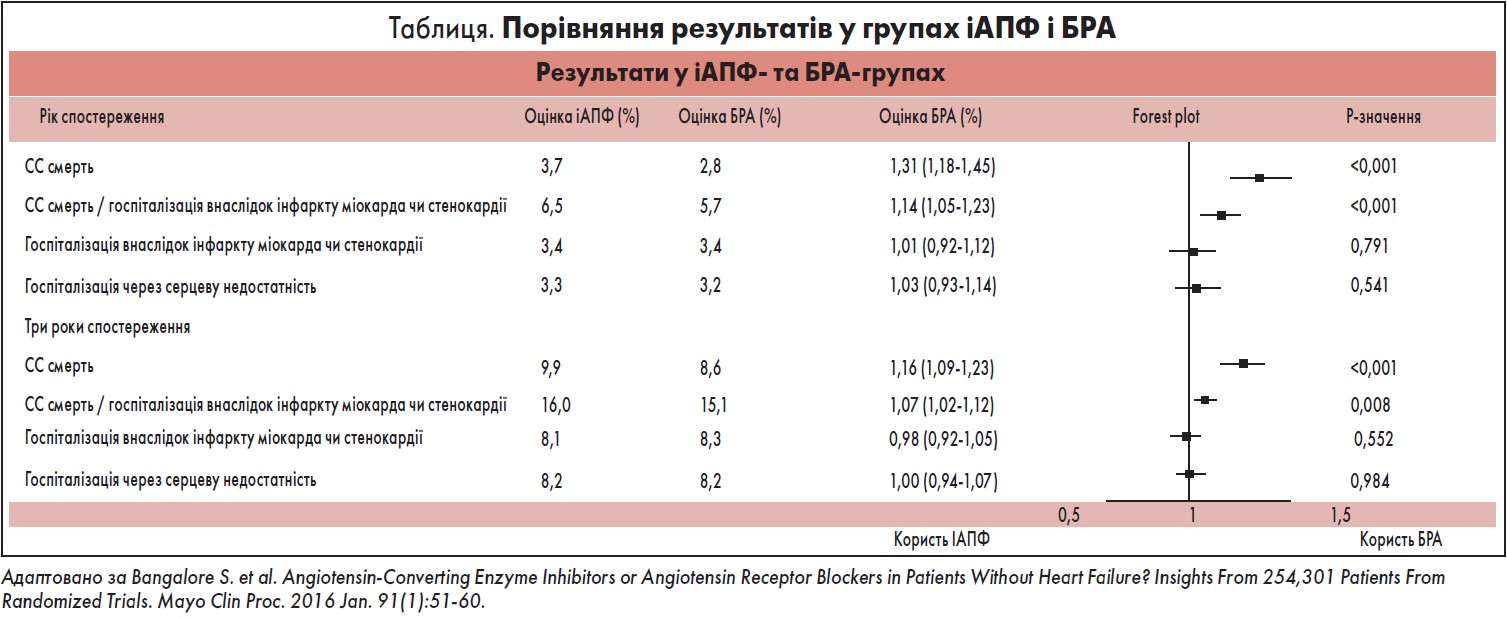
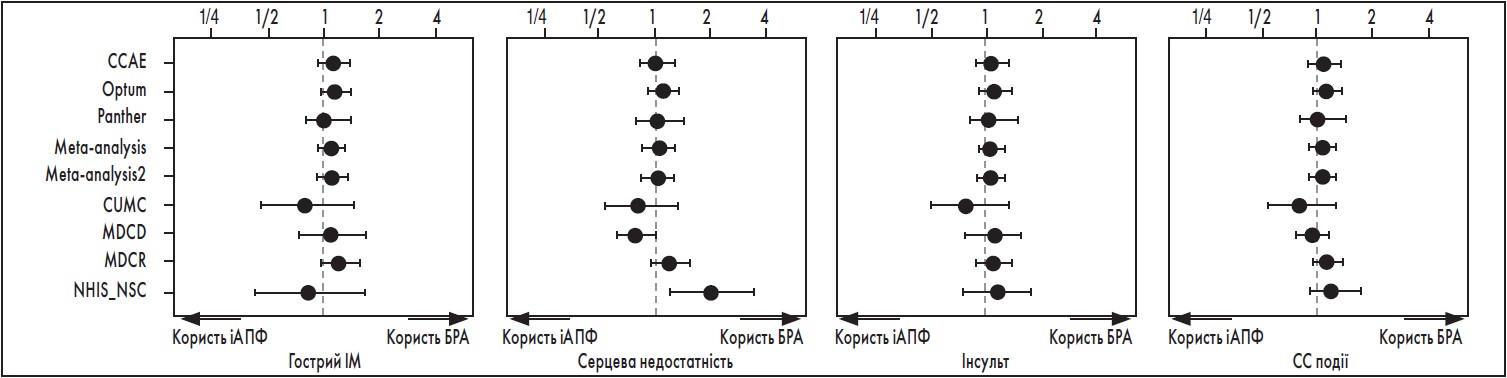
Метааналіз рандомізованих досліджень із прямим порівнянням ефективності іАПФ та БРА не виявив жодної різниці в результатах, зокрема щодо інфаркту міокарда, за винятком меншого на 29% ризику відміни препарату через відсутність побічних реакцій БРА (Bangalore et al., 2016). У великому обсерваційному дослідженні Ко et al. (2019) із прямим порівнянням результатів лікування пацієнтів з АГ іАПФ і сартанами після перенесеного ІМ (n=59 353) виявили, що терапія БРА мала нижчі показники несприятливих СС наслідків серед літніх з ІМ порівняно з іАПФ, а саме смерть від СС ускладнень/госпіталізація через ІМ або нестабільну стенокардію на 14% нижче, а ризик CC смертності на 31 % нижче, ніж іАПФ (табл.). При аналізі використовували найсучасніший статистичний метод обробки даних для унеможливлення упередженості потрапляння пацієнтів до тієї чи іншої групи і врахування всіх інших чинників із можливим впливом на результати. В обсерваційному дослідженні з прямим порівнянням ефективності і переносимості іАПФ і БРА у пацієнтів з АГ не виявлено статистично значущої різниці щодо ефективності зазначених препаратів при ІМ, СН, інсульті або важких СС подіях (рис.) (Сhen et al., 2021). Статистична обробка результатів дослідження унеможливлювала ефект упередженості, який міг би бути пов‘язаний із відсутністю рандомізаціі. Водночас БРА мали кращий профіль безпеки з меншим ризиком розвитку гострого панкреатиту, ангіоневротичного набряку, кашлю та шлунково-кишкової кровотечі.
Рисунок. Ефективність ІАПФ і БРА у пацієнтів з АГ
Адаптовано за Сhen R. et al. Comparative First-Line Effectiveness and Safety of ACE (Angiotensin-Converting Enzyme) Inhibitors and Angiotensin Receptor Blockers: A Multinational Cohort Study. Hypertension. 2021; 78: 591-603.
Які рекомендації щодо лікування АГ у пацієнтів із коморбідними захворюваннями?
Відповідно до рекомендацій міжнародних настанов при метаболічному синдромі та ЦД 2-го типу в терапії АГ слід застосовувати схему блокатор ренін-ангіотензивної системи (РАС) із ТД і БКК. За наявності стабільної ІХС або хронічного коронарного синдрому призначають блокатор РАС в комбінації з бета-блокатором, а за пароксизмальноі і персистуючоі ФП в останніх рекомендаціях американського коледжу і асоціації кардіологів (2017) передбачено використовувати для лікування АГ у цих пацієнтів конкретно БРА (клас ІІа, рівень доказовості В). При хронічній серцевій недостатності зі збереженою фракцією викиду (ФВ) показано лікування ТД, але в осіб зі зниженою ФВ – бета-блокаторами. У пацієнтів із хронічною хворобою нирок в анамнезі для терапії АГ використовують блокатор РАС.
Як обрати ефективний і безпечний БРА?
Нині велика кількість рандомізованих клінічних досліджень підтверджує ефективність валсартану. Оскільки більшість пацієнтів з АГ має коморбідні стани, серед яких частим є ожиріння, актуальним стало дослідження NAVIGATOR (2010), у якому вивчали вплив препаратів БРА (зокрема, валсартану) на зниження ризику розвитку ЦД і СС подій у пацієнтів із порушенням толерантності до глюкози. За даними дослідження, разом зі зміною способу життя одноразова добова доза валсартану на 14% знижувала ризик діабету, але не серцево-судинних подій у пацієнтів із порушенням толерантності до глюкози та встановленими серцево-судинними захворюваннями або чинниками ризику.
Інші великі дослідження, як-от Val-HeFT (2001) та VALIANT (2003), довели переваги застосування валсартану в пацієнтів із СН і супутнім ІМ або станом після перенесеного останнього. Комбінація валсартану з амлодипіном продемонструвала високу ефективність щодо зниження АТ, що підтверджують результати дослідження The EXCITE (2014).
Для лікарів-практиків також корисно знати, що застосування фіксованої комбінації валсартану з амлодипіном допомагає забезпечити антигіпертензивний ефект упродовж 24 годин до отримання пацієнтом наступної дози препарату (Qi-Fang Huang et al., 2019).
Що робити, коли не вистачає антигіпертензивної терапії для корекції АТ?
Особливу увагу слід приділяти пацієнтам, у яких не відбулося відчутного зниження АТ після призначеної адекватної терапії. У такому разі лікарю насамперед треба заспокоїти пацієнта та з’ясувати: прихильність пацієнта до лікування; режим контролю АТ вдома; правильність використання медичного приладдя для вимірювання тиску; зміни у режимі життя та харчування (зокрема, збільшення вживання солі, алкоголю, тютюнопаління тощо) протягом останнього часу.
Перш ніж визначитися з подальшою стратегією терапії пацієнта, слід призначити добовий моніторинг АТ (ДМАТ). За результатами обговорення та обстеження обрати тактику підвищення дози фіксованої комбінації, яку попередньо отримував пацієнт, або призначити додатково третій препарат з основних класів АГП. У разі, якщо для корекції АТ не достатньо потрійної комбінації, слід обов’язково повторити ДМАТ та виключити причини вторинної АГ перед призначенням додаткового четвертого антигіпертензивного засобу.
Довідка «ЗУ»
Сьогодні на фармацевтичному ринку України препаратом фіксованої комбінації валсартану з амлодипіном, що повністю відповідає стандартам лікування більшості категорій пацієнтів з АГ, є Діфорс від Европейської компанії АСІNО. Препарат забезпечує у пацієнтів з АГ ефективне зниження АТ, при цьому не чинить вплив на частоту пульсу. У більшості пацієнтів після застосування внутрішньо разової дози препарату (1 таблетка препарату Діфорс 80 або Діфорс 160, або Діфорс XL) початок антигіпертензивної активності спостерігається приблизно через 2 год, а максимальне зниження АТ досягається через 4‑6 год. Антигіпертензивний ефект зберігається понад 24 год після приймання разової дози. За умови регулярного застосування препарату максимальний терапевтичний ефект триває протягом 2–4 тижнів і тримається на досягнутому рівні при тривалому застосуванні Діофорсу.
Підготувала Ольга Загора
UA-DIFO-PUB-102022-012