6 квітня, 2023
Ведення пацієнтів з артеріальною гіпертензією та супутніми станами: фокус на покроковій фармакотерапії
Сьогодні артеріальна гіпертензія (АГ) залишається важливою медико-соціальною проблемою в усьому світі. Ця патологія спричиняє розвиток суттєвих ускладнень і зростання смертності серед хворих. Крім того, лікарі часто стикаються з наявністю у цій популяції супутніх захворювань на тлі АГ, що значно ускладнює ведення таких пацієнтів. Тому раннє виявлення АГ і призначення оптимального лікування є вкрай необхідними для зменшення глобального тягаря підвищеного рівня артеріального тиску (АТ).
Діагностика артеріальної гіпертензії
Офісне вимірювання АТ є основою для діагностики АГ і подальшого спостереження. Відповідно до рекомендацій щодо лікування АГ Міжнародного товариства з артеріальної гіпертензії (ISH, 2020), діагноз АГ встановлюється за стійкого підвищення систолічного АТ (САТ) ≥140 мм рт. ст. і/або діастолічного АТ (ДАТ) ≥90 мм рт. ст. Щоб підтвердити діагноз АГ слід вимірювати АТ під час 2‑3 візитів до лікаря з інтервалом 1‑4 тижні. АГ діагностують, якщо під час 1-го візиту показник АТ становить ≥180/110 мм рт. ст. і наявне серцево-судинне захворювання (ССЗ) (Stergiou et al., 2018; Muntner et al., 2019). За можливості діагноз АГ слід підтвердити за допомогою домашнього вимірювання АТ. Особи з підтвердженою АГ (1 і 2-го ст.) мають отримувати відповідне фармакологічне лікування (Kario et al., 2019).
Поширеною формою есенціальної АГ є ізольована систолічна АГ, яка визначається за підвищеного САТ (≥140 мм рт. ст.) та низького ДАТ (<90 мм рт. ст.). За наявності в пацієнта АГ синдрому «білого халата» та низького СС-ризику, а також за відсутності ураження органів-мішеней (УОМ), зумовленого АГ, медикаментозне лікування можна не призначати. Однак хворим слід модифікувати спосіб життя, щоб уникнути розвитку стійкої АГ, яка потребуватиме антигіпертензивної терапії. Пацієнтам із маскованою АГ і ризиком розвитку СС-подій може знадобитися призначення терапії, спрямованої на нормалізацію АТ (Asayama et al., 2014).
Часто в осіб з АГ хвороба має безсимптомний характер, проте специфічні ознаки можуть свідчити про вторинну АГ або наявність ускладнень, які потребують проведення подальших обстежень. Вивчення медичного і сімейного анамнезу має охоплювати: показники АТ; чинники ризику; загальний СС-ризик; симптоми / ознаки АГ та супутніх станів; симптоми, які можуть свідчити про розвиток вторинної АГ (Williams et al., 2018). Відповідно до настанови ISH (2020), фізикальний огляд, зокрема СС-системи та інших органів / систем, дає змогу підтвердити діагноз АГ і виявити УОМ та/або вторинну АГ. До того ж важливими є лабораторні обстеження: аналіз крові, зокрема визначення рівня натрію, калію, сироваткового креатиніну з розрахунковою швидкістю клубочкової фільтрації (рШКФ), ліпідного профілю і рівня глюкози натще, а також аналіз сечі. Крім того, у таких пацієнтів слід виконати електрокардіографію (ЕКГ) у 12 відведеннях. Додаткові обстеження необхідні, якщо потрібно підтвердити УОМ, наявність супутніх патологій і/або вторинну АГ.
Чинники СС-ризику в пацієнтів з артеріальною гіпертензією
Понад половина пацієнтів з АГ мають додаткові чинники СС-ризику (Lopez et al., 2006). Серед найпоширеніших загальних чинників ризику – цукровий діабет (ЦД), дисліпідемія, надлишкова вага, гіперурикемія, метаболічний синдром, а також нездоровий спосіб життя. Наявність більш ніж одного додаткового чинника СС-ризику в осіб з АГ підвищує ймовірність розвитку коронарних, цереброваскулярних захворювань і патології нирок (Williams et al., 2018).
В усіх пацієнтів з АГ СС-ризик слід оцінювати на підставі рівня АТ і наявності додаткових чинників ризику. Оцінювання останніх має бути частиною діагностики, особливо за сімейного анамнезу ССЗ. Аналіз СС-ризику в щоденній клінічній практиці охоплює такі характеристики:
- Інші чинники ризику: вік (>65 років), стать (більше чоловіки, ніж жінки), частота серцевих скорочень (>80 уд./хв), підвищена вага, ЦД, високий рівень холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) / тригліцеридів, ССЗ та АГ у сімейному анамнезі, рання менопауза,куріння, психосоціальні та соціоекономічні особливості.
- УОМ: гіпертрофія лівого шлуночка, хронічна хвороба нирок (ХХН) помірного / тяжкого ступеня (рШКФ <60 мл/хв/1,73 м2).
- Інші захворювання: ішемічна хвороба серця (ІХС), серцева недостатність (СН), захворювання периферичних артерій, фібриляція передсердь, ХХН ≥3-ї стадії.
Терапевтичні підходи мають полягати в модифікації способу життя хворого, зниженні АТ до цільового рівня й ефективному лікуванні інших чинників ризику для зниження резидуального СС-ризику (ISH, 2020). Комбіноване лікування АГ і додаткових чинників СС-ризику дає змогу ефективніше знизити частоту ССЗ, ніж лише контроль АТ.
Аспекти лікування артеріальної гіпертензії
Завдяки модифікації способу життя хворих можливо запобігти підвищенню АТ або відстрочити початок АГ та знизити СС-ризики. Такі зміни способу життя, що є частиною антигіпертензивної терапії першої лінії, здатні посилити її ефект (Piepoli et al., 2016).
Ключова мета терапії пацієнтів з АГ передбачає досягнення контролю АТ упродовж трьох місяців. В осіб віком <65 років цільовий рівень АТ має становити <130/80 мм рт. ст. (але >120/70 мм рт. ст.) за переносимості препаратів, а ≥65 років – <140/90 мм рт. ст. Однак показники можуть варіювати залежно від індивідуальних характеристик хворого й дотримання ним режиму лікування (Wei et al., 2018; Abegaz et al., 2017). Для лікування пацієнтів з АГ слід використовувати доступні медикаменти з максимальною кількістю сприятливих характеристик (NICE, 2019; Williams et al., 2018). Перевагу віддавати комбінованій терапії препаратами в одній таблетці. Покрокова медикаментозна терапія має такі етапи:
- Перший крок: подвійна комбінація препаратів у низьких дозах, як-от інгібітори ангіотензинперетворювального ферменту (іАПФ) або блокатори рецепторів ангіотензину (БРА) + дигідропіридинові блокатори кальцієвих каналів (ДП-БКК). У хворих на АГ І ст. групи низького ризику, осіб старечого віку (≥80 років) чи ослаблених пацієнтів слід розглянути призначення монотерапії. В осіб після інсульту, похилого віку, на початковій стадії СН або в разі непереносимості БКК доцільним може бути застосування іАПФ або БРА + тіазидоподібних діуретиків (ТПД). У пацієнтів афроамериканського походження розглянути призначення іАПФ або БРА + ДП-БКК чи ДП-БКК + ТПД.
- Другий крок: подвійна комбінація лікарських засобів, як-от іАПФ або БРА + ДП-БКК, у повному дозуванні. Також може бути доцільним використання монотерапії в осіб з АГ І ст. і низьким ризиком, хворих віком <80 років або зі старечою астенією.
- Третій крок: потрійна комбінація іАПФ або БРА + ДП-БКК + ТПД.
- Четвертий крок: за резистентної АГ потрійна комбінація іАПФ або БРА + ДП-БКК + ТПД і додатково спіронолактон чи інший засіб.
Якщо ТПД недоступні, слід призначати тіазидні діуретики. Також рекомендовані альтернативні стратегії, якщо ДП-БКК недоступні або не переносяться. За наявності специфічних показань, як-от СН, стенокардія, стан після інфаркту міокарда (ІМ) або в молодих жінок, що вагітні чи планують вагітніти, на будь-якому лікувальному етапі розглянути доцільність застосування β-блокаторів (Williams et al., 2015; Ojji et al., 2019).
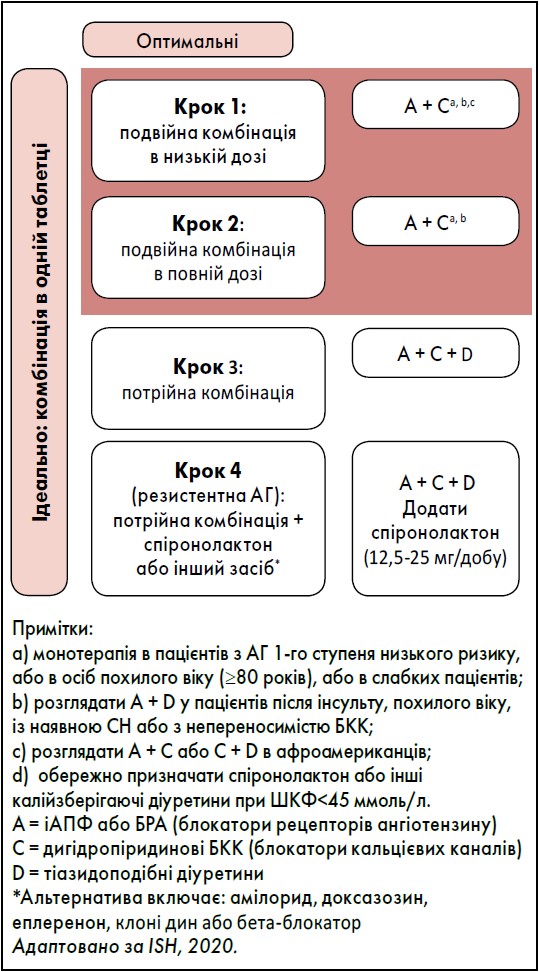
Неналежний комплаєнс серед пацієнтів, які отримують антигіпертензивну терапію, призводить до підвищення АТ і пов’язаний із поганим прогнозом. Для підвищення прихильності до терапії слід розглянути використання фіксованих комбінацій препаратів в одній таблетці, прийом ліків раз на добу, домашній моніторинг АТ, мультидисциплінарний підхід для поліпшення контролю дотримання лікувального режиму (Verma et al., 2018; Ruppar et al., 2017). Основні стратегії фармакологічного лікування хворих на АГ представлено на рисунку.
Рисунок. Основні стратегії фармакологічного лікування АГ
Супутні патології та ускладнення артеріальної гіпертензії
У пацієнтів, які страждають на АГ, можуть бути коморбідні захворювання, які чинять вплив на СС-ризики і стратегії лікування. Кількість супутніх патологій із віком зростає. Поширеними коморбідностями є ІХС, інсульт, ХХН, СН, хронічне обструктивне захворювання легень. Ревматичні та психічні патології виникають рідше, але їх значущість суттєво недооцінена. Адже пацієнти часто лікують такі стани самостійно, що теж може перешкоджати контролю АТ.
Ішемічна хвороба серця
Існує потужний взаємозв’язок між ІХС й АГ, на частку якої припадає 25‑30% випадків гострого ІМ (Yusuf et al., 2009). Для контролю цих коморбідностей пацієнтам настійно рекомендовано модифікацію способу життя і зниження АТ до цільового показника <130/80 мм рт. ст. (<140/80 мм рт. ст. в осіб похилого віку). Незалежно від рівня АТ блокатори ренін-ангіотензин-альдостеронової системи (РААС) і β-блокатори з/без БКК є препаратами першої лінії в осіб з АГ. Гіполіпідемічну терапію застосовують для досягнення ХС ЛПНЩ <55 мг/дл (1,4 ммоль/л) (Mach et al., 2020). Також доцільним є регулярне антитромбоцитарне лікування ацетилсаліциловою кислотою (Williams et al., 2018).
Інсульт
Одним із важливих чинників ризику розвитку ішемічного або геморагічного інсульту є АГ (O’Donnell et al., 2010). Знижувати АТ слід, якщо показник становить ≥140/90 мм рт. ст., зокрема, до цільового значення <130/80 мм рт. ст. (<140/80 у літніх осіб). Препаратами першої лінії лікування є блокатори РААС, БКК і діуретики. Для досягнення цільового рівня ХС ЛПНЩ <70 мг/дл (1,8 ммоль/л) в осіб з ішемічним інсультом обов’язкове застосування ліпідознижувальних засобів. Крім того, за ішемічного інсульту рекомендовано антитромбоцитарну терапію. Після перенесеного геморагічного інсульту можна розглянути використання антиагрегантів, однак лише за наявності переконливих показань (Williams et al., 2018).
Серцева недостатність
АГ є чинником ризику розвитку СН зі зниженою чи збереженою фракцією викиду (ФВ). У пацієнтів, які страждають на коморбідні АГ і СН, клінічні наслідки є гіршими, а смертність – вищою (Whelton et al., 2017). Крім модифікації способу життя, необхідним є лікування АГ, що забезпечує зниження ризику СН і пов’язані з нею госпіталізації. Важливо досягти у цих хворих цільового показника АТ <130/80 мм рт. ст. (але >120/70 мм рт. ст.). У пацієнтів, у яких встановлено СН зі зниженою ФВ, ефективними були блокатори РААС, β-блокатори й антагоністи мінералокортикоїдних рецепторів. Докази щодо діуретиків обмежуються симптоматичним поліпшенням (Williams et al., 2018). БКК призначають за поганого контролю АТ. Застосування інгібітора рецептора ангіотензину / неприлізину рекомендовано як альтернативу іАПФ чи БРА для лікування СН зі зниженою ФВ на тлі АГ. Така тактика можлива і для осіб, які мають СН зі збереженою ФВ (Bohm et al., 2017).
Хронічна хвороба нирок
АГ – основний чинник ризику розвитку і прогресування альбумінурії та будь-якої форми ХХН. Зниження рШКФ асоційоване з резистентною, маскованою АГ і підвищенням рівня АТ у нічний час (Drawz et al., 2016). Цільовим показником АТ є <130/80 мм рт. ст. (<140/80 мм рт. ст. у літніх осіб). Блокатори РААС – препарати першої лінії, оскільки здатні зменшувати альбумінурію додатково до контролю АТ. Можливе додавання БКК і діуретиків (петльові, якщо рШКФ <30 мл/хв/1,73 м2). Під час лікування важливо контролювати рШКФ, мікроальбумінурію і рівень електролітів у крові (Williams et al., 2018).
Хронічне обструктивне захворювання легень
У пацієнтів із хронічним обструктивним захворюванням легень АГ є найчастішим коморбідним станом. На додаток до модифікації способу життя призначення медикаментозного лікування є важливим для досягнення цільового рівня АТ <130/80 мм рт. ст. (<140/80 мм рт. ст. в осіб похилого віку) (Drawz et al., 2016). Терапевтична стратегія передбачає застосування блокатора AT1-рецепторів ангіотензину і БКК і/або діуретика. Хворим, які мають ІХС чи СН, можна призначити β1-селективні блокатори. Слід контролювати додаткові чинники ризику розвитку СС-подій відповідно до профілю ризику пацієнта.
Цукровий діабет
У пацієнтів із коморбідними АГ і ЦД основною метою лікування має бути досягнення зниження АТ до цільового <130/80 мм рт. ст. (<140/80 мм рт. ст. у літніх осіб) (ADA, 2017). Така терапія передбачає застосування блокаторів РААС і БКК і/або ТПД. Статини слід використовувати в межах первинної профілактики за наявності ЦД з УОМ, якщо ХС ЛПНЩ >70 мг/дл (1,8 ммоль/л), або за неускладненого ЦД, якщо ХС ЛПНЩ >100 мг/дл (2,6 ммоль/л). Крім того, важливо ретельно контролювати рівень глюкози і ліпідів у крові (ISH, 2020).
Порушення обміну ліпідів і метаболічний синдром
Стратегія зниження АТ, як у загальній популяції, передбачає використання блокаторів РААС (БРА, іАПФ) і БКК (Sever et al., 2003). Статини є ліпідознижувальними препаратами вибору з/без застосування езетимібу та/або інгібітора PCSK9 (за оптимальних умов) (Nordestgaard, 2016). Якщо рівень тригліцеридів у сироватці крові >200 мг/дл (2,3 ммоль/л), його необхідно знизити, особливо за коморбідності АГ і ЦД. Призначення фенофібрату в осіб із низьким рівнем ЛПВЩ / високим показником тригліцеридів може мати додаткові переваги. Особи, які страждають на супутні АГ і метаболічний синдром, належать до групи високого ризику. В основі лікування – модифікація способу життя, а також контроль АТ і додаткових чинників ризику на підставі СС-ризику (ISH, 2020).
Інші коморбідні стани
Запальні ревматичні захворювання зазвичай асоційовані зі зростанням поширеності АГ, що погано контролюється. Вони можуть призводити до підвищення ймовірності розвитку СС-ускладнень, що лише частково корелюють із чинниками СС-ризику. Лікувальна тактика щодо зниження АТ є такою самою, як у загальній популяції, переважно із застосуванням блокаторів РААС і БКК. Така терапія має бути спрямована на зменшення запалення, спричиненого коморбідними ревматичними патологіями, уникаючи високих доз нестероїдних протизапальних засобів. Гіполіпідемічне лікування призначають відповідно до профілю СС-ризику, зважаючи на ефекти біологічних засобів (Ikdahl et al., 2019). Частота АГ підвищується серед осіб із психічними розладами (Patten et al., 2009). Зокрема, зростає СС-ризик на тлі психосоціального стресу й основних психічних захворювань (ISH, 2020). Депресія асоціюється зі збільшенням СС-захворюваності та смертності, що свідчить про важливість контролю АТ. Для зниження АТ рекомендовані блокатори РААС і діуретики, які рідше фармакологічно взаємодіють з антидепресантами.
БКК й α-блокатори в пацієнтів з ортостатичною гіпотензією слід призначати обережно. Важливо брати до уваги ризик взаємодій ліків, порушення на ЕКГ і зміни постурального АТ (Siwek et al., 2020).
Специфічні стани
Резистентна АГ. Про резистентну АГ свідчить офісний АТ >140/90 мм рт. ст. у положенні сидячи в пацієнта, який отримував три або більше антигіпертензивні препарати в оптимальних (або максимально переносимих) дозах, зокрема діуретики. Необхідно виключити псевдорезистентність, що може асоціюватися з неправильним вимірюванням АТ, ефектом «білого халату», низьким комплаєнсом чи некоректним вибором антигіпертензивної терапії. Зокрема, слід виключити АГ, спричинену ліками / психоактивними речовинами, а також вторинну АГ (Wei et al., 2018).
Резистентна АГ підвищує ризик розвитку ІХС, хронічної СН, інсульту, термінальної ниркової недостатності та смертності від будь-яких причин. Важливо оптимізувати поточну схему лікування з модифікацією способу життя і діуретичною терапією (Rossignol et al., 2015).
Вторинна АГ. Специфічне захворювання чи стан можуть стати причиною розвитку вторинної (симптоматичної) АГ. Найпоширенішими типами вторинної АГ у дорослих є ниркова паренхіматозна, реноваскулярна АГ, первинний альдостеронізм, хронічне апное уві сні, а також АГ, індукована ліками / психоактивними речовинами (Gornik et al., 2019). Рання діагностика й початок відповідної терапії дають змогу вилікувати АГ, поліпшити контроль АТ чи зменшити кількість призначуваних антигіпертензивних засобів.
Гіпертонічний криз. Суттєве підвищення рівня АТ, що супроводжується гострим УОМ, визначається як гіпертонічний криз. Такий стан потребує швидкого діагностичного обстеження та негайного зниження АТ, щоб уникнути прогресування органної недостатності. Зазвичай необхідна внутрішньовенна терапія. Важливо контролювати зниження АТ до безпечніших рівнів для запобігання чи обмеження подальшого гіпертонічного ураження, уникаючи розвитку гіпотензії та супутніх ускладнень (Gonzalez et al., 2010). Особи, які перенесли гіпертонічний криз, мають підвищений ризик розвитку кардіоваскулярної та ниркової патології, тому обов’язковими є ретельне обстеження щодо можливих причин і оцінювання УОМ, опосередкованого АГ, щоб запобігти повторному гіпертонічного кризу. Корекція антигіпертензивної терапії в поєднанні з модифікацією способу життя покращує комплаєнс пацієнтів і довготривалий контроль АТ (Amraoui et al., 2014).
Довідка «ЗУ»
У лікуванні АГ серед групи препаратів іАПФ значні переваги продемонстрував раміприл (Хартил®). У пацієнтів з АГ додавання його до стандартної терапії є ефективним для профілактики ССЗ атеротромботичного ґенезу (ІХС чи інсульт в анамнезі, патології периферичних судин) або ЦД із щонайменше одним додатковим чинником СС-ризику. Препарат значно знижує рівень захворюваності та частоту летальних випадків від СС-причин.
Крім того, для лікування пацієнтів з АГ підтверджено належний ефект поєднання препаратів іАПФ раміприлу і БКК амлодипіну в одній таблетці (Хартил®-АМ). Раміприл ефективно знижує АТ без компенсаторного підвищення ЧСС. Своєю чергою, разова доза амлодипіну забезпечує клінічно значуще зниження АТ впродовж 24 год. Завдяки повільному початку дії амлодипін не спричиняє гострої артеріальної гіпотензії. Виразний антигіпертензивний і діуретичний ефекти продемонструвала комбінація іАПФ раміприлу й тіазидного діуретика гідрохлоротіазиду в одній таблетці (Хартил®-Н). Підтверджено, що одночасне застосування цих діючих речовин сприяє значному зниженню АТ, ніж кожної окремо. До того ж препарат має синергічний ефект, а також зменшує ризик виникнення гіпокаліємії.
Підготувала Олена Коробка