8 квітня, 2026
Настанова щодо профілактики, виявлення, оцінки та лікування дорослих пацієнтів із високим артеріальним тиском
Артеріальна гіпертензія (АГ) є найпоширенішим модифікованим фактором ризику серцево-судинних захворювань (ССЗ) і основною причиною інвалідності та смерті в усьому світі, причому її тягар упродовж останніх кількох десятиліть зростає. В осіб середнього віку ризик розвитку АГ протягом життя становить 80‑90%, зокрема в чоловіків вона виникає раніше, ніж у жінок. Поточні показники обізнаності щодо АГ й терапії в усіх категоріях пацієнтів залишаються вельми низькими. Загальна мета антигіпертензивного лікування полягає у досягненні АТ <130/80 мм рт. ст. для всіх дорослих, з урахуванням додаткових факторів в окремих групах хворих (потребують стаціонарного догляду, мають обмежену прогнозовану тривалість життя, вагітних тощо). Мультидисциплінарний підхід до менеджменту таких пацієнтів є важливим для зменшення перешкод у досягненні контролю АТ. У 2025 р. Американська колегія кардіологів (АСС) та Американська асоціація серця (АНА) розробили оновлену клінічну практичну настанову щодо профілактики, виявлення, оцінки та лікування високого АТ у дорослих. Метою науковців було створення документа на основі сучасних даних стосовно високого АТ, що покликаний допомогти клініцистам у веденні хворих на артеріальну гіпертензію (АГ). Пропонуємо вам ознайомитися із ключовими положеннями цієї настанови.
АГ часто поєднується з іншими факторами ризику ССЗ, серед яких куріння, надмірна вага або ожиріння, цукровий діабет (ЦД) і хронічна хвороба нирок (ХХН), що асоційовано із додатковою ймовірністю розвитку ССЗ (Jaeger et al., 2023; Khan et al., 2023). Підвищення АТ пов’язане з виникненням фатальних та нефатальних серцево-судинних (СС) подій, при цьому ризик подвоюється на кожні 20 мм рт. ст. зростання рівня систолічного АТ (САТ) та 10 мм рт. ст. діастолічного АТ (ДАТ). Вищий АТ корелює із підвищеним ризиком розвитку ішемічної хвороби серця (ІХС), серцевої недостатності (СН), захворювань аорти й периферичних судин, патологій нирок, ішемічного та геморагічного інсульту, деменції та когнітивних порушень (Whelton et al., 2020; Weldegiorgis et al., 2020).
У дорослих пацієнтів для профілактики та лікування високого АТ його слід класифікувати як нормальний (систолічний АТ [САТ] <120 мм рт. ст. та діастолічний АТ [ДАТ] <80 мм рт. ст.), підвищений (120‑129 та <80 мм рт. ст. відповідно), АГ 1-ї стадії (130‑139 та 80‑89 мм рт. ст. відповідно) чи 2-ї стадії (≥140 мм рт. ст. та ≥90 мм рт. ст. відповідно) (1, B-NR) (Rapsomaniki et al., 2014).
Класи рекомендацій та рівні доказовості при оцінюванні стратегій діагностики й терапії у пацієнтів із високим АТ
Клас (сила) рекомендації
- клас 1 (сильна): переваги >>> ризики
- клас 2а (помірна): переваги >> ризики
- клас 2b (слабка): переваги ≥ ризики
- клас 3: користь відсутня (помірна):
переваги = ризики - клас 3: заподіює шкоду (сильна):
ризики > переваги
Рівень (якість) доказів
Рівень А
- докази високої якості з більш ніж 1 РКД
- метааналізи даних високоякісних РКД
- ≥1 РКД, підкріплені даними якісних реєстрових досліджень
Рівень B-R (рандомізовані)
- докази помірної якості з ≥1 РКД
- метааналізи даних РКД помірної якості
Рівень B-NR (нерандомізовані)
- докази помірної якості з ≥1 добре спланованих, якісно виконаних нерандомізованих обсерваційних або реєстрових досліджень
- метааналіз даних таких досліджень
Рівень C‑LD (обмежені дані)
- результати рандомізованих або нерандомізованих обсерваційних/реєстрових досліджень з обмеженнями у дизайні
чи при проведенні - метааналіз даних таких досліджень
- дані фізіологічних або механістичних досліджень за участю людей
Рівень C-EO (експертна думка)
- консенсусні експертні висновки на основі клінічного досвіду
Примітки: РКД – рандомізовані контрольовані дослідження.
Адаптовано за АНА/АСС (2025)
Обстеження пацієнтів
Точне визначення АТ є важливим для діагностики АГ, оцінки пов’язаного із ним СС-ризику та відповіді на терапію. Оскільки індивідуальні показники АТ можуть непередбачувано варіювати, одного вимірювання недостатньо для прийняття клінічних рішень. Офісний АТ має базуватися на середньому значенні доступних вимірів, а середній показник ≥2 вимірів, отриманих за ≥2 рази, може мінімізувати похибку та забезпечити точнішу оцінку офісного АТ (Powers et al., 2011; Kronish et al., 2018).
При діагностуванні та лікуванні високого АТ у дорослих пацієнтів рекомендовано спиратися на стандартизовані підходи для точного визначення та документування офісного АТ (1, C‑LD). Під час вимірювання офісного АТ доцільно використовувати осцилометричний метод за допомогою автоматизованого пристрою, а не аускультативно (2a, C-EO). Використання безманжетних пристроїв для вимірювання АТ не рекомендоване (3: заподіює шкоду, C‑LD) (Han et al., 2023; Stergiou et al., 2022).
У дорослих із підозрою на АГ варто проводити позаофісне вимірювання АТ шляхом амбулаторного або домашнього моніторингу для підтвердження діагнозу АГ (1, А). В осіб, що приймають антигіпертензивні засоби, домашній моніторинг є доцільним для контролю титрування доз, разом із супутніми втручаннями, як-то навчання пацієнтів, консультування шляхом телемедицини та клінічні заходи (1, А) (Guirguis-Blake et al., 2021; Tucker et al., 2017).
Крім того, у дорослих пацієнтів із діагностованою АГ ретельний збір анамнезу, фізикальний огляд і рутинні лабораторні тестування є корисними для встановлення СС-ризику та прийняття рішень щодо терапії та необхідності додаткового обстеження. Лабораторні дослідження для оптимізації лікування включають загальний аналіз крові, визначення рівня електролітів і креатиніну в сироватці крові, глюкози або глікованого гемоглобіну, тиреотропного гормону, ліпідний профіль, аналіз сечі та співвідношення альбуміну до креатиніну (Ал/Кр) у сечі, а також діагностичні процедури, зокрема електрокардіограму (ЕКГ) у 12 відведеннях (1, C-EO) (Berry et al., 2021).
Особливості діагностики
Різні види АГ
Моніторинг позаофісного АТ дозволяє диференціювати АГ за кількома клінічно значущими категоріями на основі відповідності або невідповідності офісному АТ, включно з АГ «білого халата» і маскованою АГ в осіб, які не приймають чи приймають антигіпертензивні препарати (Muntner et al., 2019).
У дорослих із нелікованим офісним САТ ≥130 мм рт. ст. або ДАТ ≥80 мм рт. ст. та без офісного САТ ≥160 мм рт. ст. чи ДАТ ≥100 мм рт. ст., перш ніж буде поставлено діагноз АГ, слід виключити АГ «білого халата» за допомогою позаофісного моніторингу АТ (2а, B-NR). У пацієнтів із нелікованим офісним САТ <130 мм рт. ст. та ДАТ <80 мм рт. ст. може бути доцільно виключити масковану АГ шляхом позаофісного вимірювання АТ (2b, B-NR) (Pierdomenico et al., 2011; Thakkar et al., 2020). В осіб з АГ, резистентною до лікування, на тлі офісного вимірювання АТ також варто виключити «ефект білого халата» шляхом позаофісного контролю АТ (2а, C‑LD). Своєю чергою у пацієнтів з АГ «білого халата» або маскованою АГ позаофісний моніторинг АТ є доцільним для виключення переходу до стійкої АГ (2а, B-NR) (Cardoso, Salles, 2021; Faria et al., 2020).
У дорослих, які приймають антигіпертензивні препарати та мають підвищений офісний АТ (САТ ≥130 мм рт. ст. чи ДАТ ≥80 мм рт. ст.), але не мають резистентної АГ або офісного САТ ≥160 мм рт. ст. чи ДАТ ≥100 мм рт. ст., необхідно виключити «ефект білого халата» за допомогою позаофісного моніторингу АТ (2а, B-NR). У пацієнтів, які отримують антигіпертензивні засоби та мають офісний САТ <130 мм рт. ст. і ДАТ <80 мм рт. ст., може бути доцільно виключити масковану неконтрольовану АГ шляхом позаофісного вимірювання АТ (2b, B-NR) (Stergiou et al., 2014; Zhang et al., 2019).
Вторинна АГ
У дорослих з АГ рекомендовано проводити скринінг на специфічні форми вторинної АГ за наявності клінічної підозри, щоб поліпшити діагностику та вибір необхідної терапії (1, C-EO). З цією ж метою у пацієнтів із резистентною АГ слід виконувати скринінг на первинний альдостеронізм незалежно від наявності гіпокаліємії (1, B-NR). В осіб, які отримали позитивний результат після проведення скринінгового тесту на форму вторинної АГ, скерування до клініциста, який має досвід роботи із цією формою АГ, є доцільним для підтвердження діагнозу та призначення відповідного лікування (2а, C-EO) (Xu et al., 2020).
Первинний альдостеронізм
Скринінг на первинний альдостеронізм рекомендовано проводити для поліпшення виявлення, оцінки та вибору необхідної терапії у пацієнтів з АГ за наявності будь-якого із таких станів, як: резистентна АГ (незалежно від наявності гіпокаліємії), гіпокаліємія (спонтанна або індукована діуретиками), синдром обструктивного апное уві сні (СОАС), випадково виявлена пухлина наднирникової залози, сімейний анамнез АГ із раннім початком або інсульт у молодому віці (<40 років) (1, C-EO). Із цією ж метою скринінг на первинний альдостеронізм може бути розглянутий у дорослих з АГ 2-ї стадії (2b, C-EO).
В осіб із показаннями до скринінгу на первинний альдостеронізм для оцінки наявності його біохімічних ознак доцільно використовувати рівень альдостерону в плазмі, активність реніну та співвідношення альдостерон/ренін у плазмі (1, C‑LD). Зокрема, у дорослих із показаннями до цього скринінгу перед процедурою рекомендовано продовжувати приймати більшість антигіпертензивних препаратів, окрім антагоністів мінералокортикоїдних рецепторів (АМР), щоб мінімізувати потенційні перешкоди або затримки у її проведенні (1, C-EO). Пацієнтів з АГ та позитивним результатом тесту на первинний альдостеронізм або збереженою підозрою щодо його наявності на основі зниженого реніну плазми або непропорційного ураження органів-мішеней необхідно скерувати до спеціаліста з АГ або ендокринолога для подальшого обстеження та лікування (1, C-EO) (Maiolino et al., 2017; Brown et al., 2020).
Стеноз ниркової артерії
У дорослих з АГ й атеросклеротичним стенозом ниркової артерії для зниження захворюваності та смертності рекомендоване призначення фармакологічної терапії (1, А) (Raman et al., 2016). Якщо медикаментозне лікування виявилося неефективним (наприклад, у разі резистентної АГ, погіршення функції нирок та/або гострої СН), слід скерувати хворого на реваскуляризацію із застосуванням черезшкірної ангіопластики ниркової артерії та/або встановленням стента (2а, C-EO). При АГ та неатеросклеротичному стенозі ниркової артерії, включно із фібром’язовою дисплазією, ймовірно доцільно скерувати пацієнта на проведення черезшкірної ангіопластики ниркової артерії (2b, C‑LD) (Trinquart et al., 2010).
Синдром обструктивного апное уві сні
У пацієнтів з АГ та СОАС, які мають надмірну масу тіла або ожиріння, відповідні заходи для зниження ваги у поєднанні з постійним позитивним тиском у дихальних шляхах можуть бути ефективними для зниження САТ (2а, B-R). У дорослих із резистентною АГ та СОАС помірного/тяжкого ступеня застосування постійного позитивного тиску в дихальних шляхах може бути корисним для зниження АТ (2а, B-R) (Kovacs et al., 2022; Labarca et al., 2021).
Профілактика й контроль АТ
Модифікація способу життя та психосоціальні підходи
Надмірна вага та несприятливий спосіб життя є потужними факторами ризику підвищення АТ з віком (Guo et al., 2024). Підходи до зміни способу життя є критично важливими стратегіями для уповільнення підвищення АТ та відтермінування або запобігання розвитку АГ. Після встановлення діагнозу АГ корекція способу життя й нефармакологічні стратегії можуть знизити АТ, зменшити кількість застосовуваних ліків для його контролю та запобігти СС-подіям і смерті.
Для профілактики чи лікування підвищеного АТ та АГ дорослим із надмірною вагою або ожирінням необхідно знизити вагу щонайменше на 5% від маси тіла (1, А). З цією ж метою особам із/без АГ варто дотримуватися дієтичних рекомендацій для серцево-судинної системи, наприклад із дотриманням дієтичного підходу для боротьби з АГ (DASH) (1, А) (Yang et al., 2023; Fu et al., 2020). Окрім того, для цієї популяції хворих рекомендовано зменшити споживання натрію з їжею до <2300 мг/добу (в ідеалі – до 1500 мг/добу) для запобігання або контролю підвищеного АТ та АГ (1, А) (Filippini et al., 2021).
Дорослим з АГ або без неї замінники солі на основі калію можуть бути корисними для профілактики або лікування підвищеного АТ чи АГ, за винятком випадків ХХН або використання препаратів, що знижують екскрецію калію, коли показаний моніторинг його рівня у сироватці крові (2а, А). З цією ж метою пацієнтам із підвищеним АТ чи АГ рекомендоване помірне додавання калію, за винятком випадків ХХН або застосування препаратів, що знижують екскрецію калію, коли показаний моніторинг його рівня у сироватці крові (1, А) (Greenwood et al., 2024; Aburto et al., 2013).
Особам із/без АГ, які вживають алкоголь, слід рекомендувати утримуватися від цього або принаймні зменшити до ≤1 напою/день для жінок та ≤2 напоїв/день для чоловіків для профілактики або лікування підвищеного АТ чи АГ (1, А) (Roerecke et al., 2017). Із цією ж метою дорослим з АГ або без неї доцільно збільшити фізичну активність на основі структурованої програми вправ, що включає аеробні та/або силові навантаження (1, А) (Jabbarzadeh Ganjeh et al., 2024).
Для популяції з/без АГ зниження стресу за допомогою трансцендентальної медитації, а також інших технік контролю дихання або йоги може бути доцільним для запобігання або лікування підвищеного АТ чи АГ як доповнення до модифікації способу життя або медикаментозної терапії (2b, B-R) (Wu et al., 2019; Semlitsch et al., 2021).
Стратегії фармакотерапії
Цільовий АТ в осіб з АГ
Доступні дані свідчать про те, що інтенсивніший контроль АТ має переваги для профілактики ССЗ (Reboussin et al., 2018). У дорослих із підтвердженою АГ, які мають підвищений ризик розвитку ССЗ, рекомендований цільовий рівень САТ становить щонайменше <130 мм рт. ст. із заохоченням до досягнення <120 мм рт. ст. з метою зменшення ймовірності СС-подій та загальної смертності (1, А). Своєю чергою цільовий ДАТ має бути <80 мм рт. ст. (1, B-R) (Whelton et al., 2024; He et al., 2023). У пацієнтів із підтвердженою АГ, які не мають підвищеного ризику ССЗ, цільовий рівень САТ <130 мм рт. ст. із заохоченням до досягнення <120 мм рт. ст. може бути доцільним для зменшення ймовірності подальшого підвищення АТ (2b, B-NR). Також у цієї категорії хворих варто розглянути цільовий показник ДАТ <80 мм рт. ст. для зниження ризику СС-подій (2b, B-NR) (Fuchs et al., 2016).
Вибір антигіпертензивного лікування на основі порогових значень АТ та СС-ризику
При підвищенні рівня АТ СС-ризик варіює залежно від віку, статі та наявності ССЗ або факторів СС-ризику. Тому рішення про початок антигіпертензивного лікування має ґрунтуватися на рівні АТ і СС-ризику.
Усім хворим на АГ ініціація антигіпертензивної терапії є рекомендованою, коли середній САТ становить ≥140 мм рт. ст., а ДАТ ≥90 мм рт. ст., щоб зменшити ймовірність розвитку СС-подій та загальну смертність (1, А). Дорослим з АГ та іншими ССЗ (як-от ІХС, інсульт або СН) із метою зниження ризику СС-наслідків та загальної смертності слід починати приймати антигіпертензивні ліки у разі середнього САТ ≥130 мм рт. ст. (1, А). Своєю чергою середній ДАТ має становити ≥80 мм рт. ст. (1, C‑LD) (Guo et al., 2024; Liu et al., 2024).
Пацієнтам з АГ без інших ССЗ, але із ЦД чи ХХН, або підвищеним короткостроковим СС-ризиком старт антигіпертензивної терапії є необхідним, якщо середній САТ ≥130 мм рт. ст., щоб зменшити ймовірність СС-подій та загальну смертність (1, А). Короткостроковий СС-ризик становить ≥7,5% на основі моделі PREVENT, розробленої для оцінки 10-річного ризику виникнення ССЗ. Середній ДАТ у цій когорті хворих має бути ≥80 мм рт. ст. (1, C‑LD). Що стосується дорослих з АГ без інших ССЗ та із 10-річним СС-ризиком <7,5%, призначення антигіпертензивних препаратів є доцільним, якщо середній САТ залишається ≥130 мм рт. ст., а ДАТ ≥80 мм рт. ст. після корекції способу життя впродовж 3‑6 місяців, для запобігання пошкодженню органів-мішеней та подальшому підвищенню АТ (1, B-R) (Peng et al., 2023; Rahimi et al., 2021).
На рисунку підсумовано рекомендації щодо початку антигіпертензивної терапії в усіх дорослих пацієнтів, у яких середній рівень АТ становить ≥140/90 мм рт. ст., а також у групах хворих із середнім рівнем АТ ≥130/80 мм рт. ст., що отримають переваги від такого лікування.
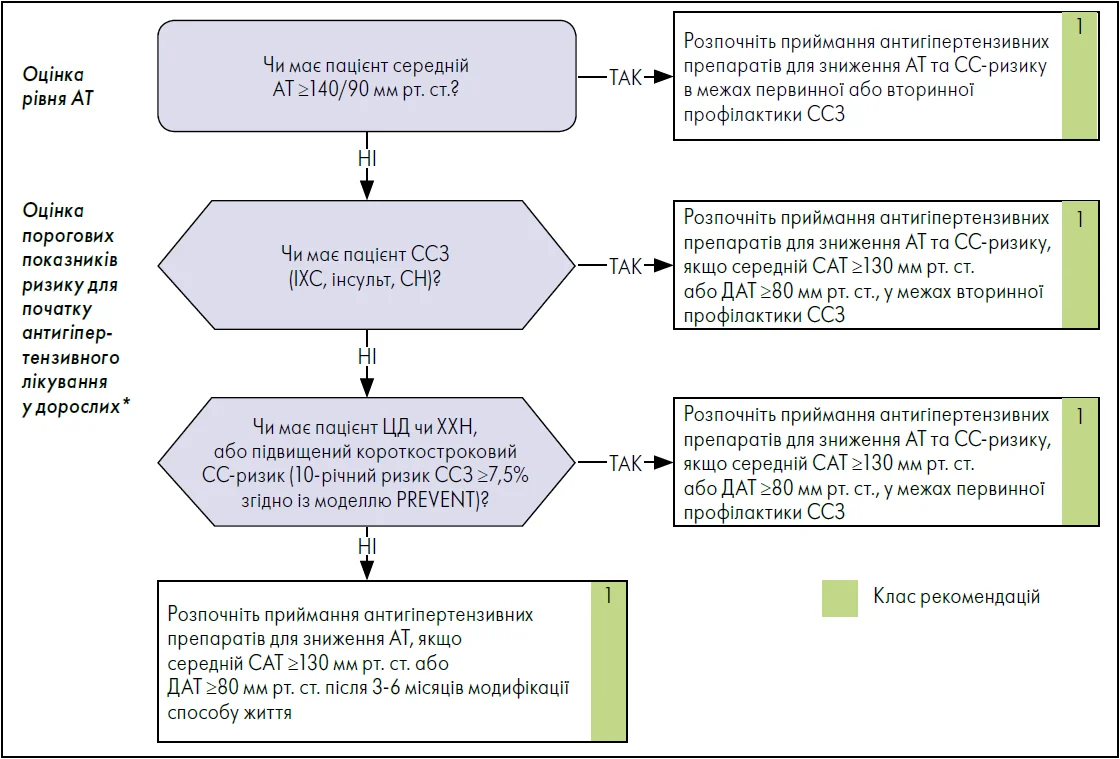 Рисунок. Призначення антигіпертензивного лікування на основі оцінювання порогових значень АТ та СС-ризику
Рисунок. Призначення антигіпертензивного лікування на основі оцінювання порогових значень АТ та СС-ризику
Примітки: * У літніх осіб, які немічні або мають обмежену тривалість життя, слід провести комплексну оцінку потенційних переваг та шкоди від зниження АТ, щоб призначити лікування з урахуванням індивідуальних особливостей, клінічних обставин та побажань пацієнта.
Адаптовано за АНА/АСС (2025)
Початок антигіпертензивної терапії та переваги застосування комбінацій ліків
Медикаментозні засоби є невід’ємним інструментом у лікуванні АГ. При початку фармакотерапії насамперед слід враховувати супутні захворювання (як-от ІХС, СН, інсульт, ЦД, ХХН), для яких показані специфічні класи препаратів, що знижують АТ. Оскільки АТ регулюється кількома взаємодоповнювальними біологічними системами, для досягнення контролю АТ більшість пацієнтів потребують призначення ≥2 антигіпертензивних засобів.
Для дорослих, які планують ініціацію антигіпертензивної терапії, тіазидні діуретики, дигідропіридинові блокатори кальцієвих каналів (БКК) тривалої дії та інгібітори ангіотензинперетворювального ферменту (іАПФ) або блокатори рецепторів ангіотензину II (БРА) рекомендовані як препарати першої лінії для профілактики ССЗ (1, А) (Wei et al., 2020). У хворих на АГ 1-ї стадії (САТ 130‑139 мм рт. ст. і ДАТ 80‑89 мм рт. ст.) доцільно розпочати лікування з антигіпертензивного препарату першої лінії з титруванням дози та послідовним додаванням інших медикаментів за потреби для досягнення контролю АТ (2а, C-EO). Пацієнтам з АГ 2-ї стадії (САТ ≥140 мм рт. ст. і ДАТ ≥90 мм рт. ст.) слід починати терапію двома антигіпертензивними засобами першої лінії різних класів, в ідеалі у формі фіксованої комбінації в одній таблетці, для поліпшення контролю АТ та підвищення комплаєнсу (1, B-R) (Schmieder et al., 2023; Wang et al., 2023). Для дорослих з АГ одночасне застосування іАПФ, БРА та/або інгібіторів реніну не рекомендоване через потенційну шкоду (3: заподіює шкоду, А) (Fried et al., 2013).
|
Таблиця. Фармакотерапія відповідно до настанов для пацієнтів з АГ та СНзнФВ |
|
|
Клас препарату |
Роз’яснення щодо застосування |
|
β-блокатори |
Пацієнтам із СНзнФВ, навіть безсимптомним, слід призначити один із трьох β-блокаторів для зниження частоти госпіталізацій та смертності, як-то бісопролол, карведилол і метопрололу сукцинат |
|
АМР |
Особам із симптоматичною СНзнФВ рекомендовано приймати спіронолактон або еплеренон для зменшення захворюваності та смертності, якщо рШКФ становить >30 мл/хв/1,73 м2, а рівень калію <5,0 мЕк/л |
|
іРААС з іАПФ або БРА, або ARNi |
Хворим на СНзнФВ II‑III ФК за NYHA рекомендоване застосування ARNi Якщо використання ARNi неможливе, доцільно призначити іАПФ або БРА |
|
іНЗКТГ‑2 |
іНЗКТГ‑2 рекомендовані пацієнтам із симптоматичною СНзнФВ для зниження частоти госпіталізацій та СС-смертності незалежно від наявності ЦД 2-го типу |
|
Додатковий препарат (слід додавати за показаннями) |
|
|
Гідралазин та ізосорбіду динітрат |
Для темношкірих пацієнтів із СНзнФВ III‑IV ФК за NYHA, що отримують оптимальну фармакотерапію, рекомендованою є комбінація гідралазину та ізосорбіду динітрату для полегшення симптомів та зменшення захворюваності й смертності Для осіб із поточною симптоматичною СНзнФВ або в анамнезі, яким не можна призначати препарати першої лінії, як-то ARNi, іАПФ або БРА, через їх непереносимість або ниркову недостатність, можна розглянути застосування комбінації гідралазину та ізосорбіду динітрату з метою зниження захворюваності та смертності |
|
Примітки: ФК – функціональний клас, NYHA – Нью-Йоркська асоціація серця. Адаптовано за Р.А. Heidenreich et al. (2022) |
|
Стратегії дотримання режиму антигіпертензивного лікування
За наявними даними, до 50% хворих не дотримуються режиму приймання антигіпертензивних засобів після одного року терапії (Lee et al., 2022). У пацієнтів з АГ використання антигіпертензивних препаратів один, а не кілька разів на день, сприяє підвищенню прихильності до лікування (1, B-R). Також із цією ж метою доцільним є застосування фіксованої комбінації в одній таблетці замість окремих ліків для зменшення медикаментозного навантаження на хворого (1, B-R) (Lauffenburger et al., 2023). Окрім того, застосування мобільних застосунків із нагадуванням про приймання ліків та навчальних програм або заходів для самоконтролю може бути корисним для покращення комплаєнсу в осіб з АГ (2а, B-R) (Al-Arkee et al., 2021).
Ведення пацієнтів із супутніми захворюваннями
Цукровий діабет
Більш як 80% дорослих із ЦД 2-го типу страждають на АГ. Поширеність АГ при ЦД 2-го типу вдвічі вища, ніж у дорослих того ж віку без ЦД. Крім того, ймовірність виникнення ССЗ у пацієнтів із ЦД 2-го типу та АГ більш ніж удвічі перевищує ризик розвитку будь-якого із цих станів окремо. АГ прискорює появу ХХН, особливо за наявності помірної або тяжкої альбумінурії.
У дорослих з АГ та ЦД 2-го типу антигіпертензивну фармакотерапію слід розпочинати при САТ ≥130 мм рт. ст. із цільовим показником <130 мм рт. ст., заохочуючи до досягнення <120 мм рт. ст., для зниження захворюваності та смертності від ССЗ (1, А). При цьому ДАТ на момент старту лікування має становити ≥80 мм рт. ст. за цільового значення <80 мм рт. ст. (1, C‑LD) (Yang et al., 2023). У пацієнтів з АГ та ЦД 2-го типу всі класи антигіпертензивних препаратів першої лінії (тіазидні діуретики, БКК тривалої дії, іАПФ та БРА) ефективні для зниження АТ (1, А). Антигіпертензивна терапія іАПФ або БРА у цій популяції хворих рекомендована за наявності ХХН, що визначається за допомогою розрахункової швидкості клубочкової фільтрації (рШКФ) <60 мл/хв/1,73 м2 або альбумінурії ≥30 мг/г, та є доцільною за легкої альбумінурії (<30 мг/г) для сповільнення прогресування захворювання нирок, пов’язаного із ЦД (1, А) (Palmer et al., 2015).
Гіпоглікемічні препарати не мають затверджених показань до застосування для зниження АТ. Однак підтверджено, що серед нових класів гіпоглікемічних засобів інгібітори натрійзалежного котранспортера глюкози 2-го типу (іНЗКТГ‑2) та агоністи рецепторів глюкагоноподібного пептиду‑1 (арГПП‑1) уповільнюють погіршення функції нирок незалежно від наявності ЦД та можуть мати певний позитивний вплив на АТ (Wu et al., 2024).
Ожиріння та метаболічний синдром
Ожиріння є основним модифікованим фактором ризику АГ, причому чим більший ступінь ожиріння, тим вищий рівень АТ. Ожиріння та АГ часто супроводжуються іншими метаболічними станами, пов’язаними з ожирінням (як-то дисглікемія, дисліпідемія), що спричиняє підвищений ризик розвитку ССЗ (Mottillo et al., 2010).
У хворих на АГ, які також мають надмірну вагу або ожиріння з індексом маси тіла (ІМТ) ≥27 кг/м2, інкретиноміметики (наприклад, арГПП‑1) при використанні для контролю ваги можуть бути ефективними як допоміжний засіб для зниження АТ (2b, B-R). У дорослих з АГ, які мають ожиріння при ІМТ ≥35 кг/м2, баріатрична хірургія (якщо розглядається для зменшення маси тіла) у поєднанні з поведінковими втручаннями та антигіпертензивною терапією може бути ефективною для зниження АТ (2b, B-R) (Lincoff et al., 2023; de Lemos et al., 2024).
Серцева недостатність
Передумови до розвитку АГ відзначаються у ~70% пацієнтів із СН; своєю чергою АГ в осіб віком <40 років тісно пов’язана із виникненням СН (Baffour et al., 2024). У пацієнтів з АГ рекомендоване зниження САТ до <130 мм рт. ст. з метою зменшення ймовірності розвитку СН (1, B-R). При цьому варто прагнути зниження ДАТ до <80 мм рт. ст. (2b, B-NR) (Siddiqi et al., 2024).
Поширеність АГ серед пацієнтів із СН зі зниженою фракцією викиду (СНзнФВ), що визначається як фракція викиду лівого шлуночка ≥40%, продовжує зростати (Khan et al., 2020). У хворих на СНзнФВ, що мають АГ, для її контролю рекомендоване збільшення дози препаратів у межах медикаментозної терапії відповідно настанов до максимально переносимої (таблиця).
АГ є основним фактором ризику СН зі збереженою фракцією викиду (СНзбФВ) та важливою метою лікування для зменшення госпіталізації, СС-подій і смертності. В осіб з АГ і СНзбФВ за наявності ознак та/або симптомів перевантаження об’ємом комбінація діуретиків з антигіпертензивними препаратами може посилити ефект терапії. Інгібітори ренін-ангіотензин-альдостеронової системи (іРААС) показані при СНзбФВ для досягнення САТ <130 мм рт. ст., особливо при застосуванні АМР або інгібіторів рецепторів ангіотензину/неприлізину (ARNі), або БРА, якщо ARNі недоступні (Kittleson et al., 2023).
іНЗКТГ‑2 часто використовуються для лікування СНзбФВ (із/без ЦД) за відсутності протипоказань, щоб зменшити ймовірність госпіталізації та СС-смертності. Ці препарати здатні знижувати АТ, тому за наявності ознак або симптомів гіпотензії може знадобитися корекція антигіпертензивної терапії (Heidenreich et al., 2022; Zhang et al., 2023).
Фібриляція передсердь
АГ відзначається у >80% пацієнтів із фібриляцією передсердь (ФП) і є найпоширенішим коморбідним станом, незалежно від віку. Контроль АТ в осіб з АГ знижує ризик виникнення ФП, особливо у пацієнтів із СН. У дорослих із ФП та АГ оптимальний контроль АТ знижує частоту серйозних несприятливих подій, включно з інсультом (Pinho-Gomes et al., 2021).
Згідно із результатами досліджень і метааналізів, іАПФ та БРА знижують частоту й рецидиви ФП, але потрібні більш переконливі докази (Joglar et al., 2024). Також є певні дані, що АМР зменшують тягар ФП (Neefs et al., 2017). Контроль АГ є ключовим компонентом лікування ФП, хоча оптимальні цілі лікування АГ при ФП залишаються неясними. Тому доцільно застосовувати загальні рекомендації щодо АГ у пацієнтів із ФП, які включають досягнення цільового АТ <130/80 мм рт. ст. (Gawalko, Linz, 2023).
Хронічна хвороба нирок
Поширеність АГ серед осіб із ХХН становить 67‑92%. ХХН є важливим фактором ризику розвитку ССЗ, а співіснування АГ та ХХН ще більше збільшує ймовірність СС-подій. Попри цей ризик, у більшості пацієнтів із ХХН АТ є неконтрольованим (Plantinga et al., 2009).
У дорослих з АГ та ХХН при рШКФ <60 мл/хв/1,73 м2 або альбумінурії (Ал/Кр ≥30 мг/г) лікування має бути спрямоване на досягнення цільового рівня САТ <130 мм рт. ст. для зменшення смертності від усіх причин (1, А). Терапія у цій когорті хворих передбачає призначення іРААС (разом з іАПФ або БРА, але не з обома) для зниження СС-ризику й уповільнення прогресування захворювання нирок (1, B-R) (Aggarwal et al., 2019; Xie et al., 2016).
Цереброваскулярні захворювання
Інсульт являє собою одну з основних причин інвалідизації та смерті. Через неоднорідність причин розвитку та гемодинамічних наслідків лікування АТ у дорослих після перенесеного інсульту є складним завданням (Martin et al., 2024).
Гострий геморагічний інсульт. У пацієнтів із гострим спонтанним внутрішньомозковим крововиливом (ВМК) та САТ 150‑220 мм рт. ст. може знадобитися негайне зниження САТ до 130‑140 мм рт. ст. протягом щонайменше семи днів після ВМК, аби покращити функціональні результати, але приймання антигіпертензивних препаратів слід припинити, якщо САТ <130 мм рт. ст. (2а, А). У хворих із гострим спонтанним ВМК, які потребують ургентного зниження АТ, ймовірно доцільним є ретельне титрування доз антигіпертензивних препаратів для забезпечення стійкого контролю АТ, уникаючи піків та значної варіабельності САТ, для поліпшення функціональних результатів (2а, B-NR) (Ma et al., 2023; Moullaali et al., 2019). У пацієнтів із гострим спонтанним ВМК і САТ >220 мм рт. ст. не варто прагнути зниження САТ ˂130 мм рт. ст. для зменшення побічних ефектів (3: заподіює шкоду, B-NR) (Qureshi et al., 2020).
Гострий ішемічний інсульт. В осіб із гострим ішемічним інсультом слід коригувати гіпотонію та гіповолемію з метою підтримання системної перфузії, необхідної для нормального функціонування органів (1, C‑LD). У пацієнтів із підвищеним АТ, які потребують призначення внутрішньовенних тромболітиків за іншими показаннями, слід знизити САТ <185 мм рт. ст. та ДАТ <110 мм рт. ст. перед початком внутрішньовенної тромболітичної терапії та підтримувати його на рівні <180/105 мм рт. ст. протягом щонайменше перших 24 год після початку лікування, щоб уникнути ускладнень (1, B-NR) (Wohlfahrt et al., 2015). У хворих, яким проводять ендоваскулярне втручання, доцільно підтримувати АТ на рівні ≤180/105 мм рт. ст. під час і впродовж 24 год після процедури, щоб покращити довгострокові функціональні результати та запобігти смерті (2а, B-NR). У пацієнтів з АТ ≤220/120 мм рт. ст. без супутніх захворювань, що потребують негайного антигіпертензивного лікування, та без проведення внутрішньовенної тромболітичної терапії або ендоваскулярного втручання ймовірно доцільним є зниження АТ на 15% протягом перших 24 год після початку інсульту для поліпшення результатів (2b, C‑LD) (Katsanos et al., 2022; Vemmos et al., 2004).
У дорослих з АТ <220/120 мм рт. ст. без коморбідних станів, що потребують негайного антигіпертензивного лікування, та яким не виконують внутрішньовенного тромболізу чи ендоваскулярного втручання, ініціація або поновлення лікування АГ упродовж перших 48‑72 год після гострого ішемічного інсульту є неефективним для запобігання інвалідності або смерті (3: користь відсутня, А). У хворих, які успішно перенесли реперфузію головного мозку шляхом ендоваскулярного лікування оклюзії великої судини, зниження САТ <140 мм рт. ст. протягом перших 24‑72 год після реперфузії може погіршити довгострокові функціональні результати (3: заподіює шкоду, А) (Liu et al., 2023; Mistry et al., 2023).
Вторинна профілактика інсульту. В осіб з АГ, які перенесли ішемічний інсульт, транзиторну ішемічну атаку або ВМК, рекомендоване лікування тіазидним діуретиком, іАПФ або БРА для зниження АТ та ризику повторного інсульту і ВМК (1, А). Цільовий показник офісного АТ у цієї категорії хворих має становити <130/80 мм рт. ст. для зменшення ймовірності повторного інсульту, ВМК та інших судинних подій (1, B-R) (Zonneveld et al., 2018). Своєю чергою у пацієнтів без АГ в анамнезі, які перенесли ішемічний інсульт, транзиторну ішемічну атаку або ВМК і мають середній рівень офісного АТ ≥130/80 мм рт. ст., застосування антигіпертензивних препаратів може бути корисним для зниження ризику повторного інсульту, ВМК та інших судинних подій (2а, B-R) (Kitagawa et al., 2019).
Резистентна АГ та ниркова денервація
За доступними даними, основні фактори ризику розвитку резистентної АГ включають похилий вік, ожиріння, ХХН та ЦД. Пацієнти з АГ, резистентною до лікування, мають щонайменше на 50% вищий ризик інфаркту міокарда, інсульту, термінальної ниркової недостатності та смерті від ССЗ, ніж дорослі з нерезистентною АГ (Jafari et al., 2024; Ebinger et al., 2023).
У дорослих пацієнтів із резистентною АГ з метою зниження АТ та спрощення схеми лікування необхідною є детальніша оцінка вторинних причин, яка включає ретельний перегляд усіх застосовуваних ліків та виключення тих, що впливають на АТ. В осіб із неконтрольованою резистентною АГ, попри оптимальну антигіпертензивну терапію першої лінії (комбінацією іАПФ або БРА + БКК і тіазидоподібного діуретика при рШКФ ≥45 мл/хв/1,73 м2), рекомендоване додавання АМР для контролю АТ (Williams et al., 2015; Vitarello et al., 2022). У хворих із неконтрольованою резистентною АГ та непереносимістю або протипоказанням до АМР для регулювання АТ варто додати один із таких препаратів чи класів, як: амілорид, β-блокатори, α-блокатори, центральні симпатолітики, подвійні антагоністи ендотелінових рецепторів або прямі вазодилататори (Hundemer et al., 2021).
У ретельно відібраних пацієнтів із офісним САТ 140‑180 мм рт. ст. та ДАТ ≥90 мм рт. ст. і рШКФ ≥40 мл/хв/1,73 м2, які мають резистентну АГ незважаючи на оптимальне лікування або непереносимі побічні ефекти на тлі додаткової антигіпертензивної терапії, ниркова денервація може бути доцільною як ад’ювантне лікування до препаратів для зниження АТ та модифікації способу життя (Azizi et al., 2024).
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті www.ahajournals.org
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 1 (104) 2026 р.



