8 квітня, 2026
Час має значення: швидке клінічне рішення щодо комбінованої ліпідознижувальної терапії
 Сучасні стратегії профілактики атеросклеротичних серцево-судинних захворювань (АССЗ) ґрунтуються на швидкому та інтенсивному зниженні рівня холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ). Оновлені європейські рекомендації суттєво посилили вимоги до досягнення цільових показників, зокрема для пацієнтів дуже високого та екстремального ризику. Нові клінічні дані підтверджують: чим раніше розпочато ефективну ліпідознижувальну терапію (ЛЗТ) і чим стабільніше утримується низький рівень ХС ЛПНЩ, тим виразнішим є довгостроковий захист пацієнта від серцево-судинних (СС) подій. У цьому контексті комбінована терапія перестає бути резервною опцією та дедалі частіше розглядається як раціональна стартова стратегія. Розглянемо сучасні доказові підход
Сучасні стратегії профілактики атеросклеротичних серцево-судинних захворювань (АССЗ) ґрунтуються на швидкому та інтенсивному зниженні рівня холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ). Оновлені європейські рекомендації суттєво посилили вимоги до досягнення цільових показників, зокрема для пацієнтів дуже високого та екстремального ризику. Нові клінічні дані підтверджують: чим раніше розпочато ефективну ліпідознижувальну терапію (ЛЗТ) і чим стабільніше утримується низький рівень ХС ЛПНЩ, тим виразнішим є довгостроковий захист пацієнта від серцево-судинних (СС) подій. У цьому контексті комбінована терапія перестає бути резервною опцією та дедалі частіше розглядається як раціональна стартова стратегія. Розглянемо сучасні доказові підход
ХС ЛПНЩ як центральна мішень і основа стратегії профілактики
На сьогодні при веденні пацієнтів із дисліпідемією фокус лишається на показнику ХС ЛПНЩ (Tokgozoglu et al., 2026). Відповідно, найголовніший принцип, якого слід дотримуватися при лікуванні хворих, – чим раніше та інтенсивніше знижувати рівень ХС ЛПНЩ, тим більший довгостроковий «виграш» у зменшенні СС-ризику. Також підкреслено, що досягнення дуже низьких показників ХС ЛПНЩ нині є доведено безпечним. Дані за 2025 р. показали: навіть якщо сильно знизити «поганий» ХС ЛПНЩ, це не підвищує ризик нейрокогнітивних порушень або геморагічного інсульту (Mach et al., 2025).
Отже, ХС ЛПНЩ залишається ключовою терапевтичною мішенню в лікуванні АССЗ. ХС ЛПНЩ є центральною та модифікованою причиною розвитку АССЗ, а інтенсивне його зниження прямо корелює зі зменшенням МАСЕ.
Інтенсивна ліпідознижувальна терапія і «якість» бляшки: що демонструють нові дані
На початку 2026 р. з’явилося багато цікавих даних щодо інтенсивності ЛЗТ. Так, інтенсивна ЛЗТ, зокрема високоінтенсивні статини, езетиміб та інгібітори пропротеїнової конвертази субтилізин-кексинового типу 9 (PCSK9), достовірно асоційована з такими змінами атеросклеротичної бляшки:
- зменшення об’єму атеросклеротичних бляшок;
- зниження ліпідного ядра;
- збільшення товщини фіброзної покришки;
- стабілізація бляшок за даними внутрішньосудинного ультразвукового дослідження чи оптичної когерентної томографії.
Таким чином, чим стабільніша бляшка і чим кращий її регрес (або призупинення зростання), тим ефективнішою є вторинна профілактика СС-подій. За останніми доказами, значення має не лише розмір бляшки, а також її структура та стабільність. Тож чим раніше та якісніше контролювати рівень ХС ЛПНЩ, тим стабільнішою і менш «агресивною» є бляшка.
Досягнутий рівень ХС ЛПНЩ є ключовим детермінантом змін бляшки: чим нижчий показник, тим виразніші регресія та стабілізація атеросклерозу. Дані проспективних досліджень показують, що зменшення вмісту ХС ЛПНЩ ≥50% та до дуже низьких значень (<1,4 ммоль/л) пов’язане зі значним зниженням ризику МАСЕ. При цьому раннє та довгострокове лікування має кумулятивний ефект: тривалість експозиції до низького ХС ЛПНЩ важлива не меншою мірою, ніж його абсолютний рівень. Навіть за відсутності повної регресії бляшок їхня стабілізація суттєво знижує ризик клінічних подій, що й пояснює користь агресивної вторинної профілактики. Отже, контроль і досягнення низьких цільових рівнів ХС ЛПНЩ є центральною стратегією впливу не лише на рівень ризику, але й на структуру та стабільність атеросклеротичної бляшки (Tam et al., 2025).
Патогенез атеросклерозу: від ранніх змін до ролі ліпопротеїну (a) у формуванні нестабільної бляшки
Безперервний розвиток атеросклерозу протягом життя – від субклінічних змін до клінічних СС-подій – підкреслює критичну роль раннього виявлення і лікування. Атеросклероз починається задовго до появи симптомів і тривалий час перебігає безклінічно, із поступовим накопиченням атеросклеротичної бляшки. Іншими словами, пацієнт звернеться до лікаря не тоді, коли у нього «почався» атеросклероз, а тоді, коли він уже став прогресувати. Водночас якщо вже на цьому етапі призначити правильне лікування та вплинути на атерогенні частки, можна забезпечити стабілізацію стану хворого і уникнути розвитку МАСЕ.
На ранніх етапах патологічний процес зумовлений атерогенними ліпопротеїнами, передусім тими, що містять аполіпопротеїн B (Апо-В), запаленням, ендотеліальною дисфункцією та порушенням ліпідного обміну. Із часом настає фаза прискореного росту і дестабілізації бляшок, що призводить до появи клінічних подій: інфаркту міокарда (ІМ), інсульту.
Окрім того, на розвиток бляшок та, відповідно, атеросклерозу може впливати ліпопротеїн (a), або Лп(a), відомий як найбільш атерогенний ліпопротеїн, що є незалежним фактором ризику ССЗ. Лп(a) має три ключові проатерогенні властивості:
- Проатерогенність – Лп(a) подібний до ЛПНЩ, але містить Aпo(a), що підсилює накопичення в судинній стінці.
- Прозапальна дія – через оксидовані фосфоліпіди стимулює запалення (інтерлейкін‑6, фактор некрозу пухлини α, високочутливий C-реактивний білок).
- Протромботичний ефект – структурна подібність до плазміногену зумовлює порушення фібринолізу та, як наслідок, підвищення ризику тромбозу.
Показник Лп(a) >30 мг/дл асоційований із підвищенням ризику гострого ІМ у 2‑3 рази. Своєю чергою зниження Лп(a) на 50 мг/дл корелює зі зниженням СС-ризику приблизно на 20%. Лп(a) – незалежний фактор ризику, а не просто маркер. Він має чіткі механістичні шляхи ушкодження судин, є клінічно значущим фактором ризику та водночас має перспективні таргетні методи лікування. Тобто це повноцінна мішень для раннього виявлення та терапевтичного втручання. Таким чином, Лп(a) активно сприяє формуванню нестабільних атеросклеротичних бляшок і підвищує ризик розвитку ІМ – це не просто біомаркер, а причинний фактор нестабільного атеросклерозу (Yu, 2024).
За наявними даними, існують чіткі гендерні відмінності у рівнях Лп(a) та пов’язаному із цим ризику. Так, у жінок вміст Лп(a) із віком зростає, особливо після 50 років (у періоді менопаузи), що асоційовано зі значно більшою ймовірністю СС-подій. Своєю чергою у чоловіків рівень Лп(a) з віком стабільніший, і його підвищення також корелює з ризиком, але менш виражено, ніж у жінок. Це підкреслює необхідність статево-специфічного підходу до скринінгу та профілактики (Simony et al., 2022).
Значення та межі застосування CAC-score у клінічній практиці
Науковці A. Mehta et al. (2022) стверджують, що для кількісного оцінювання кальцинованих бляшок у коронарних артеріях з метою виявлення раннього атеросклерозу можна використовувати шкалу CAC score (індекс Агатстона). Показник CAC ≥100 вказує на пацієнтів із підвищеним Лп(a), які мають найвищий ризик АССЗ. В осіб із високим Лп(a) навіть CAC 1‑99 уже асоційований із підвищеним ризиком. Отже, CAC score може бути цінним інструментом стратифікації ризику в осіб із підвищеним Лп(a). Комбінація показників Лп(a) + CAC дозволяє точніше оцінити СС-ризик і приймати обґрунтовані клінічні рішення.
Водночас, на думку M.H. Andersen et al. (2025), визначення коронарного кальцію не є абсолютним скринінговим методом. Було проведене дослідження, в якому автори виявили, що навіть у пацієнтів без коронарних кальцифікацій (CAC = 0) за даними комп’ютерної томографії підвищений ХС ЛПНЩ асоційований із більшою ймовірністю СС-подій. При цьому ризик зростає пропорційно рівню ХС ЛПНЩ, особливо у молодших пацієнтів (<55 років). Отже, відсутність кальцію не означає відсутність атеросклерозу або довгострокового ризику, і контроль ХС ЛПНЩ має значення навіть при «чистій» КТ, особливо з позицій довгострокової профілактики. Дослідники дійшли висновку, що не варто відкладати ЛЗТ лише через CAC = 0: ХС ЛПНЩ залишається ключовою мішенню первинної профілактики, зокрема у молодих і кардіометаболічних пацієнтів.
Сучасні стратегії інтенсифікації ЛЗТ
Минулого року Європейське товариство кардіологів та Європейське товариство атеросклерозу (ESC/EAS, 2025) оновило настанову із лікування дисліпідемій. У ній для визначення цільових показників ХС ЛПНЩ відповідно до загального СС-ризику (низький, помірний, високий, дуже високий) було додано ще одну категорію – екстремальний (надзвичайний) ризик, коли цільовий рівень ХС ЛПНЩ має бути <1 ммоль/л. Це пацієнти з АССЗ, які мають повторні судинні події на тлі максимально переносимої терапії на основі статинів, а також особи із полісудинною (наприклад, коронарною та периферичною) артеріальною хворобою.
Показники середнього зниження рівня ХС ЛПНЩ, досягнуті за різних видів фармакологічної терапії з доведеною користю для СС-системи, наведені в таблиці (ESC/EAS, 2025).
|
Таблиця. Середнє зниження рівня ХС ЛПНЩ за різних видів фармакологічної терапії з доведеною користю для СС-системи |
|
|
Метод лікування |
Зниження ХС ЛПНЩ |
|
Статин помірної інтенсивності |
~30% |
|
Статин високої інтенсивності |
~50% |
|
Езетиміб |
~20% |
|
Бемпедоєва кислота |
~23% |
|
Езетиміб + бемпедоєва кислота |
~38% |
|
Статин високої інтенсивності + езетиміб |
~60% |
|
Статин високої інтенсивності + бемпедоєва кислота |
~58% |
|
Статин високої інтенсивності + езетиміб + бемпедоєва кислота |
~68% |
|
PCSK9 mab |
~60% |
|
PCSK9 mab + езетиміб |
~70% |
|
PCSK9 mab + езетиміб + бемпедоєва кислота |
~75% |
|
Статин високої інтенсивності + PCSK9 mab |
~75% |
|
Статин високої інтенсивності + езетиміб + PCSK9 mab |
~80% |
|
Статин високої інтенсивності + езетиміб + бемпедоєва кислота + PCSK9 mab |
~86% |
|
Примітки: PCSK9 mab – моноклональні антитіла до PCSK9. Адаптовано за ESC/EAS (2025) |
|
Відповідно, найвиразніше зниження рівня ХС ЛПНЩ досягається при застосуванні комбінованої ЛЗТ, що поєднує вплив на різні механізми ліпідного обміну. Зокрема, додавання езетимібу до статину дозволяє суттєво посилити гіполіпідемічний ефект порівняно з монотерапією, що робить цю комбінацію раціональною стратегією інтенсифікації лікування. Вибір препарату має базуватися на необхідному рівні зниження ХС ЛПНЩ.
За даними реєстру SWEDENHEART (2013‑2017), раннє призначення езетимібу після гострого ІМ асоційоване із кращими довгостроковими СС-результатами. У пацієнтів, яким езетиміб додавали ще до виписки зі стаціонару, через три роки спостерігалася найнижча частота MACE порівняно з тими, хто отримував його пізніше або не отримував взагалі. Чітка градація ефекту (раннє призначення < пізнє призначення < відсутність езетимібу) свідчить про клінічну доцільність якнайшвидшої інтенсифікації ЛЗТ. Переваги раннього додавання препарату зберігалися незалежно від віку хворих, наявності цукрового діабету чи вихідного рівня ХС ЛПНЩ. Таким чином, своєчасне включення езетимібу до терапії після ІМ є ефективною стратегією зниження ризику повторних СС-подій у найближчі роки (Leosdottir et al., 2025).
Отже, сучасні дані підтримують початкову комбіновану терапію (up-front), а не покрокову ескалацію, особливо в осіб із високим та дуже високим ризиком. Тобто на сьогодні відбулася зміна парадигми: не чекати, поки статини «не впораються», а одразу починати з комбінованого підходу в пацієнтів групи високого ризику.
Окрім того, в осіб із кардіометаболічними захворюваннями слід зважати на механізми формування атеросклеротичних бляшок, зумовлені гіперглікемією. Комбіновані та послідовні терапевтичні стратегії дозволяють оптимізувати кардіометаболічні результати та зменшити поліфармацію. При цьому індивідуалізований підхід покращує прихильність пацієнтів до лікування. Фенотип-орієнтовані рішення сприяють точнішому призначенню терапії при АССЗ, серцевій недостатності, хронічному захворюванні нирок, ожирінні тощо (Dong et al., 2025).
У новітній публікації K. Ray та F. Kronenberg (2026) представлено сучасний аналітичний огляд оновлених настанов ESC/EAS (2025) щодо лікування дисліпідемій із чітким акцентом на необхідність швидкого та більш рішучого зниження ХС ЛПНЩ. Автори підкреслюють, що реальна клінічна практика значно відстає від доказової бази, а досягнення цільових рівнів ХС ЛПНЩ, особливо <1,4 ммоль/л у пацієнтів групи дуже високого ризику, у більшості випадків неможливе при застосуванні лише монотерапії статином. Зокрема, на основі даних реєстрів DA VINCI та SANTORINI наголошується, що близько 80% хворих із дуже високим ризиком потребують комбінованої ЛЗТ для досягнення рекомендованих цілей. Покроковий алгоритм вибору ЛЗТ залежно від рівня серцево-судинного ризику та цільових показників ХС ЛПНЩ, що дозволяє раціонально інтенсифікувати лікування та досягти рекомендованих цілей у найкоротші терміни, представлений на рисунку.
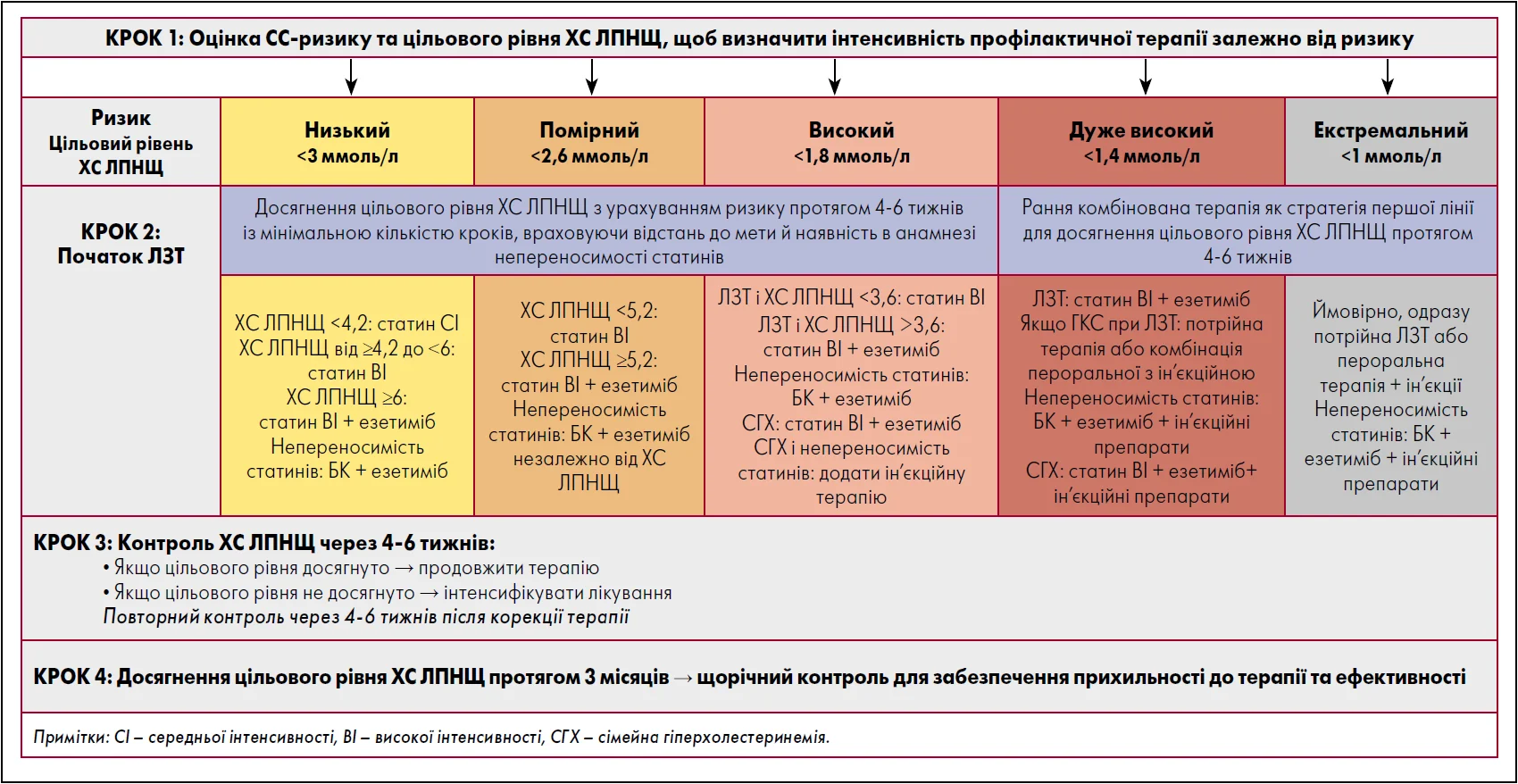 Рисунок. Покроковий алгоритм вибору ЛЗТ залежно від рівня СС-ризику та цільових показників ХС ЛПНЩ
Рисунок. Покроковий алгоритм вибору ЛЗТ залежно від рівня СС-ризику та цільових показників ХС ЛПНЩ
Примітка: Адаптовано за K. Ray et al. (2026)
На додаток, особливу увагу приділено пацієнтам із гострим коронарним синдромом (ГКС). Так, хворим, госпіталізованим із приводу ГКС, які раніше отримували будь-які гіполіпідемічні препарати, рекомендовано інтенсифікацію ЛЗТ з метою подальшого зниження рівня ХС ЛПНЩ. Початок комбінованої терапії високоінтенсивними статинами та езетимібом під час госпіталізації з приводу ГКС слід розглядати у пацієнтів, що раніше не отримували лікування, та в яких не очікується досягнення цільового рівня ХС ЛПНЩ за допомогою лише статинів (ESC/EAS, 2025).
У роботі також підкреслено користь вже згаданої вище концепції, відповідно до якої швидке і стійке зниження ХС ЛПНЩ забезпечує максимальні клінічні переваги щодо зменшення СС-ризику: «чим раніше та інтенсивніше, тим триваліший і кращий ефект» («the earlier, the lower, the longer, the better»). Комбінація статину з езетимібом дозволяє отримати додаткове зниження ХС ЛПНЩ приблизно на 20‑25% порівняно із монотерапією статином, що істотно підвищує ймовірність досягнення цільових показників без необхідності надмірного підвищення дози статину. Автори також звертають увагу, що фіксовані комбінації можуть покращити прихильність до лікування та прискорити досягнення терапевтичної мети.
Окремо розглядається місце бемпедоєвої кислоти як альтернативи при непереносимості статинів, але саме стратегія ранньої подвійної пероральної терапії (статин + езетиміб) визначається як раціональна основа лікування більшості пацієнтів груп високого та дуже високого ризику. Таким чином, К. Ray та F. Kronenberg (2026) акцентують на тому, що комбінована ЛЗТ є не ескалацією «за потреби», а логічною та часто необхідною стартовою стратегією для ефективного зниження СС-ризику.
Серед терапевтичних опцій, які можна використовувати на будь-якому етапі лікування пацієнтів різних груп ризику, варто відзначити фіксовану комбінацію розувастатину та езетимібу. Стратегія додавання езетимібу до розувастатину дозволяє суттєво посилити ліпідознижувальний ефект без необхідності підвищення дози статину, що робить її більш раціональним підходом до інтенсифікації лікування (Lee et al., 2023; Bays et al., 2011).
Висновки
Таким чином, при ухваленні клінічного рішення щодо комбінованої ЛЗТ час дійсно має значення – так само, як і точний розрахунок ризику та своєчасні дії щодо зменшення ймовірності розвитку СС-подій. Сучасні докази свідчать: чим раніше досягнуто низького ХС ЛПНЩ і чим довше він утримується, тим більшою є кумулятивна користь для пацієнта, зокрема через стабілізацію бляшок та зменшення ризику МАСЕ.
Комбінований підхід за допомогою розувастатину й езетимібу (Розуліп® Плюс) дозволяє швидше досягати цільових рівнів ХС ЛПНЩ без надмірної ескалації дози статину, а також може позитивно впливати на переносимість і прихильність до терапії. З позицій оновлених цільових рівнів у настанові ESC/EAS (2025), зокрема з урахуванням категорії екстремального ризику, комбінована ЛЗТ дедалі частіше переходить зі статусу «наступного кроку» до стартової стратегії для пацієнтів із високим та дуже високим ризиком.
Водночас ефективність будь-якої ЛЗТ у реальній практиці визначається не лише вибором препарату, а й системністю ведення пацієнта: регулярним контролем ліпідного профілю, корекцією супутніх факторів ризику та комунікацією щодо цілей лікування. І зрештою, прихильність пацієнтів до терапії значною мірою залежить від майстерності лікаря – вміння пояснити важливість раннього та тривалого контролю ХС ЛПНЩ і вчасно прийняти правильне клінічне рішення.
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 1 (104) 2026 р.



 Черська М.С.
Черська М.С.
