20 вересня, 2025
Оновлені рекомендації щодо фармакологічного лікування псоріатичного артриту
Рекомендації Європейської антиревматичної ліги (EULAR) 2023 р. щодо лікування псоріатичного артриту (ПсА) були вперше представлені в червні 2023 р. на Європейському конгресі ревматологів в Мілані (Італія). Офіційна публікація настанови відбулася в березні 2024 р. Метою оновлення рекомендацій щодо терапії ПсА було висвітлення нових механізмів дії препаратів та даних стосовно ефективності й безпеки вже наявних лікарських засобів. Положення, що були розроблені на основі систематичного огляду літератури та консенсусної думки міжнародних експертів, включають сім основних принципів і 11 рекомендацій щодо фармакотерапії ПсА. У документі наведені стратегії лікування нестероїдними протизапальними препаратами (НПЗП), біологічними засобами та інгібіторами янус-кінази (іJAK) залежно від форми захворювання. Зокрема, запропоноване використання практичного підходу до ведення пацієнтів із ПсА з огляду на супутні патології, як-от запальні захворювання кишечника (ЗЗК) та увеїт. Представляємо до вашої уваги огляд ключових положень настанови.
У лікуванні ПсА останніми роками було досягнуто значного прогресу. Зокрема, були розвинуті нові концепції, як-то дуже рання діагностика ПсА та пре-ПсА, а також встановлені цілі терапії та застосування комплексного підходу до лікування супутніх захворювань (Zabotti et al., 2023; Lubrano et al., 2023). Фармакологічні можливості розширилися завдяки схваленню нових лікарських засобів, що націлені на різні механізми дії за ПсА та псоріазу шкіри.
До препаратів, затверджених для лікування ПсА, сьогодні належать (табл. 1) (Kerschbaumer et al., 2024):
- Звичайні синтетичні хворобомодифікувальні антиревматичні препарати (зсХМАРП), такі як метотрексат, сульфасалазин і лефлуномід.
- Біологічні ХМАРП (бХМАРП), що включають інгібітори фактора некрозу пухлин (іФНП) – як оригінальні, так і біосиміляри, інгібітори IЛ‑17 і IЛ‑12‑23/IЛ‑23-p19, а також інгібітори CTLA4 (цитотоксичний антиген 4, пов’язаний із Т-лімфоцитами).
- Агенти, що інгібують янус-кіназу (JAK), як-то тофацитиніб та упадацитиніб, або фосфодіестеразу 4-го типу (ФДЕ4) – таргетні синтетичні ХМАРП (тсХМАРП).
На додаток, з’явилися нові дані щодо безпеки використання іJAK, отримані у великому рандомізованому контрольованому дослідженні впливу тофацитинібу при ревматоїдному артриті (РA) (Ytterberg et al., 2022; EMA, 2023; FDA, 2023). Із часу останніх рекомендацій EULAR щодо фармакологічного лікування ПсА 2019 р. галузь суттєво змінилася. Тому оновлення настанови EULAR щодо лікування ПсА було своєчасним (Coates et al., 2022; Coates et al., 2023).
Це оновлення стосується системного фармакологічного лікування ПсА з акцентом на опорно-рухові прояви захворювання, а також охоплює спектр ПсА, включно із впливом псоріазу шкіри, позасуглобових проявів та супутніх патологій на вибір терапії Пс А.
У чинній настанові положення щодо лікування пацієнтів із ПсА мають відповідні рівні доказовості та ступені рекомендацій. Оновлені аспекти включають 7 загальних принципів (порівняно із 6 у 2019 р.) і 11 рекомендацій (порівняно із 12 у 2019 р. через злиття пунктів), серед яких лише 4 залишилися незмінними. Із семи загальних принципів три залишилися без змін, три були переформульовані й один додано.
Порівняння змін із рекомендаціями 2019 р. представлені в таблиці 2.
|
Таблиця 1. Перелік препаратів, затверджених для лікування ПсА, згідно з EULAR (2023) |
||
|
Тип ХМАРП |
Мішень впливу |
Назва препарату |
|
зсХМАРП |
|
Метотрексат Лефлуномід Сульфасалазин |
|
бХМАРП |
ФНП |
Адалімумаб Цертолізумаб Етанерцепт Інфліксимаб Голімумаб |
|
ІЛ‑12/23 |
Устекінумаб |
|
|
ІЛ‑17A |
Іксекізумаб Секукінумаб |
|
|
IЛ‑17A/F |
Бімекізумаб |
|
|
IЛ‑23-p19 |
Гуселкумаб Різанкізумаб |
|
|
CTLA‑4 |
Абатацепт |
|
|
тсХМАРП |
ФДЕ4 |
Апреміласт |
|
JAK* |
Тофацитиніб Упадацитиніб |
|
|
Примітки: CTLA4 – антиген 4, асоційований із Т-лімфоцитами. * іJAK необхідно з обережністю призначати пацієнтам віком ≥65 років, тим, хто є нинішніми або колишніми тривалими курцями, з анамнезом атеросклеротичного серцево-судинного захворювання або іншими пов’язаними з ними факторами ризику, з іншими чинниками ризику злоякісних новоутворень, а також із відомими факторами ризику венозної тромбоемболії. |
||
|
Таблиця 2. Порівняння рекомендацій EULAR 2019 і 2023 рр. щодо лікування ПсА |
||||
|
Версія 2019 р. |
Зміни |
Версія 2023 р. |
||
|
Загальні принципи |
||||
|
A |
ПСА є гетерогенним і потенційно тяжким захворюванням, що може потребувати мультидисциплінарного підходу до лікування |
Без змін |
A |
ПСА є гетерогенним і потенційно тяжким захворюванням, що може потребувати мультидисциплінарного підходу до лікування |
|
B |
Терапія ПСА має бути спрямована на забезпечення найкращої допомоги та базуватися на спільному рішенні пацієнта і лікаря-ревматолога, з урахуванням ефективності, безпеки й вартості лікування |
Перефор-мульовано |
B |
Терапія пацієнтів із ПСА має бути спрямована на забезпечення найкращої допомоги та базуватися на спільному рішенні пацієнта і лікаря-ревматолога, з урахуванням ефективності, безпеки, вартості лікування та уподобання хворого |
|
C |
Ревматологи є фахівцями, які мають відповідати за лікування опорно-рухових проявів у пацієнтів із ПСА. За клінічно значущих уражень шкіри ревматолог і дерматолог повинні співпрацювати при діагностиці й терапії виявлених уражень |
Перефор-мульовано |
C |
Ревматологи є фахівцями, які мають переважно займатися лікуванням проявів із боку опорно-рухового апарату в пацієнтів із ПСА; за клінічно значущого ураження шкіри ревматолог і дерматолог повинні співпрацювати при діагностиці й терапії виявлених уражень |
|
D |
Основною метою лікування пацієнтів із ПСА є поліпшення якості життя шляхом контролю клінічних проявів захворювання, запобігання структурним пошкодженням, нормалізації функцій та соціальної участі. Усунення запалення є важливим компонентом досягнення цих цілей |
Без змін |
D |
Основною метою лікування пацієнтів із ПСА є максимізація якості життя, пов’язаної зі здоров’ям, шляхом контролю симптомів, запобігання структурним пошкодженням, нормалізації функцій і соціальної участі; усунення запалення є важливим компонентом для досягнення цих цілей |
|
E |
При лікуванні хворих на ПСА слід брати до уваги кожен прояв ураження опорно-рухової системи й ухвалювати відповідні рішення щодо терапії |
Без змін |
E |
При лікуванні хворих на ПСА слід брати до уваги кожен прояв ураження опорно-рухової системи і ухвалювати відповідні рішення щодо терапії |
|
F |
При лікуванні пацієнтів із ПСА необхідно враховувати позасуглобові прояви (ураження шкіри, очей та шлунково-кишкового тракту); також слід враховувати коморбідні стани, такі як метаболічний синдром, серцево-судинні захворювання або депресія |
Перефор-мульовано |
F |
При лікуванні пацієнтів із ПСА необхідно враховувати позасуглобові прояви (ураження шкіри, очей та із боку шлунково-кишкового тракту); слід також брати до уваги коморбідні стани, як-то ожиріння, метаболічний синдром, серцево-судинні захворювання або депресія |
|
– |
– |
Новий |
G |
При виборі лікування слід враховувати питання безпеки щодо індивідуальних механізмів дії для оптимізації співвідношення користі та ризику фармакологічної терапії |
|
Рекомендації |
||||
|
1 |
Лікування має бути спрямоване на досягнення ремісії або, як альтернатива, низької активності захворювання шляхом регулярної оцінки активності хвороби та відповідної корекції терапії |
Без змін |
1 |
Лікування має бути спрямоване на досягнення ремісії або, як альтернатива, на досягнення низької активності захворювання шляхом регулярної оцінки активності хвороби та відповідної корекції терапії |
|
2 і 3 |
НПЗП можуть бути використані для полегшення симптомів та ознак ураження опорно-рухового апарату. Місцеві ін’єкції глюкокортикоїдів слід розглядати як додаткову терапію при ПсА; системні глюкокортикоїди можна застосовувати з обережністю у найнижчій ефективній дозі |
Об’єднано та змінено |
2 |
НПЗП можуть бути використані для полегшення симптомів ураження опорно-рухової системи; місцеві ін’єкції глюкокортикоїдів можна розглядати як додаткову терапію |
|
4 і 5 |
У пацієнтів із поліартритом слід швидко розпочати терапію ХМАРП, надаючи перевагу метотрексату при клінічно значущих ураженнях шкіри. В осіб із поліартритом або моно-/олігоартритом та поганими прогностичними факторами (як-то структурні пошкодження, висока швидкість осідання еритроцитів / С-реактивний білок, дактиліт або ураження нігтів) слід розглянути терапію зсХМАРП |
Об’єднано та змінено |
3 |
У пацієнтів із поліартритом або моно-/олігоартритом та поганими прогностичними факторами (як-то структурні пошкодження, підвищені маркери гострої фази, дактиліт або ураження нігтів) слід якнайшвидше розпочати терапію зсХМАРП із наданням переваги метотрексату для пацієнтів із клінічно значущим ураженням шкіри |
|
6 |
У пацієнтів із периферичним артритом і недостатньою відповіддю на щонайменше один зсХМАРП слід розпочати терапію бХМАРП. Якщо є значуще ураження шкіри, перевагу можна надати інгібітору IЛ‑17 або IЛ‑12/23 |
Розділено на дві рекомен-дації |
4 |
У пацієнтів із периферичним артритом та неадекватною відповіддю на щонайменше один зсХМАРП слід розпочати терапію бХМАРП |
|
7 |
У пацієнтів із периферичним артритом і недостатньою відповіддю на щонайменше один зсХМАРП і один бХМАРП, або коли бХМАРП не підходить, слід розглянути іJAK |
Змінено |
5 |
У пацієнтів із периферичним артритом та неадекватною відповіддю на щонайменше один бХМАРП, або коли бХМАРП не підходить, слід розглянути можливість застосування іJAK з урахуванням питань безпеки |
|
8 |
У пацієнтів із легкою формою захворювання та неадекватною відповіддю на щонайменше один зсХМАРП, коли бХМАРП або іJAK не підходять, можна розглянути застосування інгібітора ФДЕ4 |
Без змін |
6 |
У пацієнтів із легкою формою захворювання та неадекватною відповіддю на щонайменше один зсХМАРП, коли бХМАРП або іJAK не підходять, можна розглянути застосування інгібітора ФДЕ4 |
|
9 |
У пацієнтів із чітко вираженим ентезитом та недостатньою відповіддю на НПЗП або місцеві ін’єкції глюкокортикоїдів слід розглянути терапію бХМАРП |
Без змін |
7 |
У пацієнтів із чітко вираженим ентезитом та недостатньою відповіддю на НПЗП або місцеві ін’єкції глюкокортикоїдів слід розглянути терапію бХМАРП |
|
10 |
У пацієнтів із переважно аксіальною формою захворювання з недостатньою відповіддю на НПЗП слід розглянути терапію бХМАРП, переважно іФНП. При значущому ураженні шкіри перевагу може бути надано інгібітору IЛ‑17 |
Змінено |
8 |
У пацієнтів із ПсА та клінічно значущим аксіальним ураженням і недостатньою відповіддю на НПЗП слід розглянути терапію інгібіторами ІЛ‑17A, ФНП, ІЛ‑17A/F або JAK |
|
– |
– |
Нова рекомен-дація |
9 |
При виборі препарату відповідно до механізму дії слід враховувати позасуглобові прояви, пов’язані з ПсА. За клінічно значущого ураження шкіри перевагу слід надавати інгібіторам IЛ‑17A або ІЛ‑17A/F, IЛ‑23 або IЛ‑12/23, за увеїту – анти-ФНП моноклональним антитілам, за ЗЗК – анти-ФНП моноклональним антитілам або інгібіторам IЛ‑23, IЛ‑12/23 чи JAK |
|
11 |
У пацієнтів із неадекватною відповіддю або непереносимістю бХМАРП слід розглянути перехід на інший бХМАРП або тсХМАРП, включно з однією зміною в межах класу |
Змінено |
10 |
У пацієнтів із неадекватною відповіддю чи непереносимістю бХМАРП або іJAK слід розглянути можливість переходу на інший бХМАРП або іJAK, включно з однією зміною в межах класу |
|
12 |
У пацієнтів зі стійкою ремісією можна розглянути поступове зниження дози ХМАРП |
Перефор-мульовано |
11 |
У пацієнтів зі стійкою ремісією можна розглянути зниження дози ХМАРП |
Загальні принципи
ПсА є гетерогенним і потенційно тяжким захворюванням, що може потребувати мультидисциплінарного підходу до лікування (без змін).
Хоча ПсА є потенційно тяжкою патологією, не у всіх пацієнтів розвиваються тяжкі форми захворювання (FitzGerald et al., 2021; Kerola et al., 2022). Мультидисциплінарний підхід до ведення осіб із ПсА є ефективним завдяки співпраці між лікарями різних спеціальностей та професіоналами галузі охорони здоров’я, які мають відповідний досвід (So et al., 2021; Wendling et al., 2022).
Терапія осіб, що страждають на ПсА, має бути спрямована на забезпечення найкращої допомоги та базуватися на спільному рішенні пацієнта і лікаря-ревматолога, з урахуванням ефективності, безпеки, вартості лікування та побажань хворого.
Цей загальний принцип був змінений порівняно із 2019 р. Було додано побажання пацієнта як елемент, який необхідно враховувати, і наголошено на важливості спільного ухвалення рішень для максимізації прихильності до лікування та його ефективності з одночасною мінімізацією ускладнень через неконтрольоване (активне) захворювання та можливі побічні ефекти препаратів (Smolen et al., 2019; Caso et al., 2020).
Ревматологи є фахівцями, які мають переважно займатися лікуванням проявів із боку опорно-рухового апарату в пацієнтів із ПсА; за клінічно значущого ураження шкіри ревматолог і дерматолог повинні співпрацювати при діагностиці й терапії виявлених уражень.
Лікарі-ревматологи забезпечують найкращий догляд за пацієнтами із ПсА на основі їхнього досвіду роботи із багатьма препаратами для терапії ревматичних та опорно-рухових захворювань, включно із важливими аспектами безпеки та наявністю супутніх патологій. Консультації з дерматологами, а іноді й іншими спеціалістами, можуть бути корисними в окремих клінічних ситуаціях.
Було зроблене незначне переформулювання, щоб наголосити на тому, що ураження шкіри є «клінічно значущим», а не «клінічно важливим» для більшої узгодженості з іншими пунктами рекомендацій.
Основною метою лікування пацієнтів із ПсА є максимізація якості життя, пов’язаної зі здоров’ям, шляхом контролю симптомів, запобігання структурним пошкодженням, нормалізації функцій і соціальної участі; усунення запалення є важливим компонентом для досягнення цих цілей (без змін).
Для отримання додаткової інформації дивіться оновлення рекомендацій 2019 р. (Gossec et al., 2020).
При лікуванні хворих на ПсА слід брати до уваги кожен прояв ураження опорно-рухової системи і ухвалювати відповідні рішення щодо терапії (без змін).
Для отримання детальнішої інформації дивіться оновлення 2019 р. (Gossec et al., 2020).
При лікуванні пацієнтів із ПсА необхідно враховувати позасуглобові прояви (ураження шкіри, очей та із боку шлунково-кишкового тракту); слід також брати до уваги коморбідні стани, як-то ожиріння, метаболічний синдром, серцево-судинні захворювання або депресія.
Формулювання «ожиріння» було додане, оскільки ожиріння часто зустрічається при ПсА і може впливати на результати лікування (Porta et al., 2020; Leung et al., 2023). Ожиріння пов’язане із надмірним відкладенням жиру в тілі, тоді як метаболічний синдром – це сукупність факторів ризику, які підвищують імовірність розвитку ССЗ та цукрового діабету 2-го типу. Ожиріння є суттєвим чинником розвитку метаболічного синдрому.
Депресія та інші можливі проблеми із психічним здоров’ям можуть впливати на вибір лікування. Центральна сенсибілізація до сприйняття болю часто зустрічається при ПсА і також впливає на результати терапії, що може ускладнювати менеджмент осіб із ПсА (Trouvin et al., 2022; Ballegaard et al., 2021).
При виборі лікування слід враховувати питання безпеки щодо індивідуальних механізмів дії для оптимізації співвідношення користі та ризику фармакологічної терапії (новий принцип).
Беручи до уваги нові дані щодо безпеки різних механізмів дії препаратів для лікування ПсА, цей новий загальний принцип було запропоновано, щоб підкреслити важливість урахування питань безпеки для кожного пацієнта (Ytterberg et al., 2022).
Рекомендації
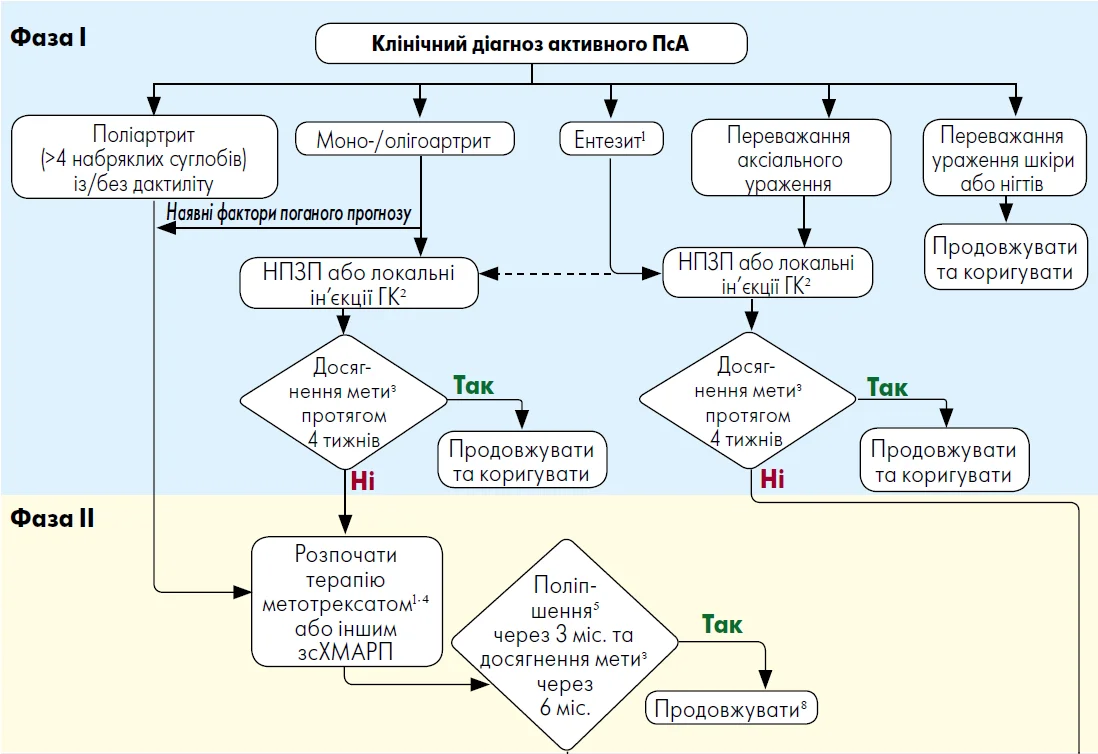
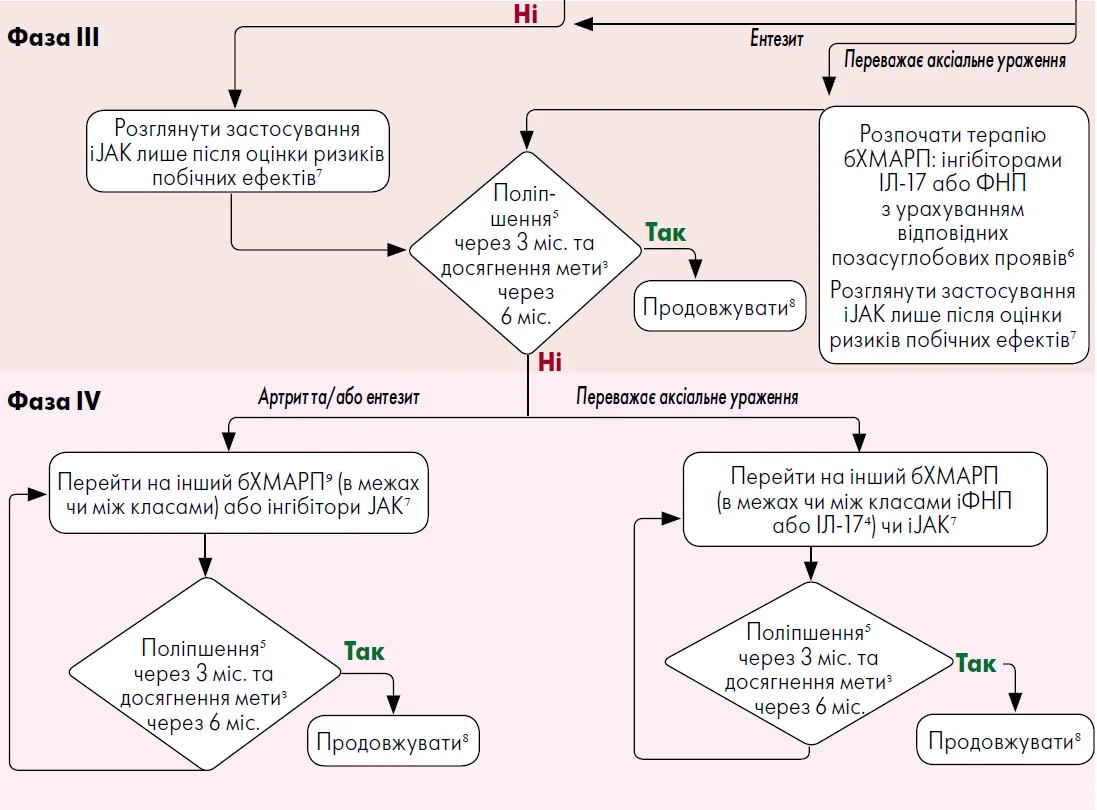
Дані рекомендації зосереджені на систематичному фармакологічному лікуванні; топічні та нефармакологічні методи терапії також важливі при ПсА, але не входять у представлений огляд. На рисунку (див. на стор. 21) наведений узагальнений алгоритм запропонованих варіантів лікування. Деякі питання безпеки будуть коротко висвітлені, але для повного розуміння профілю побічних ефектів різних препаратів слід ознайомитися з інструкціями щодо їх застосування.
Рисунок. Алгоритм рекомендацій EULAR 2023 р. для ведення пацієнтів із ПСА
Примітки: ˡ Деякі дослідження свідчать про те, що ентезит може відповідати на лікування метотрексатом, проте рівень доказовості низький. ² ГК не рекомендовані для лікування захворювання з переважанням аксіального ураження. ᶟ Метою лікування є досягнення ремісії або низької активності захворювання (особливо якщо воно тривале) відповідно до рекомендацій щодо лікування із досягненням терапевтичної мети. ⁴ Надається перевага у разі наявності виразних шкірних проявів патології, однак за супутніх ЗЗК або увеїту рекомендоване використання іФНП моноклональних антитіл або (для ЗЗК) інгібіторів IЛ‑23, або ІЛ‑12/23, або іJAK. ⁵ Поліпшення означає зменшення активності захворювання щонайменше на 50%. ⁶ Артрит/ентезит: інгібітори ФНП, або ІЛ‑17, або ІЛ‑12/23, або ІЛ‑23p19; шкіра: інгібітори ІЛ‑17, або ІЛ‑23p19, або ІЛ‑12/23, або іJAK; увеїт: іФНП моноклональних антитіл; ЗЗК: іФНП моноклональних антитіл, або ІЛ‑12/23, або ІЛ‑23p19, або іJAK; розглянути використання інгібіторів ФДЕ4 при легкому захворюванні, якщо бХМАРП та іJAK є недоцільними. ⁷ При застосуванні іJAK потрібна обережність у пацієнтів віком ≥65 років, курців у минулому чи теперішніх, з анамнезом атеросклеротичних серцево-судинних захворювань або інших СС-факторів ризику, з іншими чинниками ризику злоякісних новоутворень, а також із відомими факторами ризику венозної тромбоемболії. ⁸ Розглянути можливість поступового зменшення дози в умовах стійкої ремісії. ⁹ Включно з абатацептом.
! Лікування має бути спрямоване на досягнення ремісії або, як альтернатива, на досягнення низької активності захворювання шляхом регулярної оцінки активності хвороби та відповідної корекції терапії (1b, A).
Ця рекомендація (без змін) відповідає принципам лікування до досягнення мети (Smolen et al., 2018; Coates et al., 2015). Оскільки немає нових даних на підтримання підходу «лікування до мети» при ПсА, рівень доказовості та ступінь рекомендацій також залишаються без змін. Використання методів для оцінки активності захворювання було розглянуте в рекомендаціях щодо лікування до мети (Smolen et al., 2018). Визначення ремісії при ПсА залишається предметом дискусій (Hagеge et al., 2020; Landewе et al., 2021). Для контексту цих рекомендацій ремісія має розглядатися як усунення запалення.
Активність патології слід регулярно оцінювати для кожного окремого прояву (як-то суглоби, шкіра, ентезит, дактиліт, аксіальна форма), а корекція лікування залежатиме від переважання певного прояву захворювання у даний момент (Orbai et al., 2017).
! НПЗП можуть бути використані для полегшення симптомів ураження опорно-рухової системи (1b, A); місцеві ін’єкції глюкокортикоїдів (ГК) можна розглядати як додаткову терапію (3b, C).
Ця рекомендація стосується короткострокового симптоматичного лікування. Вона була розроблена шляхом об’єднання двох попередніх рекомендацій 2 та 3, в яких окремо розглядали НПЗП та ГК, оскільки обидва препарати призначені лише для короткострокового полегшення симптомів. Було прийняте рішення більше не згадувати системні ГК у пунктах, оскільки дані, що підтверджують їх призначення при ПсА, обмежені. Крім того, ГК мають багато потенційних побічних ефектів, особливо з урахуванням високої поширеності коморбідності та серцево-судинних (СС) факторів ризику при ПсА (Ferguson et al., 2019; Vincken et al., 2022). Однак в окремих випадках системне лікування ГК може бути корисним для деяких пацієнтів, особливо при поліартикулярних формах та/або як місткова терапія.
НПЗП забезпечують симптоматичне полегшення в осіб з опорно-руховими проявами, але не є ефективними при псоріазі. НПЗП та місцеві ін’єкції ГК є корисними для тимчасового полегшення симптомів та зниження місцевого запалення і можуть використовуватися в комбінації із ХМАРП за потреби. Однак необхідно враховувати аспекти безпеки, особливо за потенційно тривалого використання НПЗП.
Переважна більшість пацієнтів не мають отримувати лікування виключно НПЗП (без ХМАРП) відповідно до проактивного підходу до терапії ПсА до досягнення мети. Лише пацієнти із дуже легкою периферичною формою захворювання або переважно з ентезитом чи аксіальною формою можуть отримати достатню користь від монотерапії НПЗП.
Навіть у таких випадках використання симптоматичних засобів має зазвичай бути короткостроковим, наприклад, обмеженим чотирма тижнями. При периферичному артриті тривалість залежить від консенсусної думки науковців; за переважно аксіальної форми вона узгоджується з рекомендаціями Міжнародного товариства з оцінки спондилоартриту (ASAS) / EULAR для аксіального спондилоартриту (аксСпА), де активність захворювання після чотирьох тижнів лікування вважається відсутністю успіху терапії НПЗП (Ramiro et al., 2023). З іншого боку, для пацієнтів із переважно аксіальною формою патології, які мають значне зменшення клінічних симптомів, може бути запропоноване тривале використання НПЗП для контролю симптомів з урахуванням ризиків і переваг. Слід зазначити, що дані щодо ефективності НПЗП при ентезиті обмежені.
! У пацієнтів із поліартритом або моно-/олігоартритом та поганими прогностичними факторами (як-то структурні пошкодження, підвищені маркери гострої фази, дактиліт або ураження нігтів) (4, С) слід якнайшвидше розпочати терапію зсХМАРП із наданням переваги метотрексату для пацієнтів із клінічно значущим ураженням шкіри (1b, B).
Серед пацієнтів із периферичним артритом проводиться розрізнення залежно від кількості набряклих суглобів і прогностичних факторів (de Vlam et al., 2021; Kishimoto et al., 2021). У 2019 р. поліартрит та моно-/олігоартрит із поганими прогностичними маркерами розглядалися окремо, але для ясності ці пункти були об’єднані в оновленій настанові. Олігоартрит визначається як артрит (набряклі суглоби) до чотирьох суглобів включно (Gossec et al., 2020). Це формулювання стосується клінічної діагностики (а не візуалізації). Прогностичні фактори вже були визначені раніше і залишаються без змін (Gossec et al., 2020; Kerola et al., 2022).
Рекомендоване швидке призначення зсХМАРП паралельно (або майже одночасно) з початком симптоматичної терапії як для пацієнтів із поліартритом, так і з олігоартритом із поганими прогностичними факторами. Хворі на олігоартрит без поганих прогностичних факторів також мають отримувати зсХМАРП, але для них немає такої терміновості, враховуючи сприятливіший довгостроковий прогноз. Для пацієнтів даної когорти можна відкласти призначення зсХМАРП з імовірним використанням спершу тільки симптоматичного лікування.
Конкретної рекомендації для терапії дактиліту немає. Вважається, що дактиліт є комбінацією (оліго)синовіту, теносиновіту та ентезиту. Пацієнтів з ізольованим дактилітом слід лікувати подібно до осіб з олігоартритом. Лікування включає призначення ін’єкцій ГК у суглоби та зсХМАРП, які показали свою ефективність у полегшенні дактиліту (Vieira-Sousa et al., 2020).
Першим призначеним ХМАРП має бути зсХМАРП (метотрексат, лефлуномід або сульфасалазин). Продовження пріоритетності зсХМАРП відображає консенсусну думку експертів, які надали перевагу співвідношенню «користь – ризик – вартість» зсХМАРП, особливо метотрексату, над таргетними препаратами. Відсутність нових даних, які б вказували на користь б/тсХМАРП як першої лінії лікування, і наявність нових доказів щодо метотрексату підтвердили ефективність цього препарату при ПсА (Kerschbaumer et al., 2024; Coates et al., 2022).
У рекомендаціях EULAR йдеться про необхідність дотримання підходу «лікування до досягнення мети», що передбачає зниження активності захворювання щонайменше на 50% протягом трьох місяців та досягнення терапевтичних цілей протягом шести місяців. Відповідно, не слід продовжувати використання зсХМАРП, якщо терапевтичних цілей не досягнуто. У разі неефективності зсХМАРП рекомендовано призначити інший ХМАРП, наприклад бХМАРП. Загалом доцільно оцінювати ефективність зсХМАРП та ухвалювати рішення про його подальше застосування як монотерапії або ні через 12 тижнів відповідно до підходу «лікування до досягнення мети» (Smolen et al., 2018).
Хоча використання метотрексату при ПсА зазвичай ґрунтується на даних інших імуно-опосередкованих захворювань, як-от РА та псоріаз, також є дані щодо його ефективності при ПсА. При цьому нещодавні підтверджувальні дані обсерваційних та рандомізованих контрольованих досліджень свідчать про те, що частина пацієнтів позитивно реагуватиме на підвищення дози метотрексату (Smolen et al., 2023; Lindstrцm et al., 2023).
Баланс «ефективність – безпека» метотрексату слід регулярно оцінювати з огляду на загальний метаболічний профіль пацієнтів із ПсА, що може підвищувати ризик розвитку побічних ефектів, таких як гепатотоксичність (Wilsdon et al., 2019; Felten et al., 2022). Доза метотрексату має бути достатньою, зазвичай 20‑25 мг на тиждень (приблизно 0,3 мг/кг). Додатково рекомендоване використання фолатних добавок для зменшення побічних ефектів метотрексату (Liu et al., 2019).
Інші зсХМАРП (лефлуномід і сульфасалазин) є можливими варіантами лікування та продемонстрували ефективність за периферичного артриту при ПсА (Gossec et al., 2016). Недавнє дослідження ефекту комбінації метотрексату із лефлуномідом показало низьке співвідношення ефективності й безпеки, тому її застосування не рекомендоване (Mulder et al., 2022).
! У пацієнтів із периферичним артритом та неадекватною відповіддю на щонайменше один зсХМАРП слід розпочати терапію бХМАРП (1a, A).
Ця рекомендація стосується пацієнтів із периферичним артритом та охоплює як осіб із моно-/олігоартритом, так і поліартритом. Однак у випадках обмеженого периферичного ураження без поганих прогностичних факторів застосування другого курсу зсХМАРП перед початком терапії бХМАРП або тсХМАРП не є безпідставним, якщо це рішення погоджене між лікарем та пацієнтом.
У разі відсутності успіху лікування принаймні одним зсХМАРП, наступним кроком рекомендоване призначення одного із доступних бХМАРП (див. табл. 1) (Kerschbaumer et al., 2024).
Інгібітори JAK є дієвими при ПсА, але наразі співвідношення ефективності, безпеки, вартості та досвіду довготривалого застосування багатьох бХМАРП однозначно на користь останніх порівняно з іJAK. Наявність супутніх захворювань у багатьох пацієнтів із ПсА також схиляє експертів підтримати вибір бХМАРП.
Щодо бХМАРП, не обрано конкретного порядку застосування, оскільки жоден із бХМАРП не продемонстрував переваг щодо суглобового ураження над іншими бХМАРП (Mease et al., 2020; Gossec et al., 2022). У даній рекомендації вони перераховані у порядку номерів цитокінів, на які вони націлені, а не за пріоритетом. Однак інгібітори CTLA4 не вважаються хорошим варіантом через їх обмежену ефективність у клінічних випробуваннях (Mease et al., 2017). Ступінь рекомендації високий для цього пункту, що відображає накопичені надійні дані (McInnes et al., 2022).
На відміну від м’язово-скелетних проявів, для позасуглобових доменів ПсА є відмінності у порядку рекомендацій щодо бХМАРП (Kerschbaumer et al., 2024). У двох дослідженнях впливу бХМАРП при ПсА, в яких порівнювали інгібітор ІЛ‑17A з адалімумабом, було показано подібну ефективність щодо суглобів, але кращу відповідь шкіри на інгібітор ІЛ‑17A. Крім того, є дані, що свідчать про більший ефект бХМАРП порівняно з метотрексатом при псоріазі шкіри (Sbidian et al., 2023; McInnes et al., 2023).
Всі бХМАРП та іJAK показали ефективність щодо пригнічення рентгенографічного прогресування, однак такі дані відсутні для апреміласту.
Згідно з проведеним систематичним оглядом літератури, безпека різних категорій бХМАРП є прийнятною. Всі бХМАРП підвищують імовірність інфекцій (Kerschbaumer et al., 2024). Ризики використання іФНП добре відомі. Кандидоз (зазвичай слизово-шкірний) частіше виникає при інгібуванні ІЛ‑17A та ІЛ‑17A/F, особливо останнього (McInnes et al., 2023; Merola et al., 2023). Інгібітори ІЛ‑23-p19 є новішим доповненням до арсеналу лікування, але їх безпека виглядає задовільною, аналогічно устекінумабу, який також впливає на ІЛ‑23 (р40 ланцюг), профіль побічних ефектів якого добре відомий і задовільний (Kerschbaumer et al., 2024).
Загалом при ухваленні рішення про призначення нового лікарського засобу необхідно враховувати безпеку та коморбідність для кожного пацієнта окремо. Повніша інформація щодо аспектів безпеки бХМАРП надається в інструкції до препарату. На вартість також слід звертати увагу, але вона може варіювати залежно від країни. У багатьох країнах економія коштів відбувається завдяки наявності біосимілярів іФНП та потенційно інших біосимілярів у майбутньому.
Персоналізована медицина для полегшення оптимального вибору першого бХМАРП наразі складна через відсутність індивідуалізованих предикторів відповіді на лікування (Miyagawa et al., 2019). Як уже обговорювалося, важливо враховувати фенотип пацієнта та можливі позасуглобові ознаки. Також слід зважати на коморбідність у пацієнта (Leung et al., 2023; Drosos et al., 2022). Необхідно більше досліджень щодо предикторів відповіді на препарати, включно із впливом статі (Tarannum et al., 2022; Orbai et al., 2020).
Комбінація бХМАРП із зсХМАРП. Перші бХМАРП часто призначали у комбінації із зсХМАРП, таким як метотрексат (Lindstrоm et al., 2023). Однак дані щодо додаткової користі від одночасного застосування метотрексату з таргетними ХМАРП у пацієнтів із периферичним захворюванням суперечливі, до того ж немає доказів користі метотрексату в осіб з аксіальними симптомами (Ramiro et al., 2023).
Комбінацію метотрексату із бХМАРП вивчали переважно для іФНП. Дослідження показали подібну ефективність із/без супутнього використання метотрексату. Хоча в деяких дослідженнях при використанні метотрексату було виявлено більшу тривалість дії (Lindstrоm et al., 2023; Fagerli et al., 2014). Дані нещодавнього великого дослідження продемонстрували підвищення частоти ремісій за комбінованої терапії іФНП та метотрексатом (Lindstrцm et al., 2021).
Щодо механізмів дії інших фармакологічних засобів, даних для підтримки комбінацій недостатньо. Загалом рекомендовано поєднувати перший бХМАРП із раніше призначеним зсХМАРП у всіх випадках, коли таке лікування добре переносилося пацієнтом, особливо коли першим бХМАРП був іФНП.
! У пацієнтів із периферичним артритом та неадекватною відповіддю на щонайменше один бХМАРП, або коли бХМАРП не підходить (4, D), слід розглянути можливість застосування іJAK з урахуванням питань безпеки (1b, B).
Ця рекомендація викликала багато обговорень. З одного боку, із 2019 р. було отримано нові дані про ефективність іJAK, зокрема, опубліковані позитивні результати досліджень упадацитинібу при ПсА (McInnes et al., 2021). З іншого боку, наразі існує глобальне застереження, випущене як Управлінням із контролю за якістю харчових продуктів і медикаментів (FDA), так і Європейським агентством із лікарських засобів (EMA). Воно обмежує використання іJAK для всіх захворювань, включно із ПсА, на основі підвищеної ймовірності онкологічних і СС-подій, виявлених у пацієнтів похилого віку з РА та факторами СС-ризику при застосуванні тофацитинібу (Ytterberg et al., 2022; EMA, 2023; FDA, 2023).
Інгібітори JAK призводять до підвищення загальної частоти інфекцій приблизно на такому ж рівні, як і бХМАРП, але з більшою кількістю випадків герпесу (herpes zoster) (Kerschbaumer et al., 2024). Безпека застосування тофацитинібу й упадацитинібу в контексті ПсА нещодавно була оцінена й виглядала позитивно. Однак спостереження було коротким, тому потрібне проведення подальших досліджень (Burmester et al., 2023; Mease et al., 2020).
Хоча наразі дані тривалих випробувань не показують підвищеного СС-ризику або онкології, пов’язаних із використанням іJAK при ПсА, подібних до дослідження ORAL-Surveillance при ПсА наразі немає. Тому обмеження терапії іJAK при РА також повинні застосовуватися до ПсА, особливо зважаючи на те, що важливі для профілю ризику іJAK коморбідності можуть бути поширенішими при ПсА, ніж РА (наприклад, ожиріння та фактори СС-ризику). З іншого боку, контроль запалення важливий для зниження СС-ризику.
Співвідношення ефективності й безпеки для іJAK не забезпечує їм місце поряд із бХМАРП для черговості вибору (тобто не можна пропонувати іJAK як звичайне лікування після неадекватної відповіді та/або непереносимості терапії зсХМАРП). Тому іJAK зазвичай застосовується як таргетна терапія другої лінії (або ХМАРП третьої лінії).
Варто зазначити, що для деяких пацієнтів іJAK можуть бути оптимальним варіантом після зсХМАРП; це відображено у формулюванні в рекомендації «коли бХМАРП не підходить». Ця «непридатність» може включати протипоказання до бХМАРП, практичні питання, що сприяють наданню переваги пероральним препаратам (як-то відсутність умов для належного зберігання за контрольованих температур), а також уподобання пацієнта, включно з імовірністю незадовільної прихильності до ін’єкцій (відповідно до першого загального принципу щодо спільного ухвалення рішень). Проте хворі мають зважувати свої побажання із потенційними ризиками.
Ступінь рекомендації для цього пункту був низьким, особливо щодо питань безпеки, оскільки докази для ПсА обмежені, та вона базувалася на даних пацієнтів із РА. Запропоновано застосовувати іJAK після невдалої терапії бХМАРП, оскільки наразі доступні кілька нових бХМАРП зі сприятливим впливом на шкірні ураження та відносно хорошими даними щодо безпеки (інгібітори IЛ‑23, IЛ‑17), до того ж потрібні додаткові довготривалі дані щодо ефективності та безпеки іJAK при ПсА.
Нині препарати, що інгібують тирозинкіназу 2 (TYK2), перебувають на етапі оцінки при ПсА. Вони поки не схвалені для використання, і дані щодо безпеки обмежені, зокрема при псоріазі, де така терапія вже ліцензована. Тому інгібітори TYK2 не були включені до поточних рекомендацій.
! В осіб із легкою формою захворювання та неадекватною відповіддю на щонайменше один зсХМАРП, коли бХМАРП або іJAK не підходять, можна розглянути застосування інгібітора ФДЕ4 (1b, B)
Ця рекомендація залишилася без змін із 2019 р. Термін «легка форма захворювання» застосовується за наявності олігоартриту або ентезиту без поганих прогностичних факторів та з обмеженим ураженням шкіри (Gossec et al., 2020; Mease et al., 2023). Дані дослідження FOREMOST нещодавно підтвердили ефективність апреміласту за олігоартриту у хворих на ПсА (Mease et al., 2023). Однак причина, чому апреміласт посідає окреме місце порівняно із бХМАРП або іншими тсХМАРП, полягає не лише у відносно нижчій ефективності, але й у відсутності даних про структурну ефективність (що ставить під сумнів термін «ХМАРП», оскільки немає даних про сповільнення прогресування пошкоджень).
Застосування апреміласту в поєднанні з іФНП є позаліцензійним і дорожчим без підтримувальних даних, тому не може бути рекомендованим.
! У пацієнтів із чітко вираженим ентезитом та недостатньою відповіддю на НПЗП або місцеві ін’єкції ГК слід розглянути терапію бХМАРП (1b, B).
Цей пункт залишається без змін. Чітко виражений ентезит стосується підтвердженого запалення в ентезах (що може потребувати додаткової діагностичної візуалізації) для уникнення надмірного лікування болю в ентезах, не пов’язаного із ПсА (наприклад, у контексті синдромів поширеного болю або повторюваного механічного стресу) (Schett et al., 2017; Marchesoni et al., 2018). Було проведене активне обговорення нових даних, які вказують на непряму ефективність метотрексату при ентезиті (Kerschbaumer et al., 2024; Mulder et al., 2022). Однак наявні на сьогодні докази недостатньо переконливі, щоб пропонувати метотрексат у цьому пункті. Своєю чергою метотрексат може бути варіантом лікування для деяких пацієнтів з ентезитом.
У разі чітко вираженого переважання ентезиту при ПсА пропонується призначати бХМАРП (без переваги конкретного механізму дії), оскільки всі схвалені на сьогодні бХМАРП продемонстрували однакову ефективність при ентезиті, хоча порівняльні дослідження відсутні (Kerschbaumer et al., 2024). Тут вартість може мати значення, але також слід враховувати інші прояви. Слід зазначити, що хоча тсХМАРП не згадані безпосередньо в цьому пункті, вони є варіантом у деяких випадках ентезиту (завжди з урахуванням співвідношення користі й ризику, зокрема для іJAK) (EMA, 2023; FDА, 2023).
! У пацієнтів із ПсА із клінічно значущим аксіальним ураженням і недостатньою відповіддю на НПЗП слід розглянути терапію інгібіторами ІЛ‑17A, ФНП, ІЛ‑17A/F або JAK (1b, B).
Формулювання для аксіального ураження було змінене із «переважного» на «клінічно значуще». Згідно із нещодавно оновленими рекомендаціями ASAS/EULAR, у разі аксіального захворювання застосування зсХМАРП є недоречним (Ramiro et al., 2023). Препаратами вибору є бХМАРП, що націлені на ФНП, ІЛ‑17A, ІЛ‑17A/F, а також тсХМАРП, які інгібують JAK. Для іJAK слід враховувати питання безпеки. Важливо зазначити, що рекомендовано обирати між перерахованими групами ліків, а не використовувати їх комбінацію.
Для цієї рекомендації порядок перерахування препаратів має значення, оскільки інгібування ІЛ‑17A було зазначене першим через наявність єдиного на даний час дослідження MAXIMISE, в якому вивчали ефективність секукінумабу саме у пацієнтів із ПсА з аксіальним ураженням (Baraliakos et al., 2021). Отже, рівень доказовості для інгібування ІЛ‑17A сильніший, ніж для інших препаратів, дані для яких отримані з досліджень аксСпА (Ramiro et al., 2023).
Інші препарати перераховані з інгібуванням ФНП на першому місці через наявність довгострокових даних щодо безпеки, потім ідуть інгібітори ІЛ‑17A/F, які нещодавно отримали ліцензію для аксСпА, та іJAK як варіант з урахуванням питань безпеки. іJAK пропонуються у тій самій рекомендації, що й бХМАРП; це підтверджує, що профілі коморбідності хворих на переважно ПсА з аксіальним ураженням або ізольованим аксіальним ураженням при ПсА є більш схожими на осіб з аксСпА. Тому іJAK у пацієнтів з аксіальними ураженнями можуть мати сприятливіший профіль безпеки щодо онкологічних і СС-ризиків порівняно із багатьма хворими на переважно периферичний артрит.
Також обговорено непрямі дані щодо можливої ефективності інгібування ІЛ‑23 при аксіальному ПсА. Однак, зважаючи на негативні результати досліджень щодо інгібування ІЛ‑12/23 при аксСпА, препарати ІЛ‑23 таким пацієнтам не рекомендовані (Ramiro et al., 2023; Mease et al., 2021).
! При виборі препарату відповідно до механізму дії слід враховувати позасуглобові прояви, пов’язані з ПсА. За клінічно значущого ураження шкіри перевагу слід надавати інгібіторам IЛ‑17A або ІЛ‑17A/F, IЛ‑23 або IЛ‑12/23, за увеїту – анти-ФНП моноклональним антитілам, за ЗЗК – анти-ФНП моноклональним антитілам або інгібіторам IЛ‑23, IЛ‑12/23 чи JAK (1b, B).
Це нова рекомендація, яка чіткіше, ніж у 2019 р., пояснює, що при виборі препарату слід враховувати не лише фенотип ПсА, але й позасуглобові прояви.
Першою позасуглобовою маніфестацією, на яку звертають увагу при ПсА, є псоріаз шкіри. Хоча у більшості пацієнтів із ПсА відзначається псоріаз шкіри або псоріаз в анамнезі, дані реєстрів вказують, що багато осіб із ПсА мають легкі ураження шкіри (Ogdie et al., 2022). Однак навіть обмежений псоріаз шкіри може бути проблематичним, оскільки клінічно значуще ураження шкіри визначається як обширне (ураження понад 10% поверхні тіла) або вагоме для пацієнта, тобто таке, що негативно впливає на якість життя (наприклад, ураження обличчя або геніталій) (Gossec et al., 2020). Для таких хворих рекомендовано розглядати препарати, націлені на шляхи ІЛ‑17A, ІЛ‑17A/F або ІЛ‑23 (тут порядок ліків вказаний за номером цитокіну, а не за пріоритетом).
Потужні дані, зокрема порівняльних досліджень, стосовно псоріазу шкіри показують, що препарати, націлені на шляхи ІЛ‑23 та ІЛ‑17, перевершують іФНП та іJAK для лікування псоріазу шкіри (Sbidian et al., 2022; Sbidian et al., 2023). Наявні докази обґрунтовують використання ліків із такими механізмами дії переважно у випадках значущого ураження шкіри. Це узгоджується з рекомендаціями щодо псоріазу (Menter et al., 2019).
Увеїт не такий частий при ПсА, як в осіб із аксСпА, із поширеністю близько 5% (Pittam et al., 2020). Однак увеїт може бути тяжким, що впливає на вибір лікування. На сьогодні єдиним механізмом дії з прямими доказами ефективності при увеїті є інгібування ФНП через моноклональні антитіла (як в адалімумабу й інфліксимабу). Тому для пацієнтів з увеїтом слід надавати перевагу анти-ФНП моноклональним антитілам.
ЗЗК зустрічаються у 2‑4% пацієнтів із ПсА (Pittam et al., 2020). Арсенал лікування ЗЗК нещодавно розширився, тому рекомендовано використовувати препарати, затверджені для ЗЗК у разі його поєднання із ПсА. Станом на середину 2023 р., схвалені для лікування ЗЗК препарати включають анти-ФНП моноклональні антитіла (адалімумаб й інфліксимаб), інгібітор ІЛ‑12/23 устекінумаб, інгібітор ІЛ‑23 рисанкізумаб (для хвороби Крона) і два іJAK (один з яких, тофацитиніб, тільки для хвороби Крона) (Danese et al., 2022; Loftus et al., 2023). Інгібітори ІЛ‑17 (як A, так і A/F) не рекомендовані при активному ЗЗК, оскільки є дані щодо підвищеного ризику загострень (Letarouilly et al., 2022; Emond et al., 2019).
Рішення для пацієнтів із вагомим ураженням шкіри, увеїтом або ЗЗК мають обговорюватися із відповідними фахівцями, якщо це необхідно. В усіх випадках потрібно керуватися поточними авторизаціями препаратів, а також враховувати питання безпеки та коморбідностей. Для визначення порядку вибору ліків рекомендовано спочатку зважати на підтип ПсА, а потім – на позасуглобові прояви (завжди з огляду на безпеку й коморбідності).
! У пацієнтів із неадекватною відповіддю або непереносимістю бХМАРП чи іJAK слід розглянути можливість переходу на інший бХМАРП або іJAK (1b, С), включно з однією зміною в межах класу (4, C).
Ця рекомендація не змінилася (Gossec et al., 2020). Після невдалого застосування одного таргетного засобу логічно перейти на інший препарат даної групи. Наразі немає переконливих даних на підтвердження переваги зміни механізму дії перед зміною в межах того ж механізму. Варто зазначити, що ця рекомендація не обмежує загальну кількість змін для певного пацієнта. Це також не означає, що не можна зробити більше змін у межах одного класу, але практичні результати показують, що не обов’язково змінювати препарат після невдалого використання одного медикаменту із даного класу. Зміни можуть бути здійснені, як належить, між бХМАРП, або між бХМАРП та іJAK.
Рекомендованим варіантом лікування є абатацепт (Mease et al., 2017). Однак він продемонстрував помірний ефект, тому має використовуватися лише після невдалої терапії одним або більше інших таргетних препаратів. Ефективність подвійного інгібітора ІЛ‑17A/F бімекізумабу була подібною у популяціях із/без застосування іФНП, але це ще потребує підтвердження (McInnes et al., 2023; Merola et al., 2023). Комбінування бХМАРП наразі досліджується, і на даний час не може бути рекомендоване.
! У пацієнтів зі стійкою ремісією можна розглянути поступове зниження дози ХМАРП (2b, В).
Цей пункт не змінився. Однак накопичено більше даних щодо зниження доз, що привело до підвищення рівня рекомендації (Coates et al., 2021; Ruwaard et al., 2023). Важливо зазначити, що «зниження дози» не передбачає повне припинення приймання препарату, оскільки це може призвести до загострень. Зменшення дози є логічним кроком, коли хворий тривалий час почувається добре, як з погляду безпеки, так і економії коштів (пацієнт часто сам знижує дозу).
З іншого боку, відсутні довгострокові дані, і наразі зниження дози є позаліцензійною практикою. Тому в рекомендації вказане обережне формулювання «можна розглянути» (з метою наголошення, що це не є обов’язковим) і, звісно, у контексті спільного ухвалення рішення з пацієнтом (це також стосується інших рішень щодо лікування).
Висновки
В оновленій настанові щодо лікування ПсА представлені всі наявні на даний час препарати та рекомендований порядок їх застосування з урахуванням фенотипу опорно-рухових і позасуглобових проявів при ПсА.
Оновлення 2023 р. є значним, оскільки більшість рекомендацій було суттєво змінено. Із 2019 р. багато нових ліків стали доступними для лікування ПсА. Вибір препарату для конкретного пацієнта залежить від даних щодо ефективності, клінічного фенотипу, профілю ризику побічних ефектів, переносимості, віддалених наслідків, вартості та доступу до медикаментів. Хоча лабораторні біомаркери для стратифікованого підходу до терапії відсутні, було використано клінічні маркери для розробки клінічних фенотипових переваг для конкретних препаратів. Оновлені рекомендації також спираються на думку експертів щодо наявних даних, щоб запропонувати прагматичний, логічний поетапний підхід до таргетних методів лікування ПсА.
Препарати, розглянуті в настанові, наразі ліцензовані для терапії ПсА. Сьогодні також доступні й інші ліки, які або проходять випробування, або доступні для лікування інших споріднених захворювань, особливо псоріазу шкіри, однак їх розгляд виходить за межі цих рекомендацій. Наприклад, бродалумаб був схвалений лише для застосування при псоріазі, інгібітори TYK2, такі як деукравацитиніб та брепоцітиніб, також розроблені для терапії псоріазу шкіри та ПсА, ізокібеп є новим міметиком антитіл, слабким інгібітором ІЛ‑17, який наразі проходить тестування, також у розробці знаходиться пероральний інгібітор ІЛ‑23 (Kerschbaumer et al., 2024).
Активно обговорювалося місце іJAK у рекомендаціях (McInnes et al., 2021; Nash et al., 2021). Важливо дотримуватися обережності та високих стандартів безпеки при призначенні препаратів із коротким або середньостроковим досвідом застосування, з обмеженими даними щодо тривалого використання, особливо для ПсА. Такий обережний підхід також був наявний у рекомендаціях 2019 р., і подальші розробки щодо безпеки підтвердили його доцільність (EMA, 2023; FDA, 2023). Важливо продовжувати моніторинг препаратів і, за можливості, проводити контрольовані дослідження, оскільки необхідні надійні дані високого рівня.
Вартість лікарських засобів також є важливим аспектом ведення пацієнтів, та зазвичай рекомендовано призначати дешевший, якщо два препарати мають подібну ефективність і безпеку. Зокрема, навіть якщо один механізм дії демонструє дещо кращу ефективність щодо певних проявів, менш дорогий медикамент може мати переваги, якщо його ефективність у цій галузі не набагато нижча.
Біосиміляри доступні для кількох іФНП і привели до значного зниження витрат та широкого використання у багатьох країнах. Незабаром тофацитиніб і апреміласт стануть генеричними, що також зменшить їх вартість і дозволить ширше застосовувати, особливо у країнах із меншими ресурсами. Загалом при призначенні препаратів слід враховувати співвідношення ефективності, безпеки та вартості відповідно до загальних принципів та рекомендацій, які узагальнені в алгоритмі (див. рис.) (Tarannum et al., 2023).
Оновлені рекомендації 2023 р. щодо лікування ПсА будуть корисними як для клініцистів, так і для пацієнтів при обговоренні варіантів лікування. Вони також можуть поліпшити доступ до оптимальної медичної допомоги.
Підготувала Ірина Климась
Оригінальний текст документа читайте на сайті www.eular.org
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 4 (101) 2025 р.