2 березня, 2026
Кристалізація доказів, частина І. Роль сечової кислоти в кардіоренальній патології
Сечова кислота: еволюційна спадщина з подвійним біологічним значенням
Сечова кислота (СК) – кінцевий продукт катаболізму пуринів у людини, утворюється внаслідок як ендогенного розпаду нуклеїнових кислот, так і надходження екзогенних пуринів, зокрема при споживанні продуктів, багатих на тваринний білок і фруктозу. Основна роль у її синтезі належить печінковому ферменту ксантиноксидазі, проте свій внесок роблять і кишечник, нирки, м’язи та судинний ендотелій [1-3]. У фізіологічних умовах СК циркулює у вигляді розчинної натрієвої солі в позаклітинному середовищі, залишаючись ізольованою в пероксисомах [4]. Коли рівень СК у сироватці перевищує поріг розчинності 6,8 мг/дл, формуються кристали моноурату натрію (МУН), передусім у тканинах з нижчою температурою або в кислому середовищі. Саме ці кристали провокують запальні реакції, типові для подагри [5, 6]. Стрес, уживання алкоголю, гіпоксія, лактатацидоз також спричиняють кристалізацію. Кристали МУН можуть індукувати специфічну імунну відповідь з утворенням антитіл, які посилюють їхню агрегацію [7].
На відміну від більшості ссавців люди й інші людиноподібні примати втратили фермент уриказу, який перетворює СК на розчинніший алантоїн. Ця мутація відбулася приблизно 15 млн років тому, і в результаті рівень СК у крові людини еволюційно стабілізувався на вищому рівні [8, 9]. Імовірно, цей механізм мав адаптивне значення в доісторичному середовищі, допомагаючи регулювати артеріальний тиск (АТ) і забезпечувати ефективне збереження енергії. Проте в умовах сучасного харчування, багатого на пурини та фруктозу, ця спадковість стає патогенетичним чинником [9, 10]. Сьогодні гіперурикемія (ГУ) є визнаним фактором ризику ожиріння, інсулінорезистентності, артеріальної гіпертензії (АГ) та серцево-судинних захворювань (ССЗ). Водночас у популяціях із традиційним способом життя, як-от південноамериканські племена яномама, рівень СК залишається значно нижчим – ближчим до рівня в ссавців з активною уриказою [11].
СК має й захисні властивості: вона діє як потужний антиоксидант, регулює запальні сигнали та сприяє функції ендотеліальних прогеніторних клітин [12]. Спадкові форми гіпоурикемії, зокрема при мутаціях у гені SLC22A12 (кодує уратний транспортер‑1 – URAT1), пов’язані із судинною дисфункцією, що свідчить про важливість підтримання балансу СК [13]. Проте хронічне підвищення її рівня спричиняє системне запалення, активацію ренін-ангіотензинової системи (РАС) і порушення ендотеліальної функції [12].
Новітні транскриптомні дослідження показали, що різні популяції клітин ниркових канальців залучені в реабсорбцію й секрецію СК, причому ці процеси не перетинаються [14]. Патогенетична дія СК не обмежується утворенням кристалів: кристали МУН активують рецептори розпізнавання патернів (наприклад, Toll-подібні рецептори) й інфламасоми NLRP3 [15]. У макрофагах МУН призводить до зниження рівня окисленої форми нікотинамідаденіндинуклеотиду (NAD+) через активацію CD38, що посилює запалення; цей ефект можна зменшити за допомогою інгібіторів CD38 [15]. В ендотеліальних клітинах підвищені рівні СК порушують автофагію та спричиняють апоптоз; ці ефекти пом’якшує гідроксихлорохін шляхом відновлення контролю якості мітохондрій [16].
Цікавим є й той факт, що спосіб утворення кристалів МУН впливає на їхню імуногенність: зокрема, кристали, сформовані в лужному середовищі, спричиняють потужнішу запальну відповідь, аніж ті, які утворюються в нейтральних чи кислих умовах [17].
Отже, СК – це молекула з подвійною природою, що може діяти як захисник і як провокатор патологічного процесу. Її біологічні ефекти – від ендотеліальної дисфункції до активації вродженого імунітету – охоплюють різні фізіологічні системи, формуючи основу для розуміння її подвійної ролі для збереження здоров’я та розвитку хвороб (рис.).
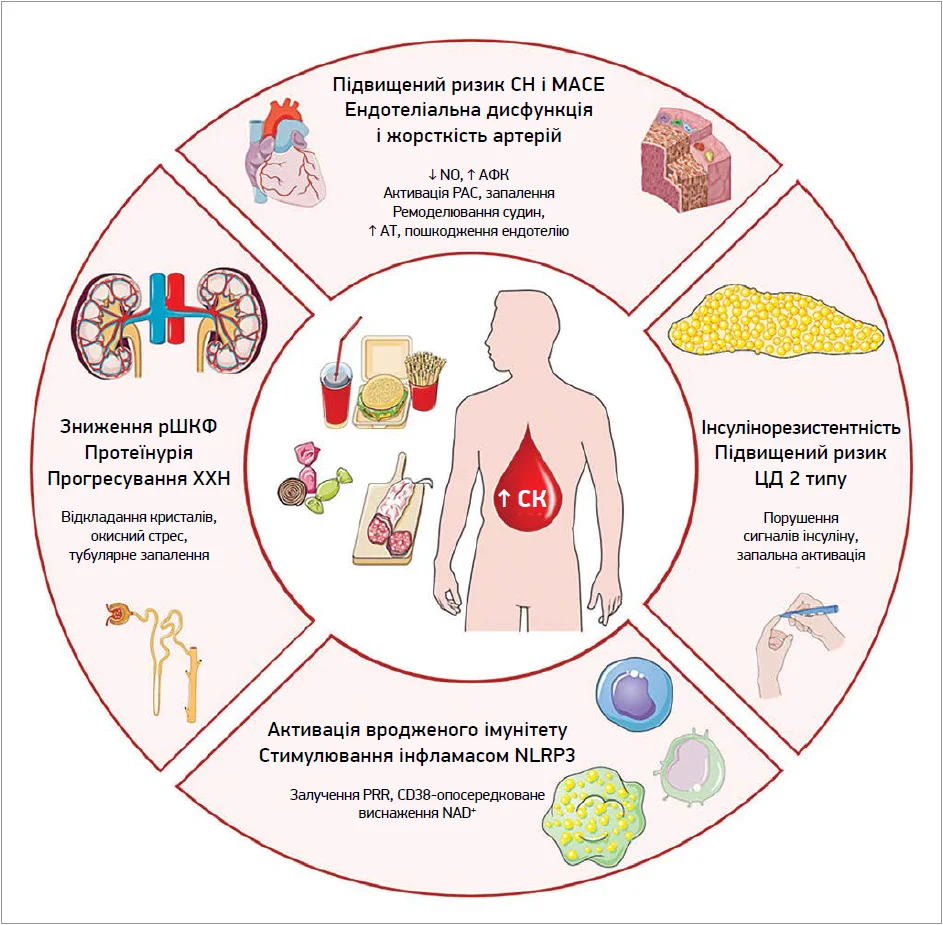 Рис. Кардіоренальні ризики гіперурикемії
Рис. Кардіоренальні ризики гіперурикемії
Примітки: СН – серцева недостатність; МАСЕ – великі серцево-судинні події; АФК – активні форми кисню; РАС – ренін-ангіотензинова система; АТ – артеріальний тиск; ЦД – цукровий діабет; PRR – патерн-розпізнавальні рецептори; NAD+ – окислена форма нікотинамідаденіндинуклеотиду; рШКФ – розрахункова швидкість клубочкової фільтрації; ХХН – хронічна хвороба нирок.
«Судинне обличчя» сечової кислоти: друг, ворог чи й те, й інше?
СК, яку довго вважали інертним кінцевим продуктом пуринового обміну, нині постає як активний чинник судинної патології. Її вплив виходить далеко за межі подагри: СК модулює запальні процеси, окисний стрес, порушення функції ендотелію та ремоделювання судинної стінки – ключові механізми в прогресуванні ССЗ [18].
Однією з мішеней СК є гладком’язові клітини (ГМК) судин, у які вона проникає та спричиняє гіпертрофію й експресію прозапальних молекул [19, 20]. Ці зміни зумовлюють підвищення жорсткості артерій і АТ. Експериментальні дані демонструють: СК стимулює проліферацію ГМК і посилює сигнальні шляхи РАС, що ще більше посилює судинозвужувальні та прозапальні ефекти [21].
Особливо вразливим до підвищених рівнів СК є судинний ендотелій. Хронічна ГУ порушує інсулінозалежну передачу сигналів в ендотеліальних клітинах: СК пригнічує активацію інсулінових субстратів і сигнального шляху фосфоінозитид‑3-кінази / протеїнкінази В (PI3K/Akt), що призводить до зменшення активності ендотеліальної NO-синтази (eNOS) і дефіциту оксиду азоту (NO) [22]. Це погіршує вазодилатацію, спричиняє інсулінорезистентність і формує патогенетичний ланцюг, що об’єднує ГУ, ендотеліальну дисфункцію та метаболічні порушення [22].
Додатковий патогенетичний вплив має ксантиноксидаза, яка відповідає за утворення СК. Підвищена активність цього ферменту супроводжується накопиченням активних форм кисню (АФК), що ушкоджують ендотелій, посилюють запалення, спричиняють розвиток АГ й атеросклерозу. Водночас інгібітори ксантиноксидази, передусім фебуксостат, зменшують окисний стрес і покращують судинну функцію [23].
Найбільше судинна токсичність СК проявляється в пацієнтів із хронічною хворобою нирок (ХХН), за якої зниження кліренсу призводить до накопичення СК і сечових токсинів. Останні активують шляхи, залучені до ушкодження ендотелію, зокрема АФК, мітоген-активовані протеїнкінази (MAPK), ядерний фактор κВ (NF-κB) та рецептори кінцевих продуктів глікації (RAGE), спричиняючи адгезію лейкоцитів, апоптоз ендотелію та протромботичні зміни [24].
У цьому контексті з’являється нова концепція – «судинна подагра», яка передбачає, що навіть розчинна СК може проникати в ендотеліальні та гладком’язові клітини, змінюючи їхній метаболізм і епігенетичні механізми [18]. Результатом стає хронічне субклінічне запалення й феномен «натренованого» імунітету, що підтримує судинне ушкодження навіть за відсутності кристалів. Підтвердженням служать клінічні дані: зниження рівня СК, особливо в комбінації з колхіцином, покращує ендотеліальну функцію та знижує частоту серцево-судинних ускладнень у пацієнтів з ішемічною хворобою серця (ІХС) [18].
Водночас надмірне зниження СК може мати зворотний ефект. У дослідженнях за участю пацієнтів із серцевою недостатністю (СН) виявлено нелінійний U-подібний зв’язок між рівнем СК і судинною реактивністю: найкращі результати спостерігалися при середніх концентраціях СК, а надто високі, як і надто низькі рівні асоціювалися з погіршенням ендотеліальної функції [25].
Додаткові дані отримано при дослідженні пацієнтів похилого віку із цереброваскулярними та метаболічними хворобами, зокрема при гострому ішемічному інсульті, судинній деменції чи цукровому діабеті (ЦД) 2 типу [26]. Виявлені зміни маркерів ендотеліального відновлення (CD31, CD34, CD144) і порушення регуляції імунітету (зокрема підвищення Th17-подібних клітин) свідчать про хронічне ураження мікросудин і виснаження регенеративних резервів [27]. Цікаво, що скелетні м’язи беруть активну участь у метаболізмі пуринів і виробленні СК, а сам ендотелій також є важливим джерелом СК. Отже, стратегії, спрямовані на відновлення функції ендотеліальних прогеніторних клітин, можуть стати новим напрямом профілактики судинних і неврологічних ускладнень ГУ [27].
Сьогодні СК уже не можна вважати лише «метаболічними відходами» чи тригером подагри. Це багатофункціональний медіатор, який впливає на проліферацію ГМК, інсулінову сигналізацію в ендотелії, рівень окисного стресу та підтримує хронічне запалення. Розуміння цього складного спектра ефектів кардинально змінює підходи до лікування ГУ: завдання полягає не лише в запобіганні подагрі, а й у зменшенні системного судинного ризику. Найефективнішим видається індивідуалізований підхід до контролю рівня СК з огляду на клінічний контекст, залучені органи-мішені та супутні хвороби.
Серцево-судинні ризики гіперурикемії
Накопичені наукові дані переконливо свідчать: підвищений рівень сироваткової СК (ССК) є не просто маркером, а активним учасником патогенезу ССЗ. Його роль реалізується через кілька взаємопов’язаних механізмів: ендотеліальну дисфункцію, окисний стрес, системне запалення та порушення функції нирок, які відіграють ключову роль у формуванні несприятливих серцево-судинних подій [28].
Клінічно ГУ чинить шкідливу дію на різні органи-мішені, проте найпереконливіші асоціації зафіксовано при ІХС і цереброваскулярній патології [31-33].
Великі когортні дослідження підтверджують існування прямого зв’язку між зростанням ССК і ризиком серцево-судинних подій. Наприклад, у дослідженні Rotterdam Study було продемонстровано чітку прогресивну залежність між рівнем ССК і частотою розвитку ІХС, інфаркту міокарда й інсульту [34]. Цікаво, що ризик проявлявся вже при рівнях ССК, нижчих за поріг, традиційно визнаний критичним у контексті подагри; це ставить під сумнів адекватність наявних референтних меж.
Цю гіпотезу підтверджує й дослідження URRAH: навіть за ССК <6,0 мг/дл було зафіксовано достовірне підвищення серцево-судинної та загальної смертності [35]. Ці дані ставлять під сумнів уявлення про «безпечні» значення ССК і підкреслюють необхідність оцінювати її як континуальну змінну в системі стратифікації ризику, особливо в пацієнтів із супутніми факторами. Підтвердження цьому надає й робота Tian і співавт., яка продемонструвала поступове зростання ризику серцево-судинних ускладнень навіть в осіб з незначною ГУ без супутніх факторів, що виключає вплив останніх як основної причини [36].
Важливі докази надають і генетичні дослідження, котрі засвідчили причинно-наслідковий зв’язок між підвищеним рівнем ССК та ризиком ІХС і раптової серцевої смерті [37]. Метааналіз, присвячений пацієнтам з АГ, також показав, що ССК є незалежним прогностичним фактором смерті (як серцево-судинної, так і від усіх причин), а також розвитку ІХС і великих серцево-судинних подій (major cardiovascular events – MACE) [38].
Попри це, ефективність терапії, спрямованої на зниження ССК, залишається предметом дискусій [39]. Великий метааналіз за участю понад 3,8 млн пацієнтів показав, що інгібітори ксантиноксидази загалом не зменшують ризику серцево-судинних подій порівняно з плацебо. Водночас в аналізі підгруп виявлено, що фебуксостат може мати переваги над алопуринолом у зниженні ризику СН [40]. Окрім того, аналізи типу phenome-wide MR (повнофеномний аналіз з менделівською рандомізацією) свідчать, що генетично знижені рівні ССК пов’язані зі зменшеним ризиком коронарного атеросклерозу, СН, цереброваскулярної оклюзії та хвороби периферичних артерій [41].
Особливу увагу привертає динаміка ССК у пацієнтів з гострою СН: саме стійке підвищення її рівня під час госпіталізації (а не лише початкове значення) асоціюється з підвищеною смертністю [42]. Це підкреслює клінічну доцільність моніторингу ССК у динаміці, передусім в уразливих групах.
Іще одним фактором, що модифікує зв’язок ССК з прогнозом, є функція нирок. У пацієнтів з тяжкою ХХН як високі, так і низькі рівні ССК асоціюються з підвищеним ризиком смерті, тоді як за помірного порушення функції нирок кращі результати спостерігаються при нижчих значеннях ССК [43]. Це свідчить про необхідність персоналізованих цільових рівнів залежно від функції нирок і серцево-судинного ризику [44]. Доказом слугує й проспективне когортне дослідження за участю понад 7 тис. пацієнтів з діабетом: верхній квінтиль ССК асоціювався з підвищенням загальної смертності на 28% і серцево-судинної – на 41% порівняно з нижнім квінтилем [45]. Отже, СК – це не просто пасивний продукт пуринового обміну, а модифікований фактор, який робить вагомий внесок у серцево-судинний ризик.
Сечова кислота при ХХН: від біомаркера до терапевтичної цілі
У багатьох популяціях підвищений рівень ССК визнано незалежним предиктором погіршення функції нирок. Зокрема, навіть у здорових нормотензивних осіб вищі початкові значення ССК асоціювалися зі значним зниженням швидкості клубочкової фільтрації (ШКФ) протягом 5 років [46]. Підтверджено, що ССК є незалежним від ШКФ фактором ризику як гострої, так і хронічної ниркової недостатності [47]. У великому дослідженні ГУ майже подвоювала ризик розвитку ниркової дисфункції впродовж 12 років [48].
У японському популяційному дослідженні навіть незначне підвищення ССК у межах референтного діапазону асоціювалося з прискореним зниженням ШКФ і вищою частотою ниркової недостатності. Особливо виражений ефект спостерігали в жінок, пацієнтів із ЦД 2 типу та протеїнурією [49]. Водночас АГ виявилася посередником цього зв’язку: в гіпертензивних осіб асоціація між ССК і втратою функції нирок була сильнішою, ніж у нормотензивних [50].
Згідно з об’єднаними даними двох великих когорт США кожне підвищення ССК на 1 мг/дл пов’язане зі зростанням ризику розвитку ХХН на 7-11% протягом 8,5 років незалежно від серцево-судинних і демографічних факторів [51]. У пацієнтів з діабетом обох типів ГУ пов’язана з раннім прогресивним погіршенням функції нирок і зростанням ризику розвитку ХХН: для ЦД 1 типу відносний ризик (ВР) дорівнює 1,4, для ЦД 2 типу – 2,1 на кожне підвищення ССК на 1 мг/дл [52, 53].
У когорті понад 5000 пацієнтів верхній квінтиль ССК асоціювався з поширеністю ниркової недостатності (ШКФ <60 мл/хв/1,73 м²) до 42% [54].
Подальші дослідження показали, що ГУ пов’язана з підвищеним ризиком термінальної стадії хвороби нирок [55, 56], втратою функції трансплантованої нирки [57, 58] і раннім нирковим ураженням у пацієнтів з АГ, які отримують первинну профілактику [59, 60]. Це підкреслює, що підвищений рівень СК може бути не лише наслідком, а й причиною погіршення функції нирок. До основних патофізіологічних механізмів належать тубулярна преципітація, окисний стрес, ендотеліальна дисфункція й індукція прозапальних цитокінів – механізми, які можуть активуватися навіть у безсимптомних осіб [61].
Дедалі більшу увагу привертає взаємозв’язок між ГУ та ССЗ. Порушення функції нирок саме собою є незалежним фактором ризику ССЗ, а при ГУ цей ризик зростає вдвічі через додаткове зниження ШКФ. З іншого боку, прогресивна дисфункція нирок зменшує екскрецію СК, поглиблюючи ГУ. У пацієнтів з СН зафіксовано вищу смертність і частоту госпіталізацій при одночасно збереженій функції нирок – імовірно, через надмірну активність ксантиноксидази, окисний стрес і негативні кардіальні наслідки [62, 63]. Підтвердженням слугує дослідження серед пацієнтів з СН зі зниженою фракцією викиду: підвищений рівень ССК асоціювався з гіршими серцево-судинними наслідками протягом року, зокрема в пацієнтів без ХХН, що свідчить про незалежне прогностичне значення ССК у цій підгрупі [64].
За ХХН рівень ССК може виступати не лише маркером прогресування, а й незалежним предиктором смерті. Метааналіз за участю понад 260 тис. пацієнтів на гемодіалізі показав парадоксальний зворотний зв’язок: кожне підвищення ССК на 1 мг/дл асоціювалося зі зниженням серцево-судинної смертності на 9% і загальної смертності на 6% [65]. Цей феномен є типовим для пізніх стадій ХХН й ускладнює інтерпретацію рівня ССК у таких пацієнтів. Такий U-подібний зв’язок виявлено й серед пацієнтів на перитонеальному діалізі. У великій ретроспективній когорті як низькі (<5,1 мг/дл), так і високі (>6,8 мг/дл) середні значення ССК асоціювалися з підвищеною смертністю протягом 48 міс [66]. Ці дані підкреслюють складність інтерпретації рівня ССК у пацієнтів з ХХН і необхідність індивідуалізованого підходу до його оцінювання з огляду на стадію хвороби, супутні стани та загальний клінічний контекст.
Останні дослідження свідчать, що співвідношення ССК до сироваткового креатиніну може підвищити точність стратифікації ризику, даючи змогу виявляти пацієнтів з підвищеним кардіометаболічним ризиком. Такий підхід фокусує увагу не на зниженні екскреції, а на надмірному виробленні СК, особливо актуальному в пацієнтів з високим серцево-судинним ризиком [67, 68].
Зростання поширеності як ХХН, так і ГУ, які часто поєднуються з метаболічним синдромом, підкреслює необхідність перегляду клінічно значущих цільових рівнів СК [69].
Експериментальні моделі засвідчили, що підвищення ССК здатне пришвидшити прогресування ХХН навіть без формування кристалів, тобто розчинна СК сама собою є патогенетичним чинником [70]. Хоча історично СК вважали антиоксидантом, нині відомо, що вона стимулює окисний стрес, погіршує ендотеліальну функцію, активує РАС і прозапальні шляхи, зокрема NF-κB й інфламасоми [71, 72]. Сукупні епідеміологічні та клінічні дані свідчать про патогенетичну роль внутрішньоклітинної токсичності СК; у цьому контексті основна користь від уратознижувальної терапії (УЗТ) може полягати передусім у кардіопротекції та меншою мірою в нефропротекції [73].
Пілотні дослідження й метааналізи засвідчили потенційну ефективність інгібіторів ксантиноксидази в сповільненні прогресування ХХН [74, 75]. Метааналіз рандомізованих контрольованих досліджень показав, що УЗТ у пацієнтів з безсимптомною ГУ сприяє збереженню ШКФ і зниженню креатиніну в коротко- та довгостроковій перспективі [76]. Водночас масштабні дослідження, зокрема PERL (ЦД 1 типу + ХХН 2-3 ст.) і CKD-FIX (ХХН 3-4 ст.) не продемонстрували достовірної користі від алопуринолу для ниркової функції [77, 78].
Ці дані змусили експертів переглянути позицію щодо рутинного призначення УЗТ при ХХН. Сьогодні доцільність такої терапії визнається лише за наявності показань до лікування подагри [79]. Деякі автори навіть припускають, що помірна ГУ може мати позитивний ефект у пацієнтів з ХХН [80], але більшість закликає до обережності й індивідуалізації [81]. Варто врахувати, що в дослідженнях PERL і CKD-FIX не включали пацієнтів з подагрою, хоча саме ця група становить до третини осіб з ХХН, а також не обмежували відбір пацієнтів рівнями ГУ; це могло завадити виявленню позитивного ефекту УЗТ. Натомість нещодавнє когортне дослідження показало, що досягнення цільового рівня ССК <6 мг/дл у пацієнтів з подагрою та ХХН 3 ст. супроводжувалося зниженням ризику прогресування до тяжкої або термінальної ХХН (ВР 0,89) [82].
Порівняльний аналіз уратознижувальних засобів і їхнього впливу на серцево-судинні та нефрологічні результати демонструє переваги персоналізованої терапії (табл. 1).
|
Таблиця 1. Уратознижувальні препарати та їхній вплив на серцево-судинні й ниркові події |
||||
|
Фармакологічний клас |
Препарат |
Серцево-судинні та ниркові ефекти |
Рівень клінічних доказів |
Основні клінічні моменти |
|
Інгібітори ксантиноксидази |
Алопуринол |
Нейтральний вплив на ниркові/серцево-судинні події |
Рандомізовані контрольовані дослідження |
Широко використовується; прийнятний профіль безпеки |
|
Фебуксостат |
Потенціал ↓ серцево-судинних подій; збереження рШКФ |
Мережеві метааналізи |
Вища уратознижувальна ефективність |
|
|
Інгібітори URAT1 |
|
Дані щодо серцево-судинних подій обмежені |
Попередні дослідження |
Часто використовуються разом з інгібітором ксантиноксидази |
|
Протизапальна терапія |
|
Покращення ендотеліальної функції; ↓ МАСЕ в пацієнтів з ІХС |
Когортні дослідження |
Додатковий протизапальний потенціал |
|
Примітки: рШКФ – розрахункова швидкість клубочкової фільтрації; URAT1 – уратний транспортер‑1; МАСЕ – великі серцево-судинні події; ІХС – ішемічна хвороба серця. |
||||
Зокрема, мережевий метааналіз за участю пацієнтів з ХХН 3-5 ст. і безсимптомною ГУ показав, що фебуксостат ефективніше за алопуринол знижував ССК і сприяв покращенню ШКФ (середня різниця: +4,99 мл/хв/1,73 м²) без зростання серцево-судинного ризику [83]. Фебуксостат також продемонстрував потенціал у зниженні альбумінурії, сповільненні втрати ШКФ і зменшенні частоти ниркових подій у пацієнтів з подагрою або ГУ [84].
Найбільше користі від УЗТ можуть отримати окремі групи пацієнтів. Це передусім хворі на подагру, які нерідко залишаються недолікованими, незважаючи на свідчення щодо відкладення уратів у коронарних артеріях, аорті та нирках. Також до цієї категорії належать пацієнти з уратною кристалурією – патологією, що активує інфламасоми в тубулярному епітелії та провокує локальне ушкодження. Попри високу поширеність подагри серед осіб з ХХН, ефективну терапію отримує менш ніж чверть пацієнтів. Причини – складність підбору препаратів, протипоказання, потреба в корекції доз і неефективна міждисциплінарна взаємодія. Нефрологи мають активніше долучатися до ведення подагри як ускладнення ХХН [85].
На окрему увагу заслуговують онкопацієнти з ГУ та ХХН – у них зростає як загальна, так і серцево-судинна смертність [86]. У Китаї, де зростає кількість пацієнтів на діалізі, ГУ є поширеною та спричиняє прогресування ХХН до термінальної стадії через кристалізацію пуринів, запалення й активацію РАС [87]. Майже половина пацієнтів на гемодіалізі має ГУ, а поширеними супутніми хворобами є АГ й анемія [88].
На відповідь на лікування також можуть впливати генетичні особливості. За даними нещодавнього дослідження з пошуком асоціацій у масштабах геному ідентифіковано 377 локусів, пов’язаних з подагрою та метаболізмом СК. Особливу роль відіграє запалення, включно з активацією інфламасом NLRP3, які можуть бути перспективною терапевтичною мішенню [89].
Сечова кислота та смертність: коли «метаболіт» стає маркером фатального ризику
Сучасні настанови й консенсуси дедалі частіше визнають підвищені рівні ССК не лише біомаркером, а незалежним фактором серцево-судинного ризику, особливо в пацієнтів з АГ, ХХН чи СН. Нові докази вказують на континуум ризику загальної та серцево-судинної смертності в широкому діапазоні рівнів ССК і популяцій.
Зокрема, вищі рівні ССК асоціюються з підвищенням загальної смертності (ВР 1,20-1,25) [90, 91]. Згідно з метааналізами кожне підвищення ССК на 1 мг/дл пов’язане зі зростанням ризику смерті на 9% [92].
ГУ також пов’язана з підвищеною серцево-судинною смертністю (ВР 1,37-1,45) [57, 91]; ця асоціація виявляється сильнішою в жінок. Дослідження URRAH зафіксувало підвищений ризик смерті навіть за ССК 4,5-5,5 мг/дл [57, 94].
У масштабному метааналізі (понад 2,5 млн осіб, 34 когортні дослідження) ГУ асоціювалася з підвищенням загальної смертності (ВР 1,32), особливо в жінок (ВР 1,91 проти 1,16 у чоловіків) [95]. Ризик був найвищим у пацієнтів європеоїдної раси середнього віку.
ГУ також підвищує смертність при АГ (ВР 1,87) [96]. Аналіз бази даних NHANES (13 363 пацієнти з АГ, 2001-2018 рр.) показав U-подібну криву ризику: підвищену смертність як за високих, так і за низьких рівнів ССК [97]. У різних квартилях ВР для загальної смертності становив: 1,557; 1,312; 1,393 (усі p<0,01), а для серцево-судинної – 1,308; 1,182; 1,151.
У пацієнтів з остеоартритом ГУ підвищує загальну (ВР 1,22) та серцево-судинну смертність (ВР 1,32) [98]. Окрім того, поєднання ГУ та ХХН значно підвищує довгострокову смертність у разі СН (ВР 1,59) [99]. Підвищений ризик також виявлено щодо інсульту (ВР 1,42 для розвитку; ВР 1,53 для смерті) [100] й ІХС (ВР 1,14 для серцево-судинної смертності; ВР 1,20 для загальної смертності [90]), особливо в жінок.
Поєднання ГУ з гіперінсулінемією істотно посилює ризик (ВР 2,32), особливо в осіб віком понад 40 років і тих, хто має нормальну масу тіла [101]. У пацієнтів з ХХН поєднання ГУ з анемією має синергічний вплив на смертність [102].
Варто також зазначити зв’язок між ССК і запаленням у пацієнтів з ІХС: у когорті 16 598 осіб підвищені рівні ССК були достовірним прогностичним маркером підвищеного ризику MACCE (великих серцево-судинних і цереброваскулярних подій) лише за рівня високочутливого С-реактивного білка (вчСРБ) ≥2 мг/л [103]. Кожне підвищення ССК на 1 мг/дл збільшувало ризик MACCE на 11,3% (p<0,001). За рівня вчСРБ <2 мг/л зв’язок не виявлявся, що вказує на значення хронічного запалення як «підсилювача» прогностичної значущості ССК.
Метааналізи підтвердили зв’язок ГУ зі смертністю від ІХС: ВР варіюється від 1,14 до 1,27 [104-107], з підвищенням ризику на 12-20% за кожного додаткового мг/дл ССК [108]. Подібні асоціації підтверджено й для смертності від інсульту (ВР 1,33-1,36), теж більшою мірою в жінок [109]. ГУ в пацієнтів з АГ асоціювалася з підвищенням загальної смертності (ВР 1,12) [110].
Останні дослідження вказують на зростання ризику інфаркту міокарда й інсульту при тривалому підвищенні ССК [111, 112], що підкреслює важливість повторного вимірювання її рівнів.
За даними метааналізу, в пацієнтів з СН рівень ССК >6,5 мг/дл асоціювався зі зростанням загальної смертності у 2,13 раза [113]. Дослідження URRAH підтвердило цей зв’язок навіть з нижчим пороговим рівнем ССК [114].
У пацієнтів з гострим коронарним синдромом ГУ асоціювалася з вищою загальною (ВР 1,86) та серцево-судинною смертністю (ВР 1,74) [115]. Серед осіб з підтвердженим або підозрюваним коронарним атеросклерозом найвищий рівень ССК асоціювався з ВР 2,09 для серцево-судинної смерті та 1,80 – для загальної [116].
У пацієнтів з ХХН підвищені рівні ССК також пов’язані з вищою серцево-судинною смертністю (ВР 1,47), зі зростанням ризику на 12% на кожен 1 мг/дл ССК [117].
У пацієнтів без ССЗ подагра асоціюється з вищою серцево-судинною смертністю (ВР 1,29) та смертністю від ІХС (ВР 1,42) [118].
У пацієнтів із ЦД 2 типу ГУ теж підвищує смертність: ВР 1,06 у метааналізі [119]; нові дані дослідження NHANES (>7000 осіб) указують на ВР 1,41 для серцево-судинної смертності [120], водночас загальна смертність зростає на 5-8% за кожного підвищення ССК на 1 мг/дл.
Отже, СК – не просто маркер, а предиктор смерті, який можливо модифікувати. У групах високого ризику – від СН і ЦД до ІХС і ХХН – моніторинг рівня ССК й УЗТ можуть мати прогностичне та потенційно рятівне значення.
Поза межами подагри: нове бачення ролі СК в сучасній медицині
Контроль рівня ССК є ключовим викликом у профілактиці та лікуванні серцево-судинних, метаболічних і ниркових захворювань. Те, що колись вважалося інертним метаболітом пуринового обміну, нині розглядається як патофізіологічно активна субстанція. ГУ – це не просто маркер ризику, а активний учасник прозапальних і проокисних процесів, які ушкоджують серце, судини, нирки та метаболічні шляхи [121].
Наростання епідеміологічної бази свідчить: підвищена ССК є незалежним предиктором як серцево-судинної, так і ниркової захворюваності та смертності [122]. Це зумовлює зміщення клінічного фокусу в бік активного моніторингу й керування цим біомаркером.
З еволюційного погляду втрата ферменту урикази призвела до хронічно підвищеного рівня ССК у людини – можливо, це мало адаптивне значення в умовах дефіциту натрію та калорій [123]. Проте в сучасному середовищі з надлишком пуринів, фруктози й солі така перевага трансформувалася на чинник ризику. Головним джерелом надлишкового утворення СК є фермент ксантиноксидаза, активність якого стимулює окисний стрес, запалення та дисфункцію ендотелію [23].
Хоча порушення ниркової екскреції також спричиняє ГУ, останні дані вказують, що саме гіперпродукція має вирішальне значення в ушкодженні тканин. Водночас взаємодія між обома механізмами складна й часто заплутує інтерпретацію результатів лікування [124].
Сучасні дослідження демонструють, що ГУ знижує біодоступність NO та порушує інсулінову сигналізацію – ключові механізми, котрі зв’язують її з АГ, метаболічним синдромом і ЦД 2 типу [3]. Водночас СК активує РАС, стимулює проліферацію ГМК судин і посилює окисне ушкодження – процеси, які спричиняють ремоделювання судин і атеросклероз [125].
Ці механізми підтверджуються клінічними спостереженнями: особи з підвищеним рівнем ССК – навіть без клінічної подагри – мають підвищений ризик ІХС, СН, інсульту та прогресування ХХН [126].
Отже, настав час переосмислити роль СК. Це не пасивний метаболічний залишок, а клінічно значущий фактор у патогенезі серцево-судинних і ниркових хвороб [61]. Хоча дискусія про «причину чи наслідок» триває, генетичні, експериментальні й інтервенційні дані схиляються до першого варіанта. Найефективнішим підходом є комплексна індивідуалізована стратегія: за потреби фармакотерапія (зокрема інгібітори ксантиноксидази), модифікація способу життя та дієтичні втручання.
У контексті клінічної неоднорідності ГУ оптимальним видається орієнтований на фенотип підхід, який ураховує особливості обміну СК, запальні процеси, функції нирок і генетичну схильність (табл. 2). Подальші дослідження мають сфокусуватися на взаємодії між дієтою, запаленням і метаболізмом СК; це дасть змогу вдосконалити стратифікацію ризику та сформувати сучасні стратегії первинної та вторинної профілактики.
|
Таблиця 2. Терапевтичні стратегії, що ґрунтуються на клінічному фенотипі |
||
|
Клінічний сценарій |
Рекомендована терапевтична стратегія |
Обґрунтування |
|
Подагра з ХХН (стадія ≥3) |
Інгібітор ксантиноксидази (± інгібітор URAT1) для досягнення ССК <6 мг/дл |
УЗТ знижує ризик термінальної стадії хвороби нирок |
|
ХХН без клінічної подагри |
Розпочати терапію, якщо ССК >7-8 мг/дл |
Користь обмежена; УЗТ за низьких рівнів ССК може бути шкідливою |
|
Атеросклеротичне ССЗ з підвищеним запаленням (вчСРБ ≥2 мг/л) |
Інгібітор ксантиноксидази + протизапальна терапія (наприклад, колхіцин у низькій дозі) |
УЗТ знижує ризик МАССЕ в пацієнтів з ГУ та супутнім запаленням |
|
Безсимптомні пацієнти з низьким ризиком |
Фармакологічна УЗТ не потрібна |
Клінічна користь не доведена; ризик надмірного лікування |
Borghi C., Fogacci F., Cicero A. F. Crystal clear – part I: The role of uric acid in cardiorenal disease. Eur. J. Intern. Med. 2025 Dec; 142: 106432. doi: 10.1016/j.ejim.2025.07.028. Epub 2025 Jul 27.
PMID: 40716974.
Адаптований переклад підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 1 (612), 2026 р