15 березня, 2026
Діацереїн при остеоартриті: сучасна доказова база, місце в настановах і клінічні переваги за метаболічного фенотипу
Остеоартрит (ОА) є найпоширенішим захворюванням суглобів і провідною причиною хронічного болю та функціональних обмежень. Сучасне розуміння патогенезу ОА виходить за межі локальної дегенерації хряща та включає синовіальне запалення, ремоделювання субхондральної кістки й системне низькорівневе запалення, особливо при метаболічному фенотипі захворювання. Обмеження традиційної симптоматичної терапії сприяли зміщенню лікувальної парадигми в бік безпечної довготривалої хворобомодифікувальної терапії (Chen B. et al., 2023).
Діацереїн посідає важливе місце серед симптоматичних препаратів повільної дії для лікування ОА завдяки інгібуванню інтерлейкіну-1β (IL-1β) – ключового медіатора запалення, деградації хряща та болю. Препарат характеризується пролонгованим симптоматичним ефектом і сприятливим профілем безпеки, а також плейотропними властивостями, зокрема чинить антиоксидантну та метаболічну дію, що має клінічне значення при коморбідних станах. Перегляд ролі анти-IL-1-стратегій підтверджує доцільність персоналізованого підходу до лікування ОА з урахуванням фенотипу пацієнта та системного запального фону (Pavelka K. et al., 2016).
ОА є найпоширенішим дегенеративно-запальним захворюванням опорно-рухового апарату та провідною причиною хронічного болю, втрати працездатності й зниження якості життя в світі. За оцінками, на ОА страждає >595 млн осіб; ця цифра неухильно зростає через старіння населення, поширення ожиріння та метаболічні порушення. Захворювання чинить значний соціально-економічний тягар, зумовлюючи високі витрати на медичну допомогу, тривалу реабілітацію та ендопротезування суглобів (Chen B. et al., 2023).
Сучасний стан проблеми ОА
Традиційні підходи до лікування ОА тривалий час були зосереджені переважно на симптоматичному контролі болю. Нестероїдні протизапальні препарати (НПЗП) і парацетамол залишаються широко застосовуваними засобами, однак їхній ефект є короткотривалим і не впливає на ключові механізми прогресування захворювання. Крім того, тривале застосування НПЗП асоціюється з підвищеним ризиком гастроінтестинальних, серцево-судинних і нефротоксичних ускладнень, що суттєво обмежує їхню безпеку, особливо в пацієнтів літнього віку та з коморбідною патологією (Magni A. et al., 2021; del Río E., 2025).
Діацереїн як один із рекомендованих міжнародними настановами SYSADOA
Сучасна парадигма ведення пацієнтів з ОА зміщується в бік пошуку безпечної довготривалої хворобомодифікуючої терапії, спрямованої не лише на зменшення болю, а й на уповільнення структурного прогресування, контроль запалення та покращення функціонального стану і якості життя. Особливу увагу приділяють симптоматичним препаратам повільної дії при ОА (SYSADOA), рекомендованим провідними міжнародними настановами ESCEO, OARSI та EULAR, які чинять кумулятивний ефект, мають хороший профіль безпеки та здатні впливати на ключові ланки патогенезу – деградацію хряща, активацію прозапальних цитокінів і синовіальне запалення (Magni A. et al., 2021). Серед них діацереїн посідає виняткове місце завдяки унікальному механізму дії, поєднанню підтвердженої клінічної ефективності, вираженого пролонгованого післядієвого ефекту та широкого спектра плейотропних властивостей (McAlindon T.E. et al., 2014; Bruyère O. et al., 2019; Yeap S.S. et al., 2021).
Механізм дії діацереїну
Механізм дії діацереїну (похідне антрахінону, активним метаболітом якого є реїн) безпосередньо пов’язаний із впливом на IL-1β – один із ключових прозапальних цитокінів у патогенезі ОА. IL-1β запускає каскад молекулярних подій у хондроцитах і синовіоцитах, активуючи NF-κB та індукуючи експресію катаболічних ферментів – матриксних металопротеїназ (MMP-1, -3, -9, -13) і агреканаз (ADAMTS-4, -5). Це зумовлює деградацію колагену ІІ типу й агрекану – основних компонентів хрящового матриксу. Паралельно стимулюється синтез простагландину Е₂ та оксиду азоту через активацію COX-2 і iNOS, що підтримує синовіальне запалення, больовий синдром та структурне прогресування захворювання. IL-1β також індукує апоптоз хондроцитів і пригнічує анаболічні сигнали (TGF-β, IGF-1), порушуючи відновлювальні механізми хряща та сприяючи хронізації процесу (Solignac M., 2004).
Реїн знижує транскрипцію і секрецію IL-1β, блокує внутрішньоклітинні сигнальні шляхи та пригнічує експресію MMP, агреканаз, COX-2, iNOS. У результаті зменшується катаболізм позаклітинного матриксу, послаблюється синовіальне запалення та сповільнюється структурне прогресування ОА (Solignac M., 2004).
Крім базового протизапального та хондропротекторного ефектів, діацереїн характеризується широким спектром різних властивостей, які значно розширюють його терапевтичний потенціал, особливо в пацієнтів із метаболічним фенотипом ОА. Зокрема, продемонстровано антиоксидантну дію діацереїну, що реалізується через зменшення утворення реактивних форм кисню та підвищення активності ендогенних антиоксидантних ферментів, – супероксиддисмутази і каталази (Pavelka K. et al., 2016).
Важливими є також гепатопротекторні властивості діацереїну, особливо в контексті неалкогольної жирової хвороби печінки, де препарат зменшує запалення та фіброгенез. Антидіабетичний ефект пов’язаний з інгібуванням протеїнтирозинфосфатази 1B (PTP1B), що сприяє покращенню чутливості тканин до інсуліну та зниженню системного запалення. Нефропротекторна дія проявляється захистом ниркової тканини при токсичних ураженнях та ішемії-реперфузії, тоді як противиразкові, антиканцерогенні й протифіброзні ефекти додатково підкреслюють багатовекторний вплив препарату (Almezgagi M. et al., 2020).
Плейотропні ефекти діацереїну
Наочне узагальнення плейотропних ефектів діацереїну схематично представлено на рисунку, де центральне місце посідає сам діацереїн, від якого розходяться стрілки до різних органів і тканин із відповідними терапевтичними діями.
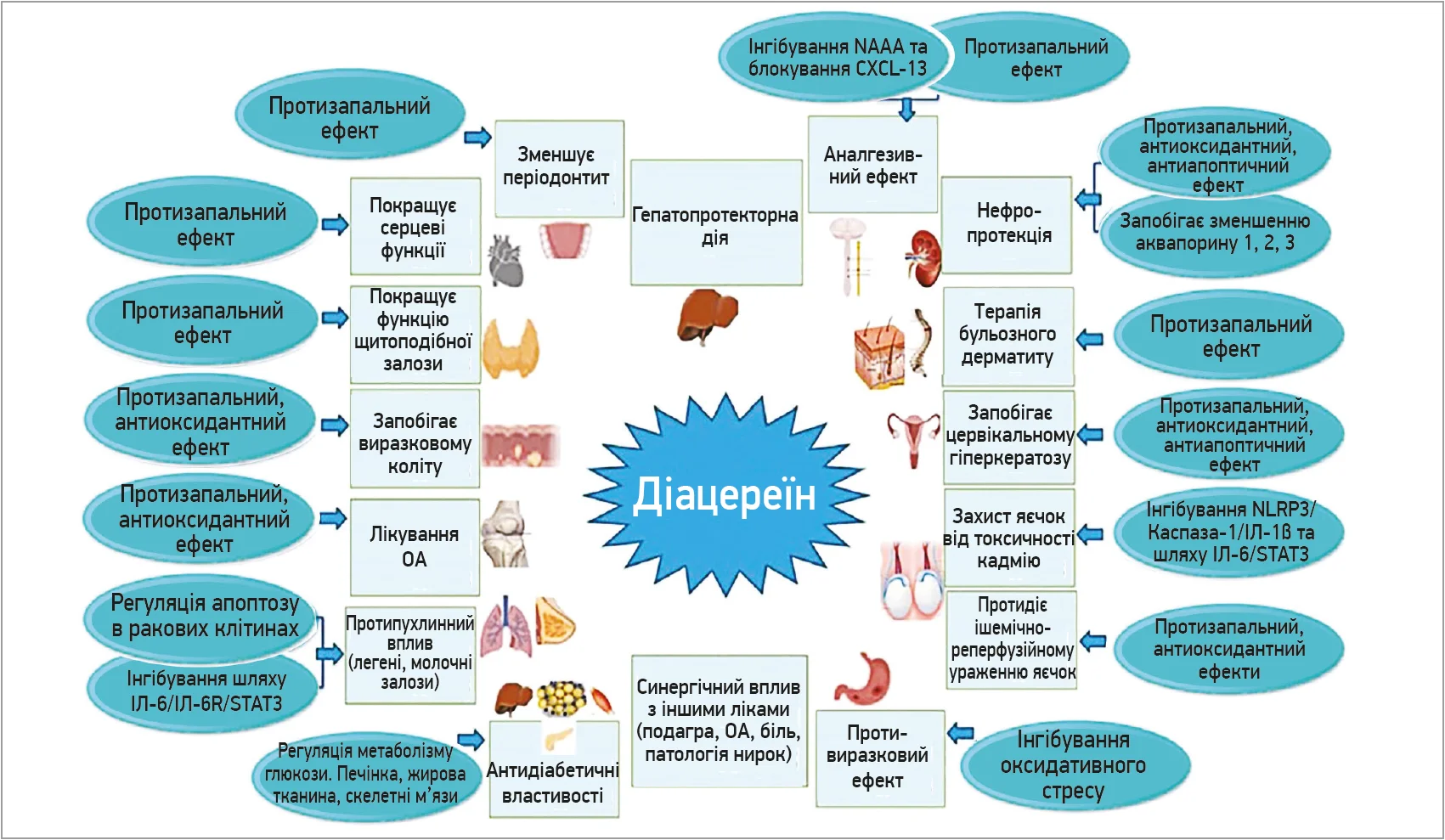 Рис. Плейотропні ефекти діацереїну в різних органах і тканинах (Almezgagi M. et al., 2020)
Рис. Плейотропні ефекти діацереїну в різних органах і тканинах (Almezgagi M. et al., 2020)
Варто виокремити такі ефекти:
- антизапальний та антиоксидантний → покращення функції серця, щитоподібної залози, нирок, печінки;
- гепатопротекторний → захист печінки;
- антидіабетичний → регуляція метаболізму глюкози в печінці, жировій тканині та скелетних м’язах;
- антинефротоксичний та антиішемічний → захист нирок при токсичному й ішемічно-реперфузійному ушкодженні;
- протипухлинний → індукція апоптозу в клітинах раку молочної залози та легень, інгібування шляхів IL-6/STAT3;
- противиразковий → захист шлунково-кишкового тракту;
- синергізм з іншими препаратами → посилення ефекту за подагри, в разі болю, ОА та раку молочної залози.
Діацереїн у стратегії НПЗП-спарингу
У численних рандомізованих клінічних дослідженнях і метааналізах показано, що діацереїн забезпечує достовірне зменшення больового синдрому та покращення функціональної спроможності суглобів у пацієнтів з ОА. За величиною аналгетичного ефекту він є зіставним із НПЗП, а в окремих дослідженнях – навіть перевищує їх при довготривалому застосуванні. Водночас діацереїн демонструє кращу ефективність порівняно з парацетамолом, який нині розглядається як менш результативний засіб контролю болю при ОА (Pavelka K. et al., 2016).
Принциповою відмінністю діацереїну від НПЗП є не лише симптоматичний, а й патогенетично спрямований механізм дії через модулювання IL-1β-залежного запалення. Це зумовлює поступовий розвиток клінічного ефекту (зазвичай протягом 2-4 тиж), проте забезпечує стійкіший результат. Важлива клінічна перевага – виражений after-effect: зменшення болю та покращення функції зберігаються протягом декількох місяців після припинення лікування, що підтверджує статус діацереїну як препарату повільної симптоматичної дії (SYSADOA) із пролонгованим ефектом (Brom M. et al., 2025).
Додавання діацереїну до традиційної терапії НПЗП дозволяє підвищити загальну ефективність лікування. Комбіноване застосування забезпечує швидший контроль больового синдрому за рахунок НПЗП у початковий період і формування стабільного довготривалого ефекту завдяки діацереїну. Такий підхід може сприяти зменшенню потреби в тривалому прийомі НПЗП, отже, потенційно знижувати ризик гастроінтестинальних і серцево-судинних ускладнень при довготривалій терапії.
Патогенетична роль IL-1β і місце діацереїну за метаболічного ОА
Сучасний перегляд ролі IL-1 у патогенезі ОА суттєво змінив парадигму ведення пацієнтів. Якщо раніше ОА розглядався переважно як дегенеративне захворювання, то сьогодні він трактується як гетерогенна патологія з вираженим запальним компонентом у частки пацієнтів. Особливо це стосується метаболічного фенотипу ОА, який асоціюється з ожирінням, абдомінальним типом жирової тканини, інсулінорезистентністю, метаболічним синдромом і хронічним низькоградієнтним системним запаленням (Brom M. et al., 2025).
У цьому фенотипі IL-1β є центральним медіатором, що поєднує системну метаболічну дисфункцію з локальним суглобовим ураженням. Активація інфламасоми NLRP3 у макрофагах жирової тканини спричиняє посилену продукцію IL-1β, який:
- стимулює катаболічні процеси в хондроцитах;
- активує NF-κB-залежну транскрипцію прозапальних генів;
- індукує продукцію MMP та агреканаз;
- підтримує синовіальне запалення;
- посилює інсулінорезистентність і ендотеліальну дисфункцію.
Отже, IL-1β є не лише локальним фактором руйнування хряща, а й системною ланкою, що інтегрує метаболічне та судинне запалення.
В цьому контексті діацереїн посідає унікальну позицію. На відміну від біологічних агентів, що блокують IL-1 безпосередньо, діацереїн (через активний метаболіт реїн) модулює синтез і активність IL-1β на рівні транскрипції та внутрішньоклітинної сигналізації (Martel-Pelletier J. et al., 2010).
Важливо, що ефекти діацереїну виходять за межі лише суглоба. Дані експериментальних і клінічних досліджень свідчать про його здатність:
- зменшувати рівень системних прозапальних цитокінів;
- покращувати показники чутливості до інсуліну;
- знижувати маркери оксидативного стресу;
- модулювати активність інфламасоми NLRP3;
- позитивно впливати на метаболічний профіль у пацієнтів із цукровим діабетом 2 типу.
Це особливо важливо з огляду на те, що метаболічний ОА має спільні патогенетичні механізми з атеросклерозом. Хронічне IL-1-опосередковане запалення сприяє прогресуванню як суглобової деструкції, так і судинного ремоделювання. Результати великих кардіоваскулярних досліджень (зокрема, CANTOS) продемонстрували, що блокада IL-1β асоціюється зі зниженням частоти серцево-судинних подій. Паралельно спостерігалося зменшення потреби в ендопротезуванні суглобів, що опосередковано підтверджує роль IL-1 у прогресуванні ОА. Схожі сигнали були отримані й при застосуванні колхіцину (LoDoCo2), який інгібує NLRP3-інфламасому (Martel-Pelletier J. et al., 2010).
Хоча діацереїн не є біологічним препаратом і не блокує IL-1β безпосередньо, тривала модуляція IL-1-залежного запалення дозволяє розглядати його як фармакологічний інструмент впливу на ті самі патогенетичні осі, але в доступнішому пероральному форматі та з кращою придатністю для довготривалої терапії.
Із клінічного погляду це означає, що в пацієнтів із метаболічним фенотипом ОА діацереїн може:
- забезпечувати контроль симптомів через зменшення IL-1-опосередкованого болю та синовіту;
- потенційно впливати на структурне прогресування за рахунок пригнічення катаболічних ферментів;
- модулювати системне запалення, що лежить в основі кардіометаболічного ризику;
- сприяти зниженню потреби в тривалому прийомі НПЗП.
Роль діацереїну виходить за межі традиційного уявлення про SYSADOA як суто симптоматичний засіб. У світлі нових даних про IL-1 та метаболічний ОА він може розглядатися як патогенетично орієнтований препарат для підгрупи пацієнтів із запально-метаболічним профілем, що потенційно здатний впливати не лише на перебіг суглобового процесу, а й на системні кардіометаболічні ризики (Pavelka K. et al., 2016).
Висновки
Діацереїн – добре вивчений представник класу SYSADOA з доведеною симптоматичною ефективністю, пролонгованим клінічним ефектом і сприятливим профілем безпеки за довготривалого застосування. Його механізм дії, пов’язаний із модуляцією IL‑1β-залежного запалення, дозволяє впливати не лише на біль і функцію суглобів, а й на ключові патогенетичні ланки ОА – катаболізм хряща, синовіальне запалення та прогресування структурних змін. Плейотропні властивості діацереїну, включно з потенційним впливом на системне низькоградієнтне запалення, інсулінорезистентність і метаболічні порушення, роблять його особливо цінним у пацієнтів із метаболічним фенотипом ОА та супутніми коморбідними станами (ожиріння, метаболічний синдром, серцево-судинні захворювання). В цій когорті препарат може розглядатися як складова персоніфікованої стратегії лікування. Місце діацереїну в міжнародних рекомендаціях (ESCEO, OARSI, EULAR) підтверджує доцільність його застосування як у монотерапії (особливо при протипоказаннях або обмеженнях до тривалого прийому НПЗП), так і в комбінації з НПЗП на старті лікування для досягнення швидкого й стійкого клінічного ефекту з подальшим зменшенням потреби в НПЗП. В українській клінічній практиці важливою є наявність якісних і доступних препаратів діацереїну. Флекцерин® (АТ «Київський вітамінний завод») – сучасний препарат діацереїну, який дозволяє реалізувати патогенетично обґрунтований підхід до лікування ОА з урахуванням сучасних уявлень про роль IL‑1β і метаболічного запалення. Ззастосування Флекцерину відкриває додаткові можливості для оптимізації довготривалої терапії, підвищення прихильності пацієнтів і формування стабільного контролю симптомів із пролонгованим ефектом.
Підготувала Світлана Самсоненко
Медична газета «Здоров’я України 21 сторіччя» № 2 (613), 2026 р



