17 квітня, 2026
Остеоартрит: від фенотипу та тератипу – персоналізація терапевтичної стратегії
За матеріалами науково-практичної конференції «Комплексний підхід до реабілітації пацієнтів з артритом колінного суглоба»
 19 березня в м. Києві в онлайн-форматі відбулася науково-практична конференція «Комплексний підхід до реабілітації пацієнтів з артритом колінного суглоба». Захід було присвячено практичним аспектам розроблення індивідуалізованих програм реабілітації пацієнтів із зазначеною патологією на різних етапах хвороби – від ранніх проявів до післяопераційного відновлення – з урахуванням ролі кожного спеціаліста в спільному клінічному маршруті хворого. У фокусі обговорення були такі теми: раннє виявлення та стратифікація пацієнтів із ризиком швидкого прогресування ураження колінного суглоба; диференційований підхід до реабілітації при остеоартриті (ОА) та запальних артритах; поєднання медикаментозної терапії та немедикаментозних методів у контролі болю й відновленні; менеджмент больового синдрому колінного суглоба; роль фізичної терапії, корекції біомеханіки і м’язового балансу в довгострокових результатах; міждисциплінарна взаємодія в амбулаторному й стаціонарному етапах реабілітації; підготовка хворих до хірургічного лікування та ведення пацієнтів після ендопротезування.
19 березня в м. Києві в онлайн-форматі відбулася науково-практична конференція «Комплексний підхід до реабілітації пацієнтів з артритом колінного суглоба». Захід було присвячено практичним аспектам розроблення індивідуалізованих програм реабілітації пацієнтів із зазначеною патологією на різних етапах хвороби – від ранніх проявів до післяопераційного відновлення – з урахуванням ролі кожного спеціаліста в спільному клінічному маршруті хворого. У фокусі обговорення були такі теми: раннє виявлення та стратифікація пацієнтів із ризиком швидкого прогресування ураження колінного суглоба; диференційований підхід до реабілітації при остеоартриті (ОА) та запальних артритах; поєднання медикаментозної терапії та немедикаментозних методів у контролі болю й відновленні; менеджмент больового синдрому колінного суглоба; роль фізичної терапії, корекції біомеханіки і м’язового балансу в довгострокових результатах; міждисциплінарна взаємодія в амбулаторному й стаціонарному етапах реабілітації; підготовка хворих до хірургічного лікування та ведення пацієнтів після ендопротезування.
Заслужений лікар України, керівник Центру ревматології Клінічної лікарні «Феофанія» Державного управління справами (м. Київ), доктор медичних наук, професор Ірина Юріївна Головач у своїй доповіді висвітлила сучасні підходи до персоналізації терапевтичної стратегії ведення пацієнта з ОА.
ОА колінного суглоба є найпоширенішою патологією, з якою лікарі мають справу як у ревматологічній, так і в ортопедичній практиці. Погляд на це захворювання останніми роками змінився. Фахівці почали говорити про те, що воно є «парасолькою» для численних фенотипів, в основі яких лежать різні патогенетичні шляхи, тому лікування пацієнтів має проводитися відповідно до клінічних фенотипів.
Другою тезою, на якій акцентувала увагу спікерка, є те, що сьогодні ОА сприймають як системне захворювання. І доклінічні, і клінічні дані чітко свідчать про те, що ОА – це захворювання всього організму; відбувається системний процес, за якого спостерігають біологічні зміни, котрі як зумовлюють, так і є наслідком цього процесу. Погляд на ОА як на системне захворювання змінює лікувальну тактику, адже при ОА метаболізм змінюється не лише локально, а й на рівні всього організму. Це спричиняє залучення до патологічного процесу різних систем і органів та формування асоціативної коморбідності.
Нині експерти одностайно вважають, що ОА – не захворювання, а синдром із безліччю фенотипів. Фенотип ОА може бути визначений як поодинока ознака чи сукупність характеристик захворювання, які описують різницю між пацієнтами, оскільки вони належать до різних релевантних наслідків (наприклад, тяжкість симптомів, прогноз, відповідь на лікування тощо) [1].
Під впливом внутрішніх і зовнішніх факторів формуються різні фенотипи:
- етіологічні;
- структурні;
- больові;
- фенотипи, пов’язані з функцією суглоба;
- фенотипи, пов’язані з інвалідністю [2].
У кожній із цих груп пацієнтів різні підходи до лікування та профілактики, а також різне передбачення прогнозу.
Біль при ОА також характеризується значною гетерогенністю. Слід розуміти, що він виникає унаслідок ушкодження різних структур і тканин (кістки, періартикулярні тканини, м’язи, нервова система, синовіальна оболонка), які можуть бути джерелом цього ноцицептивного болю.
Виокремлюють такі основні клінічні фенотипи скелетно-м’язового болю:
- запальний;
- механічний;
- ентезопатичний;
- скелетно-м’язовий біль на тлі центральної сенситизації [3].
Розглядаючи ОА за локалізацією, наприклад, навіть серед патології кистей, виокремлюють три фенотипи:
- ОА міжфалангових суглобів кистей – проксимальних і дистальних, що можуть супроводжуватися формуванням вузликів;
- ОА зап’ястково-п’ясткового суглоба I пальця, який супроводжується значними функціональними обмеженнями та больовим синдромом;
- ерозивний ОА.
Варіанти фенотипів при ОА колінного суглоба за локалізацією:
- тибіофеморальний ОА – латеральний (більш властивий посттравматичному фенотипу) та медіальний (більш властивий метаболічному фенотипу);
- пателофеморальний ОА.
Навіть запалення, з яким пов’язують формування і прогресування ОА, також має відмінності в певних когортах пацієнтів. Так, дослідження продемонструвало наявність пацієнтів з абсолютно різними метаболічними профілями [4]. В різних групах хворих виявляли різні рівні міокіну іризину, адипонектину оментину, а також інших цитокінів, різні вираженість болю та характер рентгенологічної прогресії.
Різні тканини, які формують суглоб, зумовлюють різні підходи до лікування. Кілька тканин суглобів можуть демонструвати патологічні зміни, що зумовлюють появу багатьох потенційних мішеней для лікування. Отже, малоймовірно, що одне лікування ОА буде однаково ефективним у запобіганні чи уповільненні прогресування всіх типів структурного ОА. Оскільки уражається багато тканин, малоймовірно, що всі пацієнти з ОА будуть ефективно лікуватися за допомогою однакових втручань [5].
Ще 10-15 років тому почали з’являтися роботи, в яких виокремлювали пацієнтів із кістковим, хрящовим і запальним ендотипом; було висловлено припущення, що ці хворі потребуватимуть різних підходів до лікування. Сьогодні ця теза отримала продовження і розвиток. Наразі виокремлюють хрящовий, запальний і кістковий ендотипи. Перелік препаратів, які, на думку експертів, можуть бути найефективнішими при кожному з них, представлений в таблиці 1.
|
Таблиця 1. Препарати, пов’язані з трьома основними молекулярними або механічними ендотипами ОА [6] |
|
|
Ендотип |
Препарати |
|
Хрящовий |
|
|
Запальний (синовіт) |
|
|
Кістковий |
|
Крім того, патогенез ОА не є сталим від початку до завершення; він змінюється залежно від того, чи це ранній, прогресуючий ОА або пізня стадія, яка потребує тотального ендопротезування. Слід розуміти, що зміни патогенезу є певним викликом і потребують різних лікувальних підходів. Якщо на стадії преОА та раннього ОА прогресуванню можна запобігти за допомогою певних превентивних заходів і правильних фізичних вправ, то на стадії прогресування пацієнт потребує призначення протибольової терапії, симптоматичних препаратів сповільненої дії у терапії ОА (SYSADOA) та, ймовірно, залучення ортопедичних методик. За пізнього ОА в багатьох пацієнтів єдиним виходом позбавитися болю і функціональної неспроможності є тотальне ендопротезування.
Цілком імовірно, що часткова невдача численних клінічних випробувань II-III фази при ОА, як-от інгібітори iNOS, бісфосфонати, кальцитонін, стронцію ранелат, а також потенційна відсутність перетворення структурного покращення на клінічну користь у дослідженні FORWARD пов’язувалися з нездатністю виявити конкретні субпопуляції пацієнтів зі структурними аномаліями, які відповідали фармакодинаміці досліджуваного препарату [7]. Отже, призначаючи лікування без урахування фенотипів, дискредитується сам препарат і не вдається досягти клінічного ефекту.
Професор І. Ю. Головач ще раз підкреслила значну гетерогенність ОА та потребу враховувати різні клінічні фенотипи. Якщо 15 років тому виокремлювали 4 основні фенотипи, а згодом їх виявилося 6, то сьогодні виокремлюють вторинні, вікозалежні, системні, внутрішньо- та зовнішньосуглобові – загалом >10 [8].
6 фенотипів, які підтримують більшість ревматологічних асоціацій:
- фенотип хронічного болю із центральною сенсибілізацією;
- запальний;
- метаболічний;
- фенотип кістково-хрящового обміну;
- механічний;
- мінімальний фенотип захворювання суглобів [1, 9].
У різних дослідженнях саме ці фенотипи можуть мати дещо різні назви, але суть залишається такою самою. В основі формування кожного фенотипу лежить певний ендотип, тобто той молекулярний патогенетичний шлях, через котрий реалізується метаболічний чи травматичний тригер, реалізація якого може піти різним шляхом залежно від індивідуальних особливостей пацієнта. На етапі формування ендотипів і відбувається роз’єднання патогенетичних шляхів. Різні фенотипи, що формуються ключовими факторами ризику, як-от метаболічна дисфункція, старіння та попереднє ушкодження суглобів (травми, артрит), свідчать про різні патофізіологічні шляхи. Це ставить під сумнів традиційний погляд на ОА як на єдиний хворобливий процес і порушує критичне питання: чи є ОА єдиним багатофакторним захворюванням зі спільними кінцевими точками, чи це спектр різних патологічних механізмів, що сходяться до спільного клінічного результату? [10].
Отже, сьогодні йдеться про персоналізоване лікування ОА, яке ґрунтується на визначенні ендотипу, фенотипу та виборі певного тератипу. На підставі даних про гетерогенність ОА сформована концепція стратифікації пацієнтів відповідно до різних фенотипів на підставі їхніх профілів факторів ризику з метою представлення персоналізованої терапії в епоху прецизійної медицини. Водночас фактори ризику можуть запускати різні патологічні механізми, а також поєднуватися в одного пацієнта. Альтернативою цієї концепції є стратифікація пацієнтів за молекулярними механізмами, що лежать в основі розвитку певних фенотипів ОА, – за ендотипами, що має значні перспективи, особливо для розробки лікарських препаратів. Тератипи будуть різними при генетичному, посттравматичному, віковому, метаболічному, гормональному фенотипах, за фенотипу, пов’язаного з механічним навантаженням, а також при запальному ОА. Отже, основу персоналізованої медицини формує концепція виділення клінічного фенотипу, а також розуміння, який шлях лежить в його основі, крім того, цілеспрямований вибір терапії (рис.).
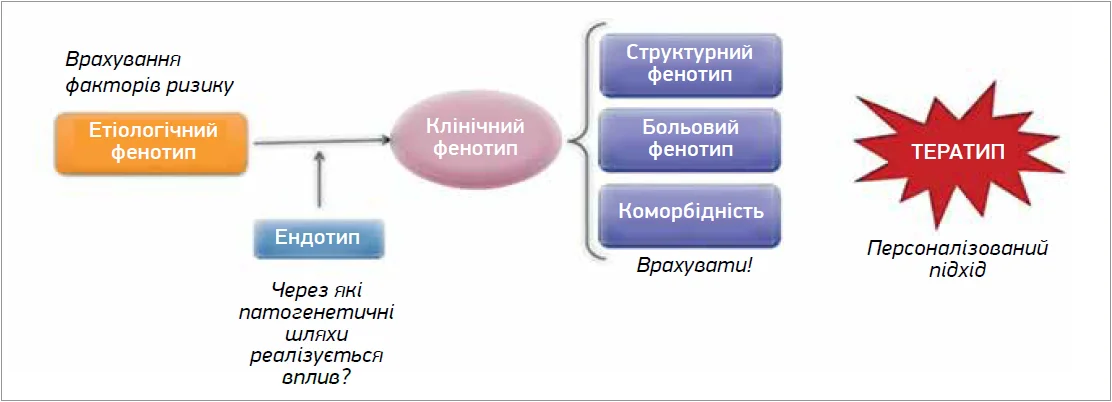 Рис. Адаптація персоналізованої медицини під фенотипи при ОА
Рис. Адаптація персоналізованої медицини під фенотипи при ОА
Професор І. Ю. Головач зазначила, що основу лікування ОА становить застосування SYSADOA. За методикою Delphi оцінено 206 конкретних консультацій, структурованих за 24 клінічними запитаннями.
Група експертів дійшла висновку, що:
- фенотип пацієнта визначає застосування SYSADOA;
- SYSADOA вважаються доречними при первинному ОА (колінні суглоби, кисті, стегна) та за деяких типів вторинного ОА; вони не вважаються доречними при ОА плеча, хребта, гомілковостопного суглоба й ерозивному ОА кистей;
- SYSADOA можуть призначатися пацієнтам із ризиком серцево-судинних захворювань, а також органів травлення, за артеріальної гіпертензії, дисліпідемії, у разі захворювань периферичних судин, цукрового діабету 2 типу та, за винятком діацереїну, пацієнтам зі стравохідним рефлюксом. Не досягнуто згоди щодо призначення SYSADOA для пацієнтів із захворюваннями печінки та нирок [11].
Можливості застосування різних SYSADOA за різних фенотипів продемонстровано в таблиці 2.
|
Таблиця 2. Можливості застосування різних SYSADOA при різних фенотипах |
||||
|
Фенотип |
Неомилювані сполуки авокадо та сої |
Глюкозамін + хондроїтин |
Неденатурований колаген II типу |
Комплементарна терапія (екстракти куркуми, босвелії, верби, шипшини тощо) |
|
Метаболічний |
++ |
+ |
– |
± |
|
Запальний |
++ |
+ |
± |
+ |
|
Посттравматичний |
++ |
+ |
? |
+ |
|
Генетичний |
? |
– |
+ |
? |
|
Вікозалежний |
± |
± |
+ |
+ |
|
Механічне перевантаження |
± |
± |
+ |
– |
Механізм дії неомилюваних сполук авокадо та сої передбачає пригнічення катаболічного запалення, зменшення болю, сповільнення руйнування суглобового хряща, стимуляцію процесів регенерації тканин суглоба [12].
Препарат Піаскледин® 300, що містить неомилювані сполуки олії авокадо та сої, доцільно застосовувати при різних фенотипах ОА:
- метаболічний: підходить завдяки модуляції хронічного низькорівневого запалення – рівнів прозапальних цитокінів: інтерлейкіну‑1β, фактора некрозу пухлини, матриксних металопротеїназ;
- запальний: підходить завдяки контролю запалення між загостреннями – рівнів прозапальних цитокінів: інтерлейкіну‑1β, фактора некрозу пухлини, матриксних металопротеїназ;
- посттравматичний: підходить завдяки зменшенню вторинного запалення та підтримці хряща після травм;
- генетичний: може застосовуватися як додаткова підтримка, але не є основним вибором при спадковій колагеновій недостатності;
- вікозалежний: може застосовуватися в комплексній терапії, у разі виникнення синовіту, запалення;
- механічне перевантаження: може бути корисним при супутньому запаленні, але не є ключовою терапією на тлі механічного перевантаження.
Хондропротекція при застосуванні препарату відбувається за рахунок інгібування вироблення прозапальних медіаторів, що доведено in vitro. Показано, що Піаскледин® 300 ефективно блокує прозапальні та прокатаболічні медіатори, котрі беруть участь у розвитку запалення при ОА. Так, у дослідженні C. Lambert і співавт. (2022) препарат продемонстрував сприятливий вплив на хондроцити завдяки інгібуванню прозапальних медіаторів [13].
Наразі Піаскледин® 300 розглядають як один із препаратів, здатних сповільнити прогресування ОА за рахунок сприяння синтезу білків матриксу хряща, в т. ч. колагену II типу. Він позитивно впливає на хрящові тканини, що зумовлює відновлення структурних компонентів в ушкодженій хрящовій матриці, а також послаблення запального процесу. Результати дослідження надали потенціал для хондропротекторного ефекту при ОА для зазначеного препарату завдяки гальмуванню розпаду колагену, а також сприянню синтезу колагену II типу та протеоглікану матриксу хряща [14].
Показано, що Піаскледин® 300 значно зменшує потребу в застосуванні нестероїдних протизапальних препаратів у пацієнтів з ОА колінного суглоба. До 90-го дня їхнє застосування достовірно знизилося не менш ніж на 50% у 71% пацієнтів, які приймали Піаскледин® 300 по 1 та 2 капсулі на день, порівняно із 36% хворих групи плацебо [15].
Симптоматична ефективність препарату при лікуванні ОА кульшового та колінного суглоба добре доведена у фундаментальних дослідженнях. Його ефективність щодо болю та функціонального стану була значно вищою за плацебо (в 1,6 та 1,4 раза відповідно), збільшувалася із часом і зберігалася після лікування, а переносимість виявилася зіставною із плацебо. Важливим є те, що навіть після 6 міс відміни прийому препарату спостерігали утримання ефекту впродовж 2 міс спостереження [16].
Піаскледин® 300 – рослинний лікарський засіб, для якого характерні:
- мінімізація ризиків побічних дій;
- безпека для довготривалого застосування;
- відсутність протипоказань для хворих на цукровий діабет і пацієнтів із погіршеною толерантністю до глюкози;
- відсутність протипоказань при алергії на молюсків;
- доведене уповільнення прогресування ОА;
- знеболювальна та протизапальна дія;
- зменшення тривалості прийому та дози нестероїдних протизапальних препаратів;
- сприятливий профіль переносимості;
- зручність прийому по 1 капсулі/добу.
Нині Піаскледин® 300 знаходиться в переліку найвідоміших хондропротекторів світу з доведеним механізмом дії.
Список літератури знаходиться в редакції.
Підготувала Віталіна Хмельницька
Медична газета «Здоров’я України 21 сторіччя» № 4 (615), 2026 р



