11 травня, 2026
Алергічний риніт: від викликів системи до ефективної терапії
Алергічний риніт (АР) залишається однією з найпоширеніших хронічних патологій, що суттєво впливає на якість життя, працездатність і ризик розвитку супутніх захворювань, зокрема бронхіальної астми (БА). Попри наявність сучасних рекомендацій, включно з ARIA, в клінічній практиці зберігаються труднощі ранньої діагностики, стратифікації тяжкості, контролю симптомів і досягнення довготривалого ефекту терапії.
В умовах трансформації системи охорони здоров’я, обмеженого доступу до вузькопрофільних спеціалістів і зростання поширеності алергічних захворювань питання оптимізації алергологічної допомоги набуває особливої актуальності, що зумовлює потребу в міждисциплінарному підході, оновленні клінічних алгоритмів і впровадженні сучасних терапевтичних та діагностичних рішень.
Ці питання стали предметом обговорення під час зустрічі провідних фахівців з алергології, що відбулася 1 квітня за підтримки компанії «Гленмарк». У межах заходу було розглянуто організаційні виклики алергологічної служби в Україні та сучасні підходи до менеджменту АР.
Особливу увагу приділено веденню пацієнтів із середньотяжким і тяжким перебігом АР, вибору фармакотерапії з урахуванням клінічної ситуації, ролі інтраназальних кортикостероїдів (ІнКС) і комбінованих препаратів у досягненні контролю симптомів, а також фармакологічним властивостям мометазону фуроату та можливостям сучасної лабораторної алергодіагностики для персоналізованого підходу.
Сучасні методи симптоматичної терапії АР
 Доповідь голови групи експертів МОЗ України за напрямом «Алергологічна допомога та імунологія», віцепрезидента Асоціації алергологів України (ААУ), доктора медичних наук, професора Євгенії Михайлівни Дитятковської була присвячена сучасним підходам до симптоматичної терапії АР.
Доповідь голови групи експертів МОЗ України за напрямом «Алергологічна допомога та імунологія», віцепрезидента Асоціації алергологів України (ААУ), доктора медичних наук, професора Євгенії Михайлівни Дитятковської була присвячена сучасним підходам до симптоматичної терапії АР.
За оцінками, ≈10-40% населення мають прояви алергічної патології, а АР уражає сотні мільйонів людей у світі, формуючи значне навантаження на систему охорони здоров’я [1, 2].
В Україні також спостерігається висока поширеність АР із вираженою регіональною варіабельністю: показники захворюваності та поширеності серед дорослого населення суттєво відрізняються залежно від області, що відображає вплив екологічних факторів і особливості діагностики (рис. 1).
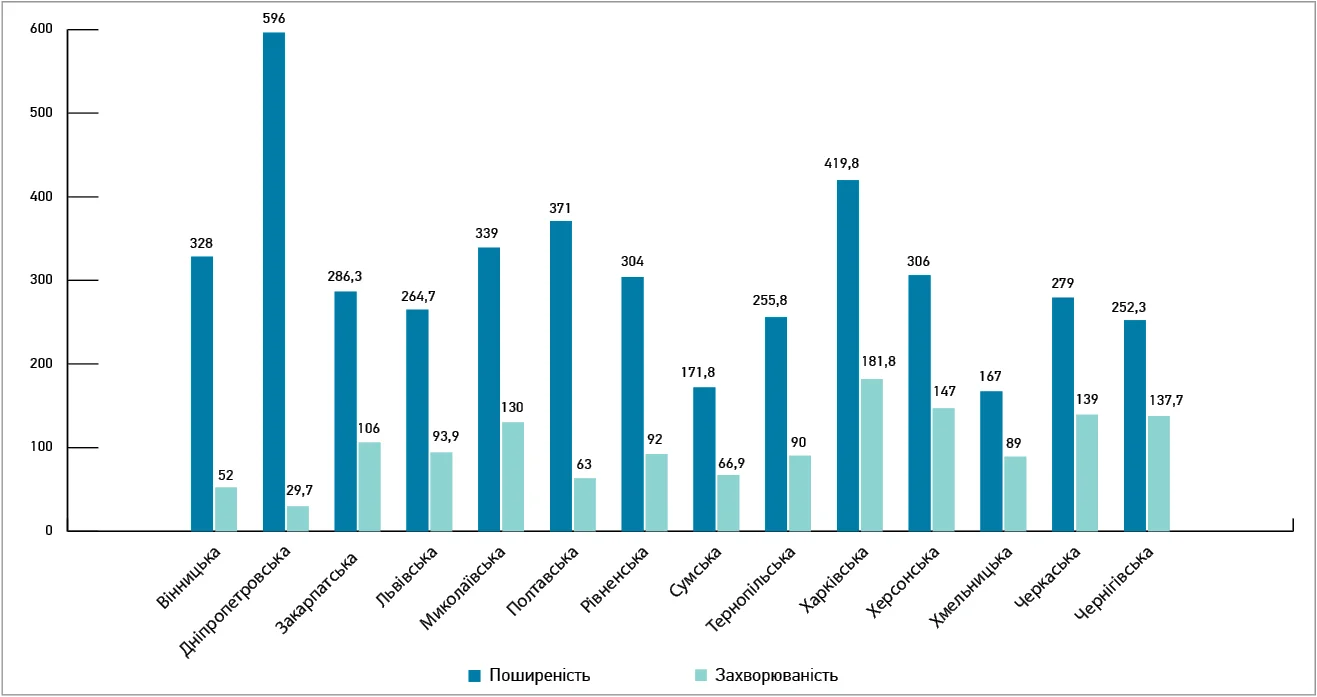 Рис. 1. Поширеність АР і захворюваність на нього серед дорослого населення України (на 100 тис. населення, 2018 р.)
Рис. 1. Поширеність АР і захворюваність на нього серед дорослого населення України (на 100 тис. населення, 2018 р.)
АР є не лише поширеним, а й клінічно значущим захворюванням, що істотно впливає на повсякденне життя пацієнтів. Неконтрольований перебіг супроводжується порушенням сну, зниженням концентрації, когнітивної продуктивності та працездатності: до 77% пацієнтів мають труднощі із засинанням, а значна частка – денну втому, що безпосередньо знижує якість життя та соціальну активність [3, 4].
АР також має тісний патофізіологічний і клінічний зв’язок із БА в межах концепції «єдиного дихального тракту», що зумовлює потребу в комплексному підході до діагностики та лікування. Крім того, АР асоціюється з підвищеним ризиком розвитку інших ЛОР-патологій, зокрема хронічного синуситу, середнього отиту та поліпозу носа [5]. З огляду на це АР слід розглядати як системне хронічне захворювання, що потребує своєчасної діагностики, адекватної оцінки тяжкості та ефективного контролю симптомів.
Патогенетично АР є хронічним запальним захворюванням слизової оболонки носа, в основі якого лежить IgE-опосередкована реакція гіперчутливості із залученням клітин і медіаторів запалення. Контакт з алергеном запускає каскад імунологічних реакцій з активацією мастоцитів, базофілів і Т-лімфоцитів і вивільненням гістаміну, лейкотрієнів, простагландинів, цитокінів, що формують прояви ранньої та пізньої фаз алергічної відповіді [6].
Ключову роль у підтриманні запалення відіграють еозинофіли, які під дією цитокінів (зокрема, інтерлейкіну-5) інфільтрують слизову оболонку та вивільняють цитотоксичні білки (ECP, MBP), спричиняючи ушкодження епітелію і підтримання запального процесу [7, 8].
Запальний процес при АР має не лише локальний, а й системний характер, що пояснює часте поєднання з іншими атопічними захворюваннями. Клінічні прояви формуються внаслідок дії різних медіаторів: гістамін зумовлює свербіж, чхання та ринорею, тоді як лейкотрієни й цитокіни – набряк слизової оболонки і назальну обструкцію. На окрему увагу заслуговують добові коливання активності запалення: рівні гістаміну та триптази в назальному секреті змінюються протягом доби, що частково пояснює варіабельність симптомів і необхідність індивідуалізації терапії [9].
Важливим аспектом сучасного розуміння АР є регіональні особливості сенсибілізації, що впливають на клінічний перебіг і вибір терапії. За даними молекулярної алергодіагностики, в Україні більшість пацієнтів сенсибілізовані до інгаляційних алергенів, зокрема пилкових (до 97%), а також до харчових алергенів (до 99%), що відображено на рисунку 2.
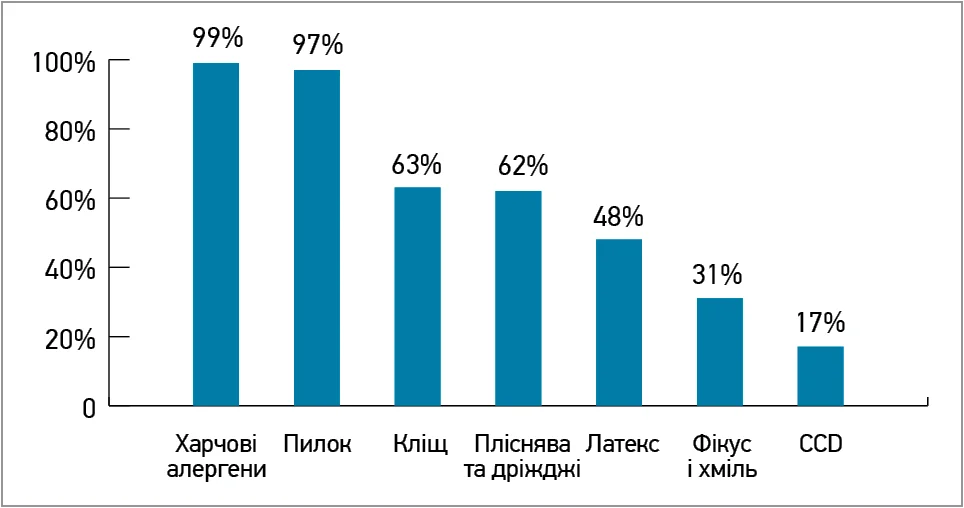 Рис. 2. Розподіл частоти сенсибілізації за групами алергенів (Україна)
Рис. 2. Розподіл частоти сенсибілізації за групами алергенів (Україна)
Згідно з рекомендаціями ARIA, терапія АР має бути поетапною та індивідуалізованою з урахуванням тяжкості перебігу, частоти симптомів і відповіді на лікування [10]. У цьому контексті ІнКС розглядаються як основа терапії, оскільки впливають на ключові механізми запалення – зменшують еозинофільну інфільтрацію, продукцію цитокінів і набряк слизової оболонки, що забезпечує достовірне зниження всіх назальних симптомів, включно із закладеністю носа [11]. Водночас інтраназальні антигістамінні препарати (ІнАГП) ефективно купіюють симптоми ранньої фази алергічної реакції, як-от свербіж, чхання та ринорея, проте їхній вплив на назальну обструкцію є обмеженим.
У пацієнтів із помірним і тяжким перебігом АР монотерапія ІнКС або ІнАГП не завжди забезпечує повний контроль симптомів, що обґрунтовує необхідність комбінованого підходу. Згідно з ARIA, в таких випадках доцільним є застосування фіксованих комбінацій ІнАГП та ІнКС, які забезпечують вищу ефективність порівняно з кожним компонентом окремо [10]. Це має чітке патогенетичне підґрунтя: ІнАГП впливають на ранню фазу алергічної реакції, тоді як ІнКС контролюють пізню фазу запалення, зменшуючи набряк і назальну обструкцію, що в сукупності забезпечує швидший початок дії та вираженіший клінічний ефект.
Серед ІнКС особливу увагу привертає мометазону фуроат, який поєднує високу протизапальну активність зі сприятливим профілем безпеки. Завдяки дуже низькій системній біодоступності (≈0,46%) ризик системних побічних ефектів є мінімальним, що має принципове значення при тривалому застосуванні, особливо в педіатричній практиці [12]. Отже, ІнКС, зокрема мометазону фуроат, залишаються базисом терапії АР, тоді як у пацієнтів із вираженими симптомами, назальною обструкцією та очними проявами доцільним є застосування фіксованих комбінацій ІнКС з ІнАГП, що дозволяє досягти швидшого та повнішого контролю захворювання.
Однією з таких комбінацій є поєднання олопатадину гідрохлориду та мометазону фуроату (Ріалтріс), яке забезпечує подвійний механізм дії: олопатадин як ІнАГП блокує H1-рецептори та швидко купіює симптоми ранньої фази (свербіж, чхання, ринорея), тоді як мометазону фуроат як ІнКС чинить виражену протизапальну дію, зменшуючи набряк і назальну обструкцію. Клінічно це проявляється швидким початком дії – уже протягом перших 15 хв після застосування, а також вираженішим і стабільнішим контролем симптомів порівняно з монотерапією окремими компонентами [13].
Ефективність та безпека фіксованої комбінації олопатадину гідрохлориду та мометазону фуроату була оцінена в рандомізованих клінічних дослідженнях (РКД) за участю пацієнтів із сезонним АР.
Так, у подвійному сліпому плацебо-контрольованому РКД III фази за участю пацієнтів із сезонним АР було продемонстровано, що застосування комбінації олопатадин/мометазон забезпечує статистично значуще зниження сумарного назального симптоматичного бала (Total Nasal Symptom Score, TNSS) порівняно як із плацебо, так і з монотерапією окремими компонентами.
Зниження TNSS спостерігалося вже на ранніх термінах після початку лікування, що свідчить про швидкий початок дії препарату. Крім того, в пацієнтів, які отримували комбінацію, спостерігалося достовірне покращення всіх основних симптомів АР, включно із закладеністю носа, ринореєю, чханням і свербежем, що є клінічно значущим, зважаючи на обмежений вплив ІнАГП на назальну обструкцію.
Окремо в РКД було продемонстровано покращення очних симптомів, зокрема свербежу та сльозотечі, що розширює можливості застосування комбінації у пацієнтів з алергічним ринокон’юнктивітом (рис. 3).
![Рис. 3. Динаміка зміни відображеного сумарного бала очних симптомів (reflective Total Ocular Symptom Score, rTOSS) у пацієнтів із сезонним АР на тлі застосування фіксованої комбінації олопатадину гідрохлориду та мометазону фуроату порівняно з плацебо [14] Рис. 3. Динаміка зміни відображеного сумарного бала очних симптомів (reflective Total Ocular Symptom Score, rTOSS) у пацієнтів із сезонним АР на тлі застосування фіксованої комбінації олопатадину гідрохлориду та мометазону фуроату порівняно з плацебо [14]](/multimedia/userfiles/images/2026/ZU_6_2026/ZU_06_2026_st26_pic3.webp) Рис. 3. Динаміка зміни відображеного сумарного бала очних симптомів (reflective Total Ocular Symptom Score, rTOSS) у пацієнтів із сезонним АР на тлі застосування фіксованої комбінації олопатадину гідрохлориду та мометазону фуроату порівняно з плацебо [14]
Рис. 3. Динаміка зміни відображеного сумарного бала очних симптомів (reflective Total Ocular Symptom Score, rTOSS) у пацієнтів із сезонним АР на тлі застосування фіксованої комбінації олопатадину гідрохлориду та мометазону фуроату порівняно з плацебо [14]
Примітка: ДІ – довірчий інтервал.
Профіль безпеки комбінації був сприятливим: частота побічних реакцій залишалася низькою, а більшість з них мали легкий або помірний характер. Найчастіше спостерігалися дисгевзія та носові кровотечі, які не потребували відміни терапії [13]. Отримані результати РКД підтверджують доцільність використання фіксованих комбінацій ІнАГП та ІнКС у пацієнтів з АР, особливо за помірного та тяжкого перебігу захворювання.
Діяльність Асоціації алергологів України: виклики сьогодення
 Президент ААУ, доктор медичних наук, професор Сергій Вікторович Зайков розповів про діяльність професійної спільноти в умовах сучасних викликів і трансформації системи охорони здоров’я.
Президент ААУ, доктор медичних наук, професор Сергій Вікторович Зайков розповів про діяльність професійної спільноти в умовах сучасних викликів і трансформації системи охорони здоров’я.
Сучасна алергологічна допомога в Україні функціонує в умовах суттєвих системних змін і викликів, що потребують як організаційної адаптації, так і переосмислення ролі професійної спільноти. Важливе місце в цьому процесі посідає діяльність ААУ, яка є не лише професійною платформою для обміну досвідом, а й активним учасником формування підходів до надання медичної допомоги.
Одне з ключових досягнень останніх років – участь фахівців ААУ в розробці нормативної бази, зокрема наказу Міністерства охорони здоров’я (МОЗ) України № 1971 «Про організацію надання алергологічної допомоги населенню України», що визначає сучасні принципи структурування служби та маршрутизації пацієнтів. Це створює підґрунтя для системнішого підходу до ведення пацієнтів з алергічними захворюваннями, включно з АР.
Паралельно активно розвиваються освітній та комунікаційний напрями діяльності. Оновлення цифрових ресурсів, зокрема офіційного сайту і професійних комунікаційних платформ, сприяє кращому доступу лікарів до актуальної інформації та клінічних матеріалів. Важливим інструментом професійної взаємодії також стали спеціалізовані спільноти, що забезпечують швидкий обмін клінічним досвідом і консультаційну підтримку.
Значну роль у підвищенні рівня обізнаності лікарів і пацієнтів відіграють освітні проєкти, зокрема «Життя без алергії» й «Точки дотику в алергології та дерматології», які поєднують науковий та практичний компоненти і реалізуються у форматі як офлайн-, так і онлайн-активностей. Додатково розвиток спеціалізованих видань, як-от освітньо-практичний журнал Allergy Practice, сприяє поширенню доказових знань серед лікарської спільноти.
Не менш важливим є міжнародний вектор співпраці. ААУ інтегрована в світову алергологічну спільноту, зокрема акредитована у Всесвітній організації алергії (WAO), що відкриває можливості для обміну досвідом, участі в міжнародних конгресах і впровадження сучасних клінічних підходів у національну практику.
Отже, сучасна алергологічна служба в Україні розвивається в напрямі інтеграції з міжнародними стандартами, цифровізації та посилення ролі професійних об’єднань. Це створює основу для покращення якості діагностики та лікування алергічних захворювань, зокрема АР, і визначає подальші напрями розвитку галузі.
Виклики у веденні пацієнтів із середньотяжким і тяжким перебігом АР
 Наступна доповідь була представлена професором ДУ «Інститут отоларингології ім. О. С. Коломійченка НАМН України» (м. Київ), доктором медичних наук Інною Володимирівною Гогунською та присвячена сучасним викликам у веденні пацієнтів із середньотяжким і тяжким перебігом АР.
Наступна доповідь була представлена професором ДУ «Інститут отоларингології ім. О. С. Коломійченка НАМН України» (м. Київ), доктором медичних наук Інною Володимирівною Гогунською та присвячена сучасним викликам у веденні пацієнтів із середньотяжким і тяжким перебігом АР.
Сьогодні клінічний перебіг АР дедалі більше визначається не лише індивідуальними особливостями пацієнта, а й впливом екологічних факторів. В умовах повномасштабної війни в Україні сформувався комплекс чинників, що негативно впливають на довкілля та здоров’я населення.
Забруднення повітря зумовлене як прямими (детонація боєприпасів, застосування артилерії, ракет і авіаційних бомб із викидом токсичних продуктів згоряння), так і непрямими чинниками (масштабні пожежі, ураження нафтобаз, промислових підприємств, енергетичної інфраструктури). За оцінками, це спричинило викид десятків мільйонів тонн забруднювачів, зокрема ≈120 млн тонн CO₂. Водночас значних ушкоджень зазнали водні ресурси та ґрунти, де накопичення агрохімікатів, важких металів і продуктів детонації формує стійке екологічне навантаження.
Такі зміни мають безпосереднє клінічне значення: вплив аерополютантів і дрібнодисперсних часток підвищує реактивність слизової, посилює запалення та зумовлює тяжчий перебіг АР, що супроводжується частішими загостреннями, зниженням ефективності стандартної терапії та потребою в її інтенсифікації.
Важливою клінічною особливістю сучасних пацієнтів є висока поширеність полісенсибілізації: до 80% хворих мають чутливість до кількох алергенів, що ускладнює перебіг АР і обмежує ефективність монотерапії. Поєднання сезонних і цілорічних тригерів сприяє перевищенню індивідуального симптоматичного порогу й формуванню вираженішої та тривалішої симптоматики.
В цих умовах ключовим є своєчасне призначення ефективної терапії з урахуванням рівня контролю симптомів і можливістю її швидкої інтенсифікації. Згідно з ARIA, в пацієнтів із помірним і тяжким АР один із найефективніших підходів – комбінація ІнАГП та ІнКС, особливо при назальній обструкції, а також очних симптомах, що не лише підвищує ефективність лікування, а й спрощує його, покращуючи прихильність пацієнтів. Прикладом такого підходу є фіксована комбінація олопатадину гідрохлориду та мометазону фуроату (Ріалтріс), яка забезпечує швидкий і комплексний контроль симптомів за рахунок впливу на різні фази алергічної реакції.
Водночас у реальній практиці недотримання рекомендацій і самолікування ускладнюють контроль захворювання, що підсилює роль лікаря та обґрунтовує використання цифрових інструментів ARIA, зокрема MASK-air, які дозволяють персоналізувати терапію на основі щоденної оцінки симптомів (ВАШ) і рівня контролю, оптимізуючи лікування та підвищуючи його ефективність.
Мометазону фуроат у лікуванні АР
 Фінальна доповідь була представлена доктором медичних наук, професором Артемієм Євгенійовичем Богомоловим і присвячена фармакологічному профілю, клінічній ефективності та безпеці мометазону фуроату в лікуванні АР.
Фінальна доповідь була представлена доктором медичних наук, професором Артемієм Євгенійовичем Богомоловим і присвячена фармакологічному профілю, клінічній ефективності та безпеці мометазону фуроату в лікуванні АР.
Мометазону фуроат поєднує виражену протизапальну активність з мінімальною системною дією та є перспективною основою для створення комбінованих препаратів.
Його ефекти реалізуються через зв’язування із ГКС-рецепторами та регуляцію експресії генів, що пригнічує продукцію прозапальних цитокінів, зменшує еозинофільне запалення, дегрануляцію мастоцитів і вивільнення медіаторів алергії, клінічно проявляючись зменшенням набряку та симптомів. Важливою перевагою є фармакокінетичний профіль з дуже низькою системною біодоступністю, що мінімізує ризик системних ефектів навіть при тривалому застосуванні.
Методика TIX базується на оцінці трьох показників ефективності (назальні й очні симптоми, загальна оцінка стану) та трьох показників безпеки (носові кровотечі, вплив на ріст, системні офтальмологічні ефекти) з подальшим розрахунком співвідношення сумарного бала ефективності до бала побічних ефектів. Такий підхід дозволяє інтегрально оцінити клінічну доцільність застосування ІнКС і перейти до обґрунтованішого вибору препарату.
За результатами аналізу, мометазону фуроат продемонстрував найвищий показник TIX серед представників класу (рис. 4), що свідчить про оптимальний баланс ефективності та безпеки й обґрунтовує його використання як базисної терапії АР, особливо за потреби довготривалого лікування. Це підкреслює доцільність вибору саме цієї молекули як базисної терапії АР, особливо в пацієнтів, для яких важливими є як ефективність контролю симптомів, так і довготривала безпека лікування.
![Рис. 4. Порівняльна оцінка ІнКС за терапевтичним індексом (TIX): співвідношення ефективності та безпеки [15] Рис. 4. Порівняльна оцінка ІнКС за терапевтичним індексом (TIX): співвідношення ефективності та безпеки [15]](/multimedia/userfiles/images/2026/ZU_6_2026/ZU_06_2026_st26_pic4.webp) Рис. 4. Порівняльна оцінка ІнКС за терапевтичним індексом (TIX): співвідношення ефективності та безпеки [15]
Рис. 4. Порівняльна оцінка ІнКС за терапевтичним індексом (TIX): співвідношення ефективності та безпеки [15]
Примітки: БЕ – бал ефективності; БПЕ – бал побічних ефектів; БДП – беклометазону дипропіонат; БУД – будесонід; ФФ – флутиказону фуроат; ФП – флутиказону пропіонат; МФ – мометазону фуроат; ТРІАМ – тріамцинолон.
Важливим, але часто недооціненим фактором ефективності лікування АР є прихильність до терапії. Однією із ключових причин її зниження залишається «стероїдна фобія» – напружено-уважне ставлення до кортикостероїдів, особливо в педіатричній практиці, де батьки побоюються впливу на ріст, гормональну систему або «звикання».
Ці уявлення значною мірою формуються під впливом соціальних мереж: аналіз 294 публікацій (YouTube, Instagram, TikTok) показав, що більшість контенту створюється немедичними фахівцями, має >400 тис. переглядів і акцентує увагу переважно на ризиках, формуючи викривлене сприйняття безпеки терапії [16].
У результаті пацієнти нерідко формують негативне ставлення до лікування ще до консультації з лікарем, що зумовлює відмову від терапії, її нерегулярне застосування або передчасне припинення.
В подоланні «стероїдної фобії» ключове значення має коректне інформування пацієнтів про безпеку ІнКС, зокрема мометазону фуроату, що визначається його фармакокінетичними особливостями. Препарат має надзвичайно низьку системну біодоступність (≈0,46%), високий рівень зв’язування з білками плазми (98-99%) і швидко метаболізується без утворення активних метаболітів, що мінімізує системний вплив. Висока рецепторна афінність (RRA ≈2200) забезпечує виражену локальну протизапальну дію при низьких дозах.
У клінічній практиці це означає, що при правильному застосуванні мометазону фуроат діє переважно локально, практично не чинить системних ефектів, не впливає на ріст у дітей і не викликає «звикання». Чітке донесення цих переваг є ключовим для зменшення тривожності пацієнтів і підвищення прихильності до лікування.
Клінічна ефективність мометазону фуроату підтверджена метааналізами. Зокрема, в метааналізі Penagos і співавт. (16 РКД, 2998 пацієнтів) продемонстровано достовірне зниження TNSS порівняно із плацебо (СРС –0,49; p<0,00001) із покращенням усіх основних симптомів АР: назальної обструкції (СРС –0,41), ринореї (СРС –0,44), чхання (СРС –0,40) та свербежу (СРС –0,39), при цьому частота небажаних явищ не відрізнялася від плацебо (відносний ризик (ВР) 0,99; p=0,91), що підтверджує хорошу переносимість терапії [17].
У мережевому метааналізі Kim і співавт. (26 РКД, >5000 пацієнтів, 2023 р.) мометазону фуроат продемонстрував найвищу ефективність серед ІнКС (СРС –0,47), випереджаючи флутиказону фуроат (–0,46) і циклесонід (–0,44), що підтверджує його провідні позиції у межах класу [18].
Порівняльні дослідження також показують переваги ІнКС над пероральними АГП, зокрема щодо контролю назальної обструкції, тоді як ефективність у зменшенні ринореї, чхання та свербежу є зіставною. Завдяки протизапальному ефекту ІнКС забезпечують повніший контроль симптомів, включно з очними проявами, що дозволяє розглядати їх як універсальний варіант терапії АР [19, 20].
Додатковою перевагою є вплив на якість сну: завдяки контролю нічних симптомів і відсутності седативного ефекту мометазону фуроат покращує сон без ризику денної сонливості, характерної для деяких АГП. Отже, ІнКС, зокрема мометазону фуроат, забезпечують повніший контроль симптомів АР і обґрунтовують свою роль як базисної терапії.
Профіль безпеки препарату добре вивчений: частота небажаних явищ не відрізняється від плацебо (ВР 0,99; 95% ДІ 0,81-1,20; p=0,91). Найчастіші місцеві реакції (носові кровотечі ≈5%, подразнення, сухість, фарингіт) зазвичай є легкими та транзиторними.
Завдяки низькій системній біодоступності інтраназальний мометазону фуроат не має клінічно значущого впливу на гіпоталамо-гіпофізарно-надниркову вісь, а також не асоціюється зі змінами внутрішньоочного тиску, ризиком катаракти чи зниженням мінеральної щільності кісткової тканини, що визначає його сприятливий системний профіль безпеки.
Застосування ІнКС у педіатрії має особливе значення через чутливість до безпеки терапії. Мометазону фуроат має чіткі вікові показання та зручні режими дозування: 100 мкг/добу в дітей віком 3-11 років і 200 мкг/добу в пацієнтів віком >12 років із можливістю зниження дози після досягнення контролю.
Мометазону фуроат дозволений до застосування з раннього віку та має переконливу доказову базу: мережевий метааналіз 43 РКД (>10 000 дітей) підтвердив його сприятливий профіль безпеки, а в РКД тривалістю до 1 року не виявлено негативного впливу на лінійний ріст [18, 22]. Окрім контролю симптомів АР, спостерігалися додаткові ефекти, зокрема покращення функції слухової труби та зменшення проявів секреторного отиту, тоді як вплив на аденоїдну гіпертрофію є менш однозначним, але може супроводжуватися зменшенням симптомів [18, 23, 24]. У сукупності це визначає його як один з оптимальних варіантів терапії АР у дітей.
Місце ІнКС, зокрема мометазону фуроату, чітко визначене в міжнародних настановах: ARIA рекомендує їх як терапію першої лінії при помірному та тяжкому АР завдяки найефективнішому контролю назальних симптомів [10]. Аналогічну позицію мають EAACI та AAO-HNS, підкреслюючи перевагу ІнКС над пероральними АГП і їхню безпеку, зокрема в дітей [25, 26]. Водночас експертні оцінки, зокрема WAO, свідчать про відмінності між молекулами за співвідношенням ефективності та безпеки, при цьому мометазону фуроат розглядається як один із найзбалансованіших варіантів, що підтверджує його ключову роль у базисній терапії АР.
Отже, мометазону фуроат є оптимальним вибором як для монотерапії, так і в складі фіксованих комбінацій, зокрема з ІнКС, що дозволяє забезпечити швидший і повніший контроль симптомів АР, як це реалізовано в препараті Ріалтріс.
Висновки
Проведення зустрічі провідних фахівців з алергології засвідчило актуальність проблеми АР і необхідність удосконалення підходів до його ведення в сучасних умовах. Обговорення охопило як системні виклики алергологічної служби, так і практичні аспекти діагностики та лікування АР.
Сучасна терапія АР має ґрунтуватися на індивідуалізованому підході з урахуванням тяжкості захворювання, рівня контролю симптомів і клінічних особливостей пацієнта. ІнКС, зокрема мометазону фуроат, залишаються основою лікування завдяки доведеній ефективності та сприятливому профілю безпеки.
Водночас у пацієнтів із помірним і тяжким перебігом АР доцільним є застосування комбінованих підходів. Фіксована комбінація олопатадину та мометазону фуроату (Ріалтріс) забезпечує швидкий і комплексний контроль симптомів, впливаючи на різні фази алергічної реакції, що сприяє підвищенню ефективності терапії та покращенню прихильності пацієнтів до лікування.
Отже, інтеграція сучасних доказових підходів, фармакологічних інновацій і персоналізованої стратегії ведення – ключ до ефективного контролю АР і покращення якості життя пацієнтів.
Список літератури знаходиться в редакції.
Підготувала Ганна Кирпач
Медична газета «Здоров’я України 21 сторіччя» № 6 (617), 2026 р



