8 квітня, 2026
Резидуальний серцево-судинний ризик і тригліцерид-збагачені ліпопротеїни: від оцінювання до терапевтичних стратегій
Попри значні досягнення сучасної ліпідознижувальної терапії (ЛЗТ), проблема резидуального серцево-судинного (СС) ризику залишається однією із ключових у кардіології. Особливу увагу нині приділяють ролі тригліцерид-збагачених ліпопротеїнів і ремнантних частинок як важливих чинників атерогенезу. Про підходи до оцінювання ризику та можливості його корекції своїми думками поділилися провідні експерти – Олена Іванівна Мітченко, д.мед.н., професор, співголова Українського товариства з атеросклерозу, завідувач відділу ендокринної кардіології та дисліпідемій ДУ ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені М.Д. Стражеска» НАМН України (м. Київ), та Альберто Замбон, професор кафедри внутрішньої медицини Падуанського університету (Італія), член Європейського товариства атеросклерозу (EAS) та Міжнародного товариства атеросклерозу (IAS).
Ремнанти й резидуальний серцево-судинний ризик: сучасні підходи до оцінювання та корекції
 Олена Іванівна Мітченко під час виступу в межах Науково-практичної конференції «Сучасні технології та дослідження в кардіології», що відбулася у березні 2026 р., зауважила, що незважаючи на суттєві успіхи сучасної ЛЗТ, у значної частки пацієнтів із серцево-судинними захворюваннями (ССЗ) зберігається так званий резидуальний СС-ризик. Під цим поняттям розуміють імовірність розвитку макро- і мікросудинних ускладнень, що відзначається навіть за умови досягнення цільових рівнів холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ), а також адекватного контролю артеріального тиску та глікемії (Fruchart et al., 2022). Відповідно до сучасних рекомендацій Європейського товариства кардіологів (ESC, 2025), першочерговим завданням ЛЗТ є досягнення цільових рівнів ХС ЛПНЩ залежно від категорії СС-ризику: <1,8 ммоль/л для пацієнтів із високим ризиком, <1,4 ммоль/л – дуже високим ризиком та <1,0 ммоль/л – екстремально високим ризиком. Однак навіть за досягнення цих цільових показників ризик атеросклеротичних подій повністю не усувається (Mach et al., 2025).
Олена Іванівна Мітченко під час виступу в межах Науково-практичної конференції «Сучасні технології та дослідження в кардіології», що відбулася у березні 2026 р., зауважила, що незважаючи на суттєві успіхи сучасної ЛЗТ, у значної частки пацієнтів із серцево-судинними захворюваннями (ССЗ) зберігається так званий резидуальний СС-ризик. Під цим поняттям розуміють імовірність розвитку макро- і мікросудинних ускладнень, що відзначається навіть за умови досягнення цільових рівнів холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ), а також адекватного контролю артеріального тиску та глікемії (Fruchart et al., 2022). Відповідно до сучасних рекомендацій Європейського товариства кардіологів (ESC, 2025), першочерговим завданням ЛЗТ є досягнення цільових рівнів ХС ЛПНЩ залежно від категорії СС-ризику: <1,8 ммоль/л для пацієнтів із високим ризиком, <1,4 ммоль/л – дуже високим ризиком та <1,0 ммоль/л – екстремально високим ризиком. Однак навіть за досягнення цих цільових показників ризик атеросклеротичних подій повністю не усувається (Mach et al., 2025).
Резидуальний ризик є багатофакторним явищем і формується як під впливом традиційних факторів ризику (нездоровий спосіб життя, дисліпідемія, артеріальна гіпертензія, ожиріння), так і нових метаболічних механізмів, що залишаються поза межами стандартного контролю ліпідного профілю. Значущу роль у формуванні резидуального ризику відіграють багаті на тригліцериди (ТГ) ліпопротеїни, що утворюються в печінці та кишківнику і відповідають за транспорт ТГ у крові. Резидуальний ризик зростає паралельно із підвищенням рівня ТГ.
Під час метаболізму ТГ-збагачених ліпопротеїнів утворюються так звані ремнантні частинки – залишкові ліпопротеїни, багаті на ХС. Вони мають виразний атерогенний потенціал, оскільки здатні проникати через ендотелій судин і накопичуватися у судинній стінці, стимулюючи запальні процеси та формування атеросклеротичних бляшок (Nordestgaard et al., 2017). Ці ремнантні частинки можуть підтримувати залишковий ризик навіть після оптимальної терапії статинами (Langlois et al., 2018; Zambon, 2025).
Для оцінювання їх внеску в атерогенез використовують показник ремнантного ХС, який розраховують на основі рівнів загального ХС, ХС ЛПНЩ та ХС ліпопротеїнів високої щільності (ЛПВЩ) за формулою: Ремнантний ХС = загальний ХС – ХС ЛПНЩ – ХС ЛПВЩ.
Підвищення рівня ТГ зазвичай супроводжується зростанням концентрації ремнантного ХС. Доведено, що підвищений уміст ремнантів, подібно до ЛПНЩ, асоційований зі збільшенням ймовірності розвитку ішемічної хвороби серця, інфаркту міокарда та інших атеросклеротичних ССЗ (АССЗ) (Varbo et al., 2015; Nordestgaard et al., 2026).
Відповідно до настанови Європейського товариства кардіологів (ESC, 2021), важливе значення має оцінка СС-ризику за шкалою SCORE‑2, яка дозволяє прогнозувати 10-річну ймовірність як фатальних, так і нефатальних СС-подій, насамперед інфаркту міокарда та інсульту. Своєю чергою попередня модель SCORE враховувала лише ймовірність фатальних епізодів. Це відображає зміну парадигми оцінювання ризику, адже дозволяє точніше стратифікувати пацієнтів і своєчасно призначати профілактичну терапію. Для осіб старшого віку (≥70 років) застосовується модифікована шкала SCORE‑2-OP, адаптована до особливостей ризику в цій віковій групі.
На відміну від попередніх моделей оцінювання ризику, у SCORE‑2 та SCORE‑2-OP використовується не загальний ХС, а показник ХС ліпопротеїнів невисокої щільності (не-ЛПВЩ). Це пояснюється тим, що не-ЛПВЩ відображає сумарну концентрацію всіх атерогенних ліпопротеїнів, які містять аполіпопротеїн B (ApoB), зокрема ЛПНЩ, ліпопротеїни дуже низької (ЛПДНЩ) та проміжної щільності (ЛППЩ), ремнантні частинки та ліпопротеїн (a) ((Lp(a)). Застосування цього показника дозволяє точніше оцінити атерогенний потенціал ліпідного профілю, особливо у пацієнтів із підвищеним рівнем ТГ. Цільові рівні ХС не-ЛПВЩ зазвичай приблизно на 0,8 ммоль/л вищі, ніж відповідні цільові значення ХС ЛПНЩ (ESC/EAS, 2019).
Показник ХС не-ЛПВЩ обчислюється досить просто: ХС не-ЛПВЩ = загальний ХС – ХС ЛПВЩ.
Важливим фактором атерогенності, крім концентрації ліпопротеїнів, є розмір їх частинок. Дрібні щільні частинки ЛПНЩ мають значно вищий атерогенний потенціал порівняно з такими більшого розміру. Вони легше проникають у судинну стінку, більш схильні до окиснення та довше циркулюють у крові. Такі частинки часто формуються саме при гіпертригліцеридемії (ГТГ) і разом зі зниженим рівнем ЛПВЩ формують тріаду, характерну для атерогенної дисліпідемії, яка є одним з основних чинників розвитку та прогресування ССЗ у пацієнтів з метаболічним синдромом та цукровим діабетом (ЦД) (Reaven et al., 1993).
У зв’язку з цим сучасні стратегії лікування дисліпідемій спрямовані не лише на зниження ХС ЛПНЩ, а й на корекцію ТГ-збагачених ліпопротеїнів. Одним із препаратів, що застосовуються з цією метою, є фенофібрат (Трайкор® 145 мг), який активує ядерний рецептор PPAR-α і впливає на ключові ланки ліпідного метаболізму (Keating, Croom, 2007). Окрім впливу на рівень ТГ, фенофібрат сприяє зменшенню концентрації дрібних щільних частинок ЛПНЩ, що є одним із механізмів зниження атерогенного ризику (Feher et al., 1999).
При цьому, як зауважила Олена Іванівна, фібрати не є однорідним класом препаратів за своїми ефектами. Зокрема, фенофібрат вирізняється серед інших представників здатністю знижувати рівень ApoB, що відображає загальну кількість атерогенних частинок і є точнішим маркером резидуального ризику. Крім того, підтверджено комплексний вплив фенофібрату на ліпідний профіль – з одночасним зниженням ТГ, не-ЛПВЩ і ApoB, що забезпечує більш повний контроль атерогенної дисліпідемії порівняно з іншими фібратами (Aggarwal, 2026). Фенофібрат, окрім цього, має виразний вплив на найбільш атерогенні дрібні щільні частинки ЛПНЩ, зменшуючи їх рівень удвічі (на 51%).
Важливе значення мають також фармакокінетичні особливості окремих форм фенофібрату. Зокрема, фенофібрат у формі наночастинок (як у препараті Трайкор® 145 мг) характеризується поліпшеною біодоступністю та повною абсорбцією, що не залежить від приймання їжі. Це дозволяє застосовувати його один раз на добу без необхідності підбору дози, що підвищує зручність і потенційно покращує прихильність пацієнтів до лікування (Jens-Uwe et al., 2008).
Переконливі дані щодо ефективності комбінованої терапії статином і фенофібратом було отримано у дослідженні ACCORD-Lipid за участю пацієнтів з атерогенною дисліпідемією і ЦД 2-го типу. У підгрупі хворих із підвищеним рівнем ТГ (>2,3 ммоль/л) та низьким рівнем ХС ЛПВЩ (<0,9 ммоль/л) додавання фенофібрату до статину супроводжувалося зниженням частоти СС-подій на 31%. Це підтверджує доцільність комбінованого підходу до лікування атерогенної дисліпідемії (The ACCORD Study Group, 2010; Tenenbaum et al., 2012).
Можливі комбінації ліпідознижувальних препаратів, що застосовуються в лікуванні дисліпідемії, представлені на рисунку 1 (Banach et al., 2021).
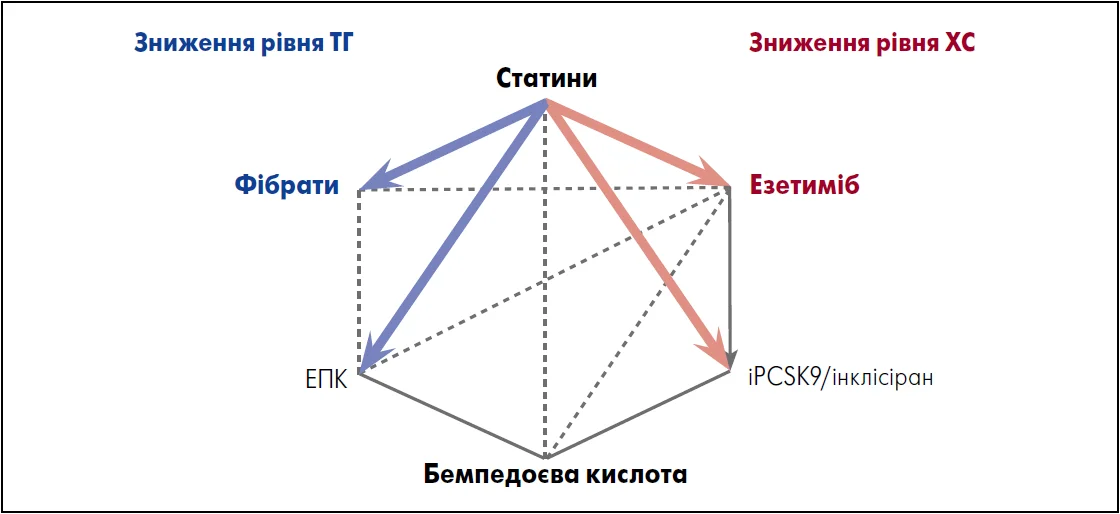 Рис. 1. Можливі комбінації препаратів, що застосовуються в лікуванні дисліпідемії
Рис. 1. Можливі комбінації препаратів, що застосовуються в лікуванні дисліпідемії
Примітки: ЕПК – ейкозапентаєнова кислота, іPCSK9 – інгібітори пропротеїнової конвертази субтилізин-кексинового типу 9.
Адаптовано за М. Banach et al. (2021)
Професор Мітченко зазначила, що у сучасних клінічних рекомендаціях запропоновано поетапний алгоритм корекції ГТГ (рис. 2). На першому етапі проводиться модифікація способу життя, а якщо цього недостатньо – призначають статини для досягнення цільових рівнів ХС ЛПНЩ. У разі збереження підвищених рівнів ТГ до терапії можуть додаватися препарати, спрямовані на їх зниження, зокрема фенофібрат (Трайкор® 145 мг) (Newman et al., 2020).
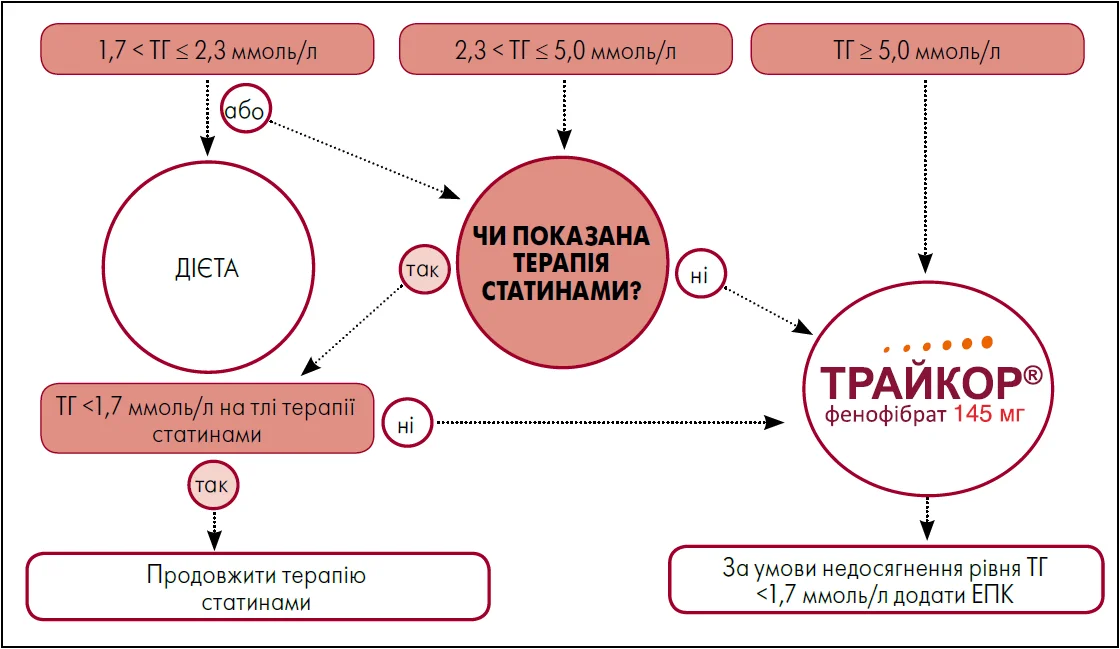 Рис. 2. Алгоритм корекції гіпертригліцеридемії
Рис. 2. Алгоритм корекції гіпертригліцеридемії
Примітка: ЕПК – ейкозапентаєнова кислота.
Таким чином, сучасне розуміння резидуального СС-ризику виходить за межі традиційного контролю ХС ЛПНЩ. Значну роль у розвитку атеросклерозу відіграють ТГ-збагачені ліпопротеїни та ремнантні частинки. Їх своєчасне виявлення і корекція, зокрема за допомогою фенофібрату (Трайкор® 145 мг), може сприяти ефективнішому зниженню СС-ризику, особливо у пацієнтів із ГТГ, метаболічним синдромом та ЦД. Фенофібрат (Трайкор® 145 мг) у складі комбінованої терапії зі статинами у пацієнтів із підвищеним рівнем ТГ і зниженим ХС ЛПВЩ дозволяє додатково впливати на атерогенний ліпідний профіль, що асоційовано зі зменшенням імовірності СС-подій.
Ліпопротеїни, багаті на тригліцериди: роль у резидуальному серцево-судинному ризику
 Альберто Замбон у своїй доповіді на XXVI Національному конгресі кардіологів України, що відбувся торік у вересні, зазначив, що ССЗ залишаються провідною причиною смерті у світі. Ішемічна хвороба серця є найпоширенішою причиною смерті, на яку припадає близько 7,2 млн випадків щорічно, що становить понад 12% усіх летальних випадків на глобальному рівні. Очікується, що загальний тягар цієї патології надалі зростатиме, а це зумовлює необхідність удосконалення підходів до профілактики та лікування АССЗ (Vaduganathan et al., 2022).
Альберто Замбон у своїй доповіді на XXVI Національному конгресі кардіологів України, що відбувся торік у вересні, зазначив, що ССЗ залишаються провідною причиною смерті у світі. Ішемічна хвороба серця є найпоширенішою причиною смерті, на яку припадає близько 7,2 млн випадків щорічно, що становить понад 12% усіх летальних випадків на глобальному рівні. Очікується, що загальний тягар цієї патології надалі зростатиме, а це зумовлює необхідність удосконалення підходів до профілактики та лікування АССЗ (Vaduganathan et al., 2022).
Упродовж тривалого часу основною мішенню ЛЗТ залишався ХС ЛПНЩ, і саме його зниження вважається першочерговою ціллю лікування відповідно до рекомендацій ESC/EAS (2019). Водночас навіть у пацієнтів, які досягають оптимальних рівнів ХС ЛПНЩ, зберігається значна ймовірність розвитку СС-ускладнень – явище, відоме як резидуальний СС-ризик.
Нині резидуальний СС-ризик розглядається як багатофакторна клінічна проблема, що формується під впливом як традиційних чинників, так і додаткових метаболічних механізмів. Він може бути пов’язаний із підвищеним рівнем ТГ, Lp(a), хронічним запаленням, протромботичними змінами та метаболічними порушеннями, зокрема на тлі ЦД (Austin et al., 1990). При цьому рівень ТГ ≥1,7 ммоль/л розглядається як важливий маркер залишкового ризику навіть у пацієнтів із досягнутими цільовими показниками ХС ЛПНЩ.
Приблизно в 1 із 4 осіб з АССЗ у загальній популяції можуть спостерігатися ГТГ та контрольований рівень ХС ЛПНЩ. У цих пацієнтів з ішемічною хворобою серця, які отримували належне лікування ЛПНЩ, поступове підвищення рівня ТГ асоціювалося із більшою ймовірністю рецидивів і нових коронарних подій, попри задовільний контроль ЛПНЩ. Отже, ТГ-збагачені ліпопротеїни мають клінічну значущість (Lawler et al., 2019).
За словами професора, останніми роками ТГ-збагаченим ліпопротеїнам, зокрема хіломікронам і ЛПДНЩ, приділяють особливу увагу. У процесі їх метаболізму утворюються ремнантні частинки – залишкові ліпопротеїни із виразними атерогенними властивостями. Надмірне їх утворення та порушений кліренс, що особливо характерно для пацієнтів із ЦД 2-го типу, призводять до накопичення ремнантів, які здатні проникати у судинну стінку та сприяти розвитку атеросклерозу.
Важливо підкреслити, що одна частинка ліпопротеїну, збагаченого ТГ, має атерогенний потенціал, зіставний із частинкою ЛПНЩ. Вони індукують ендотеліальну дисфункцію, стимулюють запалення, сприяють накопиченню макрофагів і формуванню пінистих клітин – ключових етапів розвитку атеросклеротичної бляшки (Tokgozoglu et al., 2022). Порушення метаболізму ТГ також асоційоване зі збільшенням кількості дрібних щільних частинок ЛПНЩ – характерною ознакою атерогенної дисліпідемії, особливо при інсулінорезистентності, вісцеральному ожирінні та ЦД 2-го типу (Austin et al., 1990).
У сучасних рекомендаціях дедалі більшого значення набуває показник ХС не-ЛПВЩ, який розраховується як різниця між загальним ХС і ХС ЛПВЩ та включає всі атерогенні ApoB-вмісні ліпопротеїни. Його перевагами є простота визначення, можливість використання незалежно від приймання їжі та вища прогностична цінність щодо СС-ризику порівняно з ХС ЛПНЩ (Mach et al., 2019; Tokgozoglu et al., 2022).
Для оцінки індивідуального ризику СС-ускладнень застосовується система SCORE2, яка дозволяє прогнозувати 10-річний ризик СС-подій. Для пацієнтів із ЦД 2-го типу розроблено модифіковану модель SCORE2-Diabetes, яка дає змогу точніше оцінювати ризик у цієї категорії хворих, узгоджуючи прогноз для осіб із/без ЦД та враховуючи додаткові чинники, пов’язані з його перебігом. Вона також дозволяє диференціювати внесок традиційних і специфічних для ЦД факторів ризику, а також окремо оцінювати ризик у чоловіків і жінок (ESC, 2021, 2023).
З огляду на роль ТГ-збагачених ліпопротеїнів у формуванні резидуального ризику, сучасні підходи до лікування дисліпідемії передбачають не лише досягнення цільових рівнів ХС ЛПНЩ, але й корекцію ГТГ. Основою терапії залишаються статини, які є препаратами першої лінії у пацієнтів із високим ризиком ССЗ. Якщо на тлі їх застосування досягнуто цільового рівня ХС ЛПНЩ, але зберігається підвищений рівень ТГ (>2,3 ммоль/л), рекомендації передбачають можливість призначення додаткової терапії – фенофібрату або ейкозапентаєнової кислоти (ЕПК) (ESC, 2021).
Відповідно до настанови Європейського товариства атеросклерозу (EAS, 2021), рівень ТГ у діапазоні від >2,3 до <5,6 ммоль/л потребує додаткового оцінювання та корекції навіть у пацієнтів, які досягли цільових значень ХС ЛПНЩ. Алгоритм ведення таких хворих передбачає модифікацію способу життя, застосування максимально переносимих доз статинів і повторний аналіз ліпідного профілю. У разі збереження ГТГ розглядаються додаткові фармакологічні стратегії. Вибір терапії залежить від клінічного контексту. В пацієнтів із ЦД 2-го типу та вже наявними ССЗ доцільно розглядати додавання високих доз ЕПК до терапії статинами, тоді як хворим із ЦД 2-го типу без встановленого АССЗ, але із підвищеним рівнем ТГ може бути рекомендований фенофібрат. Така тактика спрямована на корекцію атерогенних ліпопротеїнів, збагачених ТГ, і зниження залишкового атерогенного ризику (рис. 3) (Chait et al., 2024).
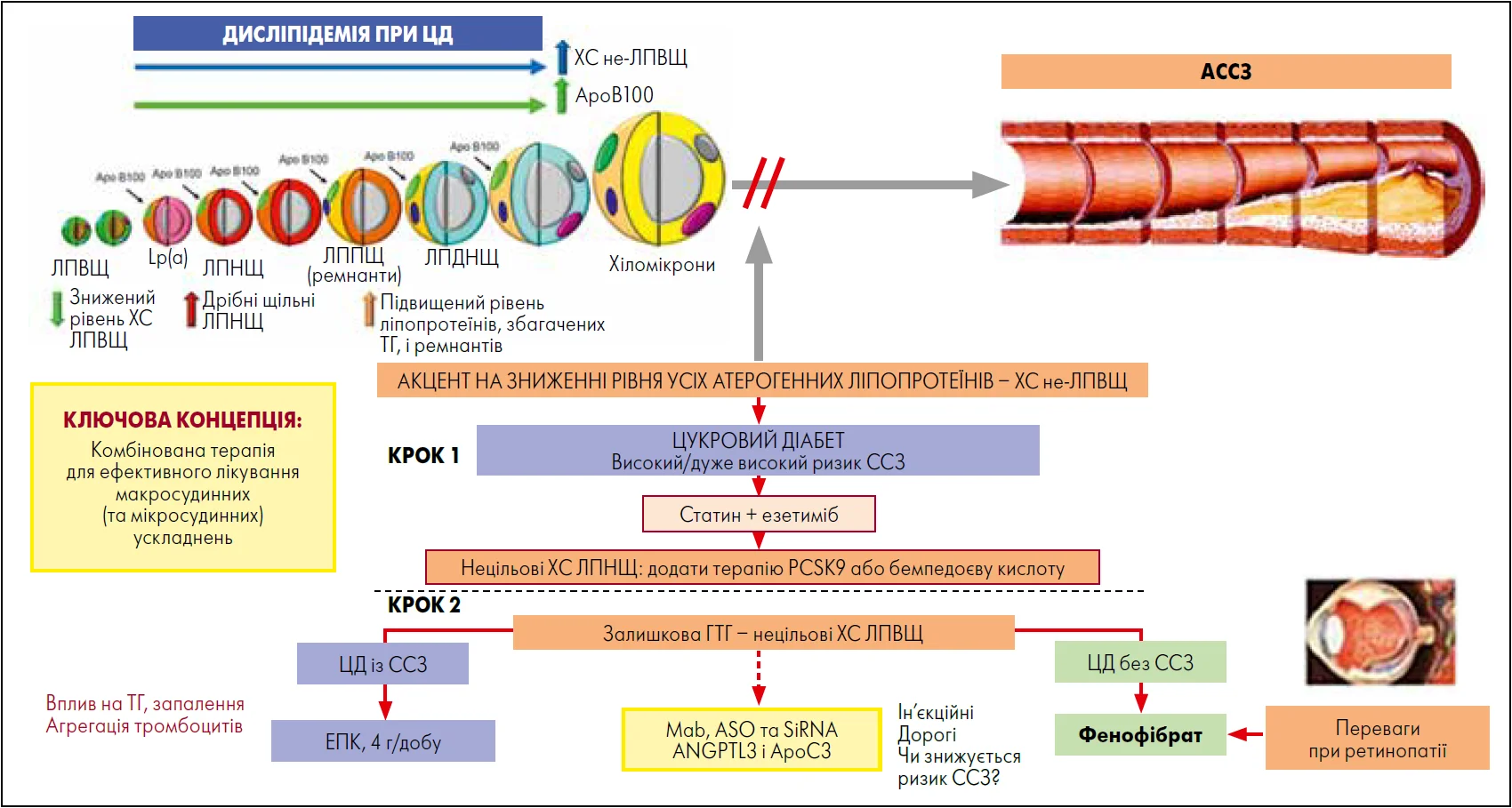 Рис. 3. За межами ХС ЛПНЩ: усунення макро- та мікросудинного ризику в пацієнтів із ЦД
Рис. 3. За межами ХС ЛПНЩ: усунення макро- та мікросудинного ризику в пацієнтів із ЦД
Примітки: mAb – моноклональні антитіла, ASO – антисмислові олігонуклеотиди, siRNA – малі інтерферуючі РНК, ANGPTL3 – ангіопоетиноподібний білок 3, ApoC3 – аполіпопротеїн C‑III.
Адаптовано за А. Chait et al. (2024)
Водночас слід враховувати, що рекомендації стосуються застосування саме чистої ЕПК, тоді як в Україні препарати з чистою ЕПК наразі не зареєстровані. Це обмежує можливості її використання в клінічній практиці, що підвищує значущість доступних альтернатив, зокрема фенофібрату у складі комбінованої ЛЗТ.
Що стосується доказової бази, фенофібрат залишається одним із найбільш досліджених препаратів для корекції ГТГ. Професор Замбон навів дані клінічних досліджень, відповідно до яких фібрати здатні знижувати ризик СС-подій у пацієнтів з атерогенною дисліпідемією (Bruckert et al., 2011; Lee et al., 2011). Поєднання фенофібрату зі статинами забезпечує виразніше зниження рівнів ХС не-ЛПВЩ та ApoB порівняно з монотерапією статинами (Kim et al., 2024). Дані великого когортного дослідження (n=29 771) також свідчать про додаткове зниження ризику серйозних СС-ускладнень при застосуванні такої комбінації в осіб із метаболічним синдромом та атерогенною дисліпідемією. особливо у хворих із високим рівнем ТГ і низьким умістом ХС ЛПВЩ (Kim et al., 2019).
Окрім впливу на ліпідний профіль, фенофібрат має значення для профілактики мікросудинних ускладнень ЦД, зокрема діабетичної ретинопатії. У дослідженні FIELD було показано, що застосування фенофібрату зменшує потребу в проведенні лазерної терапії ретинопатії на 31% при ЦД 2-го типу (Keech et al., 2007). Результати випробування ACCORD-Eye підтвердили ці дані: додавання фенофібрату до стандартного лікування асоціювалося зі зниженням швидкості прогресування ретинопатії приблизно на 36% у пацієнтів із ЦД 2-го типу. Важливо, що позитивний вплив фенофібрату на перебіг діабетичної ретинопатії спостерігався незалежно від змін показників ліпідного профілю, що свідчить про додаткові механізми його судинозахисної дії (Buse et al., 2007; Chew et al., 2010). Останні дані підтверджують, що фенофібрат може зменшувати ймовірність прогресування діабетичної ретинопатії порівняно із плацебо в осіб із ранніми змінами сітківки (Preiss et al., 2024).
Крім того, у дослідженні FIELD було показано позитивний вплив фенофібрату на функцію нирок у пацієнтів із ЦД 2-го типу, зокрема уповільнення зниження швидкості клубочкової фільтрації та прогресування альбумінурії (Davis et al., 2011).
Отже, фенофібрат (Трайкор® 145 мг) залишається одним із доступних і добре досліджених препаратів для корекції ГТГ у пацієнтів із високим або дуже високим СС-ризиком, особливо у випадках, коли попри терапію статинами зберігається підвищений рівень ТГ. Такий підхід відповідає сучасній концепції комбінованої ЛЗТ, спрямованої не лише на досягнення цільових рівнів ХС ЛПНЩ, а й на зниження резидуального ризику, пов’язаного із ТГ-збагаченими ліпопротеїнами.
Підготувала Олена Коробка
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 1 (104) 2026 р.



