8 квітня, 2026
Європейська настанова щодо ведення жінок із серцево-судинними захворюваннями під час вагітності
Серцево-судинні захворювання (ССЗ) є основною причиною материнської захворюваності та смертності, зменшення яких є одним із ключових пріоритетів систем охорони здоров’я у світі. У 2025 р. робоча група з лікування ССЗ у вагітних Європейського товариства кардіологів (ESC) представила оновлену настанову щодо менеджменту вагітних жінок із ССЗ, яку було схвалено Європейським товариством гінекологів (ESG). З моменту публікації попередньої версії рекомендацій у 2018 р. з’явилися нові дані, а також змінився клінічний фокус у різних аспектах ведення, наприклад, щодо важливості мультидисциплінарного підходу, методів консультування до вагітності та стратифікації ризику, фармакотерапії під час вагітності, лактації та/або грудного вигодовування й післяпологового періоду. Розглянемо ключові положення цієї настанови.
На сьогодні у країнах із високим рівнем доходів кількість вагітностей та пологів у жінок із вродженими, спадковими або набутими ССЗ значно зросла. Ця тенденція зумовлена низкою факторів: старшим віком матері за першої вагітності, збільшенням частки жінок із вродженими вадами серця, які досягають дітородного віку, та зростанням поширеності супутніх ССЗ. У світі 10% вагітностей супроводжуються серцево-судинними (СС) ускладненнями з урахуванням артеріальної гіпертензії (АГ) (Baumgartner et al., 2021; Kotit et al., 2021).
Нині ССЗ є основною причиною неакушерської смерті серед вагітних. Примітно, що 68% летальних випадків під час вагітності, спричинених ССЗ, можна запобігти (Majmundar et al., 2023). Частота акушерських ускладнень у жінок із ССЗ становить 17%, а несприятливі неонатальні наслідки спостерігаються приблизно у 25%. Жінки із ССЗ під час вагітності мають вищий ризик СС-подій у подальшому житті, що робить вторинну профілактику надзвичайно важливою (Drenthen et al., 2010).
Робоча група ESC сформулювала діагностичні й терапевтичні підходи, зокрема на основі оцінки співвідношення користі й ризику, що ґрунтуються на відповідних рекомендаціях і доказах. Сила рекомендацій та рівень доказовості наведені в таблицях 1 і 2.
|
Таблиця 1. Класи рекомендацій |
||
|
Клас |
Визначення |
Роз’яснення |
|
Клас І |
Докази та/або загальна згода стосовно того, що лікування чи процедура мають переваги, є корисними та ефективними |
Рекомендовано або показано |
|
Клас ІІ |
Суперечливі докази та/або розбіжності в думках щодо користі/ефективності лікування чи процедури |
Слід (ІІа) або можна (ІІb) розглянути |
|
Клас ІІІ |
Докази або загальна згода, що лікування чи процедура не є корисними/ефективними, а в деяких випадках можуть бути шкідливими |
Не рекомендовано |
|
Таблиця 2. Рівні доказовості |
|
|
Рівень |
Визначення |
|
Рівень А |
Дані, отримані з багатьох рандомізованих клінічних досліджень або метааналізів |
|
Рівень В |
Дані, отримані з одного рандомізованого або великих нерандомізованих клінічних досліджень |
|
Рівень С |
Консенсус думок експертів та/або дані, отримані з невеликих, ретроспективних досліджень, реєстрів |
Аспекти діагностики
Роль мультидисциплінарної команди. В оновленій настанові ESC (2025) підкреслено центральну роль мультидисциплінарної команди (Pregnancy Heart Team) із залученням кардіолога, акушера-гінеколога, анестезіолога, генетика, неонатолога, яка супроводжує жінку на всіх етапах: консультування до та впродовж вагітності, під час пологів та у післяпологовому періоді. Такий підхід до ведення пацієнтки пов’язаний зі сприятливими результатами для матері та плода, включно зі зниженням материнської смертності й частоти повторних госпіталізацій. До основних обов’язків мультидисциплінарної команди належать оцінка ризиків, розробка плану догляду, регулярний моніторинг прогресу, координація процесу, підвищення обізнаності пацієнток і психологічне консультування. Сприяння спільному прийняттю рішень є важливим на всіх етапах (Stephens et al., 2023; Lucа et al., 2023).
Оцінку ризику в усіх жінок із ССЗ дітородного віку рекомендовано проводити з використанням модифікованої класифікації Всесвітньої організації охорони здоров’я (mWHO 2.0) (І, С). Жінки із ССЗ ≥II‑III класу за mWHO 2.0 мають проходити обстеження та перебувати під наглядом мультидисциплінарної команди до, під час вагітності та після пологів (І, С) (Miller et al., 2022). Жінкам із ССЗ ≥II класу або тим, хто має СС-ризик, рекомендовано отримувати індивідуальні консультації для визначення оптимального методу контрацепції, включно з екстреною (І, С). За наявності ризику тромбоемболічних ускладнень слід розглянути призначення монотерапії прогестинами, контрацептивних імплантатів та/або внутрішньоматкової спіралі з левоноргестрелом (ІІа, В) (Dragoman et al., 2018; Palacios et al., 2020).
Для жінок із ССЗ IV класу за mWHO 2.0 важливим є обговорення з мультидисциплінарною командою високої ймовірності материнської захворюваності або смертності та великого ризику для плода, включно зі спільним прийняттям рішень щодо переривання вагітності та психологічною підтримкою (І, С). Жінкам із ССЗ необхідно забезпечити можливість переривання вагітності, адаптованого до їхнього клінічного стану, щоб мінімізувати ризики процедури (І, С) (Lindley et al., 2021).
Жінкам, які відповідають діагностичним критеріям спадкових ССЗ, необхідно пройти обстеження клінічним генетиком до вагітності, щоб визначити ступінь ризику та провести пренатальне генетичне тестування (І, С). Парам зі спадковими ССЗ рекомендоване генетичне консультування до зачаття, незалежно від того, розглядається чи ні генетичне тестування (І, С) (Morales et al., 2017).
Лікування безпліддя та застосування репродуктивних технологій у жінок із ССЗ є складним завданням. Відповідно до рекомендацій, пацієнткам із ССЗ доцільно радити розглянути трансплантацію ембріона (І, С) (Ombelet et аl., 2006; Dhalwani et al., 2013).
Дослідження. Трансторакальна ехокардіографія (ЕхоКГ) рекомендована як метод візуалізації першої лінії для вагітних із незрозумілими або новими ознаками чи симптомами ССЗ (І, С). Трансезофагеальна ЕхоКГ є вельми безпечною, але потенційні ризики та переваги мають бути зважені індивідуально. Спекл-трекінгова ЕхоКГ корисна для виявлення субклінічних аномалій міокарда під час вагітності (Popescu et al., 2022).
Застосування комп’ютерної томографії (КТ) є ймовірно доцільним при тромбоемболії легеневої артерії (ТЕЛА), коли клінічні переваги переважають ризики для матері та плода (ІІа, С). Рентгенографію грудної клітки можна розглядати як візуалізацію першої лінії, якщо інші методи не є успішними для встановлення причини задишки (ІІb, С). Коронарографію з мінімальним опроміненням можна розглядати під час вагітності, якщо потенційна користь переважає ризики (ІІb, С). Ймовірність проведення МРТ серця без контрастування гадолінієм має розглядатися для отримання остаточних, клінічно значущих результатів діагностики під час вагітності, якщо інші неінвазивні методи виявилися недостатньо інформативними (ІІа, С) (Cova et al., 2014; Bird et al., 2019).
Що стосується оцінки біомаркерів, жінкам із серцевою недостатністю (СН) будь-якої етіології, що включає кардіоміопатію (КМП), зокрема перипартальну, вроджені вади серця та легеневу АГ, слід розглянути визначення рівнів натрійуретичного пептиду B-типу і N-кінцевого пропептиду натрійуретичного гормону до настання вагітності та контролювати показники під час неї залежно від основного захворювання й у разі появи нових чи погіршення наявних симптомів (ІІа, В) (Sheikh et al., 2021). Вимірювання D-димеру має значення при діагностиці венозної тромбоемболії (ВТЕ), враховуючи фізіологічне підвищення його рівня під час вагітності, особливо у третьому триместрі. Рутинне вимірювання лише серцевих тропонінів під час вагітності не рекомендоване.
Фармакотерапія під час вагітності й лактації
Лікування та терміни/типи пологів
Вагінальні пологи рекомендовані більшості жінок із ССЗ (І, В). Антибіотикопрофілактика при пологах може розглядатися за наявності високого ризику: у жінок із протезом клапана серця чи інфекційним ендокардитом в анамнезі, а також пацієнток із залишковим дефектом клапана або після трансплантації серця (ІІb, С) (Delgado et al., 2023). Індукція пологів до 39-го тижня у жінок зі стабільним ССЗ не рекомендована (ІІІ, С) (Mok et al., 2022).
Ведення жінок, які отримують антикоагулянти під час пологів, є складним і потребує індивідуального підходу. Щоб антикоагулянтна терапія під час пологів була ефективною та безпечною, рекомендовано планувати їх дату (І, С).
Якщо пологи починаються тоді, коли мати приймає антагоністи вітаміну К (АВК) або менш ніж через два тижні після їх відміни, рекомендовано виконати кесарів розтин для захисту плода (І, С). Необхідно відмінити АВК та розпочати приймання низькомолекулярного гепарину (НМГ) у терапевтичній дозі або нефракціонованого гепарину (НФГ) в/в у скоригованій дозі на 36-му тижні вагітності або за два тижні до запланованих пологів (І, С) (Jackson et al., 2024). У жінок із низьким ризиком, які приймають НМГ у терапевтичній дозі, доцільними є вагінальні пологи (або кесарів розтин за акушерськими показаннями) із використанням нейроаксіальної анестезії через 24 год після останньої дози НМГ (І, С). Жінкам із високим ризиком слід перейти із НМГ на НФГ в/в щонайменше за 36 год до пологів та припинити інфузію НФГ за 4‑6 год до очікуваних пологів (Leffert et al., 2018).
У жінок, які отримують НМГ у терапевтичній дозі, планові пологи слід розглядати приблизно на 39-му тижні, щоб уникнути ризику спонтанних пологів на тлі антикоагулянтної терапії (ІІа, С). У жінок, які перебували на антикоагулянтній терапії до пологів, слід розглянути можливість введення окситоцину в третьому періоді пологів (ІІа, С) (Cauldwell et al., 2017).
Після пологів рішення щодо поновлення застосування НМГ або НФГ слід ухвалювати на основі обговорення з мультидисциплінарною командою та пацієнткою (І, С). Повернення до пероральних антикоагулянтів після гепарину доцільно відкласти на період до 7‑14 днів після пологів (коли рани загояться), попередньо проконсультувавшись із мультидисциплінарною командою (І, С) (Lester et al., 2023; van der Zande et al., 2025).
Антикоагулянти
Застосування антикоагулянтів під час вагітності являє собою складний баланс ризиків і користі, що залежить від конкретних показань та ускладнений низькою якістю доказів.
Антагоністи вітаміну К. Ці препарати проникають через плаценту й пов’язані з ризиком ембріопатії та фетопатії, навіть у низьких дозах. Тому більшість вагітних переводять на НМГ, за винятком жінок із фібриляцією передсердь (ФП) у поєднанні з помірним чи тяжким стенозом мітрального клапана або механічним клапаном серця (МКС), враховуючи нижчий ризик тромбозу при застосуванні АВК порівняно з НМГ у цієї категорії хворих. Жінки, які отримують АВК на постійній основі та планують вагітність, потребують консультування фахівця для уникнення потенційних тератогенних ефектів. Якщо пацієнтка бажає перейти на інше лікування (зазвичай на НМГ), це слід зробити якомога швидше після зачаття. Використання АВК є безпечним під час лактації та рекомендоване всім жінкам із МКС з огляду на їх антикоагулянтні властивості щодо запобігання тромбозу клапана (D’Souza et al., 2017).
Низькомолекулярний гепарин. Ембріопатія або фетопатія не спостерігалися при застосуванні НМГ навіть у терапевтичних дозах, але тромбоемболічні ускладнення у жінок із МКС є дещо частішими, ніж на тлі АВК. НМГ, імовірно, рідше викликає гепарин-індуковану тромбоцитопенію порівняно із НФГ, хоча під час вагітності цей ефект не вивчався (Steinberg et al., 2017).
Нефракціонований гепарин. НФГ при введенні в/в, хоча й не проникає через плаценту, пов’язаний із вищим ризиком тромбоцитопенії та остеопорозу порівняно із НМГ. При підшкірному введенні НФГ під час вагітності ймовірність тромбозу клапанів є неприйнятно високою, тож воно не рекомендоване (Chan et al., 2000). Жінкам із МКС, яким не можна продовжувати приймання АВК, введення НФГ в/в показане лише тоді, коли моніторинг фактора анти-Ха неможливий у першому триместрі та під час пологів.
Фондапаринукс. У жінок, які потребують профілактики ВТЕ, були зареєстровані сприятливі результати підшкірного введення фондапаринуксу в обсерваційному дослідженні (65 вагітних) та ретроспективному аналізі (84 жінок з однією або кількома попередніми вагітностями). Його застосування можна розглядати за наявності алергії або побічної реакції на НМГ (Dempfle et al., 2021).
Прямі оральні антикоагулянти (ПОАК). Попри перспективні дані досліджень, клінічні докази щодо користі й ризику ПОАК для матері та плода є недостатніми, а їх безпеку для плода порівняно з АВК протягом другого та третього триместрів не встановлено. Консультування жінок, які планують вагітність та приймають ПОАК, є необхідним, враховуючи складність переходу на альтернативні схеми лікування (НМГ, АВК) до й після зачаття та ймовірність рецидиву ВТЕ (Beyer-Westendorf, Marten, 2021; Sessa et al., 2019). Тож застосування ПОАК під час вагітності не рекомендоване, та їх слід призначати лише за відсутності будь-якого іншого варіанта після ретельного обговорення з мультидисциплінарною командою (ІІІ, С). Проте ПОАК можуть мати переваги над АВК завдяки швидкому припиненню дії у разі передчасних пологів та короткому періоду переривання лікування до пологів. Під час лактації слід надавати перевагу альтернативним препаратам через брак даних.
Антитромбоцитарна терапія
Дані щодо тератогенного ефекту ацетилсаліцилової кислоти (АСК) у дозах до 300 мг/добу відсутні. Клопідогрель вважається безпечним, якщо є потреба в подвійній антитромбоцитарній терапії протягом найкоротшого можливого періоду (Elkayam et al., 2014). Тикагрелор протипоказаний через ембріотоксичність. Призначення прасугрелю можна розглянути під час вагітності в особливих групах пацієнток, зокрема жінок із повільним метаболізмом, в яких клопідогрель чинить обмежений ефект (Serna Candel et al., 2019). Інгібітори глікопротеїну IIb/IIIa (ептифібатид і тирофібан) можна застосовувати під час вагітності лише за крайньої необхідності (Argentiero et al., 2020).
Діуретики та інгібітори натрійзалежного котранспортера глюкози 2-го типу
Діуретики можна використовувати під час вагітності для лікування системної АГ, особливо в екстрених випадках або при перевантаженні об’ємом на тлі СН. Необхідно ретельно контролювати зменшення об’єму плазми або CO та плацентарної перфузії. Доклінічні дані показали, що інгібітори натрійзалежного котранспортера глюкози 2-го типу іНЗКТГ‑2 проникають через плаценту і можуть спричинити пошкодження плода у гризунів. Тож їх приймання слід припинити до настання вагітності та під час лактації (Kuoni et al., 2024; Muller et al., 2023).
Препарати при легеневій АГ
Парентеральні аналоги простагландинів (в/в епопростенол, трепростиніл) дозволено використовувати вагітним із виразною дисфункцією правого шлуночка (ПШ), враховуючи те, що вони здатні спричиняти кровотечі (Hemnes et al., 2015). Також можна призначати пероральні інгібітори фосфодіестерази 5 (силденафіл, тадалафіл), але слід контролювати потенційні побічні ефекти, пов’язані з передчасними пологами та народженням дітей із малою масою тіла для гестаційного віку (Cesta et al., 2021). Крім того, відомо про переваги комбінованої терапії силденафілом та інгаляційним ілопростом (Horng et al., 2016). Лікування блокаторами кальцієвих каналів (БКК) слід продовжувати вагітним із нормальною функцією ПШ і легеневою АГ, що відповідають на вазодилататори. Антагоністи рецепторів ендотеліну (бозентан, амбризентан, мацитентан) не варто приймати під час вагітності через їх тератогенний потенціал. Існує мало даних щодо безпеки бозентану та силденафілу в матерів, що годують грудьми; але описано випадки успішного застосування (Nauwelaerts et al., 2022).
Антиаритміки
У жінок без структурних захворювань серця антиаритмічні препарати (флекаїнід, соталол, ібутилід) можна використовувати в межах профілактики або для лікування ФП та тріпотіння передсердь (ТП) (van der Zande et al., 2023). Бета-блокатори вважаються безпечними, особливо ліпофільні сполуки (лабеталол, метопролол, пропранолол). У вагітних із ФП та супутньою застійною СН дигоксин може бути альтернативним варіантом для контролю частоти серцевих скорочень (ЧСС). Аміодарон здатний спричиняти аномалії плода, брадикардію та дисфункцію щитовидної залози, тож його рутинне застосування під час вагітності протипоказане. Однак його можна використовувати одноразово в екстрених випадках, як-то шлуночкова тахікардія (ШТ). Обмежень щодо застосування аміодарону при зупинці серця немає (Zeppenfeld et al., 2022).
Блокатори кальцієвих каналів
Безпеку та ефективність дигідропіридинового БКК ніфедипіну у вагітних з АГ значною мірою доведено порівняно з іншими антигіпертензивними засобами (як-то лабеталол, гідралазин, метилдопа). Результати щодо безпеки для плода, новонародженої дитини та матері статистично не відрізняються між ніфедипіном та препаратами порівняння (George et al., 2022). Амлодипін демонструє подібні безпеку й ефективність до ніфедипіну (Yin et al., 2022). Докази щодо недигідропіридинового БКК дилтіазему є недостатніми, при цьому в гризунів та кроликів було виявлено суттєвий тератогенний ефект. Отже, препарат не рекомендовано застосовувати під час вагітності та лактації (проникає у грудне молоко). Пероральний верапаміл вважається безпечним, тератогенності не спостерігалося; він виділяється із молоком у низьких концентраціях.
Інгібітори ренін-ангіотензин-альдостеронової системи. Інгібітори ангіотензинперетворювального ферменту (іАПФ), блокатори рецепторів ангіотензину ІІ (БРА), інгібітори рецепторів ангіотензину/неприлізину (ARNI) й інгібітори реніну можуть спричинити вади розвитку, затримку внутрішньоутробного розвитку та смерть плода, тож протипоказані під час вагітності. Каптоприл, еналаприл та беназеприл безпечні під час лактації, тоді як БРА не рекомендовані (кандесартан може бути винятком) (Halpern et al., 2019). Антагоністи альдостерону (канренон, спіронолактон) здатні чинити антиандрогенетичний ефект та протипоказані під час вагітності. Спіронолактон вважається безпечним під час лактації. У повідомленнях про випадки застосування еплеренону вагітними із резистентною АГ побічні явища не зареєстровано (Saito et al., 2021).
Ліпідознижувальні засоби
Під час вагітності рівень холестерину ліпопротеїнів низької щільності підвищується приблизно на 30‑50%, холестерину ліпопротеїнів високої щільності – на 20‑40%, а тригліцеридів – на 50‑100% (Mulder et al., 2024). Раніше ліпідознижувальну терапію зазвичай припиняли у період вагітності через обмежені дані щодо безпеки (Regitz-Zagrosek et al., 2018). Однак у 2021 р. Управління із контролю за якістю харчових продуктів та медикаментів США (FDA) заявило, що доказів для надання висновку про підвищення ризику викидня при застосуванні статинів недостатньо, тож це протипоказання було вилучене (Mauricio, Khera, 2022). Наразі застосування статинів протипоказане лише під час лактації. Продовження приймання статинів можна розглядати у вагітних із сімейною гіперхолестеринемією або встановленим атеросклеротичним АССЗ (Schwartz et al., 2016). Крім того, випадкове зачаття під час статинотерапії не потребує переривання вагітності, але має спонукати до ретельного спостереження.
Інгібітори пропротеінової конвертази субтилізин-кексинового типу 9 (іPCSK9) та езетиміб не рекомендовані під час вагітності через відсутність клінічних даних (Ardissino et al., 2024). Бемпедоєва кислота має суворе протипоказання щодо застосування, тому жінкам при лікуванні цим препаратом необхідно приймати контрацептиви.
Бета-блокатори
Застосування β-блокаторів на ранніх термінах вагітності не пов’язане з підвищеним ризиком вроджених вад розвитку плода (Wu et al., 2021). Проте останні дані вказують на вищу частоту народження дітей із малою масою тіла для гестаційного віку в жінок, які приймали β-блокатори (лабеталол – найменшою мірою, а атенолол – найбільшою) (Ramlakhan et al., 2024). Лабеталол і ліпофільні β-блокатори (метопролол, пропранолол, карведилол) мають переваги завдяки високому метаболізму першого проходження, як селективні блокатори β1-адренорецепторів (бісопролол, метопролол), що знижують ризик гіпоглікемії та частоту затримки внутрішньоутробного розвитку.
Надолол та піндолол також безпечні у разі аритмічних подій при КМП та каналопатіях (Tamirisa et al., 2022). Атенолол викликає виразну затримку росту плода, брадикардію та гіпоглікемію і не рекомендований до застосування (Bateman et aal., 2018). У разі приймання під час лактації пропранолол, метопролол (у поєднанні з гідралазином) та лабеталол асоційовані з найнижчим, а соталол – із найвищим ризиком брадикардії у новонароджених. При використанні ліпофільних β-блокаторів під час лактації ризики, пов’язані з впливом на новонароджених, є низькими (Ryu et al., 2016).
Імуносупресанти
Питання безпеки для матері та плода на тлі імуносупресивної терапії потребує значної уваги, особливо для жінок із трансплантацією серця. Ліки можуть потрапляти у грудне молоко та спричиняти побічні ефекти в новонароджених. Інгібітори кальциневрину (циклоспорин, такролімус), інгібітори мішені рапаміцину в ссавців (еверолімус, сиролімус) та азатіоприн є препаратами вибору під час вагітності й лактації, які не слід відміняти. Похідні мікофенолату збільшують ймовірність викидня та вад розвитку плода, особливо в першому триместрі, тож їх приймання слід припинити щонайменше за шість тижнів до зачаття (Le et al., 2020; Coscia et al., 2015).
Препарати, що рекомендовані та не рекомендовані для застосування під час вагітності та лактації / грудного вигодовування, представлені на рисунку.
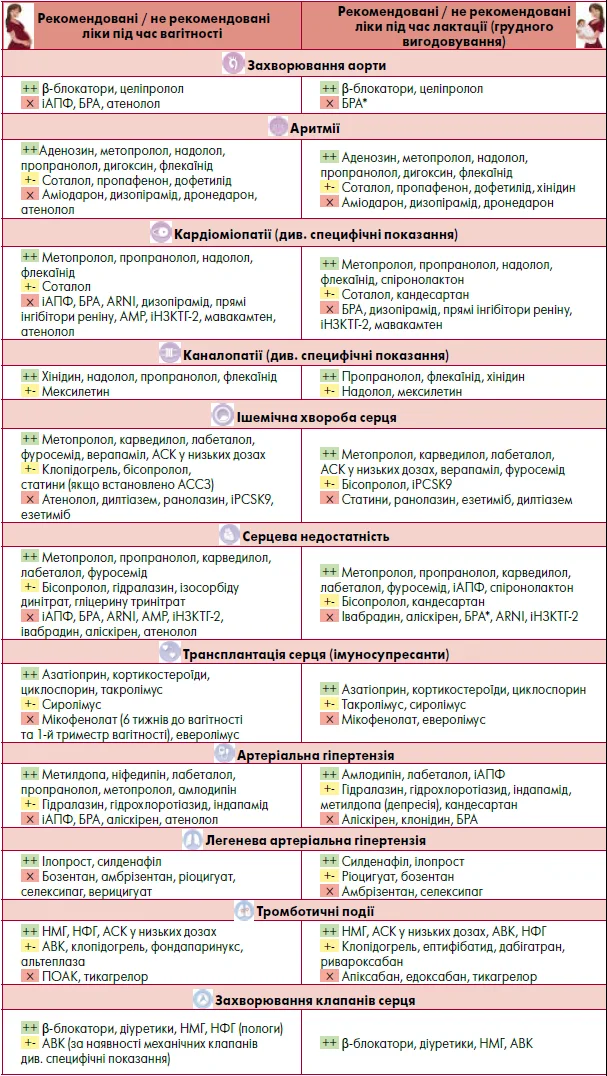 Рисунок. Вибір препаратів під час вагітності та лактації / грудного вигодовування
Рисунок. Вибір препаратів під час вагітності та лактації / грудного вигодовування
Примітки: АМР – антагоністи мінералокортикоїдних рецепторів. * За винятком кандесартану.
++ Препарат першої лінії / найбезпечніший під час вагітності, лактації та годування грудьми; +- препарат другої лінії під час вагітності, лактації та годування грудьми; Ч є докази токсичності для плода чи немовляти або дані щодо безпеки відсутні.
Ведення вагітних із різними клінічними станами
КМП та первинні аритмії
Клінічні дослідження, як-то електрокардіографія, зокрема холтерівський моніторинг, та ЕхоКГ рекомендовано проводити у вагітних із КМП, залежно від індивідуального ризику (І, С). Вагінальні пологи є доцільними для більшості хворих на КМП, якщо немає акушерських показань до кесаревого розтину, виразної СН, неконтрольованих аритмій чи тяжкої обструкції відтоку при гіпертрофічній КМП або у жінок, які на момент пологів перебувають на лікуванні АВК (І, С). Слід розглянути можливість продовження приймання β-блокаторів (за винятком атенололу) у вагітних із КМП з ретельним спостереженням за розвитком плода (ІІа, С) (Arbelo et al., 2023).
Жінкам із дилатаційною КМП та погіршенням фракції викиду (ФВ) під час вагітності рекомендовано проконсультуватися щодо можливого ризику рецидиву під час наступної вагітності, навіть за умови відновлення функції лівого шлуночка (ЛШ) (І, С) (Regitz-Zagrosek et al., 2018). У вагітних з аритмогенною КМП ПШ слід розглянути застосування флекаїніду як антиаритмічного препарату вибору на додаток до β-блокаторів (ІІа, С) (Joglar et al., 2023). Також у цієї категорії хворих може бути доцільною антиаритмічна терапія соталолом із ретельною оцінкою інтервалу QTc та моніторингом брадикардії плода, його росту та гіпоглікемії у новонароджених (ІІb, С).
Для вагітних із гіпертрофічною КМП рекомендовано використовувати той самий протокол стратифікації ризику шлуночкових аритмій, що й для невагітних хворих (І, С). Лікування β-блокаторами (за винятком атенололу) слід розпочинати у жінок із гіпертрофічною КМП, в яких під час вагітності розвинулися симптоми через обструкцію вихідного тракту або аритмію (І, С). У вагітних із гіпертрофічною КМП та ФП варто розглянути застосування кардіоверсії (ІІа, С) (Maisch, Mahrholdt, 2014). Інгібітори міозину не рекомендовані жінкам під час вагітності через відсутність даних щодо безпеки (ІІІ, С) (EMA, 2025).
Що стосується вагітних із первинними аритміями, рекомендовано провести моніторинг і лікування гіпокаліємії та гіпомагніємії у жінок, які страждають від гіперемезису (І, С). Вагітним із синдромом подовженого інтервалу QT (LQTS) слід приймати β-блокатори (за винятком атенололу) в дозі, застосовуваній до вагітності, при цьому препаратами вибору є надолол та пропранолол (І, В) (Ishibashi et al., 2017). Також цій категорії хворих доцільно продовжувати терапію β-блокаторами під час лактації для зниження ризику аритмії (І, В). Жінкам із LQTS 2-го типу рекомендовано приймати надолол чи пропранолол у дозі, застосовуваній до вагітності; особливо це важливо у післяпологовому періоді, що характеризується високим ризиком розвитку небезпечних для життя аритмій (І, В) (Joglar et al., 2023; Seth et al., 2007).
У жінок із LQTS типу P/LP (патогенним / ймовірно патогенним) та негативним фенотипом слід розглянути можливість застосування β-блокаторів упродовж вагітності, після пологів та під час лактації (ІІа, С). Симпатичну денервацію лівих відділів серця варто розглядати до настання вагітності у жінок групи високого ризику із LQTS, які не отримують належної фармакотерапії, або ж у них відзначаються розряди імплантованого карідовертера-дефібрилятора попри оптимальне медикаментозне лікування (ІІа, С) (Zeppenfeld et al., 2022).
Жінкам із катехоламінергічною поліморфною ШТ під час вагітності та лактації рекомендовано приймати β-блокатори (за винятком атенололу) в дозах, застосовуваних до вагітності, при цьому препаратами вибору є надолол та пропранолол (І, С) (Regitz-Zagrosek et al., 2018). Жінкам із катехоламінергічною поліморфною ШТ, у котрих під час вагітності спостерігалися такі кардіальні події, як непритомність, ШТ або зупинка серця, на додаток до β-блокаторів необхідно призначити флекаїнід (І, С). Жінкам із катехоламінергічною поліморфною ШТ і стабільним станом на тлі використання β-блокаторів (надололу або пропранололу) та флекаїніду до вагітності рекомендовано продовжувати приймати обидва препарати під час вагітності, а також після пологів (І, С).
Для жінок із синдромом короткого інтервалу QT слід розглянути можливість продовження приймання хінідину протягом усієї вагітності та післяпологового періоду (ІІа, С). Також терапія хінідином є ймовірно доцільною у вагітних із синдромом короткого інтервалу QT та аритміями (ІІа, С) (Joglar et al., 2023).
Аортопатії, кардіохірургічні втручання
Жінкам із захворюваннями аорти рекомендовано отримати консультацію із приводу ризику розшарування аорти під час вагітності та у післяпологовому періоді (І, С). Жінкам із розшаруванням аорти або хірургічним втручанням в анамнезі слід пройти консультування до настання вагітності в розширеної мультидисциплінарної команди із залученням фахівців з лікування захворювань аорти (І, С) (Gravholt et al., 2017; Roman et al., 2016).
Жінкам із підтвердженим або підозрюваним захворюванням аорти до настання вагітності необхідно виконати візуалізацію всієї аорти (КТ або МРТ) (І, С). У жінок із дилатацією аорти, пов’язаною з двостулковим аортальним клапаном, до настання вагітності рекомендованою є візуалізація (трансторакальна ЕхоКГ та МРТ/КТ, якщо необхідно) кореня аорти, висхідної та низхідної аорт (для виключення коарктації) (І, С) (Della Corte et al., 2013; Roman et al., 2016). У жінок із низьким ризиком захворювання аорти доцільно провести ЕхоКГ у період між 20-м та 30-м тижнями вагітності та через шість місяців після пологів (І, С). За наявності середнього та високого ризику рекомендовано виконувати повторну ЕхоКГ що 4‑12 тижнів (залежно від діагнозу та ступеня дилатації) під час вагітності та до шести місяців після пологів (І, С) (Donnelly et al., 2012).
При настанні вагітності у жінки із дилатацією аорти – підтвердженою або в анамнезі, необхідний суворий індивідуалізований контроль АТ (І, С). Терапія β-блокаторами протягом усієї вагітності та в післяпологовому періоді рекомендована пацієнткам із синдромом Марфана та іншими спадковими захворюваннями грудної аорти (І, С) (Roberts et al., 2023). Целіпролол слід призначати жінкам із судинним синдромом Елерса – Данлоса під час вагітності та лактації (І, С) (Ong et al., 2010).
Показання щодо проведення операції на корені аорти та/або висхідній аорті до вагітності мають визначатися морфологією аорти, основною патологією, сімейним анамнезом, генетичним варіантом, судинними подіями в минулому та побажаннями пацієнтки (І, С) (Czerny et al., 2024). Хірургічне втручання до настання вагітності рекомендоване жінкам: із синдромом Марфана та діаметром кореня аорти >45 мм; із синдромом Лойса – Дітца з варіантами P/LP у генах TGFBR1, TGFBR2 та діаметром кореня аорти ≥45 мм; без варіанта P/LP із діаметром кореня аорти або висхідної аорти ≥50 мм; за наявності двостулкового аортального клапана та діаметра кореня аорти або висхідної аорти ≥50 мм (І, С) (Gouda et al., 2022; Wojnarski et al., 2015).
Вроджені вади серця
Усі жінки із кровообігом Фонтена, а також пацієнтки з системною дисфункцією ПШ, СН III/IV класу за NYHA або тяжкою трикуспідальною регургітацією, які бажають завагітніти, мають отримали консультацію мультидисциплінарної команди щодо високого ризику побічних ефектів, пов’язаних із вагітністю (І, С) (Harada et al., 2022). Із пацієнтками, які мають значні гемодинамічні порушення, необхідно обговорити рекомендовані втручання до настання вагітності (І, С). Вагінальні пологи є доцільними для більшості жінок із вродженими вадами серця (І, В) (Easter et al., 2020).
Легенева АГ
Жінкам репродуктивного віку з легеневою АГ, які бажають завагітніти, рекомендовано отримати консультацію мультидисциплінарної команди щодо високого ризику можливих побічних ефектів на тлі вагітності. У вагітних слід розглянути катетеризацію правих відділів серця, якщо є діагностична невизначеність або при ухваленні важливих терапевтичних рішень (Humbert et al., 2022).
Застосування антагоністів рецепторів ендотеліну, ріоцигуату та селексипагу під час вагітності не рекомендоване (ІІІ, С) (Amann et al., 2023).
Венозна тромбоемболія
У жінок під час вагітності або після пологів із підозрою на ВТЕ (як-то тромбоз глибоких вен та/або ТЕЛА) слід виконати негайну діагностичну оцінку за допомогою валідованих методів (І, В) (van der Pol et al., 2019). Крім того, у разі значної клінічної підозри на ВТЕ під час вагітності або у післяпологовому періоді варто розглянути можливість використання НМГ у терапевтичній дозі, доки діагноз не буде підтверджено або виключено (ІІа, С). За наявності високого ризику ВТЕ під час вагітності або у післяпологовому періоді рекомендовано призначити НМГ у профілактичній фіксованій дозі, скоригованій за вагою (І, В).
У жінок під час вагітності (на ранніх термінах) або після пологів із діагнозом ВТЕ без гемодинамічної нестабільності доцільною є антикоагулянтна терапія з використанням НМГ у терапевтичній дозі, скоригованій за вагою (І, С) (Gandara et al., 2014; McDonnell et al., 2017). У жінок під час вагітності або після пологів із діагнозом гострої ТЕЛА та високим ризиком варто розглянути ймовірність застосування катетерної реперфузії або системного тромболізису (ІІа, С) (Rodriguez et al., 2020).
Ішемічна хвороба серця
У вагітних жінок із болем у грудях рекомендовано виключити загрозливі для життя ССЗ, зокрема ТЕЛА, гострий коронарний синдром (включно зі спонтанною дисекцією коронарної артерії) та гострий аортальний синдром (І, С). Слід зазначити, що аспекти ведення вагітних із гострим коронарним синдромом є такими самими, як для невагітних жінок, включно із діагностичними дослідженнями й терапевтичними втручаннями (І, С) (Gulati et al., 2021; Byrne et al., 2023).
АСК у низьких дозах є препаратом вибору під час вагітності та лактації, коли показано монотерапію антиагрегантом (І, В) (Van Doorn et al., 2021; D’Antonio et al., 2023). Якщо під час вагітності потрібне призначення подвійної антитромбоцитарної терапії, клопідогрель рекомендований як інгібітор P2Y12-рецепторів (І, С). Тривалість подвійної антитромбоцитарної терапії (АСК + клопідогрель) у вагітних, які перенесли імплантацію коронарного стента, має бути такою ж, як у невагітних жінок, із застосуванням індивідуального підходу – враховуючи ішемічний ризик та ймовірність кровотечі на тлі пологів (І, С) (Elkayam et al., 2014).
Продовження приймання статинів під час вагітності може бути розглянуте у жінок зі встановленим асоційованим атеросклеротичним ССЗ (ІІb, С) (Chang et al., 2021; Karadas et al., 2022).
Артеріальна гіпертензія
У жінок під час вагітності рекомендовано прагнути досягнення систолічного артеріального тиску (САТ) <140 мм рт. ст. та діастолічного (ДАТ) <90 мм рт. ст. (І, В). САТ ≥160 мм рт. ст. або ДАТ ≥110 мм рт. ст. у вагітної є невідкладним станом та потребує лікування в умовах стаціонару (І, С) (Tita et al., 2022; Mancia et al., 2023).
У жінок із гестаційною АГ фармакотерапію необхідно розпочинати при офісних показниках САТ ≥140 мм рт. ст. або ДАТ ≥90 мм рт. ст. (І, В). Пологи у цієї категорії пацієнток рекомендовано провести на 39-му тижні (І, В). Пацієнткам із помірним або високим ризиком прееклампсії слід приймати АСК у низьких дозах (75‑150 мг/добу) із 12-го по 36/37-й тижні (І, А). У жінок із прееклампсією без тяжких проявів варто провести пологи на 37-му тижні (І, В) (Rolnik et al., 2022; Wang et al., 2022).
Метилдопа є рекомендованим препаратом для лікування АГ у вагітних (І, В). Лабеталол, метопролол та дигідропіридинові БКК також можна призначати вагітним з АГ (І, С) (Garovic et al., 2022). У разі тяжкої АГ з метою екстреного зниження АТ доцільне застосування лабеталолу, урапідилу, нікардипіну в/в або ніфедипіну короткої дії перорально чи метилдопи. Гідралазин в/в є препаратом другої лінії (І, С) (Antza et al., 2020).
Фактори ризику прееклампсії
Значущі чинники ризику
- АГ під час попередньої вагітності
- Хронічна АГ
- Хронічна хвороба нирок
- Цукровий діабет 1-го або 2-го типу
- Автоімунні захворювання, як-то системний червоний вовчак або антифосфоліпідний синдром
- Допоміжна репродуктивна терапія
під час поточної вагітності
Помірні чинники ризику
- Вік без пологів ≥40 років
- Інтервал між вагітностями ˃10 років
- Індекс маси тіла ≥35 кг/м2 під час першого візиту до лікаря
- Сімейний анамнез прееклампсії
- Багатоплідна вагітність
Суправентрикулярна тахікардія
Негайна електрична кардіоверсія рекомендована вагітним для гострого лікування суправентрикулярної тахікардії з гемодинамічною нестабільністю (І, С). У вагітних для контролю гемодинамічно стабільних надшлуночкових тахікардій доцільними є проведення вагусних маневрів та введення аденозину в/в (І, С) (Brugada et al., 2020). Бета-блокатори в/в (за винятком атенололу), наприклад метопролол, слід застосовувати як препарати першої лінії для гострого контролю ЧСС у жінок із ФП або ФП і СН зі збереженою ФВ ЛШ та високою частотою скорочень шлуночків під час вагітності (І, С). Введення дигоксину або верапамілу в/в (за СН зі збереженою ФВ ЛШ) слід розглядати як стратегію другої лінії для початкового контролю ЧСС у вагітних із ФП або ТП та високою частотою скорочень шлуночків (ІІа, С) (Miyoshi et al., 2019). Ібутилід або флекаїнід можна розглядати для контролю ФП і ТП у вагітних без структурних захворювань серця (ІІb, С) (Ramlakhan et al., 2022).
Що стосується довгострокового лікування суправентрикулярної тахікардії та ФП, антикоагулянтна терапія НМГ у терапевтичній дозі рекомендована вагітним із персистувальною або стійкою ФП за підвищеного ризику тромбоемболії (І, С) (Hindricks et al., 2021). У вагітних із ФП, ТП або фокальною тахікардією для контролю ЧСС слід призначити селективні блокатори β1-адренорецепторів (за винятком атенололу) (І, С). Своєю чергою використання дигоксину або верапамілу варто розглянути для контролю ЧСС у цієї категорії хворих, коли β-блокатори неефективні або не переносяться (ІІа, С) (Brugada et al., 2020; Tamirisa et al., 2022).
Флекаїнід або пропафенон застосовуються для профілактики аритмій у вагітних із синдромом Вольфа – Паркінсона – Уайта (І, С). Приймання флекаїніду слід розглянути для довгострокового контролю ритму у вагітних із ФП на додаток до β-блокаторів (ІІа, С) (Bateman et al., 2018). Призначення соталолу може бути доцільним для контролю ритму при ФП та ТП з урахуванням проаритмічних факторів ризику (ІІb, С) (Singh et al., 2005). Катетерну абляцію можна розглядати у вагітних жінок із рецидивною, тривалою симптоматичною суправентрикулярною тахікардією або за наявності протипоказань до фармакотерапії (ІІb, С).
Шлуночкова тахікардія, імплантація пристрою, катетерна абляція
Застосування β-блокаторів або верапамілу є доцільним для профілактики ідіопатичної стійкої ШТ (І, С). При ідіопатичному ураженні вихідного тракту ПШ слід розглянути можливість використання флекаїніду, якщо β-блокатори неефективні, щоб запобігти рецидиву (ІІа, С).
Якщо під час вагітності показане встановлення карідовертера-дефібрилятора, кардіостимулятора або пристрою для ресинхронізувальної терапії, рекомендована імплантація з оптимальним радіаційним захистом (І, С) (Tuzcu et al., 2015). Негайна електрична кардіоверсія є доцільною у разі розвитку як нестабільних, так і стабільних ШТ під час вагітності (І, С). Для гострої конверсії у вагітних із гемодинамічно стабільною стійкою ШТ слід розглянути в/в введення β-блокатора, аденозину (при ідіопатичному ураженні вихідного тракту ПШ), верапамілу (за фасцикулярної ШТ), прокаїнаміду або прискорену стимуляцію шлуночків (ІІа, С) (Ortiz et al., 2017; Zeppenfeld et al., 2022).
Вроджені вади серця
Оперативне втручання слід розглянути до настання вагітності у пацієнток із безсимптомним тяжким аортальним стенозом після консультування щодо ризиків та переваг (ІІа, С). У пацієнток із симптоматичним тяжким аортальним стенозом або мітральним стенозом та площею клапана <1,5 см2 рекомендовано провести хірургічне втручання до настання вагітності (І, С) (Vahanian et al., 2022; Roos-Hesselink et al., 2023). Вагітні з симптоматичним мітральним стенозом або легеневою АГ мають обмежити фізичну активність та приймати β-блокатори (І, С). Жінкам із мітральним стенозом слід призначити діуретики, якщо під час вагітності симптоми застою зберігаються, незважаючи на лікування β-блокаторами (І, С) (Elkayam et al., 2016). Використання антикоагулянтів у повній терапевтичній дозі рекомендоване вагітним із мітральним стенозом, ускладненим ФП, тромбом лівого передсердя або емболією в анамнезі (І, С).
Черезшкірну мітральну комісуротомію при мітральному стенозі варто розглянути у вагітних із виразними симптомами або систолічним тиском у легеневій артерії >50 мм рт. ст., попри медикаментозну терапію (ІІа, С). Хірургічне лікування рекомендоване до настання вагітності у жінок із тяжкою аортальною або мітральною регургітацією з супутніми симптомами, порушенням функції чи виразною дилатацією шлуночків (І, С) (Vahanian et al., 2022).
Протезування клапанів
Молодим жінкам, які планують вагітність і потребують протезування клапана, рекомендоване встановлення біопротеза клапана (замість МКС) (І, В). Для жінок дітородного віку з МКС до вагітності або одразу після її підтвердження необхідно розробити план лікування, що включає узгоджену стратегію антикоагулянтної терапії (зокрема рішення про продовження приймання АВК або перехід на НМГ у терапевтичній дозі в першому триместрі) (І, С) (Lester et al., 2023; van der Zande et al., 2025).
Протягом другого та третього триместрів вагітності до 36-го тижня у жінок із протезами клапанів серця та підвищеним ризиком тромбозу слід розглянути продовження використання АВК (ІІа, С). У вагітних із МКС, які приймають НМГ у терапевтичній дозі, рекомендовано контролювати пікові концентрації фактора анти-Ха та встановлювати цільові рівні відповідно до індивідуального ризику (І, С). У другому та третьому триместрах вагітності продовження приймання НМГ із моніторингом рівня фактора анти-Ха та корекцією дози може розглядатися у жінок із нижчим ризиком тромбозу (ІІb, С).
Хронічна та гостра СН
Хронічна СН. Жінок із СН зі зниженою ФВ ЛШ необхідно інформувати про ризик погіршення функції серця під час вагітності та в післяпологовому періоді (І, С). Вагітних із СН зі зниженою ФВ ЛШ рекомендовано перевести з неселективних на селективні блокатори β1-адренорецепторів (метопролол, бісопролол) із ретельним моніторингом стану матері та плода (І, С) (Kaye et al., 2019). Антикоагулянтна терапія НМГ у терапевтичних дозах є доцільною у вагітних із внутрішньосерцевим тромбом або зниженою функцією ЛШ при ФВ <35% (І, С). Варто оптимізувати медикаментозне лікування СН після пологів відповідно до рекомендацій, враховуючи препарати, приймання яких під час лактації протипоказане (І, С) (Bauersachs et al., 2019; McDonagh et al., 2021).
Інгібітори АПФ, БРА, ARNI, антагоністи мінералокортикоїдних рецепторів, івабрадин та іНЗКТГ‑2 не рекомендовані для застосування під час вагітності через несприятливий вплив на плід (ІІІ, С).
Гостра СН. Вагітним із кардіогенним шоком необхідно призначити інотропні препарати та/або вазопресори, зокрема левосимендан, добутамін та мілринон (І, С) (Labbene et al., 2017). Жінкам із кардіогенним шоком рекомендоване термінове розродження шляхом кесаревого розтину, щойно плід стане життєздатним, з урахуванням гестаційного віку, супутніх захворювань та доступного рівня медичної допомоги (І, С) (Katz et al., 2005).
Довгострокові несприятливі наслідки вагітності
У жінок із несприятливими наслідками вагітності рекомендовано проводити оцінку СС-ризику, виявляти та документувати ці наслідки, а також консультувати їх щодо важливості здорового способу життя для підтримання нормальної роботи СС-системи (І, В). У випадках, коли лише дотримання здорового способу життя недостатньо для контролю рівня глюкози в післяпологовому періоді, необхідно розпочати фармакологічне лікування відповідно до рекомендацій (Crump et al., 2023; Adam et al., 2023).
Жінкам зі стійкою післяпологовою АГ, що зберігається впродовж 6 тижнів – 3 місяців після пологів, слід призначити антигіпертензивну терапію з урахуванням періоду лактації відповідно до рекомендацій (І, В) (Kitt et al., 2023). Застосування ніфедипіну та лабеталолу (метопрололу, якщо лабеталол недоступний) є доцільним при неускладненій післяпологовій АГ протягом перших шести тижнів після пологів (І, С) (ACOG committee, 2019).
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті www.escardio.org
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 1 (104) 2026 р.



