22 грудня, 2021
Оптимізація лікування цукрового діабету 2 типу: безпека, зниження смертності, покращання якості життя
Поширеність цукрового діабету (ЦД) неухильно зростає протягом останніх кількох десятиліть. Глобальна поширеність захворювання серед дорослого населення зросла майже вдвічі: із 4,7% у 1980 р. до 8,5% у 2014-му [1]. Метою лікування ЦД, з одного боку, є досягнення цілей глікемічного контролю, а з іншого – запобігання розвитку хронічних ускладнень і забезпечення належної якості життя. Метформін (Метфогама) майже в усіх світових рекомендаціях із лікування ЦД 2 типу визнано сучасним фармакологічним засобом першої лінії терапії. Цей пероральний цукрознижувальний препарат (ПЦЗП) належить до класу бігуанідів [2]. Він зменшує глюконеогенез у печінці і всмоктування глюкози в кишечнику, а також підвищує чутливість до інсуліну, тим самим знижуючи рівень глюкози в крові. Метформін знижує як базальний, так і постпрандіальний рівень глюкози в крові [3]. Дуже часто метформін призначають у комбінації з альфа-ліпоєвою кислотою (АЛК) (Тіогама), чиї потужні антиоксидантні властивості дають можливість запобігти прогресуванню хронічних ускладнень ЦД. У нещодавно опублікованих результатах кількох систематичних оглядів і досліджень були підтверджені нові переваги згаданих препаратів у пацієнтів із ЦД.
Ключові слова: цукровий діабет 2 типу, метформін, альфа-ліпоєва кислота, хронічна хвороба нирок, вітаміни групи В, серцево-судинний ризик, смертність, швидкість клубочкової фільтрації, лактоацидоз, інсулінорезистентність, HOMA-IR.
Цукровий діабет і хронічна хвороба нирок
Хронічна хвороба нирок (ХХН) – термін, який вказує на порушення функції і/або структури нирок. Тяжкість ХХН визначають за швидкістю клубочкової фільтрації (ШКФ) та наявністю таких маркерів ураження нирок, як альбумінурія, аномалії осаду сечі, електролітні порушення, аномалії, спричинені тубулопатіями, структурні аномалії та аномалії, виявлені за допомогою гістологічного дослідження [4]. Стадії ХХН наведені в таблиці 1.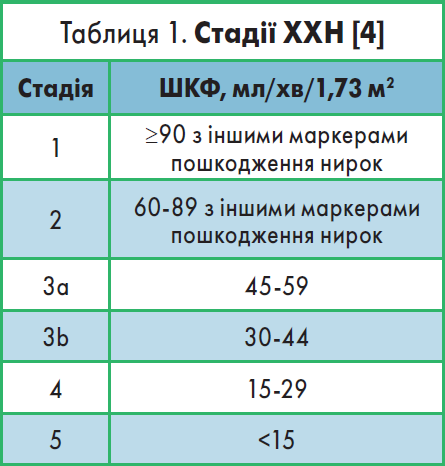
Однією з причин ХХН є погано контрольований ЦД. Зростання захворюваності на діабетичну нефропатію є ключовим фактором тягаря ХХН, її поширеність із 2005 по 2015 рік зросла на 39,5% в усьому світі. Таким чином, хворі на ЦД 2 типу із супутньою ХХН – саме та категорія, підходи до лікування якої відрізняються від загальної популяції пацієнтів.
Для уповільнення прогресування діабетичної нефропатії необхідний постійний контроль глікемії. Цього можна досягти за допомогою зміни способу життя і застосування медикаментів, у тому числі ПЦЗП та інсуліну. Чинні настанови рекомендують або використовувати меншу дозу, або не використовувати зовсім ПЦЗП першої лінії метформін у пацієнтів із нирковою недостатністю через відсутність доказів безпеки і ризики, пов’язані з лактоацидозом. Національний інститут охорони здоров’я і вдосконалення медичної допомоги Великої Британії (NICE) рекомендує зменшити дозу метформіну, коли розрахункова ШКФ (рШКФ) падає нижче 45 мл/хв/1,73 м2, і повністю припинити прийом метформіну, якщо рШКФ становить <30 мл/хв/1,73 м2. Ці рекомендації розроблені з огляду на відсутність доказів безпеки метформіну в пацієнтів із ШКФ <30 мл/хв/1,73 м2 [4]. Водночас нещодавно були отримані нові докази щодо переваг (таких як зниження смертності і серцево-судинних подій) і безпеки метформіну в дорослих пацієнтів із ЦД 2 типу і ХХН.
Метформін зменшує смертність і не впливає на ризик виникнення лактоацидозу в пацієнтів із ЦД і ХХН
Tan і співавт. (2021) провели огляд досліджень із метою оцінки якості наявних доказів щодо переваг і безпеки застосування метформіну в дорослих пацієнтів із ЦД 2 типу і ХХН. В аналіз було включено 14 статей, опублікованих до 5 листопада 2020 року.
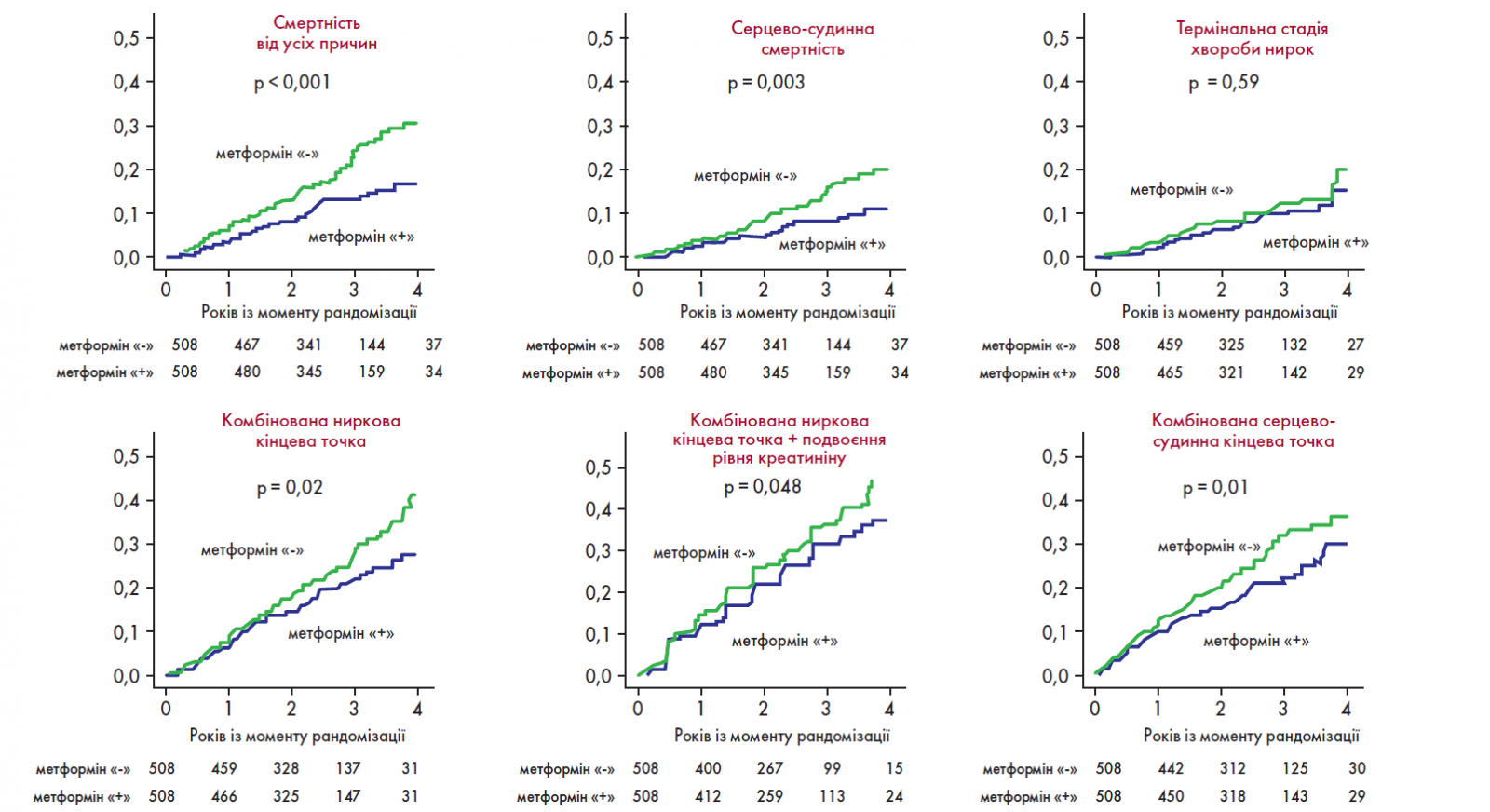
Представляємо деякі з них. Так, Charytan та співавт. (2019) у ретроспективному когортному дослідженні за участю 4038 дорослих пацієнтів із діабетом і ХХН (рШКФ 20-60 мл/хв/1,73 м2) оцінювали влив метформіну на такі кінцеві точки, як смертність від усіх причин, серцево-судинна смертність, серцево-судинні події (смерть, госпіталізація через серцеву недостатність (СН), інфаркт міокарда (ІМ), інсульт або ішемію міокарда), розвиток термінальної стадії ХН (ТСХН) і комбінована кінцева точка (ТСХН або смерть). 591 учасник випробування приймав метформін (метформін «+»), а 3447 учасників – не приймали (метформін «-») [5]. Результати дослідження відображені на рисунку 1.
Рис. 1. Виживаність без подій при використанні метформіну у відповідній когорті пацієнтів
Таким чином, було встановлено, що застосування метформіну супроводжувалося зниженням ризику смертності від усіх причин (відношення ризиків (ВР) 0,49; 95% ДІ 0,36-0,69), серцево-судинної смертності (ВР 0,49; 95% ДІ 0,32-0,74), комбінованої кінцевої серцево-судинної точки (тобто госпіталізації з приводу СН, інфаркту міокарда, інсульту, ІМ, або смерті) (ВР 0,67; 95% ДІ 0,51-0,88) і комбінованої кінцевої точки ХХН (ВР 0,77; 95% ДІ 0,61-0,98). Зв’язок між прийомом метформіну і розвитком ТСХН (ВР 1,01; 95% ДІ 0,65-1,55) виявився недостовірним.
Безпека метформіну в пацієнтів із ХХН оцінювалася в іще одному ретроспективному когортному дослідженні – Ekström та співавт. [6]. Було оцінено дані 51 675 пацієнтів із ЦД 2 типу, із них 32 848 – приймали метформін, а в групу порівняння увійшли хворі, які приймали інші ПЦЗП або інсулін. Учасників розподілили на групи залежно від рівнів рШКФ: <45 мл/хв/1,73м2, 60 мл/хв/1,73м2, >60 мл/хв/1,73м2. Кінцевими точками були смертність від усіх причин і частота ацидозу та серйозних інфекцій.
У результаті було виявлено, що в пацієнтів із рШКФ 45-60 мл/хв/1,73 м2 застосування метформіну асоціювалося зі зниженням серцево-судинного ризику, ацидозу або серйозної інфекції та смертності від усіх причин, якщо порівняти з прийомом інсуліну. Також у згаданій когорті пацієнтів спостерігалося зниження ризику смертності від усіх причин проти такого у хворих із такою самою рШКФ, які отримували інші ПЦЗП. Застосування метформіну не супроводжувалося підвищенням ризику розвитку ацидозу або серйозної інфекції навіть у пацієнтів зі значно зниженою функцією нирок (ШКФ 30-45 мл/хв/1,73 м2) (рис. 2).
Рис. 2. Час (міс) до виникнення будь-якого епізоду ацидозу / серйозної інфекції в кожній групі лікування, некорегований
Зниження загальної смертності та кардіоваскулярних подій у пацієнтів із діабетичною нефропатією на тлі застосування метформіну
Вплив метформіну на показники смертності від усіх причин був кінцевою точкою систематичного огляду Hu та співавт. (2020) [7]. Автори оцінювали дані 13 досліджень: 9 когортних випробувань, 3 ретроспективних аналізів рандомізованих клінічних досліджень (РКД), 1 дослідження «випадок-контроль». Загалом були проаналізовані дані 303 540 хворих на ЦД 2 типу і з ХХН. У результаті встановлено, що прийом метформіну супроводжувався достовірним зниженням рівня смертності від усіх причин (об’єднане ВР 0,71; 95% ДІ 0,61-0,84; р<0,001) і серцево-судинної смертності (об’єднане ВР 0,76; 95% ДІ 0,60-0,97; р=0,024) на стадіях 1-3 ХХН.
Метформін не підвищує ризик лактоацидозу
У ще одному когортному дослідженні Lazarus та співавт. (2018) оцінювався вплив метформіну на частоту госпіталізації з приводу ацидозу пацієнтів із ЦД 2 типу і ХХН [8]. Загалом у дослідженні взяло участь 75 413 пацієнтів, із яких 47 876 отримували метформін. 14 662 пацієнти мали ХХН 3 стадії, 1765 – ≥4 стадію. Було встановлено, що застосування метформіну не підвищує ризик виникнення ацидозу в пацієнтів із ХХН стадії 3a (ШКФ 45-59 мл/хв/1,73 м2) (скореговане ВР 0,75; 95% ДІ 0,58-0,97) і ХХН стадії 3b (ШКФ 30-44 мл/хв/1,73 м2) (скореговане ВР 0,83; 95% ДІ 0,42-1,62).
Висновки
Таким чином, результати проведеного огляду свідчать: застосування метформіну в пацієнтів із ЦД 2 типу і ХХН супроводжувалося зменшенням смертності від усіх причин і зниженням ризику серцево-судинних подій. При цьому ризик лактоацидозу, пов’язаний із застосуванням метформіну при ХХН, дуже низький. Схоже, цей ризик переоцінений, отже, застосування метформіну при ХХН може бути безпечнішим, ніж вважалося раніше.
Велика кількість пацієнтів із ХХН застосовують метформін, проте лактоацидоз у них виникає рідко [9]. Згаданий стан зазвичай асоціюється з гострими тяжкими захворюваннями, які супроводжуються надмірним виробленням і зниженою здатністю окислення лактату (наприклад, при ішемії або гіпоксії) [10]. Лактоацидоз при ХХН без інших гострих метаболічних порушень пов’язаний, найімовірніше, із цими гострими станами, ніж із застосуванням метформіну.
Досі до кінця не ясно, при якій рШКФ варто зменшити дозу метформіну, а при якій – зовсім припинити. Сучасні рекомендації радять зменшити дозу метформіну за рШКФ <45 мл/хв/1,73 м2 і припинити його прийом, якщо рШКФ <30 мл/хв/1,73 м2. Однак, оскільки є дані про покращення показників щодо смертності і серцево-судинних наслідків навіть у популяції пацієнтів із рШКФ 20 мл/хв/1,73 м2 [11], доцільно розглянути можливість застосування метформіну в пацієнтів із нижчими рівнями ШКФ. Імовірно, у такому разі потрібно буде проводити моніторинг рівня рШКФ, для того щоб гарантувати припинення прийому метформіну при її зниженні. Сьогодні рекомендації NICE і Kidney Disease: Improving Global Outcomes (Ініціатива з покращення глобальних наслідків хвороб нирок) (KDIGO) пропонують проводити моніторинг функції нирок 3-4 рази на рік або більше на стадіях 4 і 5 ниркової недостатності [4]. Проте, схоже, бракує даних щодо частоти моніторингу прогресування ХХН у пацієнтів із ХХН 4 стадії, які приймають метформін.
Вплив АЛК на наслідки порушення вуглеводного обміну
Інсулінорезистентість, глікемічні маркери та їх прогностичне значення
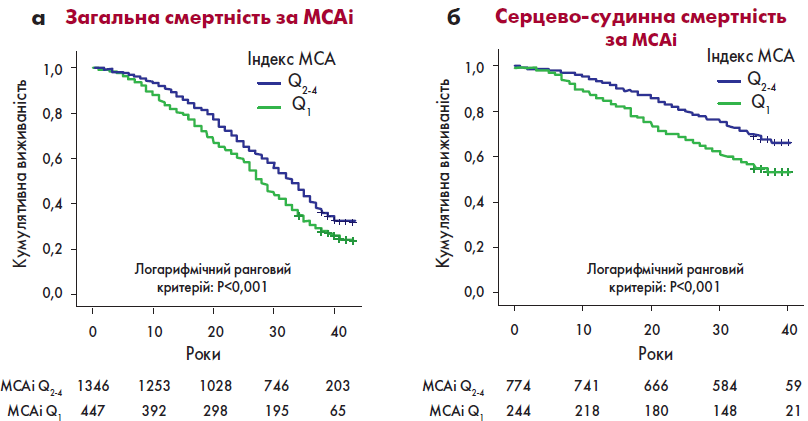
Інсулінорезистентність (ІР) – це стан, за який нормальної кількості інсуліну недостатньо для виникнення очікуваної біологічної реакції в тканинах-мішенях: жировій тканині, м’язах і печінці. ІР асоційована з цілою низкою захворювань, як-от: ЦД 2 типу, гіпертонія, серцево-судинні та цереброваскулярні захворювання, патологія периферичних судин, застійна СН, неалкогольна жирова хвороба печінки, дисліпідемія і різноманітні злоякісні новоутворення. Крім того, ІР встановлена за допомогою гомеостатичної моделі оцінки ІР (HOMA-IR, Homeostasis Model Assessment of Insulin Resistance). Індекс HOMA-IR – це дослідження, яке визначає резистентність до інсуліну шляхом оцінювання вмісту глюкози та інсуліну натще в сироватці крові і розрахунок індексу ІР. Його проводять за такою формулою: HOMA-IR = інсулін натще (мкОд/мл) × глюкоза натще (ммоль/л) / 22,5. Підвищення індексу ІР достовірно підвищує загальну і серцево-судинну смертність, що відображено в таблиці 2 і на рисунку 3 [14,15].
Рис. 3. ІР за індексом Маколі та загальна і серцево-судинна смертність:
а – ІР за індексом Маколі (MCAi) (1 квартиль vs 2-4 квартилі) і загальна смертність;
б – ІР за індексом MCAi (1 квартиль vs 2-4 квартилі) і серцево-судинна смертність [15]
Своєю чергою, зниження рівня ІР супроводжується низкою переваг (рис. 4).
Рис. 4. Переваги, пов’язані зі зниженням рівня ІР
Модифікація способу життя, зокрема дієта, може відігравати вирішальну роль у довготривалій терапії цього порушення. Водночас більшість пацієнтів стикаються зі складнощами в дотриманні рекомендацій. Для нівелювання пов’язаних із цим негативних наслідків і досягнення короткострокових результатів харчування пацієнтів доповнюють мікронутрієнтами з антиоксидантними і протизапальними властивостями, зокрема вітамінами і АЛК [16,17].
АЛК, відома також як тіоктова кислота і 1,2-дитіолан 3-пентанова кислота, – коротколанцюгова жирна кислота з амфіпатичними властивостями [17-19]. Антиоксидантні властивості АЛК пояснюються її здатністю захоплювати вільні радикали, хелатувати іони металів (Fe, Cu), підвищувати вміст глутатіону і вітаміну С у цитозолі, нейтралізувати активні форми кисню та активувати ендогенні антиоксидантні шляхи [20,21]. Крім того, було показано, що АЛК може пригнічувати адипогенез і регулювати секрецію адипокінів (наприклад, адипонектину, ептину і резистину), які сприяють кращому функціонуванню жирової тканини [17, 22, 23]. Аналогічно, протизапальні властивості АЛК реалізуються завдяки сприятливому впливу на окислювально-відновний стан плазми, зниженню запальної відповіді, індукованої ліпополісахаридами, інгібуванню експресії гена ядерного фактора кaппa (NFk)-B, активації шляхів мітоген-активованої протеїнкінази і кінази, регульованої позаклітинними сигналами, і впливу на індуцибельну синтазу оксиду азоту і циклооксигеназу‑2 [21, 23].
Більшість учених визнають наявність в АЛК антиліпідемічних ефектів і позитивного впливу на ожиріння, які, як передбачається, реалізуються шляхом активації протеїнкінази, активованої аденозинмонофосфатом (ПКАМ), інгібування активності білків, що зв’язують стеролрегулювальні елементи, і зниження синтезу триацилгліцеролу і секреції ліпопротеїнів дуже низької щільності, підвищення метаболізму і контролю ферментів, які беруть участь у метаболізмі ліпідів, таких як ГМГ-КоА-редуктаза [20,24]. Також АЛК сприятливо впливає на контроль ЦД і метаболічні фактори шляхом покращення функції ендотелію, гомеостазу глюкози і чутливості до інсуліну [21, 24].
З огляду на вищезазначене та обмежені дані РКД щодо застосування АЛК та її впливу на глікемічні фактори без консенсусного заключення про наслідки, Mahmoudi-Nezhad та співавт. (2020) провели систематичний огляд і метааналіз досліджень, опублікованих до лютого 2020 року, із метою оцінки впливу АЛК на такі глікемічні біомаркери, як глюкоза, глікований гемоглобін (HbA1с), інсулін, HOMA-IR, HOMA-β і кількісний індекс перевірки чутливості до інсуліну (QUICKI) залежно від дози [25].
Для написання поточного систематичного огляду і метааналізу було використано настанову PRISMA.
У результаті авторами було виявлено, що прийом АЛК достовірно знижував рівень інсуліну і HOMA-IR у сироватці крові. Крім того, тривалість прийому добавок AЛК дозозалежно впливала на зміну рівня інсуліну (нелінійність р=0,04). Зниження HOMA-IR спостерігали при застосуванні АЛК у дозі >600 мг/добу протягом ≤10 тижнів. У більшості включених досліджень виявлено достовірне зниження концентрації інсуліну і HOMA-IR на тлі прийому АЛК проти таких у групі плацебо [18, 19, 22, 26, 28-30]. Було також встановлено, що застосування АЛК у дозі >600 мг/добу протягом ≤10 тиж ефективніше знижує рівні HOMA-IR, що підтверджує доцільність тривалого застосування високих доз АЛК для зниження глікемічних маркерів.
Крім того, зважаючи на ключову роль оксидативного стресу в розвитку ІР, АЛК може сприятливо впливати на оксидативний статус завдяки своїм антиоксидантним властивостям [17, 24, 33, 34].
Прийом AЛК може підвищити рівень адипонектину, який активує термогенез і подальшу втрату ваги через невідомі механізми. Цей адипокін має протизапальні та інсуліносенсибілізувальні властивості [22]. Доступні дані також вказують на те, що АЛК знижує вагу та ІМТ [35]. Схоже, що це реалізується шляхом впливу на регуляторні шляхи енергетичного гомеостазу та окислення ліпідів ПКАМ, які відіграють ключову роль у харчовій поведінці і забезпеченні аноректичного ефекту [17, 22, 28]. AЛК контролює активність ферментів, що беруть участь у ліполізі і синтезі тригліцеридів, підвищує активність ліпопротеїнліпази і лецитин-холестерин-ацилтрансферази та проявляє ліпідомодулювальну дію [24, 36-38].
В аналізі «доза-відповідь» зниження концентрації інсуліну після прийому AЛК було дозозалежним. При цьому різке зниження спостерігалося до 17-го тиж прийому АЛК. Це ще раз доводить важливість тривалого прийому для реалізації корисних ефектів АЛК і вирішує суперечності у висновках попередніх звітів; наприклад, у дослідженні Atmaca та співавт. [28] було встановлено, що прийом АЛК пацієнтами з ЦД 2 типу протягом 6 тиж сприяв достовірному зниженню рівня інсуліну.
Таким чином, результати першого дослідження з оцінки дозозалежного впливу АЛК на глікемічні маркери (глюкозу, HbA1с, HOMA-IR та інсулін) показали, що прийом АЛК достовірно знижує рівень інсуліну в сироватці крові і HOMA-IR без значущого впливу на рівні глюкози в сироватці крові або Hb1с. Крім того, спостерігалася нелінійна залежність між тривалістю прийому АЛК і рівнем інсуліну.
ЦД, ХХН і дефіцит вітамінів
Встановлено, що при ЦД в організмі розвивається нестача вітамінів і мінеральних речовин, зумовлена обмеженням раціону, порушенням обмінних процесів і зниженням засвоєння корисних речовин [40, 41]. ХХН іще більше поглиблює цей дефіцит. Саме тому для максимально ефективної реалізації описаних властивостей метформіну та АЛК їх краще реалізувати в присутності вітамінів групи В. Призначення комплексу вітамінів В1, В6, В12 (Мільгама) забезпечує:
- поповнення дефіциту вітамінів В1, В6, В12, з яким асоціюється ЦД і ХХН [40-43];
- корекцію і/або профілактику дефіциту вітамінів В1, В6, В12, який може виникнути на тлі прийому метформіну [44];
- зменшення симптоматики і запобігання прогресуванню діабетичної нейропатії та ІР завдяки синергізму з АЛК і підвищенню чутливості до інсуліну [45, 46].
Висновки
Отже, нові дані підкріплюють доцільність застосування метформіну (Метфогама) у пацієнтів із ЦД 2 типу і супутньою ХХН 1-4 стадій. Це супроводжується зменшенням смертності від усіх причин і зниженням ризику серцево-судинних подій на тлі низького ризику розвитку лактоацидозу. Сучасні настанови рекомендують зменшити дозу метформіну за рівня рШКФ <45 мл/хв/1,73 м2 (стадія 3b) і припинити прийом метформіну за рівня рШКФ <30 мл/хв/1,73 м2 (стадія 4). Однак, оскільки є дані про покращення показників смертності і серцево-судинних наслідків навіть у популяції з рШКФ 20 мл/хв/1,73 м2, варто розглянути можливість застосування метформіну в пацієнтів із нижчими рівнями ШКФ. Імовірно, при цьому потрібно проводити моніторинг рівня рШКФ, оптимальну частоту якого необхідно буде встановити в подальших дослідженнях.
Супутнє призначення АЛК (Тіогама) дає можливість покращити прогноз за рахунок зменшення сироваткового рівня інсуліну та ІР. Максимальний ефект спостерігається при застосуванні доз АЛК >600 мг/добу протягом ≤10 тижнів. Доповнення комплексної терапії вітамінами групи В (Мільгама) допоможе ліквідувати дефіцит останніх і/або запобігти йому і посилити дію АЛК шляхом підвищення чутливості до інсуліну. Усе вищезазначене наголошує на доцільності застосування комбінації Метфогама + Тіогама + Мільгама в комплексній терапії ЦД 2 типу, особливо в пацієнтів із супутньою ХХН.
Література – у редакції.
Підготувала Ганна Кирпач