6 липня, 2022
Дослідження InRange: перші результати та практичні висновки
Аналоги базального інсуліну ІІ покоління мають значні переваги в застосуванні в хворих на цукровий діабет (ЦД), оскільки характеризуються тривалішим ефектом, сприятливішим фармакокінетичним профілем і забезпечують менші добові коливання рівня глікемії. Утім, і досі не було проведено прямого порівняння між безпекою та ефективністю цих препаратів в осіб із ЦД 1 типу. В дослідженні InRange вперше порівняли ефективність двох базальних аналогів II покоління за показником time in range (TIR) – час перебування значень глікемії у межах цільового діапазону. Поза сумнівом, отримані результати будуть корисними для лікарів із погляду розуміння ефектів лікарських засобів і тих перспектив, які відкриває їхнє застосування для пацієнтів. На окрему увагу заслуговує метод цілодобового моніторингу рівня глюкози, який використовувався для контролю ефективності та безпеки інсулінотерапії. Результати та висновки дослідження InRange обговорювалися на Нараді експертів, що об’єднала провідних вітчизняних діабетологів.
Кандидат медичних наук, лікар-ендокринолог Костянтин Олександрович Зуєв детально розповів про обґрунтування проведення та цілі дослідження InRange.
детально розповів про обґрунтування проведення та цілі дослідження InRange.
Доповідач звернув увагу, що значна добова глікемічна варіабельність (ГВ) є досить поширеною та важливою проблемою для осіб із ЦД, при цьому пацієнт може мати нормальне значення HbA1c, що вводитиме клініциста в оману щодо реальної картини перебігу захворювання. Саме тому останніми роками для оцінки глікемічного контролю клініцисти використовують показник TIR, який можна визначити за допомогою методу цілодобового моніторингу глікемії.
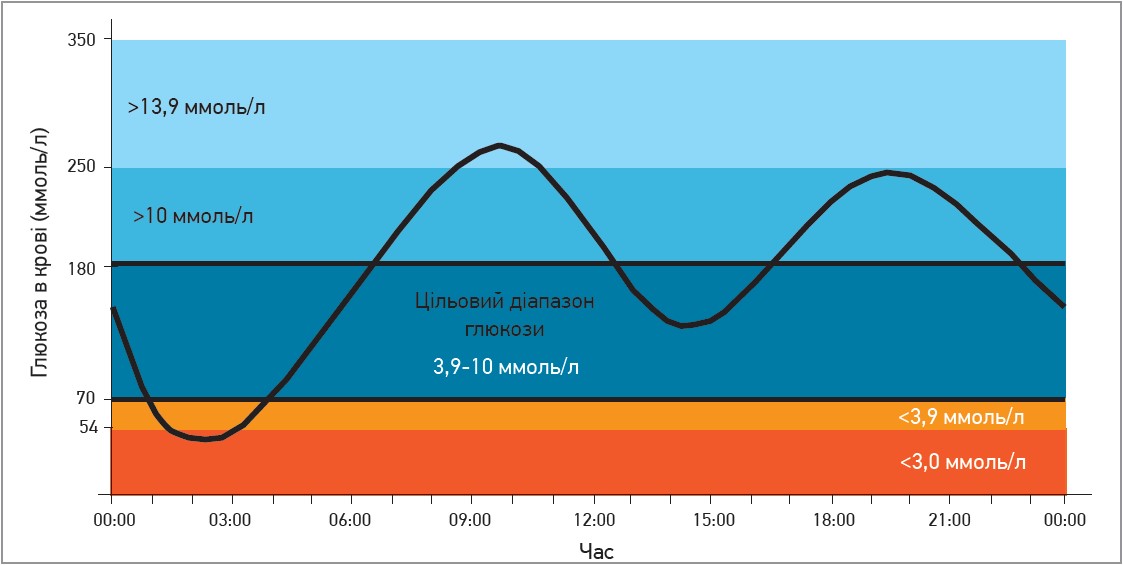
Нерідко значні коливання рівня глюкози крові з’являються без видимої причини на тлі відсутності порушень харчового режиму та зміни фізичної активності. За даними моніторингу, в 56% осіб із ЦД 1 типу спостерігається надмірна ГВ (коефіцієнт варіабельності (КВ) перевищує 36%); ≈9 год/добу середньостатистичний пацієнт із ЦД 1 типу перебуває поза межами цільових показників глікемії (у стані гіпер- або гіпоглікемії) (рис. 1).
Рис. 1. Приклад амбулаторного профілю глюкози за 24-годинний період
Часто пацієнти самі досить добре відчувають коливання глікемії; ≈57% осіб із ЦД 1 типу оцінили час перебування в цільовому діапазоні (TIR) як вимірюваний результат терапії, що мав найбільший вплив на повсякденне життя.
Для більшості пацієнтів із ЦД 1 та 2 типів TIR має становити >70%, <25% часу має припадати на стан гіперглікемії (>10 ммоль/л), <4% часу – на стан гіпоглікемії (3,9 ммоль/л). Для хворих похилого віку нормальним показником TIR вважається значення >50%.
Сьогодні відомо, що неоптимальний час у цільовому діапазоні глікемії може мати істотний негативний вплив на здоров’я пацієнтів із ЦД. Зниження TIR на кожні 10% асоціюється з підвищенням ризику ретинопатії (+64%), мікроальбумінурії (+40%), нейропатії (+25%), а також смертності від серцево-судинних захворювань (+5%) та від усіх причин (+8%).
Також відомо, що неоптимальний TIR і надмірна ГВ можуть мати істотний негативний вплив на емоційний стан та загальний настрій (втома, дратівливість, розчарування). На думку більшості пацієнтів із ЦД 1 типу досягнення цільового показника TIR є найкращим стимулом позитивного мислення про своє захворювання. Отже, здатність оптимізувати показник TIR і ГВ можна вважати запорукою успішного лікування діабету.
Оскільки оптимальними препаратами інсуліну в лікуванні хворих із ЦД 1 типу вважаються аналоги базального інсуліну II покоління, значна увага дослідників сьогодні приділяється саме їм.
Відомо, що інсулін гларгін 300 ОД/мл (ІGla‑300) та інсулін деглюдек 100 ОД/мл (IDeg‑100) мають стабільніші й триваліші фармакокінетичні, а також фармакодинамічні профілі порівняно із ІGla‑100 I покоління та інсуліном детемір із меншим ризиком гіпоглікемії. Утім, існують обмежені дані щодо безпосереднього порівняння ІGla‑300 та IDeg‑100 в пацієнтів із ЦД 1 типу. Щоб з’ясувати всі нюанси цього питання, було проведено дослідження InRange – перше рандомізоване контрольоване випробування в паралельних групах, метою якого стало порівняння аналогів базального інсуліну II покоління в пацієнтів із ЦД 1 типу щодо впливу на ГВ. У дослідженні порівнювали результати лікування ІGla‑300 та IDeg‑100.
До випробування InRange залучили 40 центрів із 7 країн світу (США, Бразилія, Німеччина, Угорщина, Нідерланди, Туреччина, Сполучене Королівство). ГВ вивчали за допомогою добового моніторингу глюкози (ДМГ).
Як первинну кінцеву точку було обрано показник TIR (час, проведений у цільовому діапазоні рівня глюкози від ≥3,9 до ≤10 ммоль/л на 12-му тижні).
Основна вторинна кінцева точка – загальний коефіцієнт ГВ на 12-му тижні.
Інші вторинні кінцеві точки: коефіцієнт ГВ упродовж усіх днів і між днями на 12-му тижні; зміна показників HbA1c і ГПН із вихідного рівня до 12-го тижня; відсоток часу та середня кількість годин на добу з рівнем глюкози <3,9 та >10 ммоль/л.
Кінцеві точки безпеки: кількість учасників із небажаними явищами, ≥1 гіпоглікемічною подією протягом 12 тиж; кількість гіпоглікемічних подій на одного учасника на рік із вихідного рівня до 12-го тижня.
Метою дослідження було продемонструвати, що ІGla‑300 не поступається IDeg‑100 щодо TIR і ГВ.
Було застосовано покрокову ієрархічну процедуру тестування:
етап 1 – продемонструвати не меншу ефективність ІGla‑300 проти IDeg‑100 щодо первинної кінцевої точки;
етап 2 – продемонструвати не меншу ефективність ІGla‑300 проти IDeg‑100 щодо основної вторинної кінцевої точки;
етап 3 – продемонструвати перевагу ІGla‑300 над IDeg‑100 щодо первинної кінцевої точки.
До випробування було залучено дорослих пацієнтів (віком 18-70 років) із ЦД 1 типу з недостатньо контрольованим перебігом захворювання (HbA1c від ≥7 до ≤10%), які не менше 1 року отримували режим базисно-болюсної терапії (будь-яким аналогом базального інсуліну 1 р/добу та аналогами швидкої дії) без застосування ІGla‑300 чи IDeg‑100 протягом останніх 30 днів.
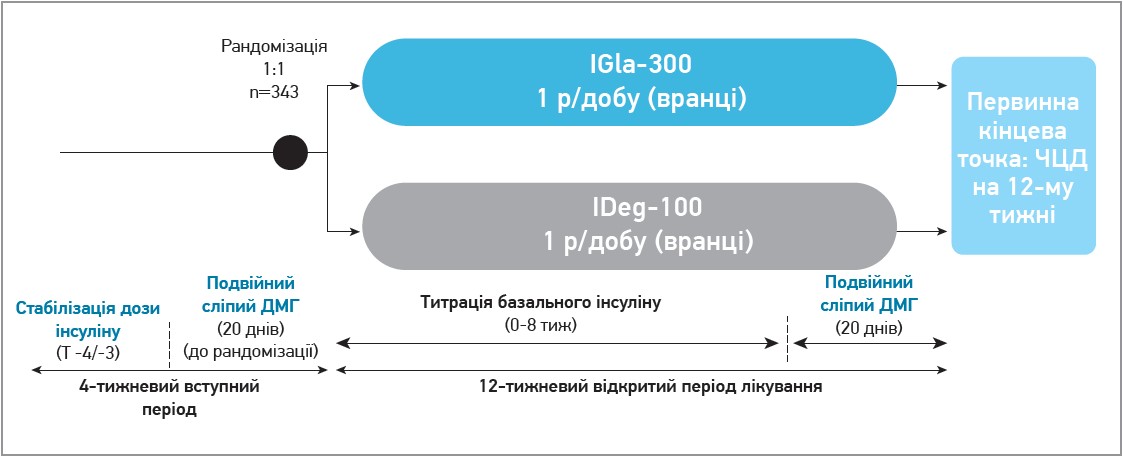
Загалом 343 пацієнтів було рандомізовано до двох груп: ІGla‑300 (1 р/добу вранці) та IDeg‑100 (1 р/добу вранці). Рандомізації передував 4-тижневий вступний період, що передбачав стабілізацію дози інсуліну та подвійний сліпий ДМГ; пацієнти і лікарі не знали результатів моніторингу, а контроль лікування проводили на основі визначення рівня глікемії натще, після сніданку, обіду та вечері. Подальший 12-тижневий відкритий період лікування включав титрації базального інсуліну протягом 8 тиж і 20-денний період подвійного сліпого ДМГ (рис. 2).
Рис. 2. Дизайн дослідження InRange
Поза сумнівом, ДМГ на сьогодні є передовим методом контролю ефективності лікування діабету; наразі в Україні він застосовується рідко, оскільки є недешевим для більшості пацієнтів, а вартість сенсорів для цього методу дослідження не компенсується державою. Незаперечна перевага ДМГ – можливість своєчасно дізнатися про небезпеку розвитку гіпоглікемій та вжити відповідних заходів для її запобігання.
Про результати дослідження InRange розповіла завідувачка відділу діагностики та лікування метаболічних захворювань ДНУ «Центр інноваційних технологій НАН України» (м. Київ), доктор медичних наук, професор Надія Миколаївна Жердьова.
 Доповідачка нагадала, що пацієнти груп ІGla‑300 та IDeg‑100 були зіставними за віком, статтю, масою тіла, індексом маси тіла, тривалістю ЦД 1 типу, рівнем HbA1c. У більшості хворих показник HbA1c на момент залучення до випробування перевищував 8%.
Доповідачка нагадала, що пацієнти груп ІGla‑300 та IDeg‑100 були зіставними за віком, статтю, масою тіла, індексом маси тіла, тривалістю ЦД 1 типу, рівнем HbA1c. У більшості хворих показник HbA1c на момент залучення до випробування перевищував 8%.
Етап 1. На 12-му тижні ІGla‑300 продемонстрував однакову ефективність з IDeg‑100 щодо показника TIR у пацієнтів із ЦД 1 типу.
Етап 2. На 12-му тижні ІGla‑300 довів однакову з IDeg‑100 ефективність щодо загального коефіцієнту ГВ у хворих із ЦД 1 типу. ІGla‑300 мав зіставну з IDeg‑100 ефективність щодо внутрішньоденної та міжденної ГВ, при цьому КВ ефективно знизився майже до однакових значень серед пацієнтів, котрі мали цей показник вище норми та в межах норми на вихідному рівні.
Етап 3. Переваг ІGla‑300 над IDeg‑100 за показником TIR, визначеним у відсотковому відношенні, продемонстровано не було.
ІGla‑300 мав однакову з IDeg‑100 ефективність у зниженні показника HbA1c у пацієнтів із ЦД 1 типу за переведення з аналогів I покоління. Важливо, що переведення хворих з аналогів інсулінів I покоління на аналоги II покоління дозволив досягти додаткового зниження рівня HbA1c за 12 тиж майже на 1%, що є досить непоганим результатом.
Час знаходження на показниках вище та нижче за цільовий діапазон глікемії був однаковим в обох групах. Не було виявлено різниці у частоті розвитку гіпоглікемій (у т. ч. тяжкі гіпоглікемії, нічні та денні гіпоглікемії). Частота виникнення небажаних явищ під час лікування була зіставною між групами. Втім, жоден із побічних ефектів не потребував відміни лікування.
Третинна кінцева точка – добова доза базального інсуліну.
Дози базальних інсулінів в обох групах пацієнтів незначно змінилися від вихідного рівня та відрізнялися між собою несуттєво.
Керівник відділу клінічної діабетології НДДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова надала експертну оцінку результатам дослідження InRange.
Доповідач зазначила, що спостереження за InRange є дуже важливим для звичайної клінічної практики. По-перше, сам метод ДМГ, який використовували в цьому дослідженні, на сьогодні є найінформативнішим щодо визначення як ефективності, так і безпеки лікування. В InRange метод ДМГ не використовували на етапі титрування інсуліну, однак і за таких умов переведення хворих на базальні аналоги II покоління виявилося безпечним та ефективним. Можна припустити, що застосування ДМГ у періоді титрування дозволило б досягти ще кращих результатів інсулінотерапії.
Рівень HbA1c знизився з 8,34/8,29 до 7,38/7,51 після переведення пацієнтів з аналогів I покоління на аналоги II покоління та їхньої титрації, що є додатковим свідченням кращих властивостей базальних аналогів II покоління. Це пов’язано насамперед із можливістю провести безпечне титрування базальних аналогів II покоління до показників компенсації ЦД без підвищення при цьому ризику розвитку гіпоглікемії.
Дози базальних інсулінів в обох групах незначно змінилися від вихідного рівня, що ще раз свідчить про кращі властивості базальних аналогів II покоління незалежно від дози.
Практично однакові результати було отримано в групах ІGla‑300 та IDeg‑100, отже, ці препарати інсуліну можна вважати взаємозамінними (за потреби легко можна перевести хворого з інсуліну Тресіба на Тожео СолоСтар і навпаки).
Наразі під час воєнного стану будь-які аналоги інсулінів для пацієнтів є безкоштовними, оскільки їхня вартість компенсується державою за системою реімбурсації. Крім того, чимало базальних аналогів II покоління було завезено до України у вигляді гуманітарної допомоги. Для пацієнтів це реальний шанс почати отримувати ефективну та безпечну інсулінотерапію принципово іншого рівня.
Як відомо, дослідження InRange було сплановано з метою довести, що ІGla‑300 не гірший за IDeg‑100 з погляду контролю захворювання (% TIR). Первинну кінцеву точку було досягнуто, оскільки ефективність контролю глікемії на обох інсулінах виявилася абсолютно однаковою. Головна вторинна кінцева точка також підтвердилася – ІGla‑300 мав не меншу ефективність для ГВ (загальний КВ глюкози) протягом доби.
Частота гіпоглікемій виявилася також практично однаковою на тлі лікування ІGla‑300 та IDeg‑100 і значно нижчою порівняно з аналогами I покоління. Було зафіксовано схожі випадки гіпоглікемії (за тяжкістю та протягом доби) без несподіваних результатів щодо безпеки.
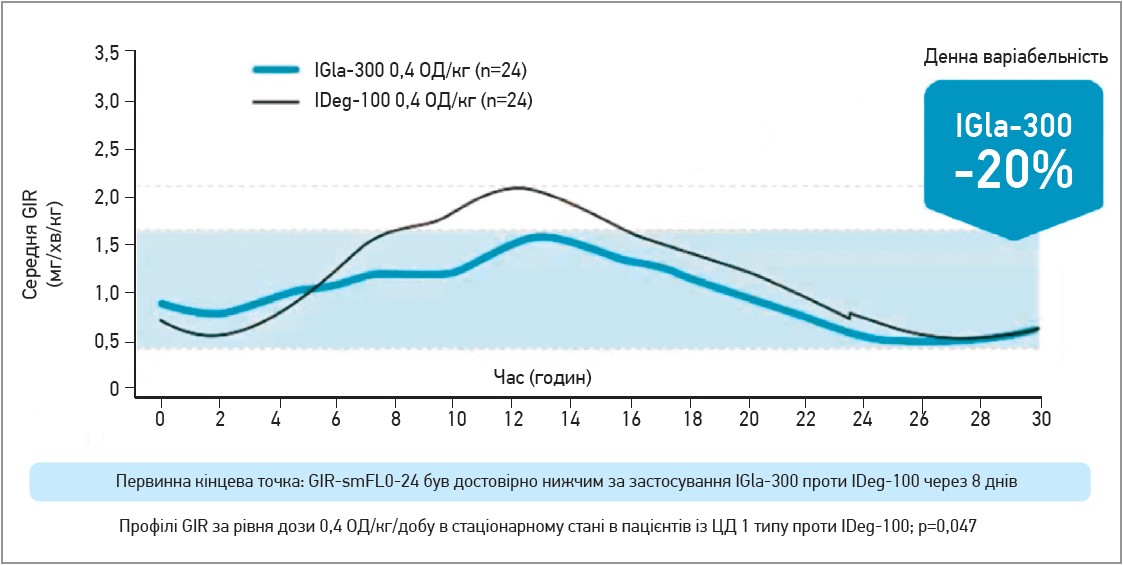
Хоча в дослідженні InRange в обох групах отримано майже однакові результати, дія ІGla‑300 та IDeg‑100 дещо відрізняється. Так, згідно з даними T. S. Bailey та співавт. (2018), ІGla‑300 продемонстрував стабільніший профіль дії та меншу добову ГВ (20%) порівняно з IDeg‑100 (рис. 3).
Рис. 3. Добова варіабельність глікемії
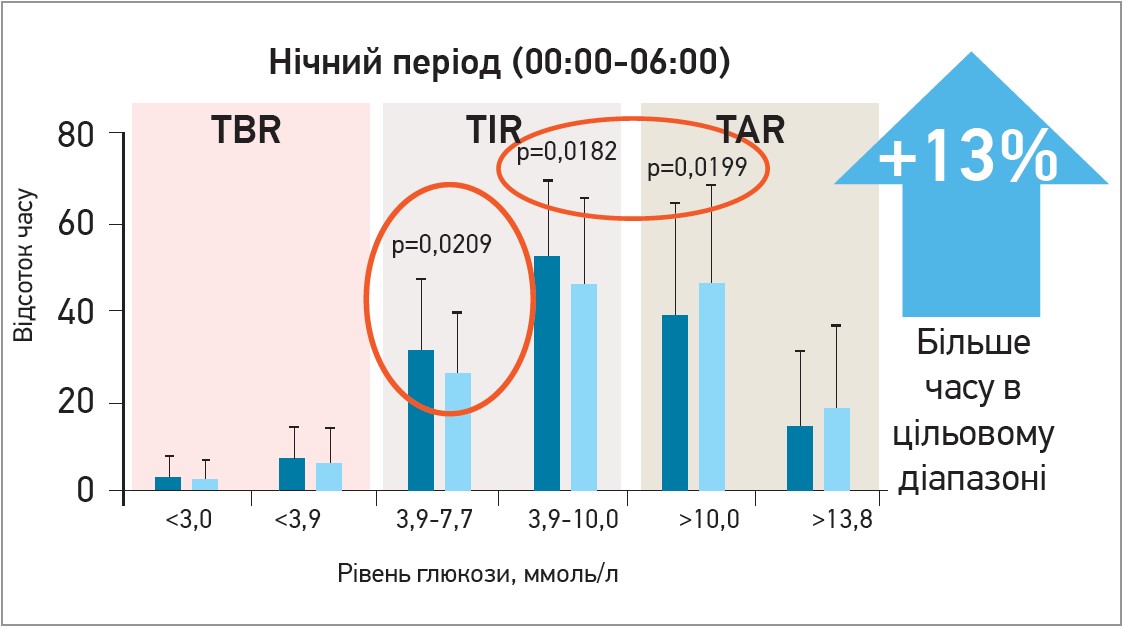
У дослідженні реальної клінічної практики OneCare ІGla‑300 продемонстрував вищий показник TIR і менший TAR (час вище цільового діапазону глікемії) у нічний час доби порівняно з IDeg‑100 у пацієнтів із ЦД 1 типу (рис. 4).
Рис. 4. Відсоток часу в цільовому діапазоні глюкози в нічні години
Примітки: – IGla‑300; – IDeg‑100.
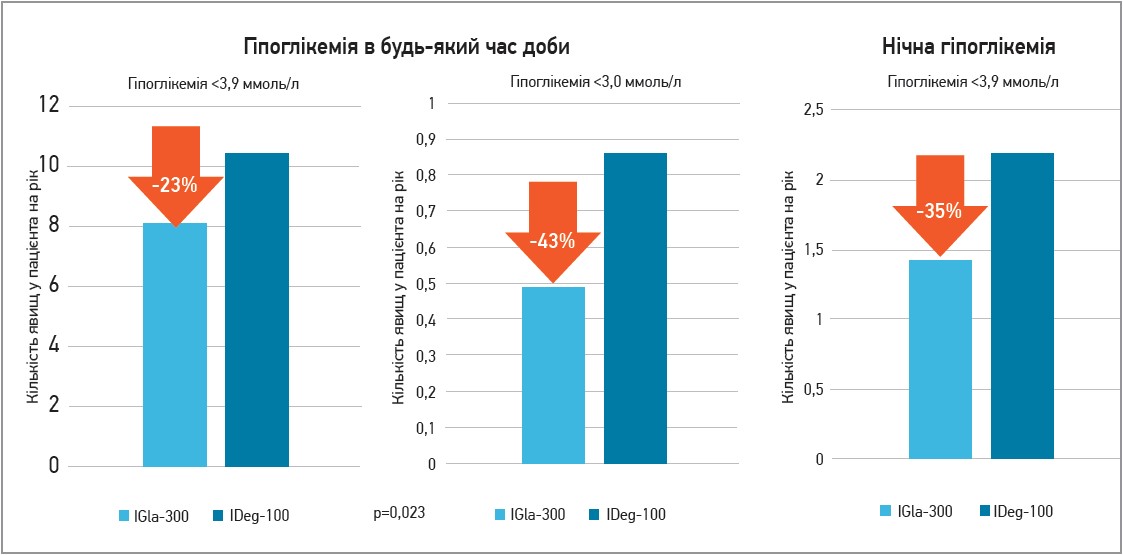
Певні переваги ІGla‑300 продемонстрував у пацієнтів із ЦД 2 типу. В дослідженні BRIGHT хворі із ЦД 2 типу, які отримували ІGla‑300, мали менший ризик гіпоглікемії під час титрації порівняно з IDeg‑100 (особливо тяжких та нічних гіпоглікемій) (рис. 5).
Рис. 5. Частота гіпоглікемій у пацієнтів із ЦД 2 типу в періоді титрації
На тлі терапії ІGla‑300 на 24% більше пацієнтів досягли рівня HbA1c <7% без випадків гіпоглікемії порівняно з IDeg‑100 в періоді титрації.
У літніх хворих (віком ≥70 років) застосування ІGla‑300 дозволило досягти достовірно більшого зниження рівня HbA1c від вихідного рівня через 24 тиж лікування (на 1,69 та 1,34% відповідно) за зіставної частоти гіпоглікемій (≤3,9 ммоль/л) у будь-який час доби.
Схожі результати отримано в підгрупі пацієнтів із ЦД 2 типу, котрі мали хронічну хворобу нирок (швидкість клубочкової фільтрації <60 мл/хв/1,73 м2). У цьому випадку зниження рівня HbA1c через 24 тиж лікування в групах ІGla‑300 та IDeg‑100 склало 1,72 і 1,3% відповідно (зниження на >32%). Частота гіпоглікемій також була зіставною.
Унікальна особливість ІGla‑300 – спрощена схема титрації (+1 ОД/добу). Така схема є ефективною, безпечною та дозволяє збільшити автономність лікування, що особливо важливо для наших пацієнтів в умовах ведення бойових дій.
Член-кореспондент НАМН України, завідувач кафедри діабетології Національного університету охорони здоров’я України ім. П. Л. Шупика (м. Київ), доктор медичних наук, професор Борис Микитович Маньковський розповів про актуальність результатів дослідження InRange для вітчизняної клінічної практики.
У випробуванні InRange досліджувалися наразі найкращі гравці на світовому ринку інсулінів – Тожео СолоСтар (ІGla‑300) та Тресіба (IDeg‑100). Саме тому ці змагання закінчилися нічиєю. Для практикуючих лікарів це чудовий результат, адже в цьому випадку спостерігається не лише розширення лінійки ефективних та безпечних інсулінів, а й підвищення їхньої доступності. У воєнний час питання безпеки інсулінотерапії посідають чільне місце, адже можливість звернутися до лікаря та отримати медичну допомогу наразі обмежена.
Метод постійного моніторування глюкози, який використовували в дослідженні InRange, на сьогодні визнано найінформативнішим. На жаль, його широке впровадження у вітчизняну клінічну практику стримують висока вартість та зумовлені війною економічні труднощі. Втім, деякі пацієнти його успішно використовують.
Від того, з якою ефективністю запроваджуватимуться передові методи моніторингу глікемії та ефективні й безпечні інсулінові аналоги II покоління, залежатимуть якість життя та здоров’я пацієнтів.
Підготував В’ячеслав Килимчук