11 липня, 2023
Цукровий діабет 1 типу в дорослих: Уніфікований клінічний протокол первинної, екстреної та спеціалізованої медичної допомоги
Повна версія статті у форматі PDF
Частина 2: Гострі ускладнення, ведення вагітних із ЦД 1 типу
Продовження. Початок у № 1 (61), 2023 р., с. 15-18
Цукровий діабет (ЦД) 1 типу – захворювання, спричинене автоімунним ураженням β-клітин острівців підшлункової залози з розвитком ендогенного дефіциту інсуліну.
Продовжуємо знайомити з Уніфікованим клінічним протоколом первинної, екстреної та спеціалізованої медичної допомоги «Цукровий діабет 1 типу в дорослих», а саме з методами медичної допомоги при гострих ускладненнях ЦД 1 типу.
Гострі ускладнення ЦД 1 типу
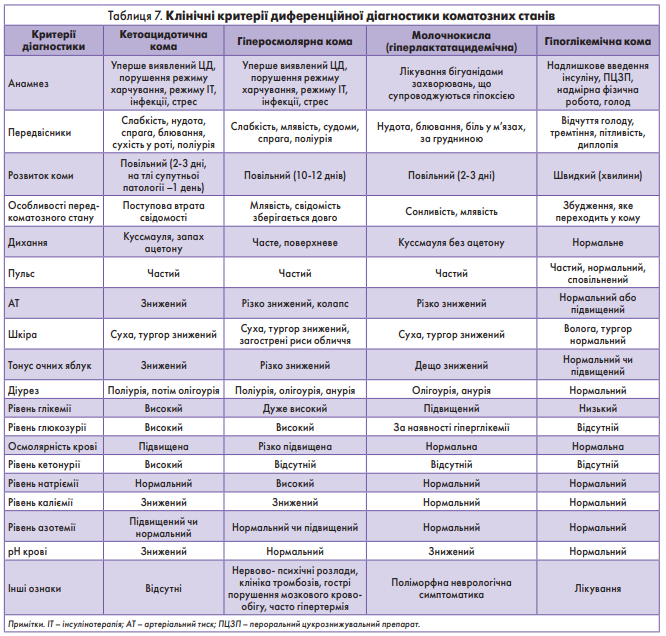
Диференційна діагностика коматозних станів наведена в таблиці 7.
Гіперглікемічна кетоацидотична кома
У разі вперше виявленого ЦД від моменту появи «великих симптомів» до розвитку гіперглікемічної кетоацидотичної коми минає кілька тижнів.
Гострі запальні захворювання прискорюють розвиток тяжкого кетоацидозу, при цьому гіперглікемічна кетоацидотична кома може розвинутися впродовж доби.
Диференційну діагностику проводить із:
- гіпоглікемією;
- перитонітом;
- іншими захворюваннями, що супроводжується порушеннями свідомості (отруєння, черепно-мозкова травма (ЧМТ), нейроінфекції тощо).
Гіперосмолярна некетоацидотична кома
Спостерігають у 3-5% випадків при ЦД.
Провокувальні чинники:
- гарячкові стани;
- надлишкове введення глюкози;
- застосування глюкокортикоїдів, діуретиків;
- стани, що супроводжуються дегідратацією;
- оперативні втручання.
Клінічна картина
Гіперосмолярна некетоацидотична кома розвивається швидше, ніж кетоацидотична (кілька днів). Для гіперосмолярної некетоацидотичної коми характерні:
- ранні неврологічні розлади (гіпертонус м’язів, ністагм, слабопозитивні менінгеальні ознаки), можуть бути судоми;
- гіпертермія;
- виражені ознаки дегідратації;
- синусова тахікардія: артеріальна гіпотензія;
- гіперглікемія ≥40 ммоль/л;
- олігоурія, у тяжких випадках анурія, виражена глюкозурія без кетонурії.
Дихання Куссмауля і запах ацетону у видихуваному повітрі не характерні.
Диференційну діагностику проводять із гіперглікемічною кетоацидотичною комою. Головною відмінністю є відсутність при гіперосмолярній некетоацидотичній комі ознак кетоацидозу на тлі значної дегідратації, високої гіперглікемії. Наявність неврологічної симптоматики може призводити до помилкового діагнозу органічної патології центральної нервової системи.
Гіперлактаатацидемічна кома
Спостерігають в 5-8% випадків при ЦД.
Провокувальні чинники:
- гіпоксія будь-якого генезу (серцева і дихальна недостатність, анемія, шок, кровотеча, надмірне фізичне навантаження, інтоксикація);
- прийом великих доз бігуанідів;
- тяжкі супутні захворювання печінки, нирок, серця, легенів.
Клінічна картина
Кома розвивається гостро, упродовж декількох годин.
Настанню коми передує біль у м’язах, біль за грудниною, нудота, блювання, діарея, тахіпное. З поглибленням ацидозу порушується свідомість, перед розвитком сопору можливе збудження. Шкіра бліда, з мармуровим відтінком, холодна, дегідратація не виражена, розвиваються дихання Куссмауля, артеріальна гіпотензія аж до колапсу, олігоурія, у тяжких випадках анурія. Запаху ацетону у видихуваному повітрі немає. Гіперглікемія до 20-25 ммоль/л, глюкозурія, гіперкетонемії і кетонурії немає, кисла реакція сечі.
Диференційну діагностику проводять з іншими діабетичними комами, а також із захворюваннями, що супроводжуються вираженим метаболічним ацидозом.
Гіпоглікемічні стани
У більшості випадків гіпоглікемічні стани виникають у пацієнтів із ЦД у разі ІТ і недотриманні часу прийому їжі. Рідше причиною гіпоглікемічних станів може бути інсулінома, фізичне навантаження.
Безпосередньою причиною гіпоглікемічних станів у разі ЦД є:
- порушення режиму прийому їжі;
- передозування ПЦЗП.
Сприяють розвитку гіпоглікемічних станів:
- хронічна ниркова недостатність;
- прийом етанолу, саліцилатів, бета-адреноблокаторів.
Клінічна картина
Стадія провісників (спостерігають не в усіх хворих): суб’єктивне відчуття раптової слабкості, відчуття голоду, тривоги, головний біль, пітливість.
Якщо на цьому рівні гіпоглікемічний стан не усунуто прийомом вуглеводів, розвивається психомоторне збудження, потім оглушення, судоми, сопор і кома.
Стадія розгорнутої гіпоглікемії:
- порушення свідомості від оглушення до коми;
- виражена пітливість, тахікардія;
- спочатку підвищення АТ, потім зниження;
- клоніко-тонічні судоми;
- тургор тканин не змінений;
- рівень 2, 3 гіпоглікемії.
Диференційну діагностику проводять із:
- гіперглікемічною/кетоацидотичною комою;
- епілепсією; енцефалітом;
- ЧМТ;
- отруєннями.
Гіпоглікемія
Відносний інсуліновий надлишок і як результат – зниження рівня глікемії, гіпоксія можуть призвести до гострих ускладнень ЦД‑1 (гіпоглікемічного стану).
Провокувальні фактори:
- безпосередньо пов’язані з медикаментозною цукрознижувальною терапією: передозування інсуліну, помилка пацієнта, помилка функції інсулінової шприц-ручки, глюкометра, свідоме передозування;
- помилка лікаря (надзвичайно низький цільовий рівень глікемії, надзвичайно високі дози);
- зміна фармакокінетики інсуліну або пероральних лікарських засобів (ЛЗ): зміна ЛЗ, ниркова і печінкова недостатність, високий титр антитіл до інсуліну, неправильна техніка ін’єкцій;
- підвищення чутливості до інсуліну: тривале фізичне навантаження (у тому числі статеві стосунки), ранній післяпологовий період, надниркова або гіпофізарна недостатність, медикаменти;харчування: пропуск прийому їжі або недостатня кількість, алкоголь, обмеження харчування для зниження маси тіла (без відповідного зменшення дози цукрознижувальних ЛЗ);
- уповільнення спорожнення шлунка (при автономній невропатії), блювання, синдром мальабсорбції;
- вагітність (перший триместр) та грудне вигодовування;
- погодні умови (спека);
- гарячий душ;
- психо-емоційні навантаження.
Необхідно надати пацієнтам та членам їхніх родин інформацію щодо профілактики гіпоглікемій перед фізичними навантаженнями: додатковий моніторинг рівня глюкози крові і вживання вуглеводів за необхідності. Рекомендувати пацієнтам носити спеціальні браслети, книжечки тощо з інформацією про наявність в особи ЦД‑1.
Діабетичний кетоацидоз (ДКА)
Моніторинг лабораторних показників у разі ДКА (табл. 8):
1. Лабораторні аналізи:
- експрес-аналіз глікемії – щогодини до зниження рівня глюкози плазми до 13 ммоль/л, потім 1 раз на 3 год;
- аналіз сечі на кетонові тіла – двічі на добу в перші 2 доби, потім 1 раз на добу;
- загальний аналіз крові й сечі: початково, потім 1 раз на 2 доби;
- Na+, К+ сироватки: кожні 2 год до зменшення основних симптомів, потім кожні 4-6 год;
- розрахунок ефективної осмолярності плазми (норма 285-295 мосмоль/л)
Осмолярність плазми = (Na+ ммоль/л + K+ ммоль/л) + глюкоза (ммоль/л);
- біохімічний аналіз сироватки крові: сечовина, креатинін, хлориди, натрію гідрокарбонат, бажано лактат – початково, потім 1 раз на 3 доби, за необхідності – частіше;
- газоаналіз та рН (можна венозної крові): 1-2 рази на добу до нормалізації кислотно-лужного стану (КЛС).
2. Інструментальні дослідження:
- погодинний контроль діурезу; контроль центрального венозного тиску (ЦВТ), АТ, пульсу і температури тіла кожні 2 год;
- ЕКГ не рідше 1 разу на добу або ЕКГ-моніторинг, пульсоксиметрія;
- пошук можливого джерела інфекції.
Інсулінотерапія в разі ДКА
Рекомендований режим малих доз (краще ведення глікемії і менший ризик гіпоглікемії та гіпокаліємії, ніж режим великих доз).
Метод малих доз інсуліну короткої дії (ІКД) внутрішньовенно струминно, а потім внутрішньовенно краплинно, ураховуючи рівень глюкози крові:
- за глікемії ≥17-39-0,1 Од/кг/год;
- за глікемії від 11 до 17-0,05 Од/кг/год;
- за глікемії <11 – переходять на 4-6 Од підшкірно кожні 3-4 год з додаванням ЛЗ 5% розчину глюкози.
Приготування розчину інсуліну: 50 Од ІКД + 2 мл 20% розчину альбуміну (для уникнення адсорбції молекул інсуліну) на кожні 100 мл довести до 500 мл 0,9% натрію хлориду (концентрація інсуліну 1 Од в 10 мл розчину).
Проведення заходів, спрямованих на відновлення та підтримання функцій внутрішніх органів (серця, нирок, легенів та ін.) згідно з відповідними медико-технологічними документами.
Швидкість зниження глікемії – не більш ніж 4 ммоль/л/год (небезпека зворотного осмотичного градієнту між внутрішньо- та позаклітинним простором і набряку мозку); у першу добу не знижувати рівень глюкози плазми <13-15 ммоль/л.
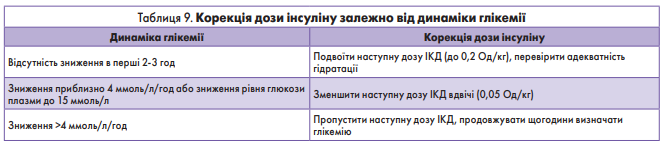
Корекція дози інсуліну в залежності від динаміки глікемії описана в таблиці 9.
Регідратація в разі ДКА
- Зменшити швидкість інфузії інсуліну до 0,05 Од/кг/год, коли рівень глюкози падає до <14 ммоль/л.
- Для поповнення рідини краще застосовувати розчини електролітів, а не колоїдні розчини.
- 0,9% розчин натрію хлориду («фізіологічний розчин») є препаратом вибору для компенсації втрати рідини.
- Обережне внутрішньовенне поповнення рідини в молодих дорослих людей.
- Введення натрію гідрокарбонату не рекомендується рутинно.
- Фосфати не треба призначати рутинно.
- Швидкість зниження рівня глюкози має бути не менше 3,0 ммоль/л/год.
Розчини:
- 0,9% натрію хлориду (рівень скорегованого Na+ плазми <145 ммоль/л; якщо рівень Na+ вищий – див. «Гіперосмолярний гіперглікемічний синдром»);
- якщо рівень глюкози плазми ≤13 ммоль/л: 5% або 10% глюкози (+ 3-4 Од ІКД на кожні 20 г глюкози);
- колоїдні плазмозамінники (за гіповолемії – систоличний АТ <80 мм рт. ст. або ЦВТ <4 мм водн. ст.);
- переваги комбінованих розчинів електролітів (Рінгера, Рінгера-Локка та ін.) над розчином 0,9% натрію хлориду при ДКА не доведені.
Швидкість регідратації: 1 л у першу годину (з урахуванням рідини, що її було введено на догоспітальному етапі), по 0,5 л – упродовж 2-ї та 3-ї год, по 0,25 л упродовж наступних годин. Загальний об’єм інфузії впродовж перших 12 год терапії – не більше 10% маси тіла. Якщо регідратація в разі ДКА починається з 0,9% розчину натрію хлориду (поодинокі випадки справжньої гіпернатріємії), швидкість інфузії зменшують до 4-14 мл/кг/год. Швидкість регідратації корегують залежно від ЦВТ: якщо ЦВТ <4 мм вод. ст. – 1 л/год, якщо ЦВТ 5-12 мм вод. ст. – 0,5 л/год, ЦВТ>12-250-300 мл/год або за правилом: об’єм рідини, що вводиться впродовж години, не має перевищувати годинний діурез більш як на 0,5-1 л.
Відновлення електролітних порушень
За відомої концентрації К+ і відсутності порушення функції нирок внутрішньовенну інфузію розчину, що містить калій, починають одночасно з введенням інсуліну (табл. 10).
Якщо рівень К+ невідомий, внутрішньовенну інфузію калію починають не раніше ніж за годину після початку ІТ, під контролем ЕКГ і діурезу.
Корекція метаболічного ацидозу
Етіологічне лікування метаболічного ацидозу в разі ДКА – інсулін.
Адекватна терапія рідиною та інсуліном усуне ацидоз у разі ДКА, та зазвичай застосування натрію гідрокарбонату не показано. Ацидоз може бути реакцією адаптації, оскільки покращує доставку кисню до тканин, спричинюючи правий зсув дисоціації кисню крові. Надлишок натрію гідрокарбонату може призвести до підвищення парціального тиску CO2 у спинномозковій рідині (СМР) і парадоксального посилення ацидозу в СМР. Крім того, використання натрію гідрокарбонату у разі ДKA може затримати падіння співвідношення лактат: піруват і кетонів у крові, порівняно з внутрішньовенною інфузією 0,9% розчину натрію хлориду. В інтенсивній терапії можливе введення натрію гідрокарбонату внутрішньовенно, якщо рН залишається низьким і потрібні препарати інотропної дії.
Критерії розрішення ДКА: рівень глюкози плазми <11 ммоль/л і як мінімум два з трьох показників КЛС: натрію гідрокарбонат ≥18 ммоль/л, венозний рН ≥7,3, аніонна різниця ≤12 ммоль/л. Незначна кетонурія може деякий час зберігатись.
Найчастіша супутня терапія
У зв’язку з високо ймовірною причиною ДКА є інфекції, застосовують антибіотики широкого спектра дії з подальшим мікробіологічним дослідженням (визначенням чутливості).
Харчування
Після повного відновлення свідомості, здатності ковтати, за відсутності нудоти та блювання – харчування невеликими порціями з достатньою кількістю вуглеводів і помірною кількістю білка (каші, картопляне пюре, хліб, бульйон, омлет, розведені соки без додавання цукру), з додатковим підшкірним введенням ІКД по 1-2 Од на 1 ХО. Через 1-2 доби від початку прийому їжі, за відсутності патології шлунково-кишкового тракту (ШКТ), – перехід на звичайне харчування.
Гіперосмолярний гіперглікемічний синдром
Регідратація як при ДКА, з такими особливостями:
- у 1-шу год – 1 л розчину 0,9% натрію хлориду, потім – залежно від рівня Na+;
- при скоригованому рівні Na+ >165 ммоль/л сольові розчини протипоказані.
Регідратацію починають із 2,5% або 5% розчину глюкози; при скоригованому рівні Na+ <165 ммоль/л регідратацію проводять 0,9% розчином натрію хлориду; у разі гіповолемічного шоку (АТ <80/50 мм рт. ст.) спочатку внутрішньовенно дуже швидко вводять 1 л розчину 0,9% натрію хлориду або колоїдні розчини.
Швидкість регідратації: 1-ша год – 1-1,5 л рідини, 2-га і 3-тя год – по 0,5-1 л, потім по 0,25-0,5 л (під контролем ЦВТ; об’єм рідини, що вводиться впродовж години, не має перевищувати годинний діурез більш як на 0,5-1 л).
Особливості ІТ
З урахуванням високої чутливості до інсуліну в разі гіперосмолярногогіперглікемічного синдрому на початку інфузійної терапії інсулін не вводять або вводять у дуже малих дозах – 0,5-2 Од/год, максимум 4 Од/год внутрішньовенно.
Якщо за 4-5 год від початку інфузії після часткової регідратації та зниження рівня Na+ зберігається виражена гіперглікемія, переходять на режим дозування інсуліну, рекомендований для лікування ДКА.
Якщо одночасно з початком регідратації 0,9% розчином натрію хлориду помилково вводять вищі дози ІКД (≥6-8 Од/год), можливе швидке зниження осмолярності з розвитком набряку легень і мозку.
Рівень глюкози плазми не можна знижувати швидше ніж на 4 ммоль/л/год, а осмолярність сироватки – не більш як на 3 ммоль/л/год.
Відновлення дефіциту калію. Проводять за тими самими принципами, що й у разі ДКА. Звичайно, дефіцит калію більш виражений, ніж при ДКА.
Найчастіша супутня терапія. Як при ДКА, плюс часто – прямі антикоагулянти (нефракційований або низькомолекулярний гепарин) через високу ймовірність тромбозів і тромбоемболій.
Хронічні ускладнення ЦД‑1
Діабетична периферична нейропатія
Пацієнти з ЦД 1 типу протягом ≥5 років мають щороку обстежуватися на діабетичну периферичну нейропатію (ДПН), використовуючи анамнез і прості клінічні тести.
У більшості пацієнтів із діабетичною дистальною симетричною полінейропатією (ДСПН) відбувається одночасне ураження тонких і товстих нервових волокон, тому важливо проводити аналіз (за місцем лікування) обох аспектів захворювання з використанням відповідних тестів. Симптоми варіюють залежно від класу сенсорних волокон. Найпоширеніші ранні симптоми зумовлені залученням дрібних волокон і проявляються біллю та дизестезією (неприємні відчуття печіння й поколювання). Залучення великих волокон може спричинити оніміння та втрату захисної чутливості (LOPS). LOPS вказує на наявність ДСПН та є фактором ризику діабетичної виразки стопи.
Для оцінки функції великих волокон і захисної чутливості можуть бути використані таки дослідження:
- Функція малих волокон: больова і температурна чутливість.
- Функція великих волокон: сприйняття вібрації і тест із монофіламентом, що згинається під дією сили в 10 г.
- Захисна чутливість: тест із монофіламент, що згинається під дією сили в 10 г.
Cиметричне порушення вібраційної чутливості, виявлене за допомогою камертона (товсті волокна) і (або) тесту шпилькового уколу (тонкі волокна), може розглядатися як мінімальний критерій діагностики ДСПН в умовах клінічної практики.
Для оцінки ознак і симптомів нейропатії можна використовувати валідовані шкали.
Під час диференційної діагностики ДСПН необхідно враховувати і аналізувати дані анамнезу і (або) лабораторні показники, щоб виключити інші причини виникнення полінейропатії.
Автономна нейропатія
За наявності в пацієнта тахікардії, лабільного АТ, ортостатичної гіпотензії провести додаткове обстеження на предмет діабетичної кардіоваскулярної автономної нейропатії.
Кардіоваскулярна автономна нейропатія маніфестує тахікардією у спокої (>100 уд./хв) і ортостатичною гіпотензією (падінням систолічного або діастолічного АТ на >20 мм рт. ст. або >10 мм рт. ст. відповідно під час зміни положення без належного збільшення частоти серцевих скорочень). Лікування, як правило, спрямоване на полегшення симптомів.
Гастропарез треба запідозрити в осіб із нестабільним глікемічним контролем або симптомами з боку верхніх відділів ШКТ без іншої встановленої причини. Виключення органічних причин обструкції вихідного відділу шлунка або виразкової хвороби (езофагогастродуоденоскопія або дослідження шлунка за допомогою барію) необхідне перед розглядом питання про діагностику гастропарезу або проведення спеціалізованого дослідження.
Золотим стандартом діагностики гастропарезу є вимірювання спорожнення шлунка зі сцинтиграфією засвоюваних твердих речовин із 15-хвилинними інтервалами протягом 4 год після прийому їжі. Використання дихального тесту з 13C-октановою кислотою є альтернативою.
Розглянути діагноз гастропарезу в пацієнтів із нестабільним контролем рівня глюкози в крові і здуттям живота без причини або з блюванням, беручи до уваги можливі альтернативні діагнози.
Розглянути доцільність прийому метоклопраміду, домперидону в пацієнтів із гастропарезом.
За підозри щодо гастропарезу розглянути направлення до спеціаліста, якщо диференційний діагноз викликає сумнів або наявне стійке або тяжке блювання.
Розглянути можливість автономної нейропатії, що впливає на кишечник пацієнта з нез’ясованою діареєю, особливо по ночах.
У разі використання ЛЗ із групи трициклічних антидепресантів і гіпотензивних ЛЗ у пацієнтів з автономною нейропатією спостерігати за підвищеною вірогідністю розвитку небажаних явищ, таких як ортостатична гіпотензія.
Обстежити пацієнта з нез’ясованою проблемою випорожнення сечового міхура щодо автономної нейропатії сечового міхура. Діабетична автономна нейропатія також може спричинити розлади сечостатевої системи, у тому числі сексуальну дисфункцію і дисфункцію сечового міхура. У чоловіків діабетична автономна нейропатія може спричинити еректильну дисфункцію і/або ретроградну еякуляцію. Жіноча статева дисфункція частіше виникає у хворих на ЦД і проявляється у вигляді зниження сексуального бажання, болю під час статевого акту, зниження сексуального збудження та недостатньої змазки. Симптоми з боку нижніх сечовивідних шляхів проявляються у вигляді нетримання сечі й дисфункції сечового міхура (ніктурія, часте сечовипускання, позиви до сечовипускання та слабкий струмінь сечі). Оцінку функції сечового міхура потрібно проводити в пацієнтів із ЦД, які мають рецидивні інфекції сечовивідних шляхів, пієлонефрит, нетримання або сечовий міхур, що пальпується.
У разі еректильної дисфункції запропонувати ЛЗ групи інгібіторів фосфодіестерази 5 типу за відсутності протипоказань і прослідкувати за досягненням цільових рівнів глікемічного контролю. Скерувати пацієнта на консультацію до уролога за необхідності – до інших фахівців із медичного, хірургічного, психологічного лікування еректильної дисфункції.
Діабетична ретинопатія
Діабетична ретинопатія (ДР) є надзвичайно специфічним ускладненням з боку судин при ЦД і 1, і 2 типу, причому його поширеність суттєво пов’язана як із тривалістю ЦД, так і з рівнем контролю глікемії.
Обов’язкові офтальмологічні методи діагностики ДР:
- Визначення гостроти зору (візометрія) і полів зору (периметрія).
- Вимірювання внутрішньоочного тиску (тонометрія).
- Біомікроскопія кришталика і склистого тіла за допомогою щілинної лампи.
- Офтальмоскопія з розширенням зіниці.
- УЗД у разі виявлення значних помутніть у склистому тілі і кришталику.
Бажані офтальмологічні методи діагностики ДР:
- Фотографування судин очного дна за допомогою цифрової фундускамери.
- Флюоресцентна ангіографія судин сітківки.
- Електрофізіологічні методи дослідження для визначення функціонального стану зорового нерва й сітківки.
- Гоніоскопія (огляд кута передньої камери ока).
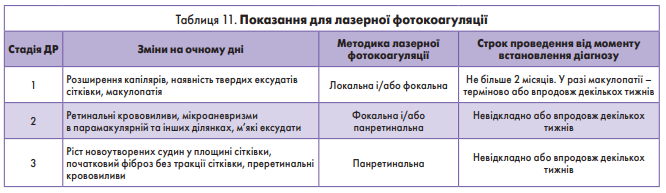
Показання для офтальмологічного втручання – лазерної фотокоагуляції – наведені в таблиці 11.
Лікування діабетичного набряку сітківки (ДНС):
Інтравітреальні ін’єкції антиваскулярного ендотеліального фактора росту (anti-VEGF) показані як лікування першої лінії для більшості пацієнтів із діабетичним макулярним набряком, який зачіпає фовеальний центр і погіршує гостроту зору.
Макулярна фокальна/сіткова фотокоагуляція та інтравітреальні ін’єкції кортикостероїдів є адекватними методами лікування очей зі стійким діабетичним макулярним набряком, незважаючи на попередню терапію антиваскулярним ендотеліальним фактором росту, або в пацієнтів, які не є кандидатами для цього підходу як першої лінії.
Хронічна (діабетична) хвороба нирок
Виявлення хронічної (діабетичної) хвороби нирок
Усі пацієнти з ЦД‑1 з/без виявленої ХХН мають 1 раз на рік здавати першу ранкову сечу для аналізу. Її відправляють для оцінки співвідношення альбуміну і креатиніну. Оцінка концентрації в сечі лише альбуміну є не повною мірою інформативною. Одночасно потрібно визначати рівень креатиніну сироватки (табл. 12).
Якщо отримано підвищені показники (за відсутності протеїнурії / інфекції сечовивідних шляхів), тест повторюють при кожному відвідуванні клініки або принаймні кожні 3-4 міс. Результат вважається підтвердженим, якщо наступний результат (з понад двох) також аномальний (>2,5 мг/ммоль у чоловіків, >3,5 мг/ммоль у жінок).
Інші захворювання нирок потрібно запідозрити за відсутності прогресивної ретинопатії, якщо АТ є особливо високим, якщо протеїнурія розвивається раптово, при значній гематурії, при систематичному поганому самопочутті.
Важливість виявлення підвищеного рівня екскреції альбуміну треба обговорити з пацієнтом.
Залежність ризику прогресування ХНН, частоти візитів і направлень до нефролога від ШКФ і альбумінурії. У сітці ШКФ та альбумінурії кольором показано ризик прогресування, захворюваності та смертності – від найкращого до гіршого (зелений, жовтий, оранжевий, червоний, темно-червоний). Цифри в клітинках орієнтують щодо частоти відвідувань (кількість разів на рік). Зелений колір може відображати ХХН із нормальними ШКФ і співвідношення альбуміну та креатиніну лише за наявності інших маркерів ураження нирок, таких як візуалізація полікістозу нирок або аномалії біопсії нирки з подальшими вимірюваннями щороку; жовтий – потребує обережності та обстень хоча б 1 раз на рік; помаранчевий – потребує вимірювань двічі на рік; червоний – тричі на рік; а темно-червоний – чотири рази на рік.
Ускладнення ХНН наведені в таблиці 13.
Це лише загальні параметри, які базуються на експертній думці та основних супутніх захворюваннях і стані захворювання, також для визначення імовірності впливу необхідно враховувати зміни в лікуванні кожного окремого «Направити» означає, що рекомендовано нефрологічні послуги.
Ведення хронічної (діабетичної) хвороби нирок
Для зменшення прогресування діабетичної нефропатії та ХХН необхідно оптимізувати глікемічний контроль, показники АТ та його варіабельності.
Не треба припиняти блокаду ренін-ангіотензинової системи в разі незначного підвищення рівня креатиніну сироватки (<30%).
У пацієнтів із незалежною від діалізу ХХН ІІІ або вище стадії споживання білка з їжею має становити максимум 0,8 г/кг маси тіла на добу (рекомендована добова норма). У пацієнтів, які перебувають на діалізі, потрібно розглянути вищі рівні споживання білка з їжею, оскільки недостатнє харчування є основною проблемою для деяких пацієнтів на діалізі.
Пацієнтам із ЦД і гіпертензією із помірно підвищеним співвідношенням альбуміну та креатиніну в сечі (30-299 мг/г креатиніну) або із співвідношенням альбуміну та креатиніну >300 мг/г і/або розрахунковою ШКФ <60 мл/хв/1,73 м2 рекомендують або інгібітор АПФ, або блокатор рецепторів ангіотензину.
Показаннями направлення до нефролога є розрахункова ШКФ <30, невизначеність щодо етіології захворювання нирки, труднощі керування захворюванням, швидке прогресування захворювання нирки.
Діабетична стопа
Виявлення проблем, пов’язаних із діабетичною стопою
Структуроване спостереження за стопами проводять з інтервалом в 1 рік. Перевірка й огляд стоп має визначити:
- стан шкіри;
- форму і деформацію стоп;
- взуття;
- порушення больової і тактильної чутливості;
- судинне кровопостачання (у тому числі периферичних імпульсів).
Для виявлення погіршення сенсорної функції нерва, достатнього для суттєвого підвищення ризику виникненню виразок на ногах, використовують хірургічну мононитку із силою впливу в 10 г, а такожнетравматичний шпильковий укол.
На основі висновків спостереження за стопами ризик виникнення виразок на ногах необхідно розділити на:
- низький (нормальна чутливість і пульсація);
- підвищений (порушення чутливості, або відсутність пульсації, або інший фактор ризику);
- високий (порушення сенсорної функції нерва і відсутність пульсації, деформація, або шкірні зміни, або попередня виразка).
У пацієнтів із підвищеним або високим ризиком ускладнення з боку стоп:
- оцінити інші фактори, які сприяють ризику, у тому числі деформацію, куріння і контроль рівня глюкози в крові; організувати/посилити спеціальні навчальні заходи з догляду за стопами і додатковий огляд;
- розглянути питання щодо спеціального взуття, у тому числі устілок та ортез, якщо є деформація, мозолі або попередні виразки.
Заходи щодо пацієнтів із виразками стоп:
- Скерувати до фахівців із лікування діабетичної стопи впродовж 1-2 днів, якщо немає явної інфекції виразки або навколишньої тканини, або негайно, якщо є така інфекція.
- Застосовувати антибіотики, якщо є будь-яке свідчення про інфікування виразки або навколишніх тканин, і продовжувати їх прийом у довгостроковій перспективі, якщо інфекція повторюється.
- Використовувати пов’язки на стопу, забезпечуючи контроль і зміну пов’язки, за необхідності.
- Видалити мертву тканину з діабетичної виразки стопи.
- Розглянути питання щодо використання методів розвантажування (наприклад, контактний підбір) у пацієнтів із невропатичними виразками стопи. Не використовувати для рутинного лікування виразок стопи культивовану людську дерму (або еквівалент), гіпербаричну кисневу терапію або фактори росту.
- Розглянути можливість забезпечення ефективних навчальних заходів із питань виразок стопи за допомогою графічної візуалізації наслідків погано лікованих виразок стопи в пацієнтів із рецидивними виразками або попередньою ампутацією.
- Постійно здійснювати спостереження за загоєнням виразки (від разу на день до разу на місяць) відповідно до потреб.
- У разі виявлення захворювання периферичних судин звернутися для ранньої оцінки до спеціалізованої команди судинних хірургів. Пацієнтів із підозрюваною або діагностованою остеоартропатією Шарко потрібно негайно направити до мультидисциплінарної команди з лікування діабетичної стопи.
Контроль судинного ризику. Виявлення судинних ризиків
Фактори судинного ризику необхідно оцінювати щороку, і оцінка має охоплювати рівні екскреції альбуміну, куріння, контроль рівня глюкози в крові, АТ, повний ліпідний профіль (зокрема, ЛПВЩ, холестерин ЛПНЩ і тригліцериди; табл. 14), вік, сімейний анамнез уражень судин, абдомінальне ожиріння.
Таблиці судинного ризику, рівняння або пристрої для розрахунку судинного ризику не можна використовувати, оскільки вони недооцінюють ризик у пацієнтів із ЦД‑1.
Пацієнтів із підвищеною швидкістю екскреції альбуміну або з двома чи більше ознаками метаболічного синдрому потрібно лікувати як категорію найвищого ризику (як ніби в них ЦД 1 типу або відоме серцево-судинне захворювання).
Пацієнти, які не належать до групи найвищого ризику, але мають спадкову схильність до хвороб серцево-судинної системи, порушення ліпідного обміну та підвищення АТ (вік >35 років), мають перебувати під наглядом лікарів як група помірного – високого ризику.
У пацієнтів без додаткових факторів ризику артеріальної гіпертензії регулювання рівня ліпідів та АТ має проводитися як у загальної популяції, згідно з відповідними галузевими стандартами у сфері охорони здоров’я.
Ураження судин
Пацієнтам із ЦД‑1, які курять, під час планового огляду потрібно рекомендувати відмову від куріння згідно з відповідними галузевими стандартами медичної допомоги.
Молодим пацієнтам, які не курять, треба рекомендувати ухилятися від цієї шкідливої звички.
Ацетилсаліцилову кислоту (75 мг/добу) призначають пацієнтам із ризиком від високого до найвищого.
Стандартну дозу статинів призначаюь пацієнтам із ризиком від помірного до високого.
Терапію не можна припиняти, якщо рівень аланінамінотрансферази підвищується щонайменше втричі від верхньої межі референтного рівня.
Фібрати треба рекомендувати пацієнтам із гіпертригліцеридемією згідно з місцевими настановами з гіполіпідемії і статусом ризику серцево-судинного захворювання.
Відповідь на терапію статинами потрібно контролювати оцінкою ліпідного профілю. Якщо відповідь незадовільна, необхідно розглянути такі причини, як невідповідність, неадекватний вибір препарату і необхідність комбінованої терапії.
Пацієнти, в яких був інфаркт міокарда чи інсульт, мають отримувати інтенсивну терапію згідно з відповідними галузевими стандартами медичної допомоги. За наявності стенокардії або іншої форми ішемічної хвороби серця мають бути розглянуті бета-адренергічні блокатори.
Ведення вагітних із ЦД 1 типу
Догляд до зачаття
Усі жінки репродуктивного віку з ЦД‑1 мають отримувати консультації щодо питань контролю за народжуваністю, важливості глікемічного контролю до вагітності, впливу індексу маси тіла (ІМТ) на результати вагітності, необхідності прийому фолієвої кислоти, а також припинення прийому потенційно ембріопатичних ліків до вагітності, у тому числі будь-яких із таких класів: інгібітори АПФ і блокатори рецепторів ангіотензину II (БРА) – до зачаття або в разі виявленні вагітності; статинів.
Перед спробою завагітніти жінки з ЦД‑1 потребують:
- Консультації щодо зачаття, що охолюєн оптимальний контроль ЦД і харчування, переважно в консультації з міждисциплінарною командою з вагітності, щоб оптимізувати материнські і неонатальні результати. Прагнути досягти до зачаття рівня НbA1c 7,0% (або якомога ближче до нормального без додаткових ризиків), щоб зменшити ризик спонтанного аборту, вроджених аномалій, прееклампсії, прогресування ретинопатії під час вагітності.
- Доповнення до раціону мультивітамінів, що містять 5 мг фолієвої кислоти не менше 3 міс до зачаття і аж до принаймні 12 тиж після зачаття. Необхідно продовжувати додавати полівітаміни, що містять 0,4-1,0 мг фолієвої кислоти від 12 тиж після зачаття до 6 тиж після пологів або доти, доки триває грудне вигодовування.
- Припинення прийому потенційно ембріопатичних препаратів, у тому числі будь-яких із таких класів: інгібітори АПФ та БРА – до зачаття або в разі виявлення вагітності; статинів.
Оцінка та ведення ускладнень
Необхідне офтальмологічне обстеження та оцінка офтальмолога. Скринінг на наявність ХХН. За наявності мікроальбумінурії або явної нефропатії – підвищений ризик розвитку гіпертонії і прееклампсії – організувати додаткове спостереження щодо зазначених станів.
Ведення під час вагітності
Вагітним із ЦД‑1:
- Призначити індивідуальну схему інсуліну та цільові глікемічні рівні, зазвичай використовуючи інтенсивну ІТ.
- Прагнути до цільових значень глюкози (рівень глюкози в плазмі натще <5,3 ммоль/л, 1 год після прийому їжі <6,7 ммоль/л).
- Переглянути в бік збільшення цільові рівні, за необхідності, через підвищений ризик розвитку тяжкої гіпоглікемії під час вагітності.
- Навчити самоконтролю рівня глюкози в крові як до, так і після прийому їжі, для досягнення цілей глікемії і поліпшення результатів вагітності.
- У разі прегестаційного ЦД‑1 можна застосовувати інсулін аспарт або лізпро під час вагітності замість звичайного інсуліну для поліпшення глікемічного контролю і зменшення рівня глюкози.
- Детемір або гларгін можна застосовувати як альтернативу НПХ.
Ведення рівня ГК під час пологів
Під час пологів необхідне уважне спостереження за жінками з цільовим рівнем глюкози крові від 4,0 до 7,0 ммоль/л, з тим щоб звести до мінімуму ризик неонатальної гіпоглікемії. Призначити адекватну кількість глюкози під час пологів для забезпечення достатнього рівня енергії.
Післяпологовий період
У післяпологовий період потрібно:
- Проводити ретельний контроль, з огляду на ризик розвитку гіпоглікемії.
- Обстежити на післяпологовий тиреоїдит за допомогою тесту на ТТГ на 6-8-му тиж після пологів.
- Заохочувати жінку до грудного вигодовування, оскільки це може зменшити ризик ожиріння в дитини, особливо в разі ожиріння в матері.
Уніфікований клінічний протокол первинної, екстреної та спеціалізованої медичної допомоги «Цукровий діабет 1 типу в дорослих» затверджено Наказом МОЗ № 151 від 26.01.2023 р.
Друкується у скороченні.
Текст адаптовано та уніфіковано відповідно до стандартів тематичного випуску медичної газети «Здоров’я України».
Повний текст Уніфікованого протоколу дивитися за посиланням: https://www.dec.gov.ua/wp-content/uploads/2023/01/43348-dn_151_26012023_dod.pdf
Тематичний номер «Діабетологія. Тиреоїдологія. Метаболічні розлади» № 2 (62) 2023 р.