15 листопада, 2021
Вивчення стабільності таблетованих препаратів левотироксину натрію
Стабільність лікарського засобу – це здатність зберігати у визначених межах протягом усього терміну зберігання і використання (тобто впродовж терміну придатності) такі самі властивості та характеристики, які він мав на момент виготовлення. Здебільшого передчасна втрата стабільності препарату відбувається за умови його неправильного зберігання. Втім, не є рідкістю ситуації, коли препарат втрачає свої властивості раніше зазначеного терміну придатності з причин, пов’язаних, найімовірніше, з порушенням технології виробництва. Звичайно, вимоги щодо стабільності стосуються всіх без винятку лікарських засобів, однак для препаратів із вузьким терапевтичним вікном вони мають критичне значення. Яскравий приклад таких лікарських засобів – препарати левотироксину, що потребують дуже ретельного підбору дози. Метою нижченаведеного дослідження була оцінка стабільності препаратів левотироксину натрію різних виробників, що реалізуються в Судані.
Стабільність лікарського засобу
Згідно з визначенням Фармакопеї США (USP), стабільність лікарського засобу – це збереження його терапевтичних властивостей та характеристик, яких він набуває одразу після виготовлення, протягом усього періоду його зберігання і використання. Стабільність препарату пов’язана з його стійкістю до різних хімічних, фізичних і мікробіологічних агентів, які можуть змінити його вихідні властивості під час транспортування, зберігання, використання. Однією з найважливіших кількісних характеристик стабільності препарату є термін придатності.
Термін придатності лікарських засобів, що зберігаються в закритій тарі за певних умов, зазвичай визначається з дати виробництва чи приготування до зменшення його початкової активності або вмісту активної речовини на 10% (t10%). Хоча часто зручно виражати термін придатності винятково з погляду хімічної стабільності активної складової, досить важливо, щоб зберігалися й інші бажані властивості продукту.
Фактори, що впливають на стабільність препарату
Кожен інгредієнт, що входить до складу лікарського засобу (терапевтично активний або фармацевтично необхідний), може впливати на стабільність лікарської речовини та лікарських форм. До основних факторів навколишнього середовища, що впливають на стабільність лікарських засобів, належить вплив несприятливої температури, світла, вологості, кисню та вуглекислого газу. Реакції, що зумовлюють втрату стабільності препарату, зазвичай не супроводжуються змінами кольору й органолептичних властивостей лікарських форм.
Стабільність левотироксину натрію
Левотироксин є стабільним на сухому повітрі, але втрачає активність у присутності світла, тепла та підвищеної вологості. Однак описано випадки прискореної втрати активності таблетованого левотироксину натрію певних виробників навіть при кімнатній температурі. Управління з контролю за якістю продуктів харчування та лікарських засобів США (FDA) визнає проблему стабільності пероральних форм левотироксину натрію з огляду на потенційну небезпеку шкоди для здоров’я, водночас акцентуючи, що таблетки тироксину слід зберігати в оригінальній упаковці в сухому прохолодному місці. Не варто продовжувати їхнє застосування після завершення терміну придатності.
Наприклад, термін придатності тироксину австралійського виробництва, що містить 200 таблеток у флаконі, становить 1 рік з дати виробництва, тому не виключена ситуація, що термін придатності лікарського засобу може завершитися ще до того, як закінчаться таблетки в упаковці. Незабаром мають з’явитися лікарські форми тироксину з терміном придатності 18 міс, що потребуватимуть зберігання в охолодженому стані.
Левотироксин натрію має вузький терапевтичний індекс, тому дуже важливо, щоб кількість активної речовини залишалася стабільною у відповідно відтитрованій дозі препарату.
Метою цього дослідження було:
- оцінити стабільність таблетованого левотироксину натрію в реальному часі;
- визначити фотостабільність левотироксину натрію в таблетках;
- оцінити якість препаратів левотироксину натрію в таблетках різних виробників, що реалізуються в Судані.
Матеріали та методи
Були проаналізовані такі препарати левотироксину натрію:
- Тироїн 100 мкг (левотироксин натрію 100 мкг виробництва Pharmedic Laboratories Ltd, Lahore, Pakistan);
- Ельтроксин 50 мкг (левотироксин натрію 50 мкг виробництва GlaxoSmithKline, New Cairo, Єгипет);
- Ельтроксин 100 мкг (левотироксин натрію 100 мкг виробництва GlaxoSmithKline, New Cairo, Єгипет).
Для проведення дослідження використовували стандартизоване лабораторне обладнання та реактиви.
Аналіз таблеток левотироксину натрію
Аналіз таблеток левотироксину натрію проводили на визначення однорідності та стабільності. Дослідження стабільності передбачало визначення фотостабільності та стабільності в реальних умовах зберігання.
Для вивчення фотостабільності таблетки досліджуваних препаратів левотироксину натрію зберігали в закритому скляному посуді та спостерігали, що відбувається з ними під впливом прямого сонячного світла (протягом 10 днів). Згодом проводили аналіз концентрації левотироксину натрію в розчині (10 таблеток препарату розчиняли в 10 мл стандартизованого розчинника). Результати порівнювали з таблетками тієї самої партії, що зберігалися в упаковці при кімнатній температурі.
Для вивчення стабільності левотироксину натрію в режимі реального часу упаковки зразків препаратів зберігали при контрольованій кімнатній температурі (23-25 °C) та періодично проводили визначення активної речовини в таблетках.
Вивчення фотостабільності таблеток левотироксину натрію
Таблетки левотироксину натрію, які зберігали в закритому скляному посуді протягом 10 днів під впливом прямих сонячних променів, втратили значну кількість активної речовини, що свідчить про суттєвий вплив сонця на стабільність левотироксину навіть у твердій лікарській формі (табл. 1).
Ці результати підтверджують важливість рекомендацій USP щодо зберігання таблеток левотироксину натрію в щільному контейнері, який здатен захищати від сонячного світла. Під впливом світла левотироксин натрію може змінити колір на рожевий. Вплив сонячного світла на тироксин, розведений у водному розчині, спричиняє його дейодування і перетворення в інші йодовані органічні молекули. Допоміжні речовини, що входять до складу таблетованого левотироксину натрію, можуть прискорювати розпад тироксину під дією сонячного світла, виконуючи роль каталізатора хімічних реакцій.
Вивчення стабільності таблеток левотироксину натрію в режимі реального часу
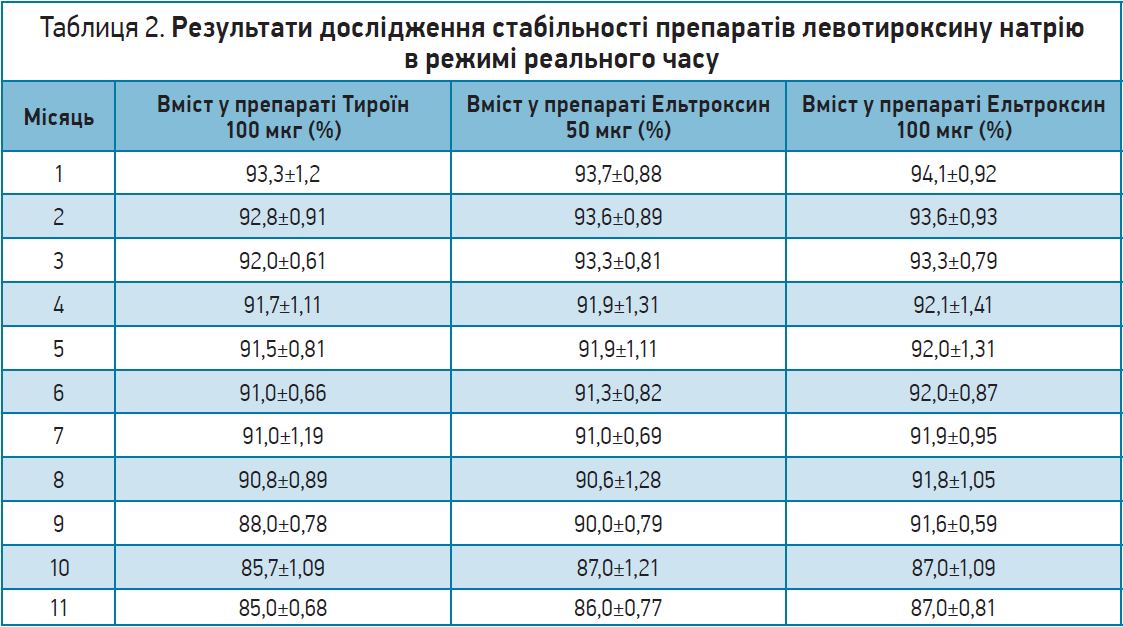
Досліджувані фармацевтичні препарати зберігали при стабільній кімнатній температурі (23-25 °C) та проводили визначення їхньої стабільності в режимі реального часу. Зразки періодично аналізували за допомогою методу BP HPLC.
Аналіз зразків проводили для таких препаратів:
- Тироїн 100 мкг – дослідження здійснювали на зразках через 7 міс з дати виготовлення;
- Ельтроксин 50 мкг – випробування проводили на зразках через 11 міс з дати виготовлення;
- Ельтроксин 100 мкг – дослідження проводили на зразках через 10 міс з дати виготовлення (табл. 2).
Дослідження продемонструвало, що Тироїн 100 мкг вийшов за межі специфікації (88,0%) через 15 міс з дати виготовлення, втративши >5% початкової концентрації через 8 міс з дати виготовлення, що свідчить про нестабільність препарату згідно з рекомендаціями Всесвітньої організації охорони здоров’я. Препарати Ельтроксин 50 мкг і Ельтроксин 100 мкг вийшли за межі специфікації (87,0%) через 20 і 19 міс з дати виготовлення відповідно. Обидва препарати втратили >5% початкової концентрації через 9 міс (рис.). Це свідчить про те, що термін зберігання впродовж 24 міс не відповідає нормативам терміну придатності для таблеток левотироксину натрію в Судані.
Рис. Динаміка зменшення вмісту активної речовини в препаратах левотироксину натрію
Отримані результати підтверджують застереження FDA стосовно того, що пероральні препарати левотироксину натрію можуть мати проблеми зі стабільністю та не зберігати достатньої активності до завершення терміну придатності. З огляду на це повідомляється про випадки відкликання пероральних препаратів левотироксину натрію з ринку через проблеми з активністю або стабільністю. Так, з 1991 р. компанії-виробники не менше 10 разів відкликали препарати левотироксину натрію, в тому числі 150 партій та >100 млн таблеток. В одній з компаній проблеми з активністю таблеток левотироксину натрію неодноразово зумовлювали відкликання продукції з її подальшою утилізацією. Інша компанія за результатами тестування готового препарату знищила 46 партій таблеток левотироксину натрію, які не відповідали специфікаціям ефективності чи однорідності вмісту. В період із 1987 по 1994 рік FDA отримало 58 повідомлень про побічні явища, пов’язані з прийомом таблетованих форм левотироксину натрію.
Висновки
Левотироксин натрію не рекомендується поставляти у великих упаковках. Також необхідно обирати тип контейнера, аби забезпечити захист від сонячного світла, що має виражений вплив на стабільність навіть твердих лікарських форм левотироксину натрію.
На сьогодні в Україні єдиним препаратом левотироксину, який має захищене від світла пакування, є L-Тироксин від компанії «Берлін-Хемі». Завдяки світлозахисному блістеру фотодеградація не призводить до зменшення вмісту діючої речовини в таблетках, а це гарантія стабільності дози L-Тироксину, яку отримує пацієнт.
Таким чином, стабільність дозування дає можливість досягнути кращого контролю гіпотиреозу.
За матеріалами: Mohamed I., Abdallah S. Stability of Levothyroxine Sodium Tablets Marketed in Sudan. J Pharm Biomed Sci 2016; 06 (05): 28-332.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (512), 2021 р.