30 травня, 2023
Алгоритми менеджменту захворювань щитоподібної залози в сучасних умовах
 У квітні відбувся Національний терапевтичний конгрес із міжнародною участю «AIM-2023 (Advances in internal medicine – Досягнення у внутрішній медицині)», присвячений широкому спектру актуальних питань різних терапевтичних напрямів. У заході взяла участь старший науковий співробітник ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), кандидат медичних наук Юлія Валеріївна Булдигіна.
У квітні відбувся Національний терапевтичний конгрес із міжнародною участю «AIM-2023 (Advances in internal medicine – Досягнення у внутрішній медицині)», присвячений широкому спектру актуальних питань різних терапевтичних напрямів. У заході взяла участь старший науковий співробітник ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), кандидат медичних наук Юлія Валеріївна Булдигіна.
Пропонуємо до уваги читачів огляд її доповіді у форматі «запитання – відповідь».
? Наскільки актуальною сьогодні є проблема захворювань щитоподібної залози (ЩЗ)?
– Захворювання ЩЗ уражають щонайменше 650 млн людей у всьому світі. На жаль, дисфункція ЩЗ часто є недіагностованою. Незважаючи на доступність тестів, які дозволяють визначати стан ЩЗ, у дослідженні патології ЩЗ залишається багато складних моментів: обрання комбінації тестів, правильна інтерпретація результатів, застосування результатів для діагностики й правильної терапії захворювань ЩЗ.
? Які захворювання ЩЗ є найпоширенішими? На що слід звертати увагу під час їхньої діагностики та лікування?
– Патологія ЩЗ може перебігати як із гіпер-, так і з гіпотиреозом. Гіпертиреоз характеризується надлишком гормонів ЩЗ. Найчастіше він зустрічається за хвороби Грейвса, тиреоїдитів, токсичної аденоми, передозування тироксином. До симптомів гіпертиреозу належать втрата маси тіла, втомлюваність, непереносимість спеки, тахікардія, систолічна гіпертензія, порушення ритму серця, діарея, тремтіння кінцівок, слабкість м’язів, роздратованість, плаксивість.
У разі первинного гіпертиреозу спостерігається знижений рівень тиреотропного гормона (ТТГ). Для діагностики необхідно оцінити Т4 та Т3 (зазвичай обидва підвищені).
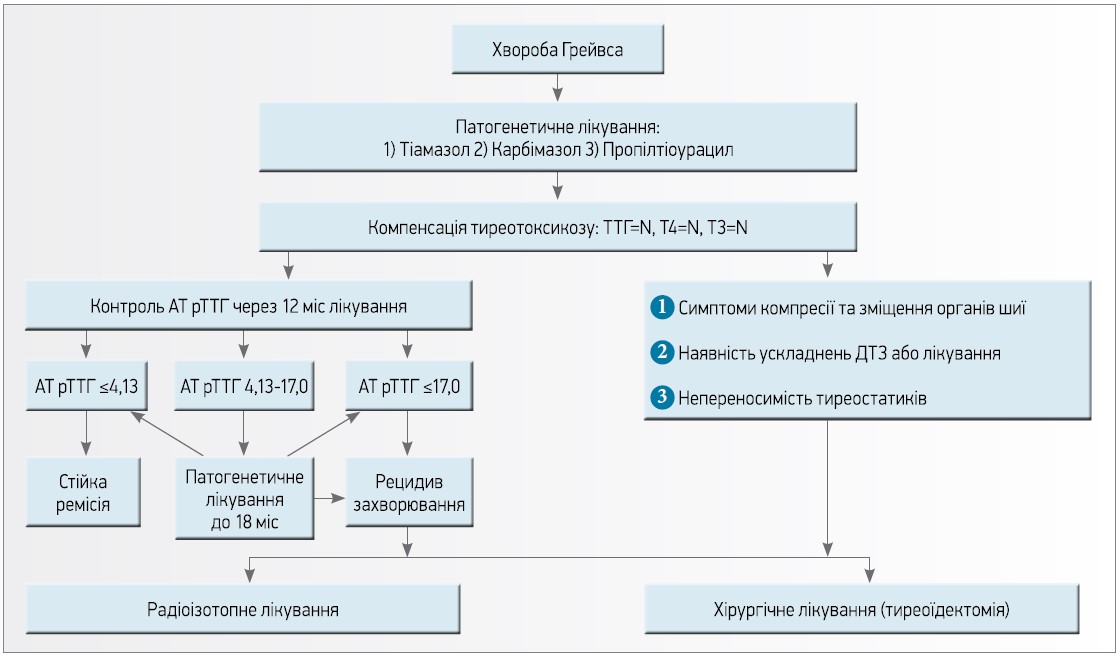
Найчастіше причиною тиреотоксикозу є хвороба Грейвса. Її діагностика базується на визначенні зменшення рівня ТТГ, підвищення рівня Т4, Т3 і рівня антитіл до рецептора ТТГ (АТ рТТГ). Варто зауважити, що саме АТ рТТГ є диференційним маркером розвитку тиреотоксикозу. Їхня наявність свідчить, що тиреотоксикоз обумовлений автоімунним захворюванням ЩЗ (рис.).
Рис. Удосконалений алгоритм лікування ДТЗ
При проведенні лікування антитиреоїдними препаратами пацієнтів із хворобою Грейвса стан гормональної ремісії досягається через 3-4 тиж, імунологічної ремісії – у середньому через 6 міс (тому недоцільно проводити визначення рівня антитіл до рецептора ТТГ через 1-2 міс від початку медикаментозної терапії).
Автономна (токсична) аденома може бути як одиночним вузлом, так і розвиватися на тлі багатовузлового зобу. Відсоток вузлового / багатовузлового токсичного зобу складає від 5 до 25% усіх випадків гіпертиреозу. Характеризується наявністю декількох вузлів, що виявляються під час УЗД, які мають властивість вибірково накопичувати радіоактивний йод і супроводжуватися клінічною картиною гіпертиреозу. Причинами розвитку автономної аденоми є йододефіцит (найбільша кількість випадків у йододефіцитних регіонах), надлишок йоду (наприклад, при застосуванні препаратів з йодом, як-от аміодарон та йодоконтрастні речовини, або за надмірного споживання йоду із продуктами харчування).
Токсична аденома може бути спадковою (сімейний неавтоімунний гіпертиреоз). Це спадкова автосомно-домінантна форма багатовузлового токсичного зобу, що характеризується автономією ЩЗ. Така патологія обумовлена мутацією рецептора ТТГ чи гена білка Gsα, які спочатку відбуваються в окремому тиреоциті, а потім завдяки моноканальному росту утворюється одна або декілька автономно функціонувальних аденом. Мутагенами є нестача йоду, активізація процесів перекисного окислення ліпідів, нестача функції антиоксидантної системи, яка проявляється в збільшенні кількості вільних радикалів.
Клінічна картина автономної (токсичної) аденоми є ідентичною до гіпертиреозу за хвороби Грейвса, однак відсутні офтальмопатія та претибіальна мікседема. Захворювання часто супроводжується субклінічним тиреотоксикозом, який із часом маніфестує в явний. Доведено, що розвиток токсичної аденоми та її автономної функціональної активності відбувається протягом декількох років (від 3 до 8). При гістологічному дослідженні видалена аденома складається із фолікулів, висланих епітелієм, і практично ніколи не малігнізується. Діагностичними критеріями є зниження ТТГ, підвищення Т4 та Т3; АТПО/АТ рТТГ не визначаються.
Дуже рідка патологія – аденома гіпофіза (тиреотропінома). В разі тиреотропіноми спостерігається підвищення Т3, Т4 і ТТГ. Для діагностики потрібні проведення МРТ гіпофіза, консультація нейрохірурга й окуліста. Необхідно зауважити таке: незважаючи на хорошу обізнаність ендокринологів про наявність тиреотоксикозу центрального ґенезу, низька поширеність тиреотропіноми часто не дозволяє перемогти стереотипність мислення лікаря.
Іншою групою захворювань, які можуть зумовити тиреотоксикоз, є тиреоїдити. Зустрічаються неавтоімунні (гострий, підгострий), автоімунні тиреоїдити (тиреоїдит Хашимото, атрофічний, лімфоцитарний, післяпологовий) та тиреоїдити за інших захворювань ЩЗ (радіаційний, травматичний, зоб Ріделя).
Причиною гострого неавтоімунного тиреоїдиту є бактеріальна інфекція. Симптоми цієї патології передбачають різке підвищення температури тіла, біль на передній поверхні шиї, локальні симптоми запалення. Смертність від гострого тиреоїдиту сягає 12% через ускладнення, пов’язані з несвоєчасним лікуванням.
Підгострий тиреоїдит провокується вірусною інфекцією (верхніх дихальних шляхів) за 2-4 тиж до запалення ЩЗ. Симптоми включають значний біль передньої поверхні шиї, дисфагію, слабкість, лихоманку, в третині випадків – ознаки тиреотоксикозу. Підгострий тиреоїдит, асоційований з вірусами, як-от SARS-CoV-2, слід визнавати як ускладнення COVID-19 і розглядати як диференційний діагноз, коли інфіковані пацієнти мають тахікардію без ознак прогресування захворювання.
Діагностичними критеріями гострого неавтоімунного тиреоїдиту є лейкоцитоз зі зсувом вліво, підвищення ШОЕ до 30-40 мм/год. При УЗД у ділянці ураження візуалізується зона зі зниженою ехогенністю. Змін рівнів ТТГ і ТГ зазвичай не виявляють. Діагностичними критеріями підгострого неавтоімунного тиреоїдиту є лейкоцитоз зі зсувом вправо, збільшення ШОЕ до ≥30 мм/год, зниження ТТГ, підвищення Т4. Тонкоголкова аспіраційна біопсія ЩЗ: гігантські багатоядерні клітини та гранульоми. За потреби додатково проводиться тест Крайля.
Згідно з рекомендацією 119 Американської тиреоїдної асоціації (АТА, 2016), лікування гострого тиреоїдиту залежно від клінічної ситуації характеризується призначенням антибіотиків і хірургічним дренуванням. За розвитку деструктивного тиреотоксикозу можуть бути призначені β-адреноблокатори. Згідно з рекомендацією 117 АТА, пацієнтам із легкими симптомами підгострого тиреоїдиту як початкова терапія показано призначення β-адреноблокаторів і нестероїдних протизапальних препаратів (НПЗП). Глюкокортикоїди показані в разі недостатньої ефективності, при зберіганні виражених больових відчуттів і симптомах тиреотоксикозу на тлі прийому НПЗП.
Післяпологовий тиреоїдит виникає у 5% жінок через 2-6 міс після пологів зазвичай у носіїв АТПО/АТТГ. Розпочинається як раптовий тиреотоксикоз протягом 2-6 тиж, за яким упродовж декількох тижнів або місяців настає фаза гіпотиреозу.
Згідно з рекомендацією 96 АТА (2016), якщо тиреотоксикоз уперше виявлено в жінки в післяпологовому періоді, необхідним є обстеження з метою диференційної діагностики післяпологового тиреоїдиту та післяпологової маніфестації хвороби Грейвса. Згідно з рекомендацією 97 АТА, жінкам із тиреотоксичною фазою післяпологового тиреоїдиту за наявності симптомів можуть бути призначені β-адреноблокатори.
Призначення тиреостатичних препаратів для лікування жінок із післяпологовим тиреоїдитом не проводиться, оскільки за тиреотоксичною фазою настає гіпотиреоїдна фаза.
Основна причина гіпотиреозу – хронічний автоімунний тиреоїдит або його атрофічна чи гіпертрофічна форма (тиреоїдит Хашимото). Іншими причинами гіпотиреозу є операції на ЩЗ, ятрогенний фактор, дефіцит йоду тощо.
Діагностика автоімунного тиреоїдиту проводиться за допомогою УЗД ЩЗ, яке дозволяє виявити характерну гіпоехогенність тканини, мозаїчність із чергуванням гіпо- та гіперехогенних ділянок. Також можлива наявність фіброзних тяжів. Додатково проводиться визначення АТПО та/або АТТГ, ТТГ, Т4-в, 25(ОН)D. Рівень антитіл за автоімунного тиреоїдиту визначають з метою встановлення діагнозу та не використовують як контроль за ефективністю терапії.
Слід згадати, що багато метааналізів продемонстрували прямий зв’язок між клінічною депресією і наявністю нелікованого гіпотиреозу.
? Які основні рекомендації щодо лікування гіпотиреозу?
– Гіпотиреоз потребує замісної терапії. Оцінка адекватності терапії первинного гіпотиреозу проводиться за рівнем ТТГ. Референтні значення для здорових – 0,4-4,0 мОд/л. Оптимальні значення при замісній терапії – 0,5-2,5 мОд/л.
У літніх пацієнтів (віком >65 років) нормальні референтні значення ТТГ при лікуванні гіпотиреозу складають 0,4-4,4 мОд/л. За рівня 4,5-6,9 мОд/л лікування не є рекомендованим. У разі підвищення рівня ТТГ до 7,0-9,9 мОд/л слід розглянути лікування L-T4. При рівні >10 мОд/л проводиться обов’язкове лікування L-T4 для запобігання розвитку гіпотиреозу, серцевих ускладнень та серцево-судинної смертності.
Як препарат першого вибору для лікування гіпотиреозу рекомендований L-тироксин. Його перевагами є ефективне усунення симптомів гіпотиреозу, тривалий досвід успішного застосування, позитивний профіль побічних явищ, простота застосування, хороша абсорбція в кишечнику, тривалий період напіввиведення та низька вартість.
Однак, незважаючи на добре відомий алгоритм розрахунку доз, при лікуванні гіпотиреозу L-тироксином еутиреоз досягається в 60,1% випадків, субклінічний гіпертиреоз – у 20,7% (Cannaris et al., 2000). Тому для ефективного лікування гіпотиреозу обов’язково потрібно ретельно підбирати дозу левотироксину. Особлива технологія виробництва таблеток L-тироксину Берлін-Хемі (виробник «Берлін-Хемі АГ», Німеччина) дозволяє зберігати максимальну точність за розподілу їх навпіл, що гарантує стабільність дози, а особлива форма таблетки забезпечує зручність поділу, що здійснюється простим натисканням пальця на насічку для поділу (метод SNAP-TAB). Це дозволяє призначати та з легкістю приймати багато варіантів доз (25; 37,5; 50; 62,5; 75; 87,5 мкг і т. ін.).
Підготував Олександр Соловйов

Медична газета «Здоров’я України 21 сторіччя» № 9 (545), 2023 р.