2 листопада, 2023
Перспективи замісної ферментної терапії: курс на комбіновані препарати бактеріального, рослинного та фунгального походження
 Останніми роками все більше дослідників звертаються до вивчення можливостей препаратів замісної ферментної терапії у лікуванні пацієнтів із хронічним панкреатитом та зовнішньосекреторною недостатністю підшлункової залози (ЗСНПЗ), причому особливий інтерес спричиняють ферментні препарати (ФП) нетваринного походження, оскільки мають багато переваг.
Останніми роками все більше дослідників звертаються до вивчення можливостей препаратів замісної ферментної терапії у лікуванні пацієнтів із хронічним панкреатитом та зовнішньосекреторною недостатністю підшлункової залози (ЗСНПЗ), причому особливий інтерес спричиняють ферментні препарати (ФП) нетваринного походження, оскільки мають багато переваг.
У вересні відбулася науково-практична конференція з міжнародною участю «ХV Український гастроентерологічний тиждень» за участю провідних учених України та світу, представників президії Європейської гастроентерологічної асоціації, у рамках якої президент Українського клубу панкреатологів, член Ради Європейського клубу та Міжнародної асоціації панкреатологів, доктор медичних наук, професор Наталія Борисівна Губергріц представила доповідь «Перспективи замісної ферментної терапії».
Пропонуємо читачам огляд цієї доповіді у форматі «запитання – відповідь».
? Важлива складова лікування ЗСНПЗ і синдрому мальдигестії – використання ФП. Практика доводить, що препарати замісної ферментної терапії тваринного походження в певних випадках можуть надавати недостатню ефективність, тому сьогодні все більшої популярності набувають ФП мікробного, фунгального та рослинного походження. Якими є перспективи та переваги їх використання?
– Адекватне застосування замісної ферментної терапії дозволяє пацієнту із ЗСНПЗ зменшити вираженість симптомів, запобігти прогресуванню трофологічної недостатності, а також суттєво покращити якість життя, адже, за словами відомого арабського письменника, вченого-енциклопедиста Абу-ль-Фараджа бін Харуна, «їжа, яка не перетравлюється, з’їдає того, хто її з’їв». Саме тому останніми роками в світі проводиться розробка нових ФП, а також дослідження особливостей їхньої дії, ефективності та безпеки, все більше зростає тенденція до використання препаратів нетваринного походження. Сьогодні ≈35% ФП, які реалізуються на світовому фармацевтичному ринку, – нетваринні. Лідер використання ФП нетваринного походження – Японія (80% ФП – бактеріальні, 10% – фунгальні, наприклад Санзим). Також нетваринні ФП популярні в Німеччині (Комбізім форте, Комбізім композитум, Елзім), США (Мілаза‑100, Діголаза, Розім CL, Панкреаза), Франції (Ліпанкріл), Іспанії (Ензімакс Дуал Реліз).
Важливою перевагою ФП нетваринного походження є збереження їхньої активності за рН від 3,0 до 9,0, тому вони не потребують надійної кислотостійкої оболонки. Навіть у шлунку ці препарати залишаються стійкими та можуть звільнятися з лікарської форми – звідси їхня висока біодоступність. Отже, при використанні ФП нетваринного походження здійснюється більш ранній гідроліз харчових субстратів.
Додаткові переваги ФП нетваринного походження:
- широка субстратна специфічність (можуть гідролізувати субстрати, які не здатні гідролізувати ФП тваринного походження);
- відсутність необхідності активації нетваринної ліпази жовчними кислотами (важливо при веденні пацієнтів після холецистектомії або з дисфункцією жовчного міхура / сфінктера Одді, холестатичними захворюваннями печінки);
- стійкість нетваринної ліпази до протеаз людини і тварин;
- відсутність придушення власної панкреатичної секреції пацієнта та навіть стимулювальний вплив на неї (посилюється у разі збільшення дози препарату);
- збереження активності в широкому діапазоні температур;
- наявність додаткових ферментів (наприклад, лактази), які не входять до складу ФП тваринного походження.
Також важливим є те, що ФП нетваринного походження можуть застосовуватися в хворих із гіперчутливістю до панкреатину (Adams D.B. et al., 2017).
? Чи проводяться наразі дослідження ефективності та безпеки ФП нетваринного походження? Про що вони свідчать?
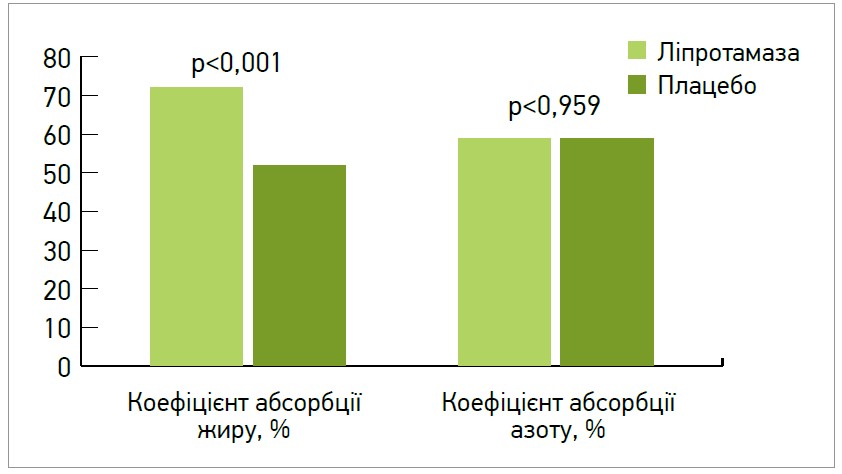
– Так, сьогодні показання до використання ФП нетваринного походження вже мають достатню доказову базу. Наприклад, подвійне сліпе рандомізоване плацебо-контрольоване дослідження ефективності та безпеки ФП на основі мікробної ліпази (ліпротамази) при муковісцидозі (тобто з тяжкою панкреатичною недостатністю) показало, що лікування ліпротамазою зумовлює достовірне підвищення коефіцієнту абсорбції жиру, але не впливає на коефіцієнт абсорбції азоту (рис. 1).
Рис. 1. Ефективність лікування ліпротамазою при муковісцидозі
? Які ФП нетваринного походження порекомендуєте призначати пацієнтам із ЗСНПЗ для відтворення процесу фізіологічного травлення?
– Ефективний і сучасний ФП – комбінований засіб нетваринного (бактеріального та фунгального) походження Панжест®, прототипом якого є Enzymax Dual Release (Aora Health, Іспанія). Ця дієтична добавка має унікальну систему доставки – «капсулу в капсулі», яка застосовується для забезпечення поступового вивільнення ферментів у певних відділах шлунково-кишкового тракту. Зовнішня (працює у кислому рН, розчинюється в шлунку) та внутрішня капсула (працює у лужному рН, розчинюється в дванадцятипалій кишці) містять різні суміші ферментів, причому, крім ліпази, амілази, протеаз, Панжест® має у складі 2 додаткових ферменти – глюкоамілазу й альфа-галактозидазу (табл.).
|
Таблиця. Унікальна система доставки препарату Панжест® – «капсула в капсулі» |
|||
|
Фермент |
Зовнішня капсула |
Внутрішня капсула |
Усього |
|
Ліпаза |
3200 FIP |
4 500 FIP |
7 700 FIP |
|
Амілаза |
1720 DU |
2 250 DU |
3970 DU |
|
Глюкоамілаза |
11,2 AGU |
6 AGU |
17,2 AGU |
|
Протеаза 4.5 |
2 496 HUT |
500 HUT |
2 996 HUT |
|
Протеаза 3.0 |
12 SAPU |
- |
12 SAPU |
|
Протеаза 6.0 |
- |
1 500 HUT |
1 500 HUT |
|
Нейтральна бактеріальна протеаза |
- |
1 500 PC
|
1500 РС
|
|
Альфа-галактозидаза |
- |
62,5 GalU |
62,5GalU |
|
Примітки: одиниці виміру ферментів – FIP (міжнародна федерація фармацевтики); HUT (одиниця виміру гемоглобіну на основі тирозину); DU (одиниця виміру декстринізації); GalU (одиниця виміру активності галактозидази); AGU (одиниця виміру амілоглюкозидази); SAPU, PC (одиниця мікробної протеази). |
|||
Глюкоамілази, що містяться в засобі Панжест®, допомагають засвоювати частково перероблений крохмаль, який надходить із клітковини харчових продуктів. Оскільки димерні олігосахариди погано перетравлюються, вони можуть ферментуватися кишковими бактеріями та зумовлювати підвищене газоутворення.
Відомо, що людина та тварини з однокамерним шлунком не можуть синтезувати достатню кількість альфа-галактозидази, щоб повністю засвоїти галактосахариди; порушення їхнього перетравлення може спричинити розвиток метеоризму. Альфа-галактозидаза, яку містить Панжест®, розщеплює специфічні незасвоювані олігосахариди перед тим, як вони метаболізуються бактеріями товстого кишечнику, що зменшує утворення кишкових газів після їжі з високим умістом клітковини (Di Nardo G. et al., 2013).
Фунгальні ліпази сьогодні привернули значну увагу промисловості завдяки специфічності та стабільності в різних хімічних і фізичних умовах. Ліпази Панжесту отримують із грибів, а біотехнологія, яка стоїть за цим, стандартизована для забезпечення їхньої активності в широкому діапазоні значень рН, що дозволяє бути активними як у кислих умовах шлунка, так і більш лужних у тонкому кишечнику. Дієтична добавка Панжест® містить 3 різних протеази, з яких 2 є фунгальними, які також стандартизовані на широкий діапазон активності рН з оптимальним значенням рН за кисліших умов (у шлунку) і є стабільними в екстремальних умовах температури (Mehta A. et al., 2017).
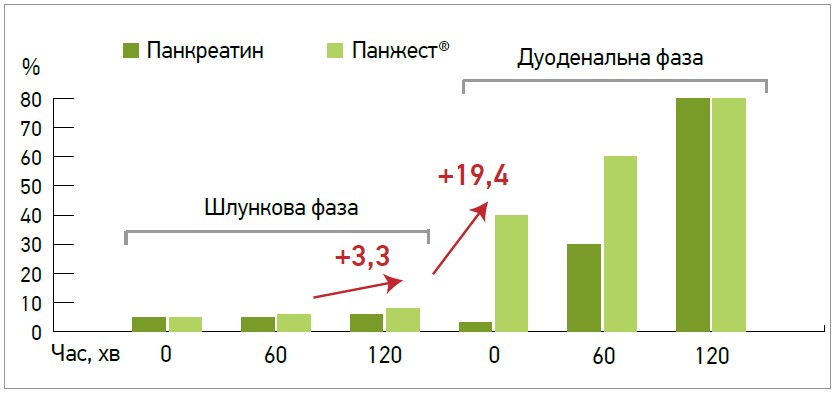
Посилення ліполізу під впливом комплексу Панжест® в порівнянні з панкреатином на вході до дванадцятипалої кишки (в 19 разів) свідчить про те, що мікробні ліпази є високоефективними та стабільними, на відміну від тваринного панкреатину (рис. 2) (Schneider M.U. et al., 1986).
Рис. 2. Вплив на процеси ліполізу при застосуванні Enzymax Dual Release (прототип Панжест®) і лікарського засобу на основі панкреатину
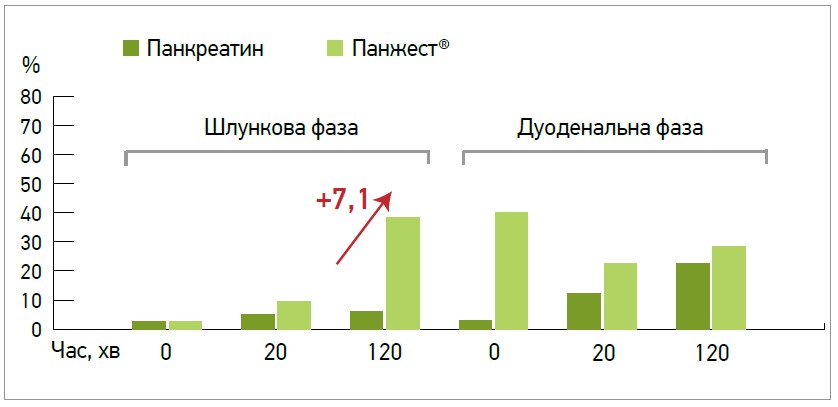
Розпад вуглеводів, індукований Enzymax Dual Release, спостерігався через 60 хв після початку процесу травлення, а через 2 год у шлунку він виявився ефективнішим у 7 разів, ніж при застосуванні панкреатину тваринного походження (рис. 3).
Рис. 3. Розпад вуглеводів, індукований Enzymax Dual Release (прототип Панжест®)
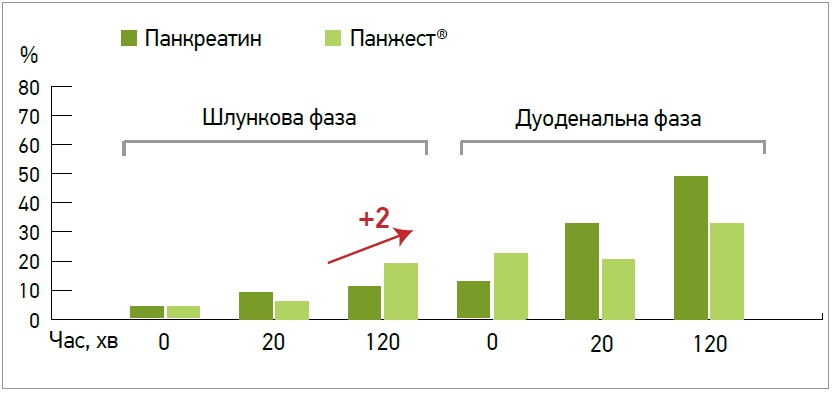
Ефективність протеолізу під впливом Enzymax Dual Release також була вдвічі ефективнішою після 2 год травлення в шлунку (рис. 4); крім того, ферменти зберігали протеолітичну активність протягом 2 год у кишечнику.
Рис. 4. Ефективність протеолізу під впливом Enzymax Dual Release (прототип Панжест®)
Отже, Панжест® може бути рекомендований лікарем до щоденного раціону харчування як додаткове джерело ферментів нетваринного походження, які сприяють повноцінному травленню жирів, вуглеводів та білків, при функціональних порушеннях травлення через дефіцит або дисбаланс травних ферментів, як-от диспепсія, дискомфорт після прийому їжі, відчуття переповнення шлунку, підвищене газоутворення під час перетравлення їжі. Панжест® рекомендований при станах, що супроводжуються ЗСНПЗ, як-от муковісцидоз, хронічний панкреатит, хірургічні втручання на верхніх відділах шлунково-кишкового тракту.
Підготував Олександр Соловйов