3 травня, 2023
Клініко-лабораторне та інструментальне дослідження ефективності й безпечності препарату Гастротек®
 На тлі прийому нестероїдних протизапальних препаратів (НПЗП) може виникнути ураження будь-якого відділу шлунково-кишкового тракту (ШКТ). Дія НПЗП реалізується через зменшення синтезу простагландинів шляхом пригнічення циклооксигенази (ЦОГ), що регулює їх синтез з арахідонової кислоти. Тому в наш час актуальним є вивчення і дослідження клініко-лабораторної та інструментальної ефективності препарату Гастротек® у пацієнтів з ерозивно-виразковими пошкодженнями шлунка та дванадцятипалої кишки (ДК), спричиненими НПЗП, на підґрунті комплексного вивчення клінічної картини, стану показників ейказоноїдного ряду, модульованих НПЗП, і структурних змін слизової оболонки (СО) до та після лікування цим препаратом.
На тлі прийому нестероїдних протизапальних препаратів (НПЗП) може виникнути ураження будь-якого відділу шлунково-кишкового тракту (ШКТ). Дія НПЗП реалізується через зменшення синтезу простагландинів шляхом пригнічення циклооксигенази (ЦОГ), що регулює їх синтез з арахідонової кислоти. Тому в наш час актуальним є вивчення і дослідження клініко-лабораторної та інструментальної ефективності препарату Гастротек® у пацієнтів з ерозивно-виразковими пошкодженнями шлунка та дванадцятипалої кишки (ДК), спричиненими НПЗП, на підґрунті комплексного вивчення клінічної картини, стану показників ейказоноїдного ряду, модульованих НПЗП, і структурних змін слизової оболонки (СО) до та після лікування цим препаратом.
Ерозивно-виразкові ураження гастродуоденальної зони є однією з найпоширеніших патологій ШКТ [1-3]. З успіхами антихелікобактерної ерадикаційної терапії частота нехелікобактерних уражень ШКТ зростає, що пов’язується в т.ч. із прийомом пошкоджуючих СО препаратів [1, 3, 4]. Так, одними з найбільш вживаних є НПЗП. Їх дія реалізується через зменшення синтезу простагландинів шляхом пригнічення ЦОГ, що регулює їх синтез з арахідонової кислоти. Проте простагландини чинять не тільки прозапальний, а й протективний ефекти, зокрема гастропротективний. Розвиток НПЗП-асоційованих ушкоджень ШКТ пов’язують із порушенням синтезу саме гастропротекторних простагландинів (ПГЕ-1) у СО [5, 6].
На тлі прийому НПЗП може виникнути ураження будь-якого відділу ШКТ, від стравохода до кишечнику. Найчастіше патологічні зміни спостерігаються в антральному відділі шлунка, рідше – у цибулині ДК у вигляді ерозивних, виразкових або запальних змін [7]. Нерідко вони проявляються такими ускладненнями, як кровотечі і перфорації, що можуть загрожувати летальними випадками [1, 2, 8, 9].
Лікування НПЗП-асоційованої гастродуоденопатії включає відміну протизапального препарату, що, ймовірно, викликав ураження СО, та призначення антисекреторних засобів [3, 7, 9]. Це забезпечує загоєння ерозивно-виразкових пошкоджень в більшості випадків, а додавання цитопротекторів покращує та прискорює ці процеси. З цією метою застосовується мізопростол, аналог природного ПГЕ-1, який сприяє загоєнню виразкової хвороби та полегшенню її симптомів. Мізопростол захищає СО ШКТ шляхом пригнічення базальної, стимульованої та нічної секреції кислоти, зменшує об’єм та протеолітичну активність шлункового соку і збільшує секрецію бікарбонату слизу [9, 10]. Його можна також використовувати у профілактичних цілях для запобігання розвитку медикаментозних ушкоджень.
В Україні з’явився вітчизняний препарат,що містить мізопростол, – Гастротек® (ПРАТ «Фармацевтична фірма «Дарниця»). В 1 таблетці містяться 0,2 мг мізопростолу у вигляді мізопростолу дисперсії (1:100 у гіпромелозі) та допоміжні речовини. В залежності від діагнозу, рекомендовано 800 мкг (0,8 мг) щодня у 2-х або 4-х розподілених дозах, що приймають зі сніданком та/або кожним основним прийомом їжі та перед сном (лікування виразки ДК, виразкової хвороби шлунка і пептичної виразки, спричиненої НПЗП). Курс становить 4-8 тижнів. При профілактиці пептичної виразки, викликаної НПЗП, приймають 200 мкг 2, 3 чи 4 рази/добу. Доза підбирається індивідуально для кожного пацієнта та відповідає його клінічному стану [11].
Метою цього дослідження стало вивчення клініко-лабораторної та інструментальної ефективності препарату Гастротек® у лікуванні пацієнтів з ерозивно-виразковими пошкодженнями шлунка та ДК, спричиненими НПЗП, на підґрунті комплексного вивчення клінічної картини, стану показників ейказоноїдного ряду, модульованих НПЗП, та структурних змін СО до та після лікування цим препаратом.
Матеріали та методи
Дослідження проведено у 30 пацієнтів з ерозивно-виразковими пошкодженнями шлунка і ДК, спричиненими НПЗП, без виразкової хвороби в анамнезі та без прийому інших пошкоджуючих СО препаратів. Серед обстежених було 12 (40%) жінок, 18 (60%) чоловіків, середній вік тих, хто брав участь у дослідженні, – 52,5±2,4 року. Середня тривалість прийому НПЗП склала 21,2±3,8 місяця, з коливанням приблизно від 1 до 60 місяців.
Найчастіше пацієнти застосовували такі НПЗП: ацетилсаліцилову кислоту – 17 (56,7%) випадків, диклофенак – 9 (30%) випадків, цитрамон – 4 (13,3%) випадка. Відповідно, патологія, через яку призначалися НПЗП, – це серцево-судинні захворювання, остеохондроз хребта, суглобовий больовий синдром та головний біль.
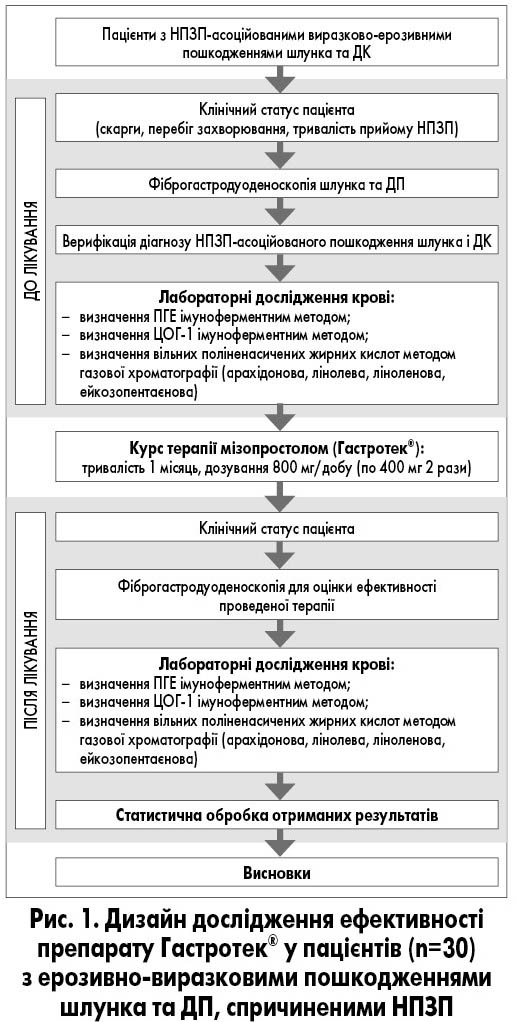 На рис. 1 представлений дизайн дослідження ефективності препарату Гастротек® у пацієнтів з ерозивно-виразковими пошкодженнями шлунка та ДК, спричиненими НПЗП.
На рис. 1 представлений дизайн дослідження ефективності препарату Гастротек® у пацієнтів з ерозивно-виразковими пошкодженнями шлунка та ДК, спричиненими НПЗП.
Усім пацієнтам проводили клінічне, лабораторне та інструментальне обстеження згідно з протоколом дослідження до та після курсу препарата Гастротек® за схемою: 2 таблетки по 200 мкг, тобто 400 мкг або 0,4 мг мізопростолу 2 рази/добу – зранку під час сніданку та ввечері перед сном протягом 1 міс. Після закінчення курсу лікування робили контрольні дослідження.
Для оцінки змін показників ейкозаноїдного ряду в сироватці крові пацієнтів імуноферментним методом (ELISA) визначали вміст ПГЕ-1 за допомогою тест-набору фірми Elabscience (США) та рівень ЦОГ-1 за допомогою тест-системи фірми Wuhan Fine BiotechCo Ltd (Китай). Принцип методу ELISA заснований на кількісному визначенні антигену безпосередньо його пошарового зв’язування зі специфічними до нього антитілами. Дослідження проводили відповідно до інструкцій для тест-набору. Імуноферментний аналіз виконували за допомогою імуноферментного аналізатора Stat Fax 303 Plus (США), на якому проводили вимірювання оптичної щільності при довжині хвилі 450 нм.
Ендоскопічне дослідження проводилося в режимі NBI за загальноприйнятою методикою з використанням відеоендоскопічної системи Evis Exera III та відеогастроскопа Olympus 190 (Японія).
Статистичний аналіз отриманих даних здійснювали за допомогою прикладних програм Statistica 6.1. Нормальність розподілу кількісних показників оцінювали за допомогою критерію Шапіро – Уїлка. Для опису даних застосовували медіану (Me), нижній (25%) і верхній (75%) квартилі. Порівняння показників медіани здійснювали за U-критерієм Манна – Уітні. Статистичну значущість оцінювали на рівні не нижче 95% (р<0,05).
Дотримання етичних аспектів
Дослідження проведено відповідно до вимог Гельсінської декларації, правил належної клінічної та лабораторної практики, національних нормативно-правових документів у сфері біоетики. До початку дослідження всі пацієнти надали інформовану згоду на його проведення. Усі процедури затверджені локальним комітетом з біоетики.
Результати дослідження
До лікування пацієнти скаржилися на біль в епігастрії (89%), правому чи лівому підребер’ї (54%), печію (35%), відрижку (26%). Після лікування стан значно покращився.
У результаті оцінки клінічної симптоматики встановлено, що прийом препарату Гастротек® сприяв зменшенню частоти больового та диспепсичного синдромів більше, ніж у 5 разів (p<0,01; рис. 2).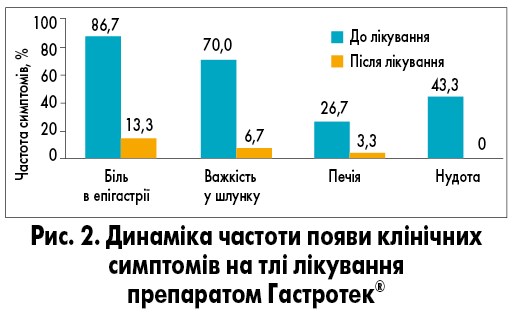
Крім того, комплексна терапія із застосуванням препарату Гастротек® сприяє вірогідному зменшенню інтенсивності клінічних симптомів вже через 7 днів (р<0,01) після початку прийому препарату та зникненню клінічних проявів через 10 днів (р<0,01; рис. 3).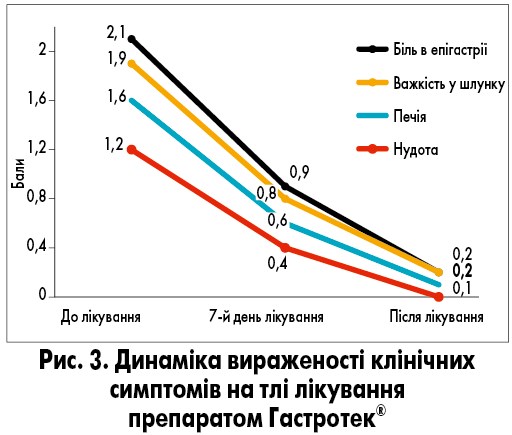
Аналіз патології, через яку пацієнту призначали НПЗП, показав, що це серцево-судинні захворювання (майже в 60% випадків), остеохондроз хребта (близько 30%) та інші больові синдроми, у т.ч. головний біль. Треба відзначити, що більшість пацієнтів мали ураження через прийом аспірину в малих кардіологічних дозах, прийом цих препаратів становив від 2 до 60 місяців, із середньою тривалістю 18,7±5,9 місяця.
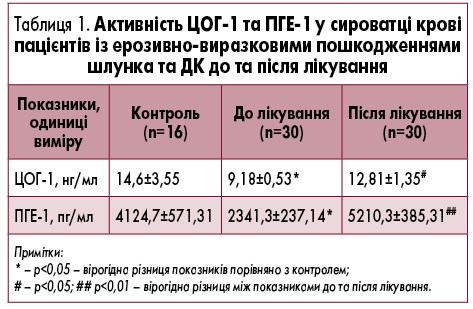 Результати оцінки змін показників ейкозаноїдного ряду показали, що до лікування у 83,3% (25 із 30) пацієнтів з ерозивно-виразковими пошкодженнями шлунка та ДК, спричиненими НПЗП, встановлено зниження рівня ЦОГ-1. Середнє його значення було вірогідно нижче в 1,6 раза (р<0,05) порівняно зі значеннями контрольної групи (табл. 1). Також до лікування у 76,7% (23 із 30) обстежених пацієнтів було встановлено зниження вмісту ПГЕ-1 в 1,8 раза (р<0,05) порівняно з контрольною групою.
Результати оцінки змін показників ейкозаноїдного ряду показали, що до лікування у 83,3% (25 із 30) пацієнтів з ерозивно-виразковими пошкодженнями шлунка та ДК, спричиненими НПЗП, встановлено зниження рівня ЦОГ-1. Середнє його значення було вірогідно нижче в 1,6 раза (р<0,05) порівняно зі значеннями контрольної групи (табл. 1). Також до лікування у 76,7% (23 із 30) обстежених пацієнтів було встановлено зниження вмісту ПГЕ-1 в 1,8 раза (р<0,05) порівняно з контрольною групою.
Після лікування препаратом Гастротек® встановлено вірогідне збільшення в 1,4 раза (р<0,05) середнього рівня ЦОГ-1 порівняно зі значеннями до лікування. Внутрішньогруповий аналіз показав, що у 76,7% (23 із 30) пацієнтів встановлено позитивну динаміку підвищення активності ЦОГ-1. Рівень ПГЕ-1 після лікування зростає на 83,3% (у 25 із 30 пацієнтів) і збільшується у 2 рази (р<0,01) порівняно з рівнем до лікування. Крім того, встановлено, що у пацієнтів із НПЗП-асоційованими ерозивно-виразковими пошкодженнями шлунка та ДК рівень ЦОГ-1 та ПГЕ-1 у сироватці крові був пов’язаний із тривалістю прийому НПЗП (табл. 2). 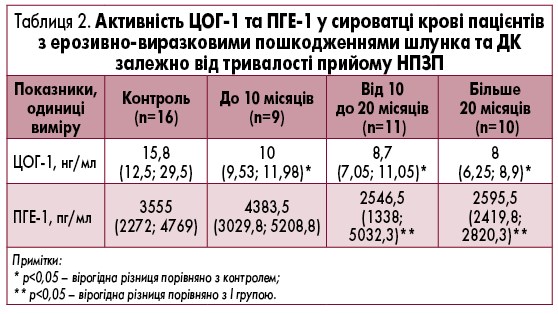
Встановлено зниження активності ЦОГ-1 в 1,6 раза (р<0,05) у групі пацієнтів із тривалістю прийому НПЗП до 10 місяців; в 1,8 раза (р<0,05) у групі пацієнтів із тривалістю прийому НПЗП від 10 до 20 місяців та в 2 рази (р<0,05) у групі пацієнтів із тривалістю прийому НПЗП більше 20 місяців. Вміст ПГЕ-1 у сироватці крові у групі пацієнтів із тривалістю прийому НПЗП більше 10 місяців був вірогідно нижче в 1,7 раза (р<0,05), ніж у тих, хто приймав НПЗП ≤10 місяців.
Так, при більшій тривалості прийому НПЗП спостерігаються більш глибокі порушення, що може потребувати додаткової корекції.
Оцінка ерозивно-виразкових ушкоджень СО шлунка та ДК при ендоскопічному обстеженні до та після лікування дозволила оцінити відновлення СО на тлі комплексного лікування.
При проведенні езофагогастродуоденоскопії до лікування у 9 (30%) пацієнтів виявлено виразку (2 – шлунка та 7 – ДК). У 76,7% пацієнтів спостерігалися ерозивні ураження СО з локалізацією переважно в антральному відділі шлунка та ДК. В усіх пацієнтів спостерігали еритему СО гастродуоденальної зони.
Оцінка ендоскопічної картини показала, що після лікування препаратом Гастротек® відбувалося зниження в 4 рази (р<0,01) частоти виявлення еритеми СО. Ерозивні ураження визначалися лише у 6,7%, виразкові дефекти загоїлися в усіх (100%) випадків. Тобто в середньому загоєння ерозій та виразок гастродуоденальної зони ШКТ склало 93,3% (р<0,01; рис. 4).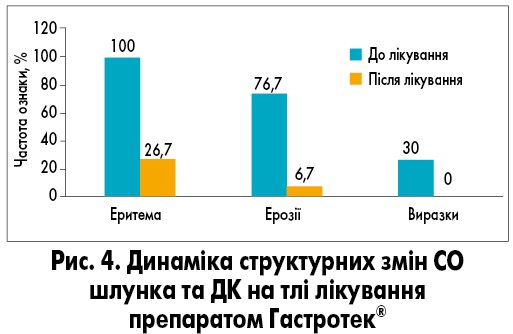
Таким чином, на тлі лікування препаратом Гастротек® спостерігалося відновлення СО шлунка та ДК, ушкоджених НПЗП.
Загальна оцінка препарату Гастротек® показала безпечність та добру переносимість у пацієнтів із НПЗП-асоційованими ушкодженнями гастродуоденальної зони ШКТ при застосуванні згідно з інструкцією протягом 1 місяця. Побічних ефектів не спостерігалося.
Отже, згідно з результатами проведених клінічних, лабораторних та інструментальних досліджень, Гастротек® є ефективним у лікуванні пацієнтів з ерозивно-виразковими ураженнями шлунка та ДК, спричиненими прийомом НПЗП.
Висновки
- Прийом препарату Гастротек® зняв больовий синдром та диспептичні явища у більшості пацієнтів – у 82,6% випадків (p<0,001).
- Встановлено нормалізуючий вплив препарату Гастротек® на активність ЦОГ-1 у сироватці крові у 76,7% пацієнтів, що зумовлено підвищенням рівня цього показника в 1,4 раза (р<0,05) порівняно з даними до лікування.
- Терапія препаратом Гастротек® призводить до збільшення в 2 рази (р<0,01) рівня ПГЕ-1 у пацієнтів із НПЗП-асоційованими ушкодженнями гастродуоденальної зони ШКТ.
- Прийом препарату Гастротек® чинить позитивний вплив на структурні зміни СО шлунка та ДК, сприяючи загоєнню ерозій та виразок у 93,3% випадків (р<0,01).
- Препарат Гастротек® показав безпечність та добру переносимість у пацієнтів із НПЗП-асоційованими ушкодженнями гастродуоденальної зони ШКТ при застосуванні згідно з інструкцією протягом 1 місяця.
- Гастротек® ефективний для лікування пацієнтів з ерозивно-виразковими ураженнями шлунка та ДК, спричиненими НПЗП, що підтверджується даними клінічних, лабораторних та інструментальних досліджень.
Література
- Schneider C., Venerito M. Gastroduodenale Ulkuskrankheit und Helicobacter pylori [Peptic ulcer disease and H. pylori gastritis: key advances in clinical management]. Deutsche medizinische Wochenschrift. 2022. N 147 (17). P. 1103-1108. https://doi.org/10.1055/a-1640-2830.
- Azhari H., King J.A., Coward S., Windsor J.W., Ma C., Shah S.C. et al. The Global Incidence of Peptic Ulcer Disease Is Decreasing Since the Turn of the 21st Century: A Study of the Organisation for Economic Co-Operation and Development (OECD). The American journal of gastroenterology. 2022. 117 (9), 1419-1427. https://doi.org/10.14309/ajg.0000000000001843.
- Lanas A., Chan F.K.L. Peptic ulcer disease. Lancet (London, England). 2017. 390 (10094), 613-624. https://doi.org/10.1016/S0140-6736(16)32404-7.
- Herszenyi L., Juhasz M., Mihaly E., Tulassay Z. A fekelybetegseg es a stressz [Peptic ulcer disease and stress]. Orvosi hetilap. 2015. 156 (35), 1426-1429. https://doi.org/10.1556/650.2015.30249.
- Miyake K., Ueki N., Suzuki K., Shinji Y., Kusunoki M., Hiratsuka T., Nishigaki H., Tatsuguchi A., Futagami S., Wada K., Tsukui T., Nakajima A., Yoshino S., Sakamoto C. Preventive therapy for non-steroidal anti-inflammatory drug-induced ulcers in Japanese patients with rheumatoid arthritis: the current situation and a prospective controlled-study of the preventive effects of lansoprazole or famotidine. Alimentary pharmacology & therapeutics, 21. 2005. Suppl 2, 67-72. https://doi.org/10.1111/j.1365-2036.2005.02477.x.
- Bourgeois S., Carr D.F., Musumba C.O., Penrose A., Esume C., Morris A.P., Jorgensen A.L., Zhang J.E., Pritchard D.M., Deloukas P., Pirmohamed M. Genome-Wide association between EYA1 and Aspirin-induced peptic ulceration. 2021. EBioMedicine, 74, 103728. https://doi.org/10.1016/j.ebiom.2021.103728.
- Свінціцький А.С. Механізми терапевтичної ефективності та побічної дії нестероїдних протизапальних препаратів//Практикуючий лікар. – 2012. – № 4. – С. 5-12.
- Hawkey C., Avery A., Coupland C. A. C., Crooks C., Dumbleton J., Hobbs F.D.R., Kendrick D., Moore M., Morris C., Rubin G., Smith M., Stevenson D., HEAT Trialists. Helicobacter pylori eradication for primary prevention of peptic ulcer bleeding in older patients prescribed aspirin in primary care (HEAT): a randomised, double-blind, placebo-controlled trial. Lancet (London, England), 2022. 400 (10363), 1597-1606. https://doi.org/10.1016/S0140-6736(22)01843-8.
- Chu S.J., Yoon K.T., Kim J.S. The Korean journal of gastroenterology//Taehan Sohwagi Hakhoe chi, 76 (5), 232-237. 2020. https://doi.org/10.4166/kjg.2020.139.
- Taha A.S., McCloskey C., McSkimming P., McConnachie A. Misoprostol for small bowel ulcers in patients with obscure bleeding taking aspirin and non-steroidal anti-inflammatory drugs (MASTERS): a randomised, double-blind, placebo-controlled, phase 3 trial. The lancet. Gastroenterology & hepatology, 3 (7), 469-476. 2018. https://doi.org/10.1016/S2468-1253(18)30119-5.
- Гастротек, інструкція https://compendium.com.ua/info/550032/.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (67) 2023 р.



