7 листопада, 2024
Нутритивна підтримка дорослих пацієнтів із кахексією
Стандарт медичної допомоги
Кахексія, або виснаження жирових запасів організму, втрата загальної і м’язової маси тіла, є поширеним ускладненням важких форм багатьох гострих і хронічних захворювань. Зокрема, біля половини всіх пацієнтів із пізніми стадіями раку страждають на кахексію. Подібне виснаження енергетичних та поживних ресурсів організму становить безпосередню загрозу виникнення ускладнень, небезпечних для життя хворої людини.
Пропонований стандарт медичної допомоги (СМД) не стосується якоїсь специфічної нозологічної форми, а представляє сучасні рекомендації щодо лікувального харчування пацієнтів дорослого віку з онкологічними захворюваннями.
Загальна частина
Назва діагнозу: Злоякісні новоутворення.
Коди стану або захворювання. НК 025:2021 «Класифікатор хвороб та споріднених проблем охорони здоров’я»: Кахексія (R64).
Розділ І. Організація надання медичної допомоги пацієнтам із кахексією
Положення СМД. Призначений для лікарів загальної практики – сімейної медицини, терапевтів, педіатрів, онкологів, хірургів-онкологів, анестезіологів, хіміотерапевтів, онкогематологів, гастроентерологів, нефрологів, лікарів-дієтологів, дієтологів, середнього медичного персоналу для організації надання медичної допомоги та покращення результатів лікування хворих завдяки оптимізації комплексної терапії та лікувального харчування.
Обґрунтування. Терапевтичні інтервенції кахексії включають коригування лікування основного захворювання, що сприятиме засвоєнню та метаболізму нутрієнтів для кращого забезпечення енергією, поживними речовинами та анаболічними стимулами, а також комплексну підтримку щодо усунення дисфункцій, пов’язаних з емоційними та соціальними аспектами харчування. Нутритивні та метаболічні втручання варіюються від консультування з метою оптимізації дієти до фармакологічних засобів, ентерального (ЕХ) і парентерального харчування (ПХ).
Критерії якості медичної допомоги
Обов’язкові
- Наявні затверджені на рівні закладів охорони здоров’я (ЗОЗ) документи, що координують та інтегрують медичну допомогу для забезпечення своєчасної діагностики та лікування пацієнтів із кахексією.
- Наявний розроблений та задокументований індивідуальний план обстеження, лікування та спостереження, узгоджений із пацієнтом, членами сім’ї/особами, які здійснюють догляд.
- Пацієнтів і, за згодою, членів сім’ї/осіб, що здійснюють догляд, забезпечують дохідливою інформацією щодо стану пацієнта з кахексією.
Бажані
4. У ЗОЗ, де надають медичну допомогу хворим із кахексією, розміщують та поширюють інформаційні матеріали стосовно проявів патологічного стану, профілактики його виникнення та прогресування; за запитом пацієнтів та членів сім’ї/осіб, які здійснюють догляд, надають посилання на надійні джерела для отримання додаткової інформації.
Розділ ІІ. Діагностика
Положення СМД. Пацієнти з важкими формами захворювань, які зумовлюють високий ризик мальнутриції та кахексії, мають підлягати скринінгу мальнутриції відповідно до універсального інструмента скринінгу мальнутриції (УІСМ) або іншого аналогічного інструмента.
Втрата понад 5% ваги за попередні шість місяців та наявність трьох із таких ознак, як втома, анорексія, зменшення м’язової сили та м’язової маси, а також системних ознак запалення визначають високу ймовірність наявності кахексії.
Згідно з визначеним ступенем ризику погіршення нутритивного статусу визначається періодичність його оцінки (табл. 1).
|
Таблиця 1. Універсальний інструмент скринінгу мальнутриції (УІСМ) |
|
|
Кроки |
Кількість балів |
|
Крок 1. Індекс маси тіла (ІМТ), кг/м2 |
|
|
>30 >20 18,520 <20 |
0 0 1 1 |
|
Крок 2. Ненавмисна втрата ваги у відсотках упродовж 36 місяців |
|
|
<5% 510% >10% |
0 1 2 |
|
Крок 3. Активність та важкість основного захворювання |
|
|
Якщо прояви гострої хвороби або важкість хронічного захворювання призвели до припинення харчування тривалістю >5 днів |
2 |
|
Крок 4. Сума балів (крок 1+2+3) та план ведення пацієнта |
|
|
· Низький ризик – рутинне ведення · Середній ризик – активне спостереження · Високий ризик – невідкладний план лікування |
0 1 2 |
|
Крок 5. Диференційоване ведення пацієнтів |
|
|
Низький ризик. Повторний скринінг: · ЗОЗ – щотижня · будинки догляду – щомісяця · вдома – щороку · для окремих популяцій – >75 років |
0 |
|
Середній ризик. Спостереження: · оцінка дієти за три дні · за адекватності – повторний скринінг · ЗОЗ – щотижня · будинки догляду – щомісяця · вдома – кожні 23 місяці · за неадекватності – модифікація дієти, моніторинг |
1 |
|
Високий ризик. Лікування: · направлення до дієтолога · визначення цілей, надходження нутрієнтів · моніторинг + коригування · ЗОЗ – щотижня · будинки догляду – щомісяця · вдома – кожні 23 місяці |
2 |
|
Всі категорії ризику |
|
|
Лікування основного захворювання, консультація щодо змін харчування, реєстрація ознак мальнутриції, потреби у спеціальних дієтах Ожиріння: наявність ожиріння фіксується у медичній документації. Поліпшення контролю основного захворювання |
– |
Обґрунтування. Зниження маси тіла з одночасним виснаженням жирових запасів і м’язової маси часто розвивається у пацієнтів із важкими формами хронічних захворювань та на пізніх стадіях онкологічних захворювань. Погіршення забезпечення нутрієнтами, розлади метаболічних процесів, які призводять до системного запалення та активації катаболізму внаслідок низки патофізіологічних механізмів, можуть призвести до втрати ваги на фоні одночасного впливу комплексу факторів включно із обмеженнями або повним припиненням споживання їжі, зниженням фізичної активності та виключенням пов’язаних з нею анаболічних ефектів.
Кахексія може розвиватися поступово, тому виділяють її ранні фази без помітної втрати маси тіла та прогресуючі стадії із вираженими ознаками мальнутриції.
Найбільш поширеними проявами розладів травлення у пацієнтів із кахексією є анорексія та раннє насичення, нудота, здуття живота, спотворення смаку, ксеростомія, дисфагія та закрепи. Крім того, можуть виникати інші вторинні симптоми – прояви недостатнього харчування, такі як задишка, сильна втома тощо.
Критерії якості медичної допомоги
Обов’язкові
- Для виявлення кахексії або ризику кахексії в усіх пацієнтів, які лікуються амбулаторно, госпіталізовані до ЗОЗ, перебувають у будинках догляду, проводять оцінку ризику порушень нутритивного статусу за методологією та із застосуванням інструментів (табл. 1-3).
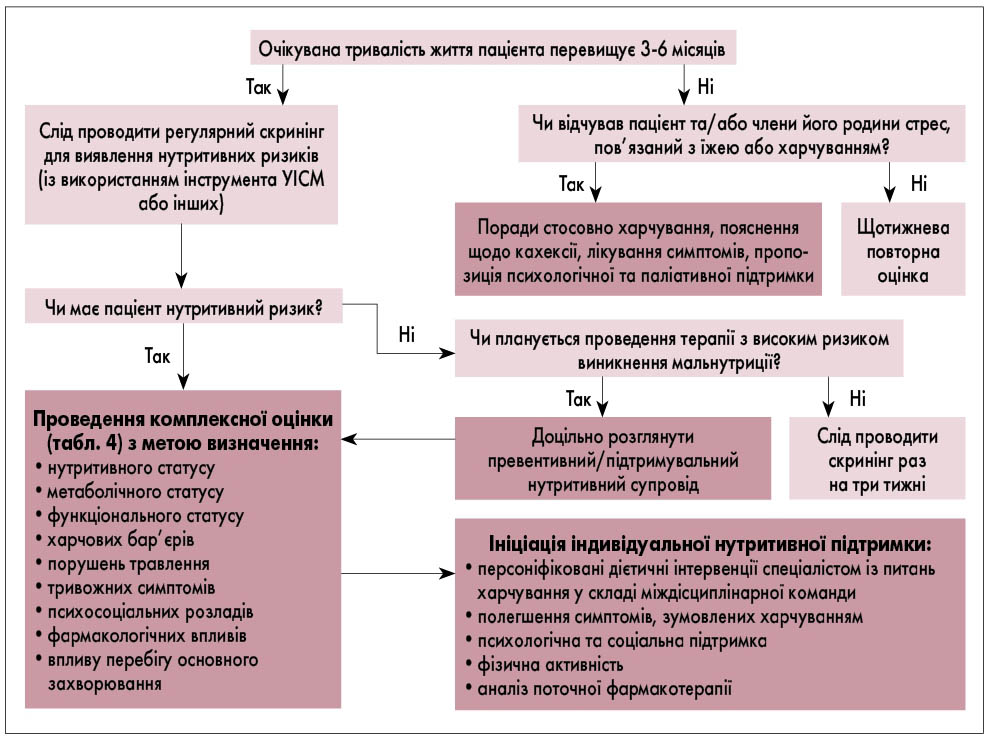
- З метою виявлення ранніх стадій порушення нутритивного статусу проводиться регулярна оцінка споживання їжі, зміни ваги та ІМТ, починаючи від встановлення діагнозу захворювань, які супроводжуються високим ризиком мальнутриції та кахексії (див. рис. 1).
- Якщо пацієнти мають ознаки мальнутриції та кахексії або у разі високого ризику цих станів, їм проводять скринінг на наявність дисфагії та її лікування, а також заохочують та навчають підтримувати функцію ковтання під час ЕХ.
- Для пацієнтів із патологічними результатами скринінгу порушення нутритивного статусу застосовується алгоритм моніторингу та планування дієтичних інтервенцій (рис. 1).
- Діагноз мальнутриції, оцінка її важкості базуються на визначенні критеріїв, наведених у табл. 2-3. Наявність саркопенії підтверджується вираженою втратою м’язової маси та функціональної рухової спроможності – сила рукостискання, вставання зі стільця, хода, підйом по сходах. Ризик кахексії збільшується за наявності активного системного запалення.
|
Таблиця 2. Діагностичні критерії мальнутриції |
||||
|
Фенотип |
Етіологія |
|||
|
Втрата ваги |
Зниження ІМТ |
Втрата м’язової маси |
Зменшення споживання їжі або засвоєння нутрієнтів |
Запальний стан |
|
>5% протягом останніх шести місяців; >10% за строк понад шість місяців |
<20 кг/м2 для віку <70 років; або <22 кг/м2 для віку >70 років |
Зменшення, підтверджене валідованим методом оцінки складу тіла (біоімпеданс, КТ 2, МРТ 3) |
≤50% ЕП1 >1 тижня, або будьяке зменшення >2 тижнів, або будьяка хронічна патологія ШКТ4, що погіршує абсорбцію |
Гостре захворювання/травма або хронічне ЕП |
|
Діагноз мальнутриції підтверджується за наявності одного критерію фенотипу та одного етіологічного критерію |
||||
|
1ЕП – енергетичні потреби. 2КТ – комп’ютерна томографія. 3МРТ – магнітнорезонансна томографія. 4ШКТ – шлунковокишковий тракт. |
||||
|
Таблиця 3. Ступені важкості мальнутриції |
|||
|
Стадія |
Втрата ваги (%) |
Зменшення ІМТ (кг/м2) |
Втрата м’язової маси |
|
Стадія 1/помірна мальнутриція (потрібний один критерій, що відповідає цій стадії) |
510% протягом останніх шести місяців або 1020% за строк понад шість місяців |
<20 – <70 років |
Легкий – помірний дефіцит відповідно до валідованого методу дослідження |
|
Стадія 2/важка мальнутриція (потрібний один критерій, що відповідає цій стадії) |
>10% протягом останніх шести місяців або >20% за строк понад шість місяців |
<18,5 – <70 років |
Важкий дефіцит відповідно до валідованого методу дослідження |
Рис. 1. Скринінг, діагностична оцінка, індивідуальні нутритивні інтервенції та моніторинг ефективності
Розділ ІІІ. Лікування
Положення СМД. Ведення пацієнтів із кахексією передбачає індивідуальний комплексний мультидисциплінарний підхід на основі своєчасного виявлення об’єктивних ознак недостатності харчування (мальнутриції) з метою невідкладного запровадження інтервенцій, спрямованих на стабілізацію метаболічних процесів та сприяння відновленню нутритивного статусу.
Доцільність модифікації дієти, збільшення споживання харчових продуктів із метою поліпшення забезпечення пацієнта енергією та поживними речовинами має бути визначена ще до появи ознак мальнутриції.
Загальноприйнятною є практика нутритивної підтримки із включенням консультації дієтолога, лікаря-дієтолога або іншого фахівця із профільною освітою та досвідом щодо харчування. Рекомендації мають включати інтервенції для кращого контролю симптомів, заохочення до споживання високобілкової та висококалорійної їжі та напоїв, які добре засвоюються.
Обґрунтування. Клінічні прояви, показники об’єктивних, лабораторних та інструментальних тестів у пацієнтів із кахексією динамічно змінюються протягом траєкторії захворювання; зміни компенсаторних можливостей організму та характеру метаболізму, а також погіршення фізичної працездатності є важливими терапевтичними мішенями для пацієнтів, що проходять лікування раку та інших хронічних захворювань, перебіг яких відбувається на фоні мальнутриції, водночас вони втрачають свою важливість ближче до кінця життя.
Проте виснажливі симптоми необхідно лікувати та полегшувати, наскільки це можливо, протягом життя кожного пацієнта із залученням членів сім’ї та осіб, які здійснюють догляд.
Вихідна оцінка нутритивного статусу, розроблення індивідуальних комплексних та послідовних дієтичних інтервенцій, моніторинг їхнього дотримання та інтервенцій є провідною стратегією ведення пацієнтів із мальнутрицією (табл. 4 та рис. 2).
|
Таблиця 4. Параметри комплексної оцінки кахексії та рекомендовані інструменти для досліджень |
||
|
Категорія |
Параметр |
Рекомендовані інструменти |
|
Нутритивний статус |
Маса тіла Втрата маси тіла Споживання їжі Споживання енергії та білкаa Мікронутрієнти або дефіцит макронутрієнтівa Композиція тілаa |
ІМТ % від здорової, звичайної маси тіла; % від звичайної кількості ккал/кг/добу, г/кг/добу Харчовий щоденник або 24годинне відтворення і програмний аналіз Дослідження біологічних рідин Антропометрія БІМ1, КТ або ПРАМ2 |
|
Метаболічний статус |
Системне запалення Витрати енергіїa |
Модифікована прогностична оцінка Глазго Непряма калориметрія |
|
Функціональний статус |
ЗС3 Фізична активність Залежність Сила рукостисканняа Швидкість ходиа |
ECOG4/WHO5 index ADL6 Northwick Park Dependency Score Динамометр Тест швидкості ходи на дистанції 4 м |
|
Харчові бар’єри |
Симптоми впливу харчування |
PGSGA7 контрольний список впливу харчування |
|
Порушення травлення |
Жування, смак, ковтання, перистальтика кишечника, закрепи, діарея, стеноз, порушення всмоктування |
Діагностична співбесіда, візуальні дослідження, функціональні тести, візуальні аналогові шкали |
|
Симптоми тривоги |
Оцінка симптомів і фактори ризику (пізнання, емоції, депресія) |
ESAS8 |
|
Психологічна і соціальна тривога |
Психосоціальна оцінка |
FAACT9 EORTC10 QLQCAX2411 |
|
Побічні реакції від дії ліків |
Можливий негативний вплив на апетит, ШКТ, центральну нервову систему, втома |
Фармакологічне консультування |
|
Перебіг основного захворювання |
Ступінь і активність онкологічного або іншого захворювання |
Перебіг основного захворювання |
|
aЯкщо доступно та доречно, залежно від наявних ресурсів і здатності пацієнта. 1БІМ – біологічна імпедансометрія; 2ПРАМ – подвійна рентгенівська абсорбціометрія; 3ЗС – загальний стан; 4ECOG – Східна об’єднана онкологічна група; 5WHO – Всесвітня організація охорони здоров'я; 6ADL – повсякденна діяльність; 7PGSGA – суб’єктивна глобальна оцінка пацієнта; 8ESAS – Едмонтонська система оцінки симптомів; 9FAACT – функціональна оцінка лікування анорексії/кахексії; 10EORTC – Європейська організація з дослідження та лікування раку; 11QLQCAX24 – опитувальник якості життя, характерний для кахексії. |
||
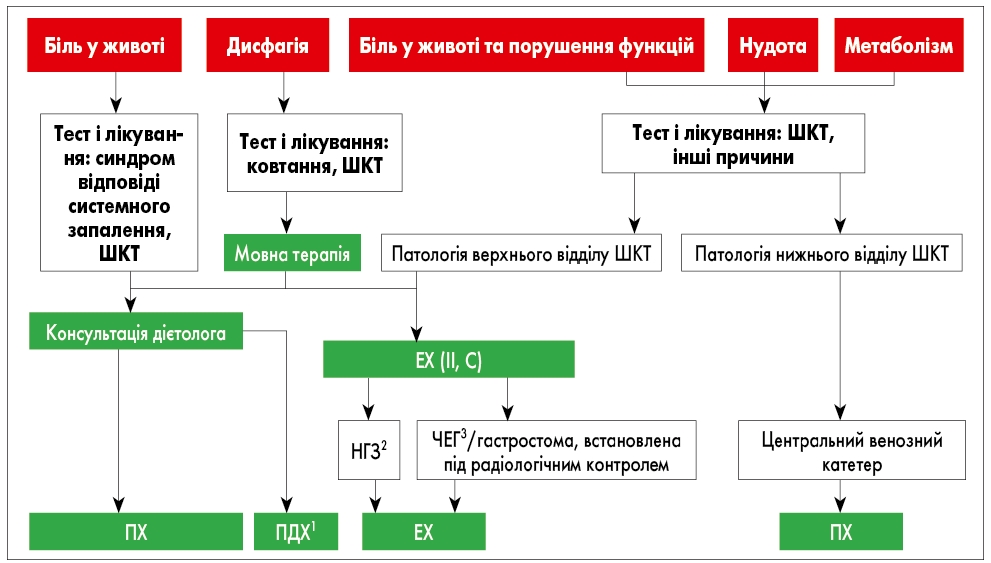
Рис. 2. Вибір варіантів нутритивних інтервенцій
Червоний колір: мішені для інтервенцій; зелений: нутритивні інтервенції; білий: інші аспекти ведення.
1ПДХ – пероральне додаткове харчування; 2НГЗ – годування через назогастральний зонд; 3ЧЕГ – черезшкірна ендоскопічна гастростомія.
Споживання їжі може бути порушено внаслідок впливу багатьох факторів та вторинних симптомів, що впливають на харчування, деякі з яких можуть ефективно лікуватися. Якщо після пом’якшення цих факторів споживання їжі залишається недостатнім, слід розпочати нутритивні втручання.
Порівняно із поліпшенням забезпечення енергією та поживними речовинами за допомогою нутритивних втручань, модулювання метаболічних порушень є більш складним процесом. Розвиток інсулінорезистентності та анаболічної резистентності погіршує підтримку м’язової маси всього тіла. Отже, втручання для зменшення катаболізму та збільшення анаболічних шляхів метаболізму включають забезпечення достатньої кількості енергії та білків; тренування м’язів; фармакологічні засоби для підвищення апетиту, зменшення системного запалення та стимулювання росту м’язів; психосоціальні взаємодії для полегшення дистресу.
Нутритивну підтримку та фізіотерапію можна запропонувати індивідуально з ретельним моніторингом індивідуальних цілей та якості життя. Впродовж останніх тижнів життя дуже важливо полегшити страждання, пов’язані з харчуванням, а також із втратою маси тіла. Необхідно розглянути підходи, які полегшують страждання, пов’язані з наближенням смерті, та співчутливе спілкування з пацієнтом і його родиною.
Критерії якості медичної допомоги
Обов’язкові
- Кожному пацієнтові з кахексією слід запропонувати інтервенції з метою або покращення, або полегшення наслідків кахексії.
- Лікування кахексії потребує мультимодального підходу, спрямованого на полегшення симптомів, що впливають на споживання їжі, забезпечення адекватного споживання енергії, надходження та засвоєння поживних речовин, мінімізацію катаболічних змін, підтримку тренування м’язів і надання психологічної та соціальної допомоги.
- Під час протипухлинного або іншого лікування та пацієнтам із очікуваною тривалістю життя більше 3-6 місяців рекомендоване втручання не лише для протидії погіршенню ресурсів організму та метаболізму, а й для полегшення виснажливих симптомів.
- Якщо очікувана виживаність становить менше 3-6 тижнів, рекомендовано зосередитись на втручаннях проти кахексії, спрямованих на полегшення виснажливих симптомів, таких як спрага, нудота, блювання та дисфагія, а також психологічного та екзистенційного страждання пацієнта і членів його родини (рис. 2).
- Якщо важко ухвалити рішення щодо відповідної стратегії втручання проти кахексії, можна розглянути попереднє втручання впродовж обмеженого періоду, щоб оцінити ймовірність покращення.
- Нутритивна підтримка пацієнтів, які можуть споживати їжу, має ґрунтуватися на консультаціях щодо дієти, рекомендаціях щодо вибору високоенергетичних продуктів із високим вмістом білка, збагачення їжі (наприклад, завдяки додаванню жиру/олії, білкового порошку) та використання ПДХ.
- Якщо цього недостатньо, слід запропонувати годування через зонд (ЕХ), за умови, що нижня частина ШКТ функціонує, в іншому разі ПХ є методом вибору. Окремі способи годування можна комбінувати для досягнення оптимального ефекту. Варіанти нутритивних інтервенцій наведені на рис. 2.
- Пацієнтів із кахексією внаслідок значного обмеження харчування або повного голодування, в яких ІМТ становить 14,0-15,0 кг/м2 і нижче, доцільно госпіталізувати. У таких випадках нутритивний супровід рекомендовано починати із ПХ сумішами, які містять всі макро- та мікронутрієнти, протягом достатнього періоду часу для стабілізації гемодинамічних та метаболічних показників із поступовим переходом на оральне харчування або ЕХ.
- Якщо очікувана виживаність пацієнта становить менше кількох місяців, перевагу надають нутритивним інтервенціям із низьким ризиком/обтяженням для пацієнта (наприклад, консультування та ПДХ).
- Якщо це безпечно, пероральний шлях має бути першим вибором нутритивної підтримки. Ентеральне зондове годування може застосовуватися у разі дисфагії, якщо функція тонкої кишки збережена.
- ПХ слід розглянути, якщо пероральне харчування і годування через зонд не переносяться або залишаються недостатніми.
- Нутритивні інтервенції мають бути спрямовані на задоволення потреб у енергії та поживних речовинах. Їх варто супроводжувати тренуванням м’язів і терапевтичними втручаннями для нормалізації метаболічного стану (зменшення системного запалення, полегшення дистресу).
- Надходження поживних речовин та енергії слід забезпечити на рівні не менше 25-30 ккал/кг маси тіла/день, включаючи принаймні 1,2 г білка/кг маси тіла/день. У хворих із кахексією рекомендоване співвідношення макронутрієнтів, в яких жир становить половину небілкових калорій.
Бажані
14. Можливе призначення кортикостероїдів для підвищення апетиту впродовж короткого терміну (до двох-трьох тижнів). Стимулювальний вплив на апетит зазвичай зникає при їхньому тривалому застосуванні.
15. Прогестини можна використовувати для підвищення апетиту та маси тіла, але не для збільшення м’язової маси, якості життя чи фізичної витривалості у пацієнтів із раковою кахексією. Необхідно враховувати ризик серйозних побічних ефектів включно із тромбоемболічними ускладненнями.
16. Існують помірні докази, які свідчать про можливість застосування оланзапіну для лікування апетиту та нудоти у пацієнтів із прогресуючим раком.
17. Пацієнтам із кахексією, які отримують хіміотерапію, променеву або хіміопроменеву терапію, можна запропонувати ПДХ з омега‑3 поліненасиченими жирними кислотами (ПНЖК) та протеїнами для збільшення маси тіла, зменшення втрати його м’язової маси та покращення якості життя.
18. Якщо пероральне харчування було суворо обмежене або відсутнє впродовж тривалого періоду, вдаються до повільного збільшення (перорального, ентерального чи парентерального) харчування впродовж декількох днів і вживання додаткових запобіжних заходів для профілактики синдрому відновленого годування (СВГ). Рекомендоване проведення скринінгу СВГ (табл. 5), його профілактика і лікування (табл. 6).
|
Таблиця 5. Скринінг для визначення ризику СВГ |
||
|
Критерії для індентифікації дорослих пацієнтів |
Помірний ризик: необхідна присутність двох критеріїв |
Значний ризик: необхідна присутність одного критерію |
|
ІМТ Втрата ваги Споживання калорій |
1618,5 кг/м2 5% протягом одного місяця Відсутність або мінімальне вживання протягом 56 днів Або <75% від потреби в енергії >7 днів протягом гострої хвороби або травми Або <75% від потреби в енергії >1 міс. |
<16 кг/м2 7,5% за 3 міс.; >10%/6 міс. Відсутність або мінімальне вживання протягом >7 днів Або <50% від потреби в енергії >5 днів протягом гострої хвороби або травми Або <50% від потреби в енергії >1 міс. |
|
Патологічні рівні калію, фосфору чи магнію до відновлення годування |
Мінімально знижений рівень або нормальний нещодавній рівень, які потребували незначної або однодозової саплементації |
Мінімально/значно знижений рівень або нормальний нещодавній рівень, які потребували значної або багатодозової саплементації |
|
Втрата підшкірного жиру Втрата м’язової маси |
Ознаки мінімальної втрати Ознаки мінімальної або помірної втрати |
Ознаки значної втрати Ознаки значної втрати |
|
Супутні хвороби |
Неважка хвороба |
Важка хвороба |
|
Таблиця 6. Профілактика та лікування СВГ у дорослих пацієнтів із високим ризиком |
|
|
Напрямки нутритивної підтримки |
Рекомендації |
|
Відновлення надходження калорій (енергії) |
|
|
Обмеження рідини Обмеження натрію Обмеження білка |
|
|
Електроліти |
|
|
Тіамін та мультвітаміни |
|
|
Моніторинг та довготривала підтримка |
|
19. Помірні фізичні вправи під керівництвом професійних експертів є безпечними для пацієнтів із кахексією і рекомендовані для підтримки та збільшення м’язової маси.
20. Також два-три рази на тиждень пацієнтам із кахексією потрібно виконувати помірне аеробне (на витривалість) тренування. Призначення вправ має здійснювати фізіотерапевт або лікар, належно підготовлений професіонал. Слід дотримуватись структурованого підходу, що включає режими (аеробіка, опір, гнучкість), частоту, інтенсивність і тривалість, а також визначений час для повторної оцінки.
Розділ ІV. Подальше спостереження за пацієнтами
Положення СМД. Пацієнти із групи середнього чи високого нутритивного ризику мають проходити регулярну оцінку нутритивного статусу (табл. 1) для ранньої діагностики його порушення та виникнення мальнутриції (табл. 2-3). Пацієнти з ризиком неоптимального харчування мають отримати рекомендації щодо харчування та фізичної активності.
Обґрунтування. Деякі пацієнти з кахексією продовжують жити впродовж багатьох місяців та років виключно на ПХ, тобто такий часовий проміжок, протягом якого будь-яка особа без їжі за інших умов загинула б від голодного виснаження. Перш ніж розпочати програму тренінгів із домашнього ПХ, важливо оцінити когнітивні та фізичні можливості пацієнта.
Критерії якості медичної допомоги
Обов’язкові
- Для пацієнтів із хронічною недостатністю надходження поживних речовин та (або) неконтрольованим синдромом мальабсорбції проводиться забезпечення ЕХ або ПХ вдома за наявності відповідних умов.
- Для пацієнтів із кахексією, які зазнали хірургічного втручання, рекомендована належна нутритивна підтримка не лише під час госпіталізації, а й після виписки зі стаціонару.
Індикатори якості медичної допомоги
Наявність у лікаря загальної практики – сімейного лікаря клінічного маршруту пацієнта (КМП).
Цей індикатор характеризує організаційний аспект запровадження сучасних медико-технологічних документів у регіоні. Якість надання медичної допомоги пацієнтам, його відповідність вимогам КМП, відповідність КМП чинним СМД цей індикатор висвітлювати не може, але для аналізу цих аспектів необхідне обов’язкове запровадження КМП в ЗОЗ.
Лікарі первинної медичної допомоги; лікарі-онкологи, що надають спеціалізовану медичну допомогу пацієнтам, подають дані до структурних підрозділів із питань охорони здоров’я місцевих державних адміністрацій.
Затверджено Наказом МОЗ України 17 вересня 2024 р. № 1601
Дата оновлення стандартів – 2029 р.
Текст адаптовано та уніфіковано відповідно до стандартів Тематичного випуску Медичної газети «Здоров’я України».
Повний текст за посиланням: https://www.dec.gov.ua/wp-content/uploads/2024/09/smd_1601_17092024_dod.pdf
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (73) 2024 р.