1 травня, 2026
Метаболічно асоційована стеатотична хвороба печінки: від оновлення класифікації до персоналізованої терапії
За матеріалами Міжнародного медичного форуму
 Метаболічно асоційована стеатотична хвороба печінки (МАСХП) є одним із найпоширеніших хронічних захворювань у світі: за поточними оцінками, понад 1,5 млрд осіб мають ті чи інші її прояви, і ця цифра продовжує зростати. В межах Міжнародного медичного форуму «Гастроентерологічна патологія у внутрішній медицині» доктор медичних наук, професор Ігор Ярославович Господарський, завідувач кафедри клінічної імунології, алергології і загального догляду за хворими Тернопільського національного медичного університету імені І.Я. Горбачевського, презентував доповідь, присвячену сучасним підходам до діагностики та лікування МАСХП – від переосмислення класифікаційної парадигми до обґрунтування персоналізованих терапевтичних стратегій. Він приділив особливу увагу недооціненому в рутинній практиці MetALD-фенотипу – комбінованому токсично-метаболічному ураженню печінки, питанням неінвазивної стратифікації фіброзу та місцю метадоксину (Ліверія®) у терапії пацієнтів із поєднаним впливом метаболічних і токсичних чинників.
Метаболічно асоційована стеатотична хвороба печінки (МАСХП) є одним із найпоширеніших хронічних захворювань у світі: за поточними оцінками, понад 1,5 млрд осіб мають ті чи інші її прояви, і ця цифра продовжує зростати. В межах Міжнародного медичного форуму «Гастроентерологічна патологія у внутрішній медицині» доктор медичних наук, професор Ігор Ярославович Господарський, завідувач кафедри клінічної імунології, алергології і загального догляду за хворими Тернопільського національного медичного університету імені І.Я. Горбачевського, презентував доповідь, присвячену сучасним підходам до діагностики та лікування МАСХП – від переосмислення класифікаційної парадигми до обґрунтування персоналізованих терапевтичних стратегій. Він приділив особливу увагу недооціненому в рутинній практиці MetALD-фенотипу – комбінованому токсично-метаболічному ураженню печінки, питанням неінвазивної стратифікації фіброзу та місцю метадоксину (Ліверія®) у терапії пацієнтів із поєднаним впливом метаболічних і токсичних чинників.
МАСХП належить до провідних гепатологічних проблем сучасності. За прогностичними оцінками, кількість хворих продовжує зростати й упродовж наступних 7-8 років сягне 2 млрд. Показники поширеності суттєво варіюють залежно від регіону – від 13,48% в Африці до 31,79% на Близькому Сході, тоді як у Південній Америці, Азії та Європі вони становлять 30,45; 27,37 і 23,71% відповідно (Younossi Z.M., 2016).
! Стрімке зростання захворюваності обумовлене пандемією ожиріння і метаболічного синдрому, а також об’єктивними труднощами ранньої діагностики на амбулаторному етапі. Через відсутність специфічної симптоматики на початкових стадіях фіброзні зміни нерідко діагностують на пізніх стадіях, коли можливості терапевтичного втручання суттєво обмежені.
Нова номенклатура: від НАЖХП до МАСХП
Переосмислення класифікації стеатотичних уражень печінки відбулось у 2023 р.: термін «неалкогольна жирова хвороба печінки» (НАЖХП) поступився місцем концепції стеатотичної хвороби печінки (Steatotic Liver Disease – SLD), більш загальному поняттю, що охоплює різні етіологічні форми стеатозу. МАСХП визначають як стеатоз печінки у поєднанні з хоча б одним із п’яти кардіометаболічних факторів ризику. Термін «стеатогепатит» визнано важливим патофізіологічним поняттям оновленої номенклатури.
! Вагомою новацією є введення самостійної категорії MetALD (метаболічно-алкогольної хвороби печінки), що описує пацієнтів із верифікованою МАСХП, які додатково вживають алкоголь.
Ця категорія відображає реальність клінічної практики, у якій чітке розмежування (або/або) алкогольного та метаболічного ураження нерідко не відповідає дійсності. Осіб, у яких відсутні метаболічні параметри і причина стеатозу досі нез’ясована, класифікують як криптогенний варіант SLD.
Описана зміна парадигми принципово важлива: замість виключення алкоголю як єдиного діагностичного критерію акцент тепер на розгляді метаболічного синдрому як системної основи захворювання з можливим мультифакторним внеском різних шкідливих чинників.
Алкоголь як ко-фактор перебігу МАСХП: актуальність для України
Алкоголь є модифікатором перебігу практично всіх хронічних захворювань печінки, однак щодо МАСХП його роль особливо вагома. Навіть помірне або епізодичне споживання алкоголю у пацієнтів із метаболічним стеатозом значно підвищує токсичне навантаження на паренхіму печінки, підтримує хронічний цитоліз, прискорює фіброгенез і сприяє розвитку когнітивних порушень. Не існує чіткої безпечної межі споживання алкоголю за будь-якої хронічної патології печінки (Altamirano J., 2013).
! Особливу актуальність ця проблема набуває в контексті сучасної ситуації в Україні. За даними соціологічного опитування ВООЗ (листопад 2024 р.), алкоголь упродовж останніх 12 місяців вживали до 78% дорослих українців, а середня частота вживання становила 46 днів на рік (67 – для чоловіків і 27 – для жінок). Тобто майже кожного тижня печінка страждає від токсичного навантаження.
На формуванні цих показників позначилося шестирічне безперервне стресове навантаження: спершу пандемія COVID‑19, згодом повномасштабна війна. Наслідком хронічного стресу є зростання частоти компенсаторних поведінкових стратегій, зокрема збільшення вживання алкоголю, що суттєво ускладнює перебіг метаболічних захворювань печінки у значної частки населення.
Необхідно враховувати, що офіційна статистика традиційно відображає меншу поширеність алкогольних уражень, ніж є насправді: за даними ВООЗ, у країнах ЄС 41% смертей від захворювань печінки пов’язаний з алкоголем, тоді як 46% мають невизначену етіологію, частина якої, вірогідно, також обумовлена алкоголем (Altamirano J., 2013; EASL, 2018).
Ще одним недооціненим джерелом токсичного навантаження є ендогенний етанол – продукт метаболічної активності кишкової мікробіоти. У пацієнтів із порушенням якісного і кількісного складу мікробіому, що закономірно спостерігається при метаболічних розладах, продукція ендогенного спирту суттєво зростає.
Отже, реальна частота комбінованих (метаболічно-алкогольних) уражень печінки суттєво вища за традиційно визнану. Дихотомічний поділ уражень на алкогольні та неалкогольні в клінічній практиці значною мірою застарів, і впровадження категорії MetALD засвідчує адекватніше відображення клінічної реальності.
МАСХП як системна патологія: коморбідні стани і генетичні детермінанти
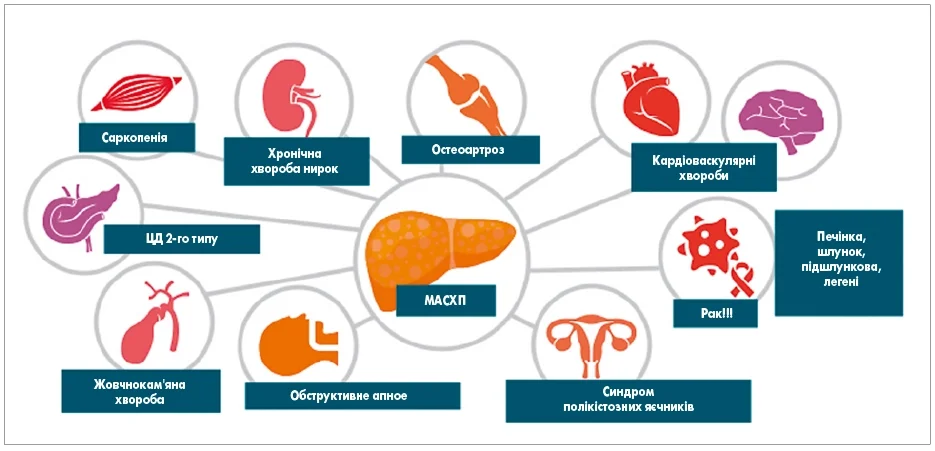
Згідно із сучасною концепцією, МАСХП розглядають не як ізольоване ураження печінки, а як орган-специфічний прояв системного метаболічного захворювання. Асоційовані стани охоплюють цукровий діабет (ЦД) 2-го типу, серцево-судинну патологію, хронічну хворобу нирок, синдром полікістозних яєчників, обструктивне апное сну, саркопенію, остеоартроз та гепатоцелюлярну карциному (рис. 1). Окрім кардіологів і ендокринологів, до його лікування нині активно долучаються нефрологи та акушери-гінекологи, що свідчить про краще розуміння системного характеру метаболічного синдрому (Zobair M., 2019).
Рис. 1. МАСХП та її асоційовані стани
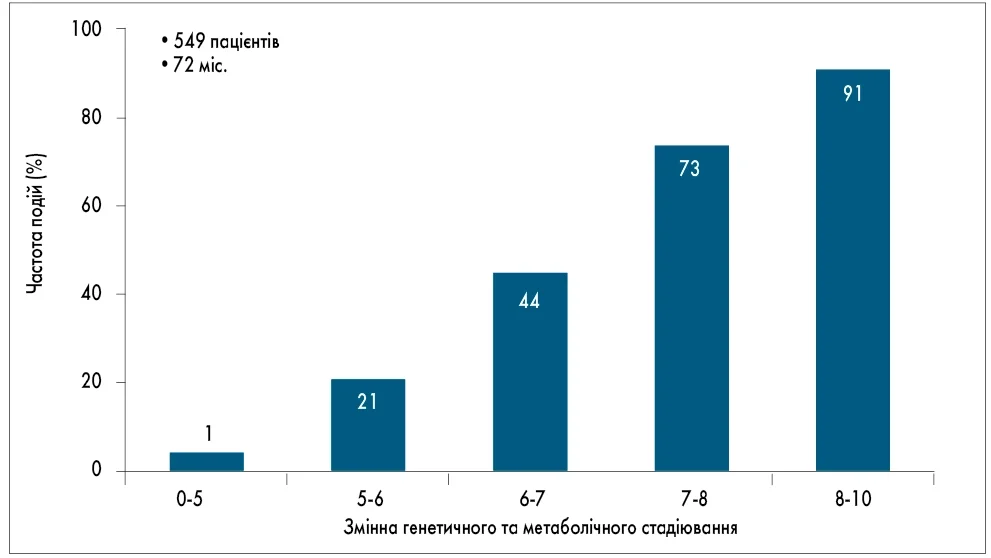
Гетерогенність фенотипів МАСХП значною мірою зумовлена генетичними факторами. Показовими є дані дослідження в когорті UK Biobank (549 пацієнтів із прогресуючим МАСХП, 72-місячний термін спостереження): сформований інтегральний GEMS-коефіцієнт, що враховує генетичні та метаболічні показники, демонструє чіткий зв’язок із ризиком прогресування захворювання. До генотипів, що провокують її виникнення, зараховують варіанти PNPLA3 I148M, TM6SF2 E167K та MBOAT7; до захисних – HSD17B13, MARC1 та CIDEB (рис. 2; Pennisi G., 2022). Пацієнти, що є носіями захисних варіантів, мають нижчий ризик метаболічних ускладнень навіть за наявності надмірної маси тіла, тоді як у решти фіброгенез прискорений незалежно від ступеня ожиріння.
Рис. 2. Дослідження ролі генетичних факторів і ризику прогресування частоти несприятливих подій, пов’язаних із печінкою (за Pennisi G., 2022)
! Важливим предиктором тяжкого фіброзу є обтяжений сімейний анамнез: ризик цирозу, асоційованого зі стеатогепатитом, достовірно вищий у пацієнтів, близькі родичі яких мали цироз печінки, асоційований з неалкогольним стеатогепатитом (НАСГ) (Caussy C., 2017).
Серед факторів ризику прогресування фіброзу – ЦД 2-го типу, ожиріння, дисліпідемія, метаболічний синдром і синдром полікістозних яєчників (Chalasani N., 2018).
Принципи терапії МАСХП
Корекція способу життя залишається невіддільним і першочерговим компонентом лікування МАСХП на будь-якій стадії. Зниження маси тіла на 5-10% супроводжується гістологічно підтвердженим регресом стеатозу, а зменшення маси на 10% і більше може призводити до регресу стеатогепатиту і ранніх стадій фіброзу. Обов’язковими елементами немедикаментозної корекції є раціональне харчування (обмеження насичених жирів, простих вуглеводів, фруктози), дозована фізична активність (щонайменше 150 хв/тиждень помірної аеробної активності) та нормалізація режиму сну, оскільки хронічне недосипання через низку нейроендокринних механізмів сприяє переїданню, зниженню фізичної активності та прогресуванню інсулінорезистентності.
! Фармакологічна терапія показана пацієнтам зі стадією фіброзу F2 і вище або за наявності факторів ризику швидкого прогресування.
В оновлених у 2024 р. рекомендаціях об’єднаної робочої групи європейських асоціацій із вивчення захворювання, діабету та ожиріння (EASL-EASD-EASO) визначено такі основні фармакологічні опції для пацієнтів із МАСХП/метаболічно асоційованим стеатогепатитом (МАСГ) без цирозу (F0-F3): агоністи рецепторів GLP‑1, інгібітори SGLT‑2, метформін (при ШКФ > 30 мл/хв) (EASL, 2024).
GLP‑1-агоністи та інсулінорезистентність як ключова терапевтична мішень
Патогенетичною основою МАСХП у переважної більшості пацієнтів є інсулінорезистентність і пов’язане з нею хронічне запалення. Дисбаланс між лептином та адипонектином, підвищення секреції прозапальних цитокінів (TNF-α, IL‑6, MCP‑1, резистину), ліпотоксичність вільних жирних кислот і активація зірчастих клітин із подальшим фіброгенезом є взаємопов’язаними ланками єдиного патогенетичного каскаду (Gastaldelli A., 2024).
Глюкагоноподібний пептид‑1 (GLP‑1) є новою терапевтичною мішенню, що виходить за межі традиційних метаболічних показань. Агоністи рецепторів GLP‑1 реалізують свою дію через численні органи-мішені: підшлункову залозу (стимуляція секреції інсуліну, пригнічення глюкагону, захист β-клітин), печінку (зниження продукції глюкози), м’язову тканину (підвищення засвоєння глюкози), шлунково-кишковий тракт (уповільнення шлункової евакуації) та головний мозок (нейропротекторні ефекти, регуляція апетиту) (Armstrong M.J., 2017). Раніше ці препарати призначали лише пацієнтам із ЦД або переддіабетом; нині вони схвалені також для хворих із надмірною масою тіла та МАСХП без діабету.
! Суттєвою проблемою у разі тривалого застосування агоністів GLP‑1 є розвиток саркопенії – значущої втрати м’язової маси, яка спостерігається практично у всіх пацієнтів і погано піддається корекції.
Ще однією клінічно важливою проблемою є синдром зворотного набору маси у разі відміни препарату, що відбувається переважно завдяки жировій тканині. Зазначені обмеження обумовлюють пошук раціональних стратегій поєднання GLP‑1-агоністів із фізичними навантаженнями і підходами, що зберігають м’язову масу.
Субклінічний гіпотиреоз і внутрішньопечінкова тиреорезистентність
Субклінічний гіпотиреоз є поширеним і нерідко недооціненим ко-фактором розвитку і прогресування МАСХП. Ця проблема особливо актуальна для України, де дві третини регіонів є йододефіцитними, а гіпотиреоз частіше трапляється у жінок. Виявлення субклінічного гіпотиреозу потребує ендокринологічного супроводу і корекції замісною терапією (L-тироксин 0,5-1 мкг/кг маси тіла).
Водночас нерідко системний еутиреоз не призводить до нормалізації жирового обміну в печінці внаслідок феномену внутрішньопечінкової тиреорезистентності – зниження чутливості гепатоцитів до тиреоїдних гормонів з допомогою блокування тиреоїдних рецепторів β-типу (THR-β).
Ацетальдегідний механізм ураження печінки: сліпа зона стандартної гепатопротекції
У разі поєднаного метаболічно-алкогольного ураження печінки центральну патогенетичну роль відіграє ацетальдегід – основний токсичний метаболіт етанолу. Послідовність шкідливих подій: виснаження детоксикаційної системи алкогольдегідрогенази (АДГ) та ацетальдегіддегідрогенази (АЛДГ) із порушенням балансу НАД+/НАДН; формування оксидативного стресу внаслідок накопичення реактивних форм кисню; відкладання жиру в гепатоцитах; зниження рівня ендогенного глутатіону; пошкодження і загибель гепатоцитів; активація зірчастих клітин із подальшим фіброгенезом (Carlo А., 2025; Mello T., 2008).
Принципово важливо, що жоден із сучасних нових засобів терапії МАСХП не має документально підтвердженого прямого впливу на метаболізм ацетальдегіду. Ацетальдегідна ланка ураження залишається недосяжною для стандартних гепатопротективних підходів, навіть найбільш сучасних. Це суттєва невирішена терапевтична проблема під час ведення хворих із MetALD або будь-яким захворюванням печінки на тлі вживання алкоголю.
Метадоксин у терапії комбінованих уражень печінки
! Метадоксин є препаратом із доведеним впливом саме на ацетальдегідну ланку ушкодження, що вигідно відрізняє його від традиційних гепатопротекторів.
На фармацевтичному ринку України метадоксин представлений препаратом Ліверія® ІС у формі таблеток. Механізм дії метадоксину реалізується через декілька взаємодоповнювальних шляхів.
По-перше, препарат активує АДГ і АЛДГ, прискорюючи двоетапне окислення етанолу: перетворення етанолу на ацетальдегід і подальший розклад ацетальдегіду до нетоксичного ацетату. Результатом є прискорена елімінація етанолу та ацетальдегіду з організму, що знижує їхній токсичний вплив.
По-друге, метадоксин підвищує синтез глутатіону, зменшує оксидативний стрес і стабілізує мембрани гепатоцитів, що клінічно виражається в зупинці цитолізу та нормалізації рівня трансаміназ.
По-третє, препарат чинить протизапальну та антифібротичну дію: блокує прозапальні медіатори TNF-α та IL‑6, пригнічує активацію зірчастих клітин, уповільнюючи прогресування фіброзу незалежно від етіології ураження.
По-четверте, метадоксин виявляє нейропротективні властивості: підвищує рівень ГАМК та ацетилхоліну, відновлює рівень АТФ, що клінічно проявляється гальмуванням розвитку печінкової енцефалопатії, покращенням когнітивних функцій та зменшенням астенічного синдрому (Guerrini I., 2023).
Отже, МАСХП є однією з визначальних нозологій сучасної гастроентерології та гепатології. Оновлена номенклатура, що вводить категорію MetALD, відображає реальну клінічну ситуацію, у якій поєднані метаболічно-алкогольні ураження значно поширеніші за офіційну статистику. Ацетальдегідна ланка ураження залишається сліпою зоною стандартної гепатопротекції. На відміну від сучасних таргетних препаратів, жоден з яких не чинить прямого впливу на метаболізм ацетальдегіду, метадоксин (Ліверія® ІС) при MetALD і при хронічній патології печінки з алкогольним компонентом посідає самостійну терапевтичну позицію, активуючи систему АДГ/АЛДГ і забезпечуючи елімінацію токсичних метаболітів.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (79) 2026 р.