17 квітня, 2026
Печінка під тиском сучасного способу життя: метаболічні виклики та можливості нутритивної підтримки
 Печінка перебуває під постійним метаболічним тиском, зумовленим сучасним способом життя. Надлишкове харчування, низька фізична активність й інші чинники формують хронічне метаболічне навантаження на організм. У цих умовах печінка, ключовий орган метаболічної регуляції, виконує важливу роль у підтриманні метаболічного гомеостазу. Особливої значущості набуває необхідність збереження та підтримання оптимального структурно-функціонального стану гепатоцитів.
Печінка перебуває під постійним метаболічним тиском, зумовленим сучасним способом життя. Надлишкове харчування, низька фізична активність й інші чинники формують хронічне метаболічне навантаження на організм. У цих умовах печінка, ключовий орган метаболічної регуляції, виконує важливу роль у підтриманні метаболічного гомеостазу. Особливої значущості набуває необхідність збереження та підтримання оптимального структурно-функціонального стану гепатоцитів.
Якими є метаболічні виклики для печінки та як можна підтримати її функцію за допомогою нутритивної корекції, розглянемо в цій статті в зручному для сприйняття форматі «запитання – відповідь».
Як сучасні метаболічні епідемії змінюють уявлення про природу хронічних захворювань та яке місце серед них посідає ураження печінки?
В епоху метаболічних викликів, зумовлену епідеміями ожиріння, інсулінорезистентності (ІР) та цукрового діабету (ЦД) 2 типу, змінюється розуміння хронічних неінфекційних захворювань. Доведено, що порушення енергетичного та ліпідного обміну має системний характер і активує міжорганні взаємодії за участю жирової тканини, печінки, скелетних м’язів, підшлункової залози, серця й нирок. У межах цієї метаболічної осі патологія проявляється не окремими ізольованими захворюваннями, а взаємопов’язаними клінічними станами.
Цю концепцію відображено в настанові Європейського товариства атеросклерозу (European Atherosclerosis Society, 2025), де запроваджено поняття системних метаболічних захворювань (СМЗ) [12]. СМЗ визначають як багатофакторний стан, який формується на тлі надлишкової та дисфункціональної адипозності й поступово зумовлює мультиорганну дисфункцію. До ключових проявів СМЗ належать ІР, предіабет і ЦД 2 типу, ожиріння, метаболічно-асоційована стеатотична хвороба печінки (МАСХП), атерогенна дисліпідемія, артеріальна гіпертензія, хронічна хвороба нирок [12].
МАСХП, гепатологічний прояв СМЗ, нині є найрозповсюдженішим хронічним захворюванням печінки в світі: її поширеність становить 30-38% у загальній популяції та перевищує 60-70% серед осіб з ожирінням або ЦД 2 типу [18]. У глобальному масштабі це означає, що ознаки СМЗ уже спостерігаються в >1 млрд людей, а збереження сучасних тенденцій може спричинити подальше стрімке зростання його поширеності найближчими десятиліттями [6, 17].
МАСХП – суто гепатологічна проблема? Чи вона може впливати на розвиток інших системних захворювань?
Печінка є одним із ключових регуляторів метаболічного гомеостазу. Вона координує обмін вуглеводів, ліпідів і білків, підтримує енергетичний баланс, бере участь у детоксикації ендогенних й екзогенних сполук, інтегрує сигнали між жировою тканиною, скелетними м’язами, підшлунковою залозою та серцево-судинною системою. Саме тому навіть субклінічні порушення функції печінки здатні впливати на загальний стан організму.
Нині доведено, що МАСХП – не лише локальне ураження печінки, а й важливий маркер і патогенетичний чинник СМЗ. Накопичення жиру в гепатоцитах супроводжується активацією запальних та метаболічних сигнальних шляхів, порушенням ліпідного обміну, змінами секреції гепатокінів і прозапальних медіаторів, що призводить до формування ІР, атерогенної дисліпідемії, хронічного системного низькоінтенсивного запалення. Внаслідок цього МАСХП дедалі частіше розглядають як один із чинників розвитку різноманітних позапечінкових ускладнень: атеросклерозу, ішемічної хвороби серця, серцевої недостатності [2], ендокринопатій [3], хронічної хвороби нирок [4], неопластичних уражень [14]. З огляду на системний характер цих процесів профілактика розвитку багатьох тяжких кардіометаболічних, ниркових й онкологічних ускладнень значною мірою пов’язана із запобіганням виникненню та прогресуванню МАСХП.
Які фактори провокують розвиток МАСХП та її позапечінкових ускладнень?
Печінка як ключовий орган метаболічної регуляції постійно перебуває під тиском чинників сучасного життя: нераціональне харчування з надлишком калорій, низька фізична активність, вживання алкоголю, дія лікарських препаратів і ксенобіотиків; усе це створює складний комплекс метаболічних і запальних сигналів, що порушують нормальне функціонування печінки.
Сучасні уявлення про патогенез МАСХП ґрунтуються на концепції багатофакторного механізму, коли розвиток захворювання зумовлюється одночасною дією декількох взаємопов’язаних метаболічних і запальних процесів [3]. Центральним елементом патогенезу є порушення ліпідного гомеостазу (рис. 1). За ІР та дисфункції жирової тканини зростає потік вільних жирних кислот (ЖК) до печінки, активується ліпогенез de novo та знижується ефективність β-окиснення ЖК, що зумовлює накопичення тригліцеридів у гепатоцитах і розвиток стеатозу.
![Рис. 1. Багатофакторний патогенез МАСХП: значущість порушення ліпідного обміну [3] Рис. 1. Багатофакторний патогенез МАСХП: значущість порушення ліпідного обміну [3]](/multimedia/userfiles/images/2026/ZU_4_2026/ZU_04_2026_st18_pic1.webp) Рис. 1. Багатофакторний патогенез МАСХП: значущість порушення ліпідного обміну [3]
Рис. 1. Багатофакторний патогенез МАСХП: значущість порушення ліпідного обміну [3]
Однак патологічний процес не обмежується накопиченням ліпідів. Надлишок ЖК і їхніх токсичних метаболітів запускає каскад ушкоджувальних процесів: оксидативний та ендоплазматичний стрес, мітохондріальну дисфункцію, активацію запальних сигнальних шляхів [3, 9]. Важливу роль також відіграють зміна кишкового мікробіому та підвищена проникність кишкового бар’єра, що спричиняє надходження ендотоксинів до портального кровотоку, а також підтримує системне запалення.
Як порушення ліпідного обміну призводить до ушкодження гепатоцитів при МАСХП?
Порушення ліпідного обміну за наявності МАСХП спричиняє не лише стеатоз, а й ліпотоксичність. Це стан, за якого надлишок ЖК та їхніх токсичних метаболітів безпосередньо ушкоджує гепатоцити. Одним із важливих наслідків ліпотоксичності є ушкодження клітинних мембран: продукти пероксидації змінюють їхній склад і проникність, що порушує транспорт ліпідів та внутрішньоклітинні процеси; крім того, спостерігаються активація запальних реакцій, загибель гепатоцитів (рис. 2) [8].
Сучасні дослідження розширюють ці уявлення через концепцію «пан-ліпотоксичності», відповідно до якої порушення накопичення, розподілу та транспорту ліпідів може спричиняти дисфункцію різних органів і формувати системний характер метаболічних захворювань [5]. Саме тому підтримання оптимального складу мембранних фосфоліпідів розглядається як один із напрямів метаболічної підтримки.
![Рис. 2. Роль ліпотоксичності в розвитку та прогресуванні МАСХП [8] Рис. 2. Роль ліпотоксичності в розвитку та прогресуванні МАСХП [8]](/multimedia/userfiles/images/2026/ZU_4_2026/ZU_04_2026_st18_pic2.webp) Рис. 2. Роль ліпотоксичності в розвитку та прогресуванні МАСХП [8]
Рис. 2. Роль ліпотоксичності в розвитку та прогресуванні МАСХП [8]
Що таке мембранні фосфоліпіди і яку роль вони відіграють у підтриманні структури та функції гепатоцитів?
Мембранні фосфоліпіди становлять основу клітинних мембран і формують своєрідний каркас, що визначає цілісність, плинність та функціональну активність гепатоцитів. Від стану мембран залежить робота ендоплазматичного ретикулуму, мітохондрій, транспортних систем і сигнальних шляхів, пов’язаних із ліпідним обміном [13]. Окрім структурної ролі, мембранні фосфоліпіди регулюють активність ліпогенних сигнальних шляхів і беруть участь у транспорті ліпідів із печінки.
Одним із ключових представників цієї групи є фосфатидилхолін (ФХ) – один з основних мембранних фосфоліпідів гепатоцитів. Він забезпечує стабільність і плинність клітинних мембран, бере участь у формуванні ліпопротеїнів дуже низької щільності, які транспортують тригліцериди з печінки до периферичних тканин, а також впливає на сигнальні шляхи запалення й апоптозу [15]. Особливу увагу привертають ненасичені форми ФХ, які мають високу мембранотропність і здатні вбудовуватися в ушкоджені мембрани гепатоцитів. Показано, що застосування ненасиченого ФХ асоціюється зі зниженням ризику фіброзу, покращенням функціональних показників печінки та нормалізацією ліпідного профілю в пацієнтів із МАСХП [10, 11]. Цей факт пояснюють здатністю ФХ відновлювати мембранну плинність, зменшувати оксидативний стрес, моделювати запальні сигнальні шляхи та покращувати транспорт ліпідів із печінки.
Холін, ФХ і лецитин: чим вони відрізняються та хто з них має найбільше значення для підтримання функції печінки?
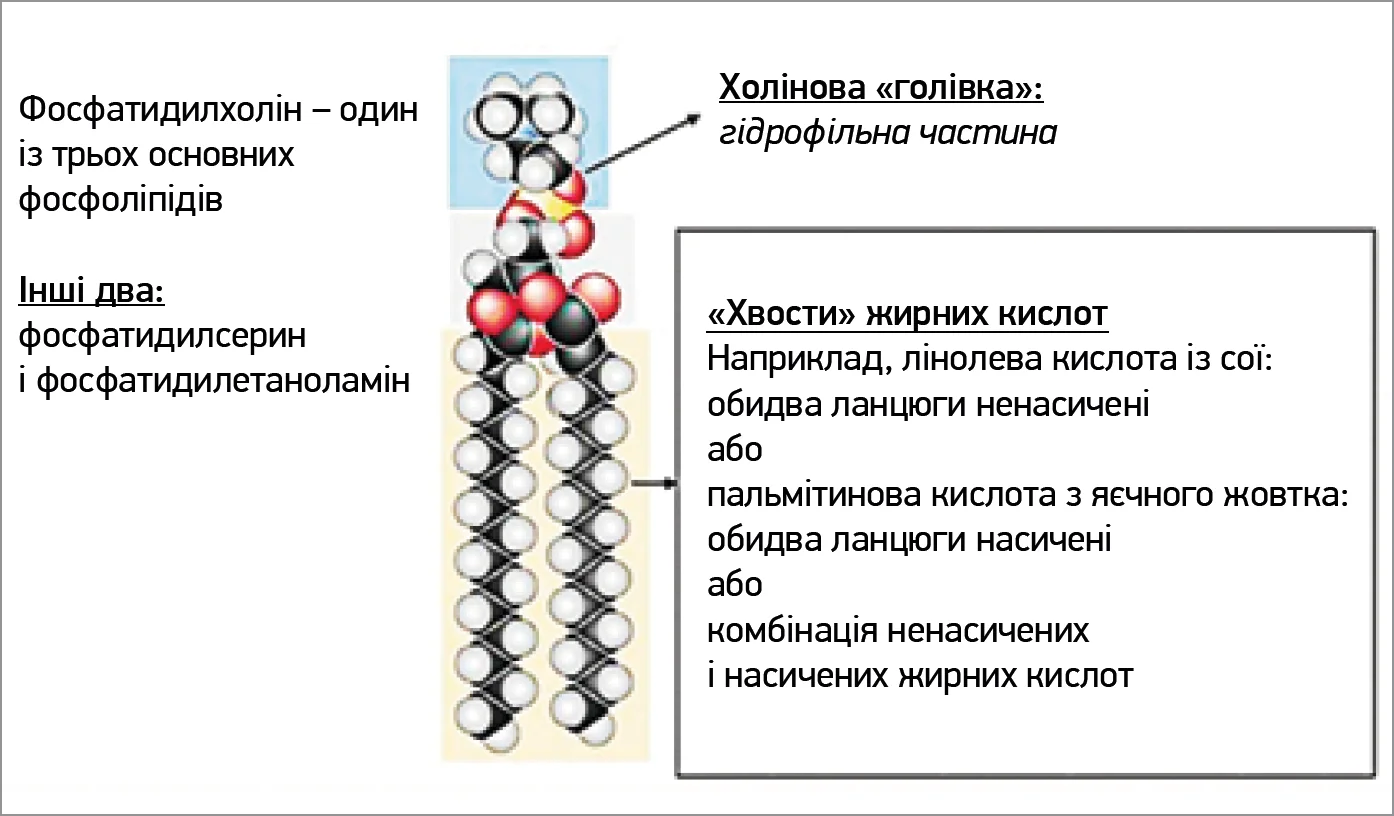
Холін, ФХ і лецитин – взаємопов’язані, але різні хімічні сполуки. Холін є поживною речовиною, яку організм отримує переважно з їжею і використовує як субстрат для синтезу фосфоліпідів, насамперед ФХ [13]. ФХ, складний фосфоліпід, має «голівку», утворену холіном, і «хвіст», сформований ЖК (рис. 3). Особливу біологічну активність мають його ненасичені форми, які містять поліненасичені ЖК, завдяки чому ФХ краще інтегрується у фосфоліпідні мембранні шари [10, 11]. Лецитин – природна суміш фосфоліпідів (фосфатидилсерин, фосфатидилетаноламін, фосфатидилінозитол), основним компонентом якої є ФХ [7]. Отже, холін – попередник ФХ, а лецитин – його природне джерело. Найбільше значення для підтримання нормального стану клітинних мембран гепатоцитів має ненасичений ФХ.
Чи підтверджена ефективність поліненасиченого ФХ (ПФХ) у клінічних дослідженнях?
Ефективність ПФХ доведена в різних клінічних випробуваннях. Нещодавно опубліковано дані великомасштабного дослідження, проведеного в умовах реальної клінічної практики, в якому проаналізовано результати лікування 22 705 хворих на МАСХП, з яких 7093 отримували ПФХ протягом 24 тиж [11]. Установлено, що прийом ПФХ сприяє поліпшенню функціональних печінкових проб: уже через 12 тиж у групі ПФХ зафіксували вираженіше зниження рівня АСТ порівняно із представниками контрольної групи, які не отримували гепатопротекторного засобу (середнє зниження від початкового рівня: -6,25 проти -2,41 Од/л відповідно; р=0,039). Спостерігали тенденцію до зниження АЛТ і достовірне зменшення загального білірубіну як через 12 тиж, так і через 24 тиж лікування (рис. 4).
![Рис. 4. Динаміка печінкових проб на тлі прийому ПФХ [11] Рис. 4. Динаміка печінкових проб на тлі прийому ПФХ [11]](/multimedia/userfiles/images/2026/ZU_4_2026/ZU_04_2026_st18_pic4.webp) Рис. 4. Динаміка печінкових проб на тлі прийому ПФХ [11]
Рис. 4. Динаміка печінкових проб на тлі прийому ПФХ [11]
Спостерігалися позитивні зміни в ліпідному обміні. В підгрупі пацієнтів із МАСХП і гіперліпідемією через 12 тиж терапії зафіксовано достовірне зниження вмісту холестерину ліпопротеїнів низької щільності – ХС ЛПНЩ (середнє зниження: -0,23 ммоль/л), тоді як у контрольній групі цей показник зріс на 0,13 ммоль/л (р=0,044) (рис. 5).
![Рис. 5. Динаміка рівня ХС ЛПНЩ на тлі прийому ПФХ [11] Рис. 5. Динаміка рівня ХС ЛПНЩ на тлі прийому ПФХ [11]](/multimedia/userfiles/images/2026/ZU_4_2026/ZU_04_2026_st18_pic5.webp) Рис. 5. Динаміка рівня ХС ЛПНЩ на тлі прийому ПФХ [11]
Рис. 5. Динаміка рівня ХС ЛПНЩ на тлі прийому ПФХ [11]
Важливі дані отримано щодо фіброзу печінки. Через 24 тиж у пацієнтів, які отримували ПФХ, спостерігали достовірне зниження індексу FIB‑4, тоді як у контрольній групі цей показник, навпаки, мав тенденцію до підвищення (-0,12 проти +0,11; p=0,034), що свідчить про ймовірне уповільнення прогресування фіброзу на тлі ПФХ (рис. 6).
![Рис. 6. Динаміка індексу FIB‑4 на тлі прийому ПФХ [11] Рис. 6. Динаміка індексу FIB‑4 на тлі прийому ПФХ [11]](/multimedia/userfiles/images/2026/ZU_4_2026/ZU_04_2026_st18_pic6.webp) Рис. 6. Динаміка індексу FIB‑4 на тлі прийому ПФХ [11]
Рис. 6. Динаміка індексу FIB‑4 на тлі прийому ПФХ [11]
Отже, застосування ПФХ асоціюється з покращенням печінкових ферментів, ліпідного профілю та індексу фіброзу FIB‑4, що підкреслює його роль як компонента комплексної терапії МАСХП.
Чи зареєстрований в Україні препарат, що містить ПФХ?
На полицях вітчизняних аптек представлений Ліволін Форте (фірма-виробник – Mega Lifesciences), до складу якого входить лецитин у вигляді ПФХ. Кожна капсула Ліволіну Форте містить 300 мг лецитину (35% ПФХ – форми фосфоліпідів, які мають високу мембранотропність і здатні інтегруватися в клітинні мембрани гепатоцитів) [1].
Особливістю Ліволіну Форте є його комбінований склад, у якому ПФХ поєднаний з комплексом метаболічно активних вітамінів: тіамін, рибофлавін, піридоксин, ціанокобаламін, нікотинамід, що беруть участь у процесах енергетичного обміну, синтезі фосфоліпідів і регуляції метаболізму ліпідів [1]. Ліволін Форте також містить вітамін Е, який виконує роль антиоксиданта та сприяє захисту клітинних мембран в умовах оксидативного стресу [1]. Дози зазначених компонентів дещо нижчі за верхні допустимі рівні добового споживання, але достатні для покриття підвищеної потреби організму в умовах метаболічного навантаження.
Яким пацієнтам може бути рекомендована нутритивна підтримка з використанням ПФХ (Ліволін Форте)?
Ліволін Форте може бути рекомендований пацієнтам із метаболічним навантаженням на печінку на тлі супутніх ІР, ожиріння, дисліпідемії, ЦД 2 типу, а також хворим на МАСХП [1]. Його можна застосовувати у випадках незбалансованого харчування, регулярного вживання алкоголю чи тривалого прийому медикаментів, які створюють додаткове метаболічне навантаження на печінку [1].
У таких ситуаціях Ліволін Форте доцільно використовувати як складову комплексного підходу разом із корекцією способу життя. Важливо, що засіб зручний у застосуванні й економічний, оскільки містить декілька метаболічно активних компонентів в одному комплексі та вживається лише по 1 капсулі/добу. Рекомендований курс становить 1-2 міс, після чого за потреби його можна періодично повторювати [1].
Висновки
Сучасний спосіб життя створює постійний метаболічний тиск на організм, формуючи передумови для розвитку СМЗ і МАСХП. Центральною ланкою цих процесів є порушення ліпідного обміну та ліпотоксичність, які зумовлюють ушкодження мембран гепатоцитів. У цих умовах важливим компонентом комплексної терапії є нутритивна підтримка, зокрема використання ПФХ. Клінічні дані свідчать, що застосування ПФХ сприяє покращенню функціональних показників печінки, ліпідного профілю та маркерів фіброзу. Ліволін Форте, який містить лецитин (35% ПФХ) у поєднанні з метаболічно активними вітамінами, є доцільним засобом нутритивної підтримки за умов метаболічного навантаження на печінку.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 4 (615), 2026 р



 Дуда О.К.
Дуда О.К.