14 грудня, 2024
Замісна ферментна терапія в пацієнтів із зовнішньосекреторною недостатністю підшлункової залози та цукровим діабетом: досвід паризької клініки
Екзокринна недостатність підшлункової залози (EНПЗ) є типовим проявом цукрового діабету (ЦД), вторинного щодо захворювань підшлункової залози, також відомого як панкреатогенний діабет. Цей тип діабету здатен уражати осіб із гострим або хронічним панкреатитом, раком підшлункової залози або муковісцидозом. Панкреатогенний діабет може становити до 10% усіх причин діабету (щонайменше серед госпіталізованих пацієнтів). Однак клінічно значуща ЕНПЗ також може спостерігатися в 11-30% осіб із ЦД 1 типу, у 8% пацієнтів із ЦД 2 типу, а також у хворих зі спадковими формами ЦД у молодому віці (MODY).
Запідозрити EНПЗ слід у пацієнтів із типовими симптомами, як-от біль у животі, втрата маси тіла, порушення травлення або часті епізоди гіпоглікемії. ЕНПЗ пов’язана з такими ускладненнями, як втрата маси тіла, діарея та стеаторея, недоїдання, остеопороз і підвищений серцево-судинний ризик. Багато досліджень показали, що замісна терапія ферментами підшлункової залози (ЗФТ) має як короткочасні, так і довгострокові вигоди. В короткостроковій та середній перспективі ЗФТ покращує усмоктування жиру й азоту, зумовлює збільшення маси тіла, зменшує частоту та тяжкість шлунково-кишкових симптомів. У довгостроковій перспективі ЗФТ покращує якість життя, знижує ризик переломів кісток, поліпшує виживаність у пацієнтів із хронічним панкреатитом або раком підшлункової залози.
У пацієнтів із панкреатогенним діабетом може розвинутися т. зв. злоякісний діабет, якому притаманні швидкі зміни рівня глюкози, ризики тяжкої гіпоглікемії та гіперглікемії. Проведено лише декілька досліджень щодо впливу ЗФТ на глікемічний контроль. Було показано, що ЗФТ покращує секрецію глюкагоноподібного пептиду‑1 (GLP‑1) і глюкозозалежного інсулінотропного поліпептиду (GIP), тому очікується позитивний вплив ЗФТ на спорожнення шлунка та концентрацію глюкози в крові після їди. Дійсно, дослідження в пацієнтів із муковісцидозом продемонстрували, що ЗФТ нормалізує секрецію GLP‑1, сповільнює спорожнення шлунка, знижує постпрандіальний рівень глюкози в крові без повної його нормалізації. В іншому дослідженні, проведеному в пацієнтів із фіброзно-калькульозним панкреатитом, ЗФТ пов’язувалася зі зниженням HbA1c і постпрандіального рівня глюкози в плазмі.
L. Alexandre-Heymann і співавт. нещодавно опублікували результати ретроспективного дослідження типу «випадок – контроль», під час проведення якого вивчали вплив початку ЗФТ на глікемічний контроль в осіб із діабетом та ЕНПЗ в умовах реальної клінічної практики. Дослідження проводилося на базі відділення діабетології лікарні Кошен (Париж). Автори порівняли пацієнтів з ЕНПЗ і діабетом, яким призначили ЗФТ, із хворими з діабетом, котрі не отримували ЗФТ. До групи ЗФТ включали всіх пацієнтів, у яких діабет був діагностований щонайменше за 3 міс до початку ЗФТ і котрі мали тяжку ЕНПЗ, що визначалася як вміст фекальної еластази FEC <100 мкг/г. До контрольної групи відбирали пацієнтів, які не отримували ЗФТ, крім того, вони були зіставними за віком, статтю із хворими групи ЗФТ (1:1). Також пацієнти контрольної групи повинні були мати діагноз діабету та відносно низький рівень FEC (<300 мкг/г), щоб бути клінічно схожими з пацієнтами групи ЗФТ.
Клінічні дані для аналізу отримували з електронних медичних записів пацієнтів. Основним результатом, який цікавив дослідників, був вплив ЗФТ на частоту та тяжкість гіпоглікемії. Як вторинні наслідки ЗФТ вивчали вплив на шлунково-кишкові розлади, рівень глікованого гемоглобіну (HbA1c), індекс маси тіла (ІМТ) і на загальну успішність лікування діабету.
До кожної групи було включено по 48 осіб (73% учасників – чоловіки). Пацієнти, котрі отримували ЗФТ, частіше мали панкреатогенний діабет, ніж особи контрольної групи, які частіше мали діагнози ЦД 1 або 2 типу. Хворі, котрі отримували ЗФТ, мали нижчий ІМТ, ніж контрольна група; ≈75% пацієнтів в обох групах отримували інсулін. Рівень FEC був нижчим, а шлунково-кишкові розлади, аномалії підшлункової залози (за даними комп’ютерної томографії), а також дефіцит вітаміну А частіше спостерігалися в хворих, що отримували ЗФТ, ніж у контрольній групі.
Вплив ЗФТ на перебіг і лікування діабету
Гіпоглікемія
Часта та/або тяжка гіпоглікемія була звичайним явищем в обох групах (по 15 пацієнтів, 31%); вона виявилася поширенішою в пацієнтів, котрі отримували інсулін. Симптоми гіпоглікемії зменшилися у 8 осіб після початку застосування ЗФТ, крім того, в 7 контрольних хворих протягом періоду спостереження. Отже, в цьому дослідженні ЗФТ, імовірно, не була основною причиною покращення симптомів гіпоглікемії. Зменшення частоти та тяжкості гіпоглікемії могло бути наслідком покращення лікування діабету в умовах стаціонару. Слід зазначити, що після початку застосування ЗФТ симптоми гіпоглікемії зменшилися в 4 із 5 пацієнтів із панкреатогенним діабетом (80%), але лише в 40% хворих з іншими типами ЦД.
HbA1c
Рівень HbA1c знизився після початку застосування ЗФТ в обох групах (рис. 1). Середній рівень HbA1c знизився із 8,8 до 7,6% у групі ЗФТ і з 8,2 до 7,6% у контрольній групі (p=0,0029; p=0,0038 відповідно). Проте різниця між групами не була значущою. Зниження HbA1c в обох групах протягом періоду дослідження, ймовірно, також зумовлювалося ефектом госпіталізації та покращення лікування діабету.
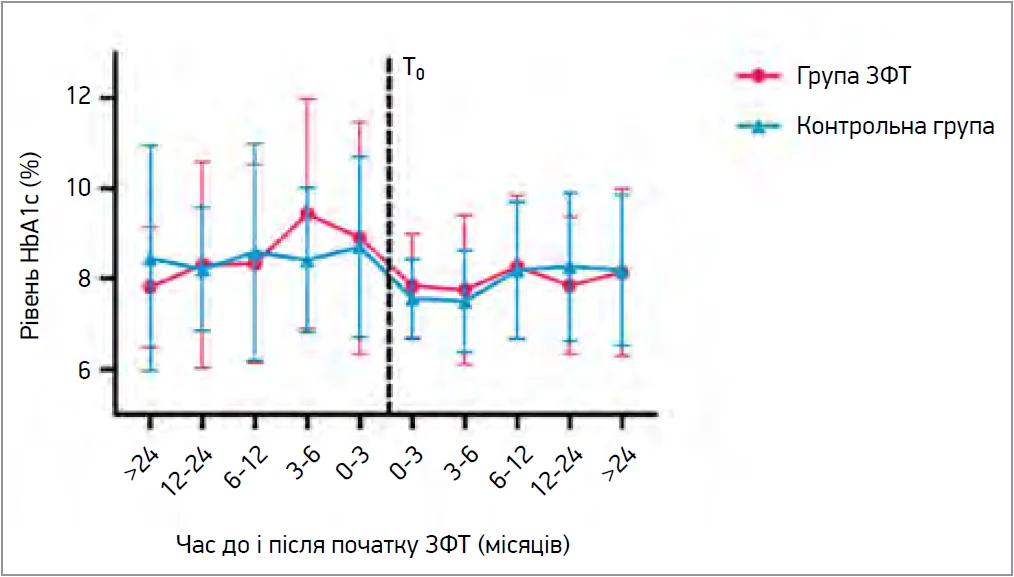 Рис. 1. Динаміка змін рівня HbA1c у групах пацієнтів із діабетом, які отримували та не отримували ЗФТ
Рис. 1. Динаміка змін рівня HbA1c у групах пацієнтів із діабетом, які отримували та не отримували ЗФТ
Гіперглікемія після початку застосування ЗФТ
Ризик гіперглікемії через покращення всмоктування компонентів їжі під дією ферментів часто згадується як побічний ефект ЗФТ у пацієнтів із діабетом. У дослідженні цей ризик не підтвердився, оскільки не спостерігалося жодного випадку кетоацидозу чи госпіталізації через гіперглікемію після початку застосування ЗФТ. Приблизно 20% пацієнтів мали незначну гіперглікемію після початку застосування ЗФТ. Серед них ≈80% мусили збільшити дозу інсуліну на декілька одиниць. 1 пацієнту розпочали лікування інсуліном через супутню інфекцію, але він згодом повернувся до свого звичайного лікування. Ще 1 хворий через гіперглікемію розпочав приймати репаглінід. Отже, призначення ЗФТ є безпечним для пацієнтів із діабетом. Після початку застосування ЗФТ слід порадити пацієнтам ретельніше контролювати рівень глюкози в крові протягом перших декількох тижнів, щоб у разі потреби адаптувати лікування.
Вплив ЗФТ на шлунково-кишкові розлади
На початку спостереження шлунково-кишкові розлади мали 44% осіб, яким призначили ЗФТ (6 пацієнтів із ЦД 1 типу, 6 хворих із панкреатогенним діабетом, 1 учасник із MODY-HNF1B, 1 – із медикаментозно-індукованим діабетом, 9 – з невизначеним типом діабету), а також 21% пацієнтів контрольної групи (5 осіб із ЦД 1 типу, 3 хворих – із ЦД 2 типу, 1 – із посттрансплантаційним діабетом, 1 – із невизначеним типом діабету). Ці симптоми зменшилися у 80% пацієнтів після початку застосування ЗФТ і лише в 20% хворих контрольної групи протягом періоду спостереження (p=0,002) (рис. 2). Отже, ЗФТ чинить сприятливий вплив на шлунково-кишкові розлади в пацієнтів із діабетом.
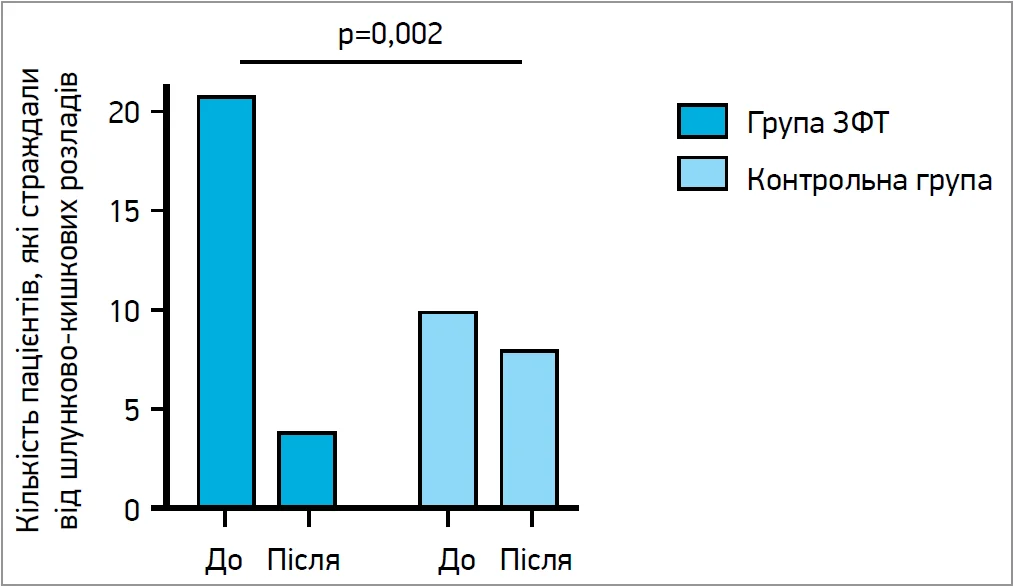 Рис. 2. Вплив ЗФТ на шлунково-кишкові розлади
Рис. 2. Вплив ЗФТ на шлунково-кишкові розлади
Вплив ЗФТ на масу тіла
Початок застосування ЗФТ раніше асоціювався зі збільшенням маси тіла (здебільшого в пацієнтів із панкреатогенним діабетом) через покращення всмоктування поживних речовин. Дослідження цього не підтверджує. ІМТ був стабільним протягом періоду дослідження в обох групах. Слід зауважити, що він не збільшився після початку застосування ЗФТ. У пацієнтів із хронічним панкреатитом ІМТ мав тенденцію до збільшення після початку застосування ЗФТ із 24,9 до 25,8 кг/м2, але різниця виявилася статистично незначущою, імовірно, через недостатню вибірку.
Порівняння пацієнтів із рекомендованим і недостатнім дозуванням ЗФТ
В Європейських настановах із лікування хронічного панкреатиту рекомендовано призначення ЗФТ із розрахунку 40 000-80 000 ОД ліпази під час основних прийомів їжі та половину дози під час перекусів. У групі ЗФТ 14 пацієнтам не призначили рекомендовану дозу. Вони приймали в середньому 25 000 ОД ліпази під час прийому їжі та належали до підгрупи недостатнього дозування (НД). 34 пацієнти належали до підгрупи рекомендованого дозування (РД). Симптоми гіпоглікемії зменшилися в 55% (6 з 11) пацієнтів групи РД і в 50% (2 із 4) хворих групи НД. Шлунково-кишкові розлади покращилися у 87% (13 із 15) пацієнтів групи РД і в 50% (2 із 4) хворих групи НД. ІМТ був стабільним протягом періоду дослідження в обох підгрупах. Із 9 осіб, котрі мали помітну гіперглікемію після початку застосування ЗФТ, 3 хворих належали до підгрупи НД. Динаміка зміни рівня глікованого гемоглобіну не відрізнялася між підгрупами.
Отже, зміни ІМТ, HbA1c та вплив лікування на гіпоглікемію виявилися схожими в пацієнтів, які отримували РД панкреатичних ферментів або дозу нижче рекомендованої. Частота гіперглікемії після початку застосування ЗФТ також була схожою між підгрупами. Полегшення шлунково-кишкових розладів частіше спостерігали в пацієнтів, які отримували вищу дозу ЗФТ, але різниця з підгрупою НД була несуттєвою. Цей результат збігається з тим, що було описано в літературі: вплив ЗФТ на короткострокові та середньострокові симптоми не корелює з дозуванням ферментів, за винятком шлунково-кишкових розладів. Адаптація дози ЗФТ із метою полегшення шлунково-кишкових симптомів шляхом підбору дози на прийом їжі виглядає можливим варіантом задля покращення якості життя пацієнтів [14].
Висновки
- Призначення ЗФТ було безпечним для хворих із різними типами діабету, навіть незважаючи на те, що в ≈1/5 пацієнтів після початку застосування ЗФТ довелося посилити медикаментозну терапію діабету.
- Призначення ЗФТ асоціювалося зі значущим полегшенням шлунково-кишкових розладів.
- Динаміка HbA1c та ІМТ була схожою між групами пацієнтів із діабетом, які отримували та не отримували ЗФТ.
- Вищі дози ЗФТ зазвичай пов’язувалися із сильнішим впливом на шлунково-кишкові розлади.
Джерело: Alexandre-Heymann L., Yaker F., Lassen P. B., Dubois-Laforgue D., Larger E. Pancreatic enzyme replacement therapy in subjects with exocrine pancreatic insufficiency and diabetes mellitus: a real-life, case-control study.
Diabetol Metab Syndr. 2024 Feb 9; 16 (1): 39.
doi: 10.1186/s13098-024-01265-4.
Реферативний огляд підготував Ігор Петренко
Довідка «ЗУ»
В Україні панкреатичні ферменти європейського виробництва представлені, зокрема, лікарськими засобами лінійки Мезим від компанії «Берлін-Хемі»:
- Мезим® капсули 10 000 або 25 000 – у капсулах із кишковорозчинними мінітаблетками;
- Мезим® форте 10 000 або 20 000 – у таблетках із кишковорозчинною оболонкою.
Число в назві означає ферментну активність препарату в одиницях Європейської фармакопеї за ліпазою. Ліпаза є найкритичнішим ферментом підшлункової залози, за дефіциту якого розвивається стеаторея. Крім ліпази, всі препарати Мезим містять амілазу та протеазу. Кишковорозчинна оболонка лікарських форм Мезиму захищає від передчасного вивільнення ферментів у шлунку та сприяє їхньому надходженню до цільового відділу шлунково-кишкового тракту – дванадцятипалої кишки. Дозування препарату визначається ступенем порушення травлення та складом раціону, зокрема споживанням жирів. Для полегшення застосування (наприклад, дітям, пацієнтам літнього віку, при порушенні ковтання) тверді капсули можна розкрити та проковтнути лише їхній вміст (мінітаблетки), запиваючи невеликою кількістю рідини. Простота дозування й альтернативні лікарські форми дозволяють підібрати терапію кожному пацієнту вже на першому візиті, коли після оцінки скарг та об’єктивного обстеження в лікаря виникає підозра на зовнішньосекреторну недостатність підшлункової залози.
Медична газета «Здоров’я України 21 сторіччя» № 21 (583), 2024 р




