11 січня, 2022
Ведолізумаб у лікуванні виразкового коліту: результати досліджень
Виразковий коліт (ВК) – хронічне імуноопосередковане запальне захворювання кишечнику (ЗЗК) невідомої етіології, поширеність якого у світі, на жаль, продовжує зростати (L. Du, C. Ha, 2020). ВК характеризується персистуючим подразненням слизової оболонки товстої кишки, що призводить до формування на ній ерозій та/або виразок і появи таких симптомів, як абдомінальний біль, діарея та наявність крові у калі. Хоча етіологія ВК залишається невідомою, існує міжнародний консенсус щодо того, що запалення слизової оболонки кишечнику асоціюється з генетичною схильністю та порушенням регуляторних механізмів, за допомогою яких різноманітні фактори навколишнього середовища впливають на мукозальну імунну систему кишечнику. Враховуючи складну патофізіологію ВК та визначну роль, яку відіграють у ній імунологічні механізми, наразі увага вчених та лікарів прикута до тих можливостей, що відкриваються сьогодні у лікуванні цього захворювання завдяки появі інноваційних біологічних препаратів – у першу чергу, селективного кишкового імуносупресанту ведолізумабу. Цей унікальний за своїм механізмом дії біологічний препарат являє собою гуманізовані моноклональні антитіла, котрі специфічно зв’язуються з експресованим переважно на лімфоцитах класу Т-хелперів трансмембранним рецептором – інтегрином α4β7 і, як наслідок, інгібують їх адгезію до адгезивних молекул адресину слизової оболонки кишечнику 1 (MAdCAM-1). У цьому огляді стисло висвітлено дані щодо оцінки ефективності та безпеки ведолізумабу у клінічних випробуваннях, обсерваційних дослідженнях та метааналізах.
Планування належного лікування пацієнта із ВК залежить від стадії, поширеності уражень та ступеню тяжкості захворювання. Патологічна стадія ВК зазвичай класифікується як активна фаза (при якій пацієнти скаржаться на наявність крові у калі, а ендоскопічне дослідження виявляє втрату судинного малюнку, пухкість слизової оболонки, наявність на ній ерозій та/або виразок) або як ремісія (при якій крові у калі немає, а ендоскопія визначає повторну появу судинного малюнку та зникнення ерозій та/або виразок на слизовій оболонці). Крім того, ВК можна класифікувати за типом залежно від поширеності уражень слизової оболонки кишечнику: проктит, дистальний коліт, лівобічний коліт, панколіт. За критеріями Трулов-Віттса виділяють легкий, середньотяжкий та тяжкий перебіг ВК відповідно до частоти дефекації та кров’янистих випорожнень і наявності системних симптомів (лихоманки, тахікардії, анемії тощо). Ендоскопічна оцінка тяжкості ураження слизової оболонки кишечнику має вирішальне значення для оцінки результату лікування ВК. У клінічних дослідженнях широко використовується ендоскопічна частина шкали клініки Мейо: загоєння слизової оболонки оцінюється у 0 балів (нормальна слизова оболонка чи неактивне захворювання) або в 1 бал (легке захворювання: еритема, послаблення судинного малюнку та пухкість слизової оболонки).
Сучасна терапія ВК
Препарати 5-аміносаліцилової кислоти (5-АСК) ефективні в індукції та підтриманні ремісії у пацієнтів із ВК. Кортикостероїди з потужними протизапальними властивостями також ефективно індукують ремісію. Азатіоприн та 6-меркаптопурин сприяють попередженню рецидиву в пацієнтів із ВК у фазі ремісії, особливо в осіб, які залежать від стероїдів, або у тих хворих, в яких неможливо підтримувати ремісію на тлі застосування препаратів 5-АСК (C.W. Ko et al., 2019; D.T. Rubin et al., 2019; K. Matsuoka et al., 2018). Згідно з метааналізами та даними рандомізованих контрольованих досліджень (РКД), застосування інгібіторів фактору некрозу пухлини α (ФНП-α) – інфліксимабу (P. Rutgeerts et al., 2005; A.C. Ford et al., 2011) та адалімумабу (A.C. Ford et al., 2011; W.J. Sandborn et al., 2012) – відіграє важливу роль в індукції ремісії у пацієнтів зі стероїд-рефрактерним або стероїдозалежним ВК середньотяжкого чи тяжкого перебігу. Проте показано, що приблизно у 60% пацієнтів, які реагували на лікування інгібіторами ФНП-α, може відзначатися вторинна втрата відповіді протягом приблизно 5-річного періоду подальшого спостереження (C. Ma et al., 2015). Більш того, враховуючи, що ці препарати були асоційовані з підвищеним ризиком розвитку серйозних небажаних явищ (НЯ), включаючи інфекції, значна частка пацієнтів потребує альтернативних варіантів лікування, які характеризуються кращим профілем безпеки (рис. 1). 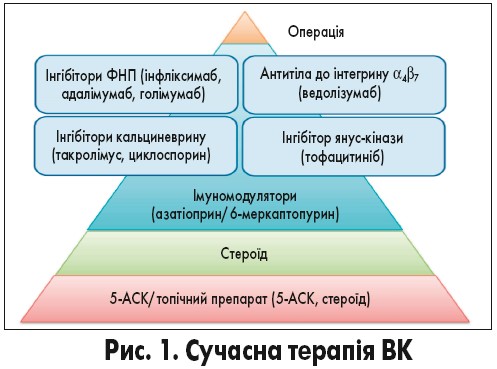
Оперативне втручання може знадобитися для уникнення життєво небезпечних ускладнень ВК у тому випадку, коли у пацієнта розвивається тяжке захворювання, рефрактерне до медикаментозної терапії (P. Rutgeerts et al., 2005; A.C. Ford et al., 2011). Крім того, кандидатами на оперативне втручання можуть бути ті пацієнти, якість життя яких значно порушена через симптоми захворювання, його позакишкові прояви або побічні ефекти медикаментозної терапії (A. Dignass et al., 2012). Усунення цих симптомів після операції може покращити якість життя пацієнтів (J.T. Heikens et al., 2012).
Механізм дії ведолізумабу
Ведолізумаб, який по суті є гуманізованими моноклональними антитілами IgG1, селективно інгібує взаємодію між інтегрином α4β7 і MAdCAM-1. Завдяки цьому він попереджає переміщення Т-лімфоцитів із крові до запаленої тканини кишечнику, тим самим зменшуючи місцеве запалення (G. Fiorino et al., 2010; F. Cominelli, 2013; N. Takatsu et al., 2020; рис. 2). При цьому ведолізумаб не інгібує адгезію Т-лімфоцитів до адгезивних молекул судинних клітин 1 (VCAM-1) та не зв’язується з інтегринами α4β1 і αEβ7 і не пригнічує їхню функцію.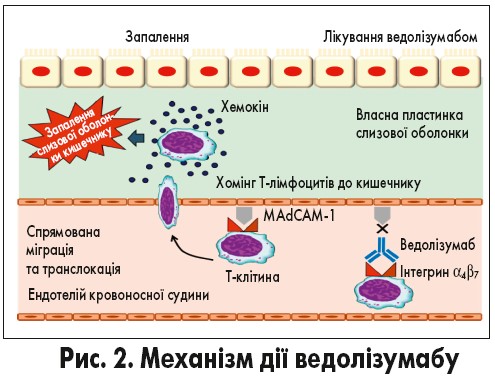
Рандомізовані контрольовані дослідження
Дослідження I фази
У 2000 р. Feagan та співавт. виконали РКД Ib/IIa фази, до якого було включено 29 пацієнтів із середнім та тяжким перебігом ВК. Пацієнти були розподілені на групи для застосування гуманізованих моноклональних антитіл до α4β7 або плацебо (у вигляді однократних доз). Було встановлено, що 40% пацієнтів у групі гуманізованих моноклональних антитіл до α4β7 (0,5 мг/кг) досягли глибокої ремісії, у той час як у групі плацебо ремісії не досяг жоден пацієнт.
Дослідження II фази
У 2005 р. Feagan та співавт. провели багатоцентрове подвійне сліпе плацебо-контрольоване дослідження з вивчення ефективності антитіл до α4β7 (MLN02) за участю 181 пацієнта з активним ВК. У ході цього дослідження пацієнтам із середньотяжким або тяжким перебігом захворювання призначали 0,5 мг/кг MLN02, 2 мг/кг MLN02 або плацебо внутрішньовенно (в/в) на 1-й та 29-й день. Через 6 тижнів після початку терапії частота досягнення ремісії були вищою у групах лікування, ніж у групі плацебо, що стосується як клінічної ремісії (0,5 мг/кг – 33%, 2 мг/кг – 32%, плацебо – 14%; p=0,03), так і ендоскопічної (0,5 мг/кг – 28%, 2 мг/кг – 12%, плацебо – 8%; p=0,007).
У 2012 р. Parikh та співавт. виконали подальше РКД II фази, метою якого було визначення оптимальної дози препарату. Участь у дослідженні взяли 47 пацієнтів із ВК, які були рандомізовано розподілені на групи для отримання ведолізумабу (n=38): 2 мг/кг (n=13), 6 мг/кг (n=14), 10 мг/кг (n=11) або плацебо (n=9) на 1-й, 15-й, 29-й та 85-й дні. Період подальшого спостереження становив 253 дні. Дози ведолізумабу, що застосовувалися у цьому дослідженні, були вищими, а інтервал між введенням доз коротшим, ніж у попередніх дослідженнях. У період між 29-м та 253-м днем частота клінічної відповіді у групах ведолізумабу перевищувала 50% порівняно з лише 22-33% у групі плацебо. У пацієнтів з активним захворюванням у вихідному стані частота клінічної ремісії варіювала від 53 до 79% у групах ведолізумабу порівняно з 25-50% у групі плацебо. Також було показано зниження рівнів кальпротектину у випорожненнях у групах ведолізумабу порівняно з групою плацебо (A. Parikh et al., 2012). Під час періоду подальшого спостереження у більшої частки пацієнтів, які отримали лікування ведолізумабом, було продемонстровано клінічну відповідь (A. Parikh et al., 2013).
Дослідження III фази
У 2013 р. Feagan та співавт. повідомили про результати подвійного сліпого плацебо-контрольованого РКД GEMINI 1, яке оцінювало ефективність, безпеку та переносимість застосування ведолізумабу (MLN002) як препарату для індукції ремісії та підтримувальної терапії у пацієнтів із середьотяжким та тяжким перебігом ВК. Пацієнти були рандомізовані на групи для отримання однократної дози ведолізумабу (300 мг в/в) або плацебо на 1-й та 15-й дні. На 6-му тижні були виявлені статистично значущі відмінності між групами ведолізумабу та плацебо щодо показників частоти клінічної відповіді (47,1 порівняно з 25,5%; p<0,001), клінічної ремісії (16,9 порівняно з 5,4%; p=0,001) та загоєння слизової оболонки (40,9 порівняно з 24,8%; p=0,001). Пацієнти, в яких на 6-му тижні була констатована відповідь, а також пацієнти, котрі відповіли на відкриту індукційну терапію ведолізумабом, були включені у дослідження підтримувальної терапії та отримували ведолізумаб або плацебо кожні 4 або 8 тижнів до настання 52-го тижня. У групах ведолізумабу було продемонстровано кращі результати порівняно з групою плацебо за показниками частоти досягнення клінічної ремісії (ведолізумаб кожні 8 тижнів – 41,8%; p<0,001; кожні 4 тижні – 44,8%; p<0,001; плацебо – 15,9%) та загоєння слизової оболонки кишечнику. Відкрите довготривале розширене дослідження продемонструвало вищу частоту досягнення клінічної відповіді (98%) та ремісії (90%) на 248-му тижні у пацієнтів, які відповіли на індукційну терапію та завершили участь у дослідженні GEMINI 1 (E.V. Loftus et al., 2017).
У 2019 р. Motoya та співавт. виконали подвійне РКД III фази з оцінки ефективності ведолізумабу в японських пацієнтів із середньотяжким або тяжким перебігом ВК. Пошукові аналізи результатів дослідження GEMINI 1 засвідчили, що вища ефективність може бути отримана за умови більшої тривалості індукційної терапії (B.G. Feagan et al., 2013). У цьому популяційному дослідженні первинною кінцевою точкою була клінічна відповідь на 10-му тижні для індукційної фази та клінічна ремісія на 60-му тижні – для підтримувальної фази. Загалом до індукційної фази було включено 292 пацієнта; з них 83 пацієнта досягли відповіді на застосування ведолізумабу і згодом були включені до фази підтримувальної терапії. Показники частоти клінічної відповіді на 10-му тижні склали 39,6 та 32,9% у групах ведолізумабу та плацебо відповідно (скориговане відношення шансів (ВШ)=1,37; 95% довірчий інтервал (ДІ) 0,779-2,399; p=0,2722). У підтримувальній фазі частота клінічної ремісії на 60-му тижні була достовірно вищою у групі ведолізумабу – 56,1% порівняно з групою плацебо, де цей показник становив 31% (скориговане ВШ=2,88; 95% ДІ 1,168-7,108; p=0,021).
Систематичний огляд та метааналіз
Систематичний огляд та метааналіз вищезгаданих РКД був проведений Mosli та співавт. (2015), а також Bickston та колегами (2014). В об’єднаному аналізі, що включав дані пацієнтів із активним ВК, ведолізумаб продемонстрував перевагу перед плацебо в плані індукції ремісії (ВР=0,86; 95% ДІ 0,8-0,91), клінічної відповіді (ВР 0,82; 95% ДІ 0,75-0,91) та ендоскопічної ремісії (ВР 0,82; 95% ДІ 0,75-0,91). Більш того, підтримувальна терапія ведолізумабом дозволяла досягти кращої клінічної ремісії (ВР 2,73; 95% ДІ 1,78-4,18) та ендоскопічної ремісії (ВР 2,71; 95% ДІ 1,88-3,93), ніж застосування плацебо.
Докази, отримані в умовах реальної клінічної практики
З моменту схвалення застосування ведолізумабу регуляторними органами у 2014 р. він широко застосовується у клінічній практиці для лікування ВК та хвороби Крона (ХК), і зараз вже доступні дані щодо багатьох випадків покращення стану пацієнтів. Так, у 2018 р. Schreiber та співавт. повідомили про результати систематичного огляду з метааналізом оцінки реальної ефективності та безпеки ведолізумабу у пацієнтів із ВК або ХК. Показники частоти досягнення клінічної ремісії у разі лікування ВК складали 24% на 6-му тижні (95% ДІ 13-41) та 32% на 14-му тижні (95% ДІ 27-39) та збільшилися до 39% через 6 міс (95% ДІ 30-48) та до 46% через 12 міс (95% ДІ 37-56). Показники частоти клінічної відповіді при лікуванні ВК становили 43% на 6-му тижні (95% ДІ 38-49), 56% – на 14-му тижні (95% ДІ 50-62) та 52% через 12 міс (95% ДІ 37-65). У пацієнтів із ВК показники частоти клінічної ремісії, досягнутої без застосування кортикостеродів, складали 14% на 6-му тижні (95% ДІ 6-32), 26% на 14-му тижні (95% ДІ 20-34) та 32% через 6 міс (95% ДІ 21-45); при цьому через 12 міс цей показник збільшився до 42% (95% ДІ 31-53). Через 12 міс частота загоєння слизової оболонки кишечнику у пацієнтів із ВК варіювала від 33 до 77%. У пацієнтів із ВК, які раніше не отримували біологічної терапії, частота досягнення клінічної ремісії становила 51% на 14-му тижні (95% ДІ 40-62) та 61% через 12 міс (95% ДІ 48-72). Підгрупові аналізи, до яких були включені дані пацієнтів, які раніше не отримували біологічної терапії та яким було вперше призначено ведолізумаб, показали, що частота досягнення ремісії у них була істотно вищою порівняно з такою у загальній популяції пацієнтів (S. Schreiber et al., 2018; A. Amiot et al., 2016; D.C. Baumgart et al., 2016; U. Kopylov et al., 2017; E. Shelton et al., 2015; E.E. Vivio et al., 2016; M.A. Samaan et al., 2017).
N. Narula та співавт. (2018) повідомили про результати відкритої оцінки ефективності ведолізумабу в рамках функціонування багатоцентрового госпітального консорціуму US VICTORY (Vedolizumab for Health Outcomes in Inflammatory Bowel Disease). У 321 пацієнта із ВК, у більшості з яких (71%) виявилося неефективним лікування інгібітором ФНП, через 12 міс. кумулятивна частота клінічної ремісії склала 51%, а ендоскопічної – 41%. Відповідні показники частоти досягнення безстероїдної та глибокої ремісії становили 37 та 30% відповідно. При проведенні багатоваріантних аналізів виявилося, що попереднє застосування інгібіторів ФНП-α було асоційовано зі зниженою ймовірністю досягнення клінічної ремісії (ВР 0,53; 95% ДІ 0,38-0,75) та ендоскопічної (ВР 0,51; 95% ДІ 0,29-0,88). Загальна кумулятивна частота виконання колектомії протягом 12 міс. становила 13%, при цьому у пацієнтів, які раніше не отримували терапії інгібіторами ФНП, спостерігалися нижчі показники (2%) порівняно з хворими, які вже отримували ці препарати (19%).У своїй сукупності ці відкриті дослідження демонструють, що ведолізумаб, імовірно, є більш ефективним у лікуванні пацієнтів із ВК, які раніше не отримували інгібітори ФНП, а також свідчать, що багато пацієнтів, котрі вже отримували лікуваннями цими препаратами, на тлі лікування ведолізумабом з часом також можуть досягти позитивних клінічних та ендоскопічних результатів.
Фармакокінетика, фармакодинаміка та імуногенність
Фармакокінетичний профіль ведолізумабу у пацієнтів із ЗЗК та у здорових добровольців був оцінений за допомогою двохкамерної моделі (паралельні компоненти лінійної та нелінійної елімінації; M. Rosario et al., 2015). Лінійний період напіввиведення ведолізумабу, згідно з оцінками, становив 25,5 дня, а значення лінійного кліренсу – 0,159 л/добу при ВК та 0,155 л/добу при ХК (R. Battat et al., 2019; M. Rosario et al., 2015). На підставі об’єднаних популяційних даних з програми GEMINI 1 як предиктори прискореного кліренсу ведолізумабу були ідентифіковані низька концентрація альбуміну та дуже велика маса тіла (M.T. Osterman et al., 2019). Проведені в умовах реальної клінічної практики дослідження засвідчили, що ці фактори дійсно є клінічно значущими (B. Al-Bawardy et al., 2019; E. Dreesen et al., 2018; L. Pouillon et al., 2019).
У програмі GEMINI 1 імуногенність ведолізумабу була низькою; 3,7% пацієнтів мали щонайменше один позитивний результат тестування на наявність антитіл до ведолізумабу, отриманий у будь-який момент часу, а 1% пацієнтів постійно отримував позитивний результат тестування на антитіла до ведолізумабу (B.G. Feagan et al., 2013).
Докази, що наразі з’являються, підтверджують припущення про те, що сироваткові концентрації ведолізумабу асоціюються з його ефективністю. Дослідження GEMINI 1 показало, що показники частоти клінічної відповіді та досягнення ремісії були вищими при підвищених концентраціях ведолізумабу (B.G. Feagan et al., 2013). Аналіз залежності «експозиція – відповідь» у клінічних дослідженнях з оцінки ефективності терапії ведолізумабом виявив, що на 6-му тижні показники ймовірності досягнення клінічної ремісії, клінічної відповіді та загоєння слизової оболонки кишечнику у пацієнтів із ВК збільшилися на 31, 34 та 43% з 1-го по 4-й квартиль концентрації відповідно (B.G. Feagan et al., 2013; M. Rosario et al., 2017; R. Maria et al., 2014). Декілька когортних досліджень також продемонстрували позитивний взаємозв’язок між сироватковими концентраціями ведолізумабу та ефективністю (E. Dreesen et al., 2018; W. Yacoub et al., 2018; M. Rosario et al., 2017; R. Maria et al., 2014; N. Williet et al., 2017; B. Ungar et al., 2018; A. Yarur et al., 2017).
Загальна безпека
У пілотному дослідженні GEMINI 1 (B.G. Feagan et al., 2013), у ході якого 374 пацієнти із ВК були рандомізовані для в/в введення ведолізумабу в дозі 300 мг (n=225) або плацебо (n=149), не спостерігалося важливих відмінностей між досліджуваними групами щодо НЯ, про які повідомлялося найчастіше. Частота серйозних інфекцій у групах ведолізумабу та плацебо була співставною. Не було зафіксовано жодного випадку розвитку прогресуючої мультифокальної лейкоенцефалопатії (ПМЛ), а також значущих відмінностей між досліджуваними групами у показниках аналізів крові або результатах оцінки печінкових функцій. Лікування ведолізумабом не збільшувало загальну кількість лімфоцитів у периферичній крові.
S.J. Bickston та співавт. (2014) виконали систематичний огляд даних 4 досліджень із помірною та високою якістю доказів. Було встановлено, що частота НЯ у пацієнтів, які отримували лікування ведолізумабом, співставна з такою у пацієнтів, які отримували плацебо. Два дослідження оцінювали пацієнтів, у яких виникло як мінімум одне НЯ (A. Parikh et al., 2012; B.G. Feagan et al., 2013). Згідно з результатами об’єднаного аналізу цих досліджень (n=941), не відзначалося статистично достовірної різниці у частоті виникнення НЯ між пацієнтами, котрі отримували ведолізумаб, та тими, що отримували плацебо. Щонайменше одне НЯ було зафіксовано у 79% пацієнтів, яким вводили ведолізумаб, порівняно з 80% пацієнтів, які отримували плацебо (ВР 0,99; 95% ДІ 0,93-1,07). У двох дослідженнях повідомлялося про вибуття з дослідження через виникнення НЯ як кінцевої точки (A. Parikh et al., 2012; B.G. Feagan et al., 2013). Об’єднаний аналіз цих досліджень показав, що припинення застосування препарату через НЯ відбувалося навіть рідше у пацієнтів, яким вводився ведолізумаб, ніж у пацієнтів, які отримували плацебо. Подальший об’єднаний аналіз даних 1122 пацієнтів, які брали участь у 3 дослідженнях (B.G. Feagan et al., 2005; A. Parikh et al., 2012; B.G. Feagan et al., 2013), продемонстрував, що ведолізумаб не був достовірно асоційований зі збільшеною ймовірністю розвитку виникнення серйозних НЯ. Частота серйозних НЯ склала 12% в обох групах пацієнтів, котрі отримували ведолізумаб та плацебо (ВР 1,01; 95% ДІ 0,73-1,42). НЯ, про які часто повідомлялося у дослідженні Parikh та співавт. (2012): головний біль, погіршення перебігу ВК, інфекція верхніх дихальних шляхів та назофарингіт; у жодного пацієнта не було виявлено системних опортуністичних інфекцій або новоутворень. Частими НЯ, про які повідомлялося у дослідженні GEMINI 1 (2013), були погіршення перебігу ВК, головний біль, назофарингіт, артралгія, інфекція верхніх дихальних шляхів, нудота, кашель, анемія, біль у животі, стомлюваність та грип. Серйозні НЯ включали загострення коліту, інфузійну реакцію з ангіонабряком, нудоту та блювання (B.G. Feagan et al., 2005), а також компресійні переломи грудних хребців та гастродуоденіт (A. Parikh et al., 2012). У жодному з 4-х досліджень не повідомлялося про випадки ПМЛ (B.G. Feagan et al., 2000; B.G. Feagan et al., 2005; A. Parikh et al., 2012; B.G. Feagan et al., 2013).
Дані щодо безпеки ведолізумабу (травень 2009 – червень 2013), отримані в ході 6 досліджень, були узагальнені Colombel та співавт. (2017). Застосування ведолізумабу не асоціювалося з підвищеним ризиком виникнення будь-якої інфекції. Про серйозні клостридіальні інфекції, сепсис та туберкульоз повідомлялося рідко (≤0,6% пацієнтів). Випадків розвитку ПМЛ не спостерігалося. Незалежні фактори ризику розвитку серйозної інфекції при ВК включали попередню неефективну терапію інгібіторами ФНП-α (ВР 1,99; 95% ДІ 1,16-3,42; p=0,0122) та використання наркотичних аналгетиків (ВР 2,68; 95% ДІ 1,57-4,58; p=0,0003). Про пов’язані з інфузією реакції повідомлялося у ≤5% випадків у кожному дослідженні. Таким чином, було зроблено висновок про те, що об’єднані дані клінічних досліджень за участі 2932 пацієнтів із середньотяжким та тяжким активним ВК або ХК надали дані про відсутність значущих проблем із безпекою, асоційованих з лікуванням ведолізумабом. Ведолізумаб має кишково-селективний механізм дії, його застосування не характеризується підвищенням ризику розвитку серйозних системних опортуністичних інфекцій або інших частих ускладнень.
Schreiber та співавт. (2018) розглянули результати оцінки безпеки ведолізумабу в реальній практиці, отримані у 46 дослідженнях. Вони узгоджувалися з даними досліджень GEMINI, і нових неочікуваних сигналів щодо безпеки використання виявлено не було. Представлені дані щодо безпеки підтримують позитивний довгостроковий профіль «ризик – користь», яким характеризується ведолізумаб у лікуванні ЗЗК.
Місце в терапії
Мережевий метааналіз РКД за участі пацієнтів із ВК визначив, що ведолізумаб оцінюється як високоефективний засіб для індукції клінічної ремісії та загоєння слизової оболонки кишечнику в пацієнтів, які раніше не отримували біологічної терапії (S. Singh et al., 2018). Що стосується пацієнтів, яким раніше вже призначалися біологічні препарати, то застосування у них ведолізумабу наразі підтримується доказами низької якості. На відміну від оцінюваних препаратів, терапія ведолізумабом не характеризується підвищенням ризику виникнення інфекцій. Allamneni та співавт. (2018) виконали двоспрямоване когортне дослідження серед пацієнтів із середньотяжким та тяжким ВК, у ході якого порівняли показники частоти клінічної відповіді на індукційну терапію ведолізумабом порівняно з інфліксимабом. Це дослідження виявило загалом чисельно вищу частку пацієнтів, які відповіли на застосування ведолізумабу порівняно з індукцією ремісії інфліксимабом серед пацієнтів, які мали середньотяжкий або тяжкий перебіг активного ВК. Однак при корекції результатів за часом між індукцією та оцінкою клінічної відповіді показники частоти досягнення клінічної відповіді були аналогічними. Ключовою відмінністю між групами була вища частота відповіді серед пацієнтів, що раніше отримували інгібітор ФНП, у групі ведолізумабу.
Нещодавно було проведене проспективне пряме порівняльне дослідження VARSITY, у ході якого ведолізумаб порівнювали з адалімумабом (S. Schreiber et al., 2020). Воно являло собою подвійне сліпе багатоцентрове дослідження IIIb фази з подвійним маскуванням та активним контролем. До участі були включені пацієнти із середньотяжким та тяжким перебігом активного ВК, у лікуванні яких виявилися неефективними інші традиційні методи (NCT02497469). Попереднє застосування інгібіторів ФНП мало місце у 25% пацієнтів. Пацієнти були рандомізовані у співвідношенні 1:1 для отримання в/в інфузій ведолізумабу (300 мг)/плацебо у вигляді підшкірних ін’єкцій або в/в інфузій плацебо/підшкірних ін’єкцій адалімумабу (160/80/40 мг). Загалом 769 пацієнтів були рандомізовано розподілені для проведення терапії ведолізумабом (n=383) або адалімумабом (n=386) у 330 центрах 37 країн світу та отримали щонайменше одну дозу досліджуваного препарату. На 52-му тижні у пацієнтів із групи ведолізумабу було продемонстровано достовірно вищі показники частоти досягнення клінічної ремісії (первинна кінцева точка) та загоєння слизової оболонки; обидва досліджувані препарати були загалом безпечними та добре переносилися. Результати дослідження можуть змінити позиціонування ведолізумабу як препарату першої або другої лінії терапії найближчим часом.
Висновки
Таким чином, ефективність ведолізумабу при ВК наразі переконливо доведена у РКД та в умовах реальної клінічної практики. Ведолізумаб ефективний і при застосуванні як терапії першої лінії, і при його призначенні після неефективного лікування блокаторами ФНП-α. Зважаючи на те, що профіль безпеки ведолізумабу є співставним із таким у плацебо, в цьому контексті він може мати переваги перед іншими препаратами.
Takatsu N., Hisabe T., Higashi D., Ueki T., Matsui T. Vedolizumab in the Treatment of Ulcerative Colitis: An Evidence-Based Review of Safety, Efficacy and Place of Therapy. Core Evid. 2020 Apr 1; 15:7-20.
Підготувала Ірина Горобець
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (62) 2021 р.



