30 листопада, 2024
IDWeek 2024: результати новітніх досліджень у контексті раціональної антибіотикотерапії
![]() IDWeek – це щорічна міжнародна наукова подія, котра об’єднує фахівців охорони здоров’я в галузі інфекційних хвороб, епідеміології та профілактики: представників Американського товариства інфекціоністів, Американського товариства епідеміології охорони здоров’я, Асоціації медицини ВІЛ, Товариства дитячих інфекціоністів і Товариства інфекціоністів-фармацевтів. Цьогоріч вона проходила 16-19 жовтня в сонячному Лос-Анджелесі (США). IDWeek є визнаною платформою для презентацій нових досліджень, присвячених науковим досягненням і практичним підходам до профілактики, діагностики, лікування й епідеміології інфекційних захворювань, включаючи ВІЛ-інфекцію. До вашої уваги огляд результатів кількох найцікавіших досліджень стосовно призначень і тривалості антибіотикотерапії в госпіталізованих пацієнтів, уперше представлених на IDWeek 2024
IDWeek – це щорічна міжнародна наукова подія, котра об’єднує фахівців охорони здоров’я в галузі інфекційних хвороб, епідеміології та профілактики: представників Американського товариства інфекціоністів, Американського товариства епідеміології охорони здоров’я, Асоціації медицини ВІЛ, Товариства дитячих інфекціоністів і Товариства інфекціоністів-фармацевтів. Цьогоріч вона проходила 16-19 жовтня в сонячному Лос-Анджелесі (США). IDWeek є визнаною платформою для презентацій нових досліджень, присвячених науковим досягненням і практичним підходам до профілактики, діагностики, лікування й епідеміології інфекційних захворювань, включаючи ВІЛ-інфекцію. До вашої уваги огляд результатів кількох найцікавіших досліджень стосовно призначень і тривалості антибіотикотерапії в госпіталізованих пацієнтів, уперше представлених на IDWeek 2024
7 проти 14 днів антибіотикотерапії в пацієнтів з інфекціями кровотоку: результати дослідження BALANCE
 Нік Данеман, професор медицини в Університеті Торонто (Канада), у співавторстві з Робом Фаулером (канадська група дослідників) представили результати багатоцентрового міжнародного (7 країн) випробування BALANCE (Bacteraemia Antibiotic Length Actually Needed for Clinical Effectiveness), рандомізованого контрольованого дослідження для оцінювання ефективності 7-денної антибіотикотерапії (короткого курсу) порівняно з 14-денною в пацієнтів з бактеріємією.
Нік Данеман, професор медицини в Університеті Торонто (Канада), у співавторстві з Робом Фаулером (канадська група дослідників) представили результати багатоцентрового міжнародного (7 країн) випробування BALANCE (Bacteraemia Antibiotic Length Actually Needed for Clinical Effectiveness), рандомізованого контрольованого дослідження для оцінювання ефективності 7-денної антибіотикотерапії (короткого курсу) порівняно з 14-денною в пацієнтів з бактеріємією.
Вони зауважили, що такий показник, як тривалість застосування антибіотика, який призначається хворому, наразі є одним з наріжних каменів у контексті боротьби зі зростанням антибіотикорезистентності. Адже занадто коротке лікування може призвести до клінічної невдачі, рецидиву та селекції резистентності в патогенних збудників. Водночас занадто тривале лікування може призвести до селекції резистентності в сторонніх мікроорганізмів, які не є мішенню для призначених антибіотиків; розвитку інфекції Clostridium difficile; виникнення побічних ефектів і пов’язаних із цим витрат.
Актуальність визначення оптимального терміну призначення антибіотикотерапії при інфекціях кровотоку (ІК) визначає той факт, що їхня частота становить 600 тис. випадків щорічно в Північній Америці, вони фіксуються в 15% пацієнтів відділень інтенсивної терапії (ВІТ) і входять до 7 основних причин смерті.
Оптимальна тривалість лікування ІК недостатньо вивчена. До початку випробування BALANCE з метою вивчення цього питання не проводилися рандомізовані контрольовані дослідження, а після старту BALANCE добре сплановані дослідження були зосереджені на грамнегативних збудниках і залучали переважно не критично хворих осіб.
Для відповіді на запитання «Чи коротша 7-денна антибіотикотерапія не поступається тривалішій 14-денній антибіотикотерапії за рівнем 90-денної смертності в госпіталізованих пацієнтів з ІК?» було оцінено результати лікування у 3608 хворих, залучених до фінального аналізу.
Учасниками дослідження BALANCE були пацієнти, які відповідали таким критеріям:
- перебування в лікарні на момент отримання позитивного результату посіву крові;
- позитивний результат посіву крові з наявною патогенною бактерією.
Критерії виключення були такі:
- пацієнт уже залучений у дослідження;
- тяжка імуноскомпрометованість;
- протезований серцевий клапан;
- синдром, який доведено потребує тривалого лікування;
- виявлення Staphylococcus aureus;
- виявлення Candida spp. або інших грибів.
Пацієнти були розподілені на дві групи: група втручання – 7 календарних днів відповідної антибіотикотерапії та група порівняння – 14 календарних днів відповідної антибіотикотерапії. Первинним результатом вважали 90-денну смертність. Як вторинні результати оцінювали:
- смертність у лікарні й у ВІТ;
- тривалість перебування в лікарні й у ВІТ;
- тривалість штучної вентиляції легень і призначення вазопресорів;
- рецидив бактеріємії;
- кількість днів без антибіотиків;
- алергію на антибіотики та побічні реакції;
- розвиток інфекції C. difficile;
- інфікування/колонізація антибіотикорезистентними мікроорганізмами.
Характеристика пацієнтів
Середній вік пацієнтів, які увійшли до фінального аналізу, становив 70 (59-80) років, 53% були чоловічої статі. Частка хворих, які проходили лікування у ВІТ, становила 55%, у палатах відділення – 45%. Пацієнти з цукровим діабетом становили третину від усіх учасників дослідження, їх частка становила 31,8%; рак солідних органів мали 21,7% хворих, імуносупресію – 12,2%, ниркову недостатність – 11,8%. У переважної більшості учасників (75,4%) інфекція була позалікарняною. Джерелом інфекції найчастіше були сечові шляхи – 42,2%, далі йшли органи черевної порожнини / біліарний тракт – 18,8%, легені – 13%, судинний катетер – 6,3%, шкіра / м’які тканини – 5,2%, інше – 1,9%, у 12,6% хворих джерело інфекції не вдалося встановити.
Характеристика патогенів
Дослідники визначили топ-11 патогенних мікроорганізмів, які найчастіше висівалися у хворих з бактеріємію. Зокрема, частка Escherichia coli становила 43,8%, Klebsiella spp. – 15,3%, Enterococcus spp. – 6,9%, коагулазонегативного стафілокока – 4,8%, Pseudomonas spp. – 4,7%, Streptococcus pneumoniae – 4,5%, Enterobacter spp. – 4,4%, Proteus spp. – 3,7%, Serratia spp. – 2,4%, Streptococcus pyogenes – 2,1%, Streptococcus agalactiae – 2,1%.
Первинний результат: 90-денна смертність
Аналіз результатів показав, що смертність протягом 90 днів у групі пацієнтів 7-денної антибіотикотерапії становила 14,5%, у групі 14-денної – 16,1% з різницею ризиків -1,6% (95% довірчий інтервал від -4 до 0,8), що свідчить на користь коротшого лікування. Отримані результати також підтвердилися в додаткових аналізах і в різних підгрупах пацієнтів.
Нік Данеман зазначив: «Отже, можна чітко бачити, що 7 днів антибіотикотерапії не поступаються 14 дням для лікування ІК».
Вторинні результати
Численні вторинні результати дослідження також були схожими між двома групами порівняння. Автор дослідження виокремив три з них, які показали значне поліпшення при скороченні тривалості антибіотикотерапії: тривалість перебування в лікарні, виписка з лікарні в період до 28 днів і відсутність прийому антибіотиків у період до 28 днів.
Підсумовуючи отримані результати, Нік Данеман сказав, що 7-денний курс антибіотикотерапії, на думку дослідників, має бути загальною стратегією лікування пацієнтів з ІК. Такий підхід не погіршить результатів, при цьому забезпечить значну економію коштів на ліках і, що набагато важливіше, вірогідно сприятиме зменшенню частоти побічних ефектів і резистентності до антибіотиків. Однак ці результати не поширюються на кілька груп пацієнтів з високим ризиком (у яких було виявлено S. aureus або грибкові інфекції крові, наявний тяжкий імунодефіцит, протезовані серцеві клапани), які були виключені з дослідження.
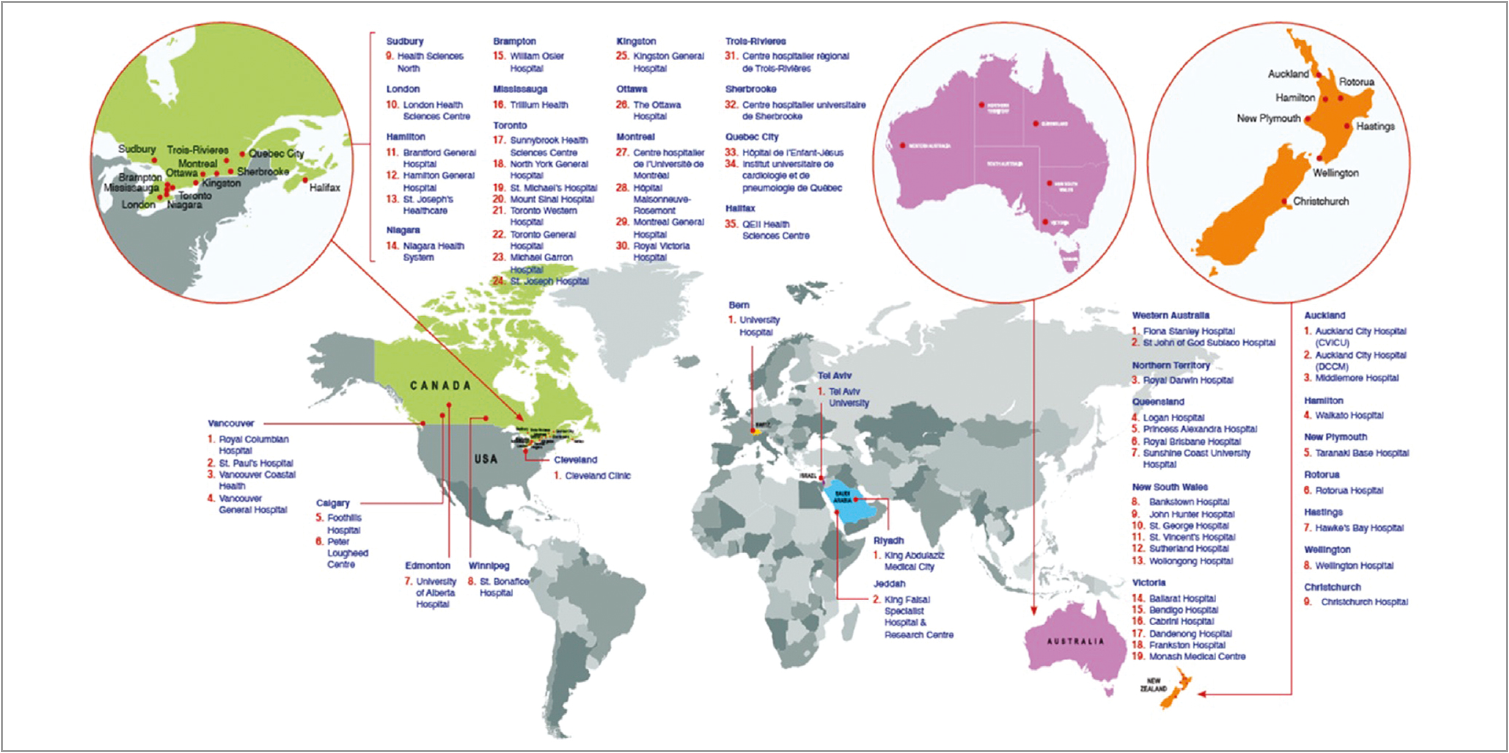
Рис. 1. Мапа розташування дослідницьких центрів
Дослідження INSPIRE: інтелектуальні підказки в режимі реального часу для покращення емпіричного вибору антибіотиків у пацієнтів з інфекціями шкіри та м’яких тканин
 Шруті К. Гохіл, доцентка кафедри інфекційних хвороб Медичної школи Каліфорнійського університету в Ірвіні (США), представила результати дослідження INSPIRE (INtelligent Stewardship Prompts to Improve Real-time Empiric Antibiotic Selection for Patients), у якому порівнювали рутинний метод вибору препарату для емпіричної антибіотикотерапії та метод з використанням комп’ютерних підказок. У межах цьогорічної IDWeek було представлено один з кількох фрагментів INSPIRE, а саме дослідження в когорті хворих з інфекціями шкіри та м’яких тканин.
Шруті К. Гохіл, доцентка кафедри інфекційних хвороб Медичної школи Каліфорнійського університету в Ірвіні (США), представила результати дослідження INSPIRE (INtelligent Stewardship Prompts to Improve Real-time Empiric Antibiotic Selection for Patients), у якому порівнювали рутинний метод вибору препарату для емпіричної антибіотикотерапії та метод з використанням комп’ютерних підказок. У межах цьогорічної IDWeek було представлено один з кількох фрагментів INSPIRE, а саме дослідження в когорті хворих з інфекціями шкіри та м’яких тканин.
Чи можемо ми змінити підходи до емпіричного вибору антибіотиків у некритичних пацієнтів? Дослідниця зазначила, що тільки в США реєструється понад 2,8 млн антибіотикорезистентних інфекцій щорічно та що саме надмірне призначення антибіотиків є основною причиною цього явища. Зокрема, 40% антибіотиків, які призначаються в стаціонарах, мають занадто широкий спектр дії.
Поточна практика призначення антибіотикотерапії зазвичай передбачає таку послідовність: старт з антибіотика широкого спектра (задля покриття можливих резистентних інфекцій) і надалі призначення антибіотика вузького спектра дії.
Нова практика передбачає протилежну тактику: старт з антибіотика вузького спектра з урахуванням даних про ризик резистентності, що дасть змогу уникнути використання антибіотиків широкого спектра. Відстрочка з призначенням останніх безпечна для переважної більшості випадків. Надалі препарат із широким спектром призначають за потреби.
Нозології, за яких найчастіше призначаються антибіотики в лікарнях США (Gohil S.K. et al., 2024):
- пневмонія;
- інфекції сечовивідних шляхів;
- абдомінальні інфекції;
- інфекції шкіри / м’яких тканин.
До мультирезистентних патогенів, які викликають найбільше занепокоєння в лікарів, належать:
- метицилінорезистентний S. aureus (MRSA);
- Pseudomonas spp.;
- ентеробактерії, що продукують β-лактамази розширеного спектра дії (ESBL);
- ентерококи, стійкі до ванкоміцину (VRE);
- ентеробактерії, стійкі до карбапенемів (CRE).
У дослідженні за участю 60 725 пацієнтів з інфекціями шкіри та м’яких тканин у 92 лікарнях оцінювали стандартне емпіричне призначення антибіотика порівняно з призначенням антибіотикотерапії з урахуванням «комп’ютерних підказок» (CPOE) в разі обрання лікарем антибіотиків широкого спектра дії. Електронні підказки з оцінкою ризику для конкретного пацієнта та рекомендації щодо вибору протимікробних препаратів надавалися в режимі реального часу.
У випробуванні брали участь пацієнти дорослого віку з інфекціями шкіри та м’яких тканин, госпіталізовані у звичайні відділення (не ВІТ).
Процес емпіричного призначення лікування з використанням CPOE полягав у такому. Коли лікар обирав антибіотик широкого спектра, на екрані активувалася підказка, згенерована на підставі оцінки абсолютного ризику мультирезистентної інфекції в цього пацієнта шляхом урахування всіх можливих складових:
- ризик, специфічний для пацієнта;
- ризик, специфічний для певного інфекційного синдрому;
- патогеноспецифічний ризик;
- ризик, специфічний для самої лікарні.
Антибіотиками розширеного спектра дії вважали такі препарати:
- даптоміцин, лінезолід (активні стосовно VRE);
- азтреонам, цефепім, цефтазидим, піперацилін/тазобактам (антипсевдомонадні);
- ертапенем, іміпенем, меропенем, цефтолозан/тазобактам (активні щодо ESBL).
Моделі для розрахунку ризику мультирезистентних збудників у пацієнтів з інфекціями шкіри та м’яких тканин у дослідженні INSPIRE були сформовані шляхом аналізу даних понад 195 тис. хворих з патологією за період 2017-2019 рр. з наступним розробленням алгоритму. Загалом було оцінено понад 60 змінних: демографічні показники, супутні хвороби, попереднє приймання антибіотиків, перебування в будинку престарілих, госпіталізація, лабораторні аналізи під час госпіталізації, попередні мультирезистентні інфекції.
Приклад: лікар призначає хворому з інфекцією шкіри / м’яких тканин цефепім. Комп’ютерна система оцінює можливий ризик інфікування Pseudomonas для цього пацієнта. Якщо ризик оцінюється як високий (≥10%), підказка не активується; в протилежному випадку система видає рекомендацію про недоцільність призначення цефепіму й натомість пропонує для цього пацієнта цефазолін (рис. 2).
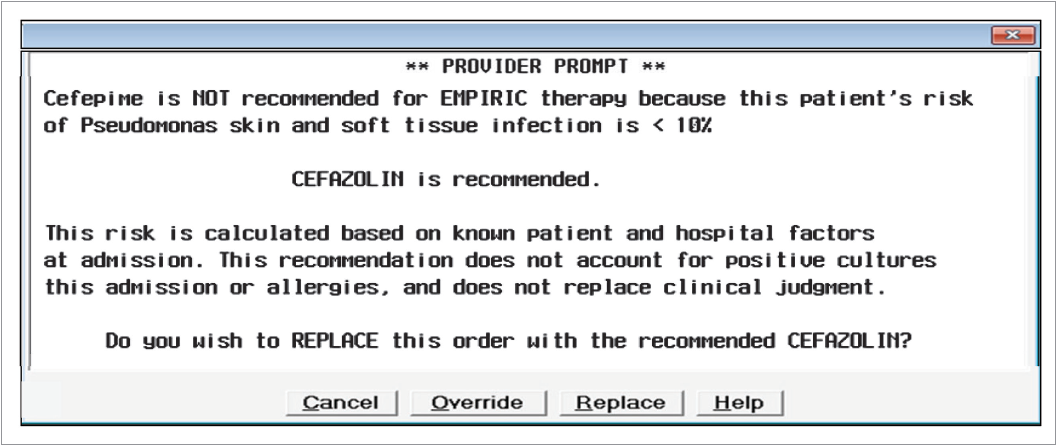
Рис. 2. Комп’ютерна підказка
Якщо лікар відхиляє запропонований системою препарат, відбувається перехід на наступний етап (нове віконце), де лікар має вказати причину своїх дій: наявність алергії в пацієнта; необхідність переведення його у ВІТ, зумовлена тяжкістю перебігу інфекційного процесу; позитивний результат на наявність мультирезистентних збудників; нейтропенія тощо.
Результати
Використання комп’ютерних підказок порівняно з рутинним веденням було пов’язане зі значно меншим призначенням (на 28%) антибіотиків широкого спектра дії й антипсевдомонадних препаратів у пацієнтів з інфекціями шкіри та м’яких тканин, які проходили стаціонарне лікування.
Показники безпеки (кількість днів до переведення у ВІТ) і тривалість перебування в лікарні не відрізнялися між групами порівняння.
Слід зауважити, що в представлених раніше результатах дослідження INSPIRE в когорті пацієнтів з пневмонією було показано зменшення кількості днів використання антибіотиків широкого спектра на 28%, а при інфекціях сечовивідних шляхів – на 17% (Gohil S.K. et al., 2024).
Підбиваючи підсумки, Шруті К. Гохіл зазначила, що використання системи CPOE з можливістю отримання персоналізованих підказок у режимі реального часу може зменшити частоту призначення антибіотиків широкого спектра для емпіричної терапії. Переваги автоматизованого підходу дають змогу застосовувати цю опцію незалежно від можливих збоїв у роботі лікарні (погодні умови, COVID-19); ця система працює в масштабах усієї лікарні, в нічний час та у вихідні. Також важливим є те, що ризик, оцінений системою й задокументований в електронній картці пацієнта, може бути використаний при вирішенні медико-правових проблем у лікарів.
|
Таблиця. Чинники, що були враховані при формуванні моделі ризику інфікування шкіри та м’яких тканин мультирезистентними збудниками в дослідженні INSPIRE |
|
|
Патоген |
Чинники, що свідчать про абсолютний ризик ≥10% |
|
VRE |
Відсутність чинників, за якими можна прогнозувати ризик ≥10% |
|
Pseudomonas |
Наявність інфекції, спричиненої синьогнійною паличкою, в анамнезі |
|
ESBL (не Pseudomonas) |
Наявність в анамнезі ESBL, % ESBL як причинного фактора інфекцій шкіри та м’яких тканин у медичному закладі |
|
ESBL (включно з Pseudomonas) |
Наявність в анамнезі ESBL/Pseudomonas, % ESBL як причинного фактора інфекцій шкіри та м’яких тканин у медичному закладі |
|
CRE |
Відсутність чинників, за якими можна прогнозувати ризик ≥10% |
За матеріалами:
https://www.jwatch.org/na58052/2024/10/23/idweek-2024-meeting-report-highlights-hospitalists
Підготувала Марія Ареф’єва
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (581), 2024 р



