24 листопада, 2025
Сучасна терапія пацієнтів із гострим та рецидивуючим циститом
За матеріалами майстер-класу «Алгоритми діагностики та лікування при захворюваннях нирок і сечовивідних шляхів. Огляд року: передова практика в нефрології та урології»
 21 жовтня 2025 року в Києві відбувся майстер-клас для нефрологів, урологів і фахівців суміжних спеціальностей «Алгоритми діагностики та лікування при захворюваннях нирок і сечовивідних шляхів. Огляд року: передова практика в нефрології та урології». У межах програми заходу було розглянуто широкий спектр проблемних питань, цікавих цільовій аудиторії. Зокрема, доповідь головного наукового співробітника відділу сексопатології та андрології ДУ «Інститут урології НАМН України» (м. Київ), професора кафедри урології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктора медичних наук, професора Юрія Миколайовича Гурженка присвячувалася питанню сучасної терапії хворих на гострий та рецидивуючий цистит.
21 жовтня 2025 року в Києві відбувся майстер-клас для нефрологів, урологів і фахівців суміжних спеціальностей «Алгоритми діагностики та лікування при захворюваннях нирок і сечовивідних шляхів. Огляд року: передова практика в нефрології та урології». У межах програми заходу було розглянуто широкий спектр проблемних питань, цікавих цільовій аудиторії. Зокрема, доповідь головного наукового співробітника відділу сексопатології та андрології ДУ «Інститут урології НАМН України» (м. Київ), професора кафедри урології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктора медичних наук, професора Юрія Миколайовича Гурженка присвячувалася питанню сучасної терапії хворих на гострий та рецидивуючий цистит.
Сечовипускання – це єдине задоволення, за яке не треба платити.
Арістотель
Цистит – інфекційно-запальний процес стінки сечового міхура (СМ), що локалізується переважно в слизовій оболонці. Гострий цистит уражає переважно жінок репродуктивного віку. Рецидиви також створюють серйозні клінічні проблеми та чинять значний вплив на якість життя пацієнтів. Рецидивний цистит – одна з найактуальніших клінічних проблем в урологічній практиці. Так, у 27% жінок спостерігають другий рецидив протягом подальших 6 міс, а ще в 3% розвивається третя інфекція сечовивідних шляхів (ІСШ) упродовж того самого періоду часу. Приблизно половина пацієнтів з уролітіазом страждають на ще один епізод протягом перших 5 років.
Деякі біологічні особливості СМ певною мірою забезпечують захист проти ІСШ. Вони включають механічний бар’єр, механічне очищення, хімічний склад сечі, бар’єр трикутника Льєто, імунний захист уретри, фагоцитарну функцію уротелію. Є й особливості та слабкі ланки, як-от близькість розташування сечовивідних і статевих органів, гормональна залежність (особливо в жінок старшого віку), венозна мережа СМ, анатомічні особливості уретри, зовнішній сфінктер уретри, вплив вегетативних розладів.
Серед факторів ризику виокремлюють:
- генітальні – хронічні захворювання матки та придатків, інфекції, що передаються статевим шляхом, бактеріальний вагіноз, урогенітальні захворювання в партнера, наявність в анамнезі ускладнень запального характеру;
- екстрегенітальні – цукровий діабет, порушення ліпідного обміну, анемія, захворювання нирок і сечовидільної системи, імунодефіцитні стани, дисбактеріоз, тривале застосування антацидів та глюкокортикоїдів;
- соціальні – хронічний стрес, низький рівень життя, недостатнє та нераціональне харчування, хронічний алкоголізм і наркоманія;
- поведінкові – ранній початок статевого життя, висока частота статевих контактів, велика кількість статевих партнерів, нетрадиційні форми статевих контактів, статеві зносини під час менструації.
Збудників гострого циститу досить багато; це можуть бути як неспецифічні, так і специфічні уропатогени (табл.).
|
Таблиця. Основні збудники гострого циститу |
|
|
Неспецифічні уропатогени |
Специфічні уропатогени |
|
◆ Escherichia сoli (найчастіше) ◆ Staphylococcus saprophyticus ◆ Proteus mirabilis ◆ Klebsiella pneumoniae ◆ Бета-гемолітичні стрептококи ◆ Enterobacter spp. ◆ Pseudomonas aeruginosa |
◆ Neisseria gonorrhoeae ◆ Chlamydia trachomatis ◆ Вірусна інфекція (вірус простого герпесу, аденовіруси) ◆ Ureaplasma spp. ◆ Mycoplasma spp. ◆ Урогенітальні мікози (Blastomyces dermatitidis, Candida spp., Torulopsis glabrata) |
Найчастіший шлях проникнення інфекції – висхідний, або уриногенний. Гематогенний шлях спостерігають не більш ніж у 3-5% випадків (на тлі тонзиліту, пульпіту, фурункульозу). Лімфогенний шлях інфікування можливий за наявності гострих та хронічних кишкових інфекцій. Можливий контактний шлях (нориці між піхвою і СМ або піхвою та прямою кишкою). Однією із причин розвитку циститу також може бути активація сапрофітної флори.
Патогенез циститу включає етапи адгезії, інвазії, колонізації, проліферації та ушкодження тканин.
Як зазначено в таблиці, найчастішим збудником циститу є Escherichia сoli (70-95% випадків), а також Staphylococcus saprophyticus (5-20% випадків). Водночас найважливіший фактор вірулентності Escherichia сoli та мікробів сімейства Enterobacteriaceae – здатність до адгезії до уротелію за допомогою спеціальних ворсинок різного типу – ворсинки 1 типу (pili), ворсинки (pap), S-ворсинки (sfa), а також афімбріального адгезину-1 (afa1) й антигенів полісахаридної капсули мікроорганізму [1]. Крім того, бактерії можуть переміщуватися уретрою вглиб у СМ за допомогою спеціальних пристосувань. Також уропатогенні штами Escherichia coli (UPEC) здатні виходити з апоптотичних клітин, уникаючи кліренсу завдяки процесу експоліації, та інфікувати сусідні епітеліальні клітини.
Ушкодження зовнішнього шару клітин уротелію супроводжується утворенням внутрішньоклітинних бактеріальних колоній. Потрапивши всередину клітини, Escherichia сoli може утворювати внутрішньоклітинну бактеріальну спільноту або здійснювати процес філаментації, у якому Escherichia сoli підтримує ріст бактерій, але не ділиться, щоб утворювати філаменти, що сприяє більшому контакту із клітинами-«парасольками» та дозволяє розпочати новий цикл інфекції. Відлущування уротелію відбувається природним шляхом або за допомогою зовнішніх сигналів, спричинених UPEC, як-от вивільнення α-гемолізину (HlyA), цитотоксичного некротизувального фактора‑1 (Cnf‑1) та вакуолізуючого самотранспортувального токсину (Sat), які зумовлюють ушкодження клітин, індукуючи апоптоз і надмірне відлущування [2].
Біль за циститу зумовлений ушкодженням стінки СМ, а саме двох її шарів: епітелію СМ (уротелію) із глікозаміноглікановим шаром і власної пластинки уротелію. При його руйнуванні токсичні речовини, що містяться в сечі, впливають на уротелій без захисту, спричиняючи викид гістаміну та інших медіаторів запалення. У відповідь на це у власній пластинці уротелію починає збільшуватися кількість нервових закінчень – т. зв. С-волокон, які відповідають за передачу до головного мозку сигналів хронічного болю. У разі будь-якого, навіть незначного, впливу на слизову оболонку СМ виникає позив до сечовипускання, що переходить у біль. Що більше руйнується глікозаміноглікановий шар, то сильнішими є постійні позиви до сечовипускання.
Захворювання характеризується гострим початком. Перший епізод – первинний гострий неспецифічний цистит, повторний випадок – хронічний цистит у стадії загострення. Крім того, виокремлюють т. зв. дефлораційний цистит, посткоїтальний цистит, а також гострий цистит, зумовлений захворюваннями, що передаються статевим шляхом. Вторинний цистит спостерігають при таких захворюваннях, як сечокам’яна хвороба, пієлонефрит, простатит, везикуліт, колікуліт, аномалії сечостатевої системи, інвазивні маніпуляції. Можливий розвиток циститу як ускладнення за розвитку лікарської алергії, цукрового діабету, імуносупресивної терапії, прийому антибіотиків, хіміопрепаратів, що передують інфекції, променевої терапії на тазовій ділянці, а також особливостей стану організму (вагітність, літній вік).
Загальні симптоми циститу неспецифічні та пов’язані з виходом токсинів зі слизової оболонки СМ до крові. Вони можуть включати загальну слабкість, головний біль, підвищення температури тіла (іноді до високих показників), нудоту, блювання.
Місцеві симптоми пов’язані безпосередньо із запаленням СМ і включають:
◆ біль унизу живота в проєкції СМ;
◆ біль при сечовипусканні ріжучого характеру;
◆ нетримання сечі (найчастіше в жінок);
◆ відчуття неповного випорожнення СМ;
◆ хибні позиви до сечовипускання – за сильного бажання помочитися;
◆ каламутна сеча, іноді із зеленуватим відтінком;
◆ неприємний запах сечі (пов’язаний з наявністю продуктів життєдіяльності бактерій у сечі).
Етапи діагностики циститу: ретельний збір анамнезу, загальний аналіз сечі, загальний аналіз крові з лейкоцитарною формулою, біохімічні дослідження крові, бактеріологічне дослідження сечі, огляд гінеколога, обстеження на наявність інфекцій, що передаються статевим шляхом, ультразвукове дослідження нирок і СМ.
Терапія розпочинається, по-перше, з немедикаментозних втручань – дієти (стіл № 10), пиття в кількості, достатній для підтримки діурезу (2000-2500 мл). При рецидивному циститі призначають фізіотерапію, фітотерапевтичні засоби.
Що стосується антибіотикотерапії, то існує думка, що немає «хороших» антибіотиків; натомість є чутливі мікроорганізми. Згідно з рекомендаціями Європейської асоціації урології (European Association of Urology, EAU) 2025 р., препаратом вибору в терапії гострого неускладненого циститу є фосфоміцину трометамол 3 г одноразово. Ця терапія дуже ефективна: до фосфоміцину високочутливі майже всі мікроорганізми – як грампозитивні (Staphylococcus, Streptococcus), так і грамнегативні (Escherichia сoli, Proteus, Klebsiella, Enterobacter), у т. ч. мультирезистентні штами Escherichia сoli, а також штами Escherichia сoli, що продукують бета-лактамази розширеного спектра.
При гострому неускладненому циститі препарат призначають у 1-й день хвороби в дозі 3 г, курс лікування становить 1 день. У разі хронічного (рецидивуючого) циститу призначають 3 г фосфоміцину 1 раз на 10 днів (протирецидивна терапія).
Препаратом резерву є нітрофурантоїн – уроантисептик, протимікробний засіб групи нітрофурану.
Для патогенетичної та симптоматичної терапії при гіперрефлексії СМ для зниження тонусу детрузора СМ застосовують М-холіноблокатори: толтеродин, оксибутинін, соліфенацин. За інтерстиціального, променевого, хімічного циститу призначають аналгетики. Перевагу у виборі віддають найприйнятнішим препаратам, що характеризуються значною вираженістю аналгезивного ефекту та меншою гастротоксичністю (німесулід, диклофенак, піроксикам, кетопрофен, кеторолак, напроксен, ібупрофен, метамізол натрію).
Новинкою у профілактиці циститу в жінок є комплекс компонентів Bacillus, який забезпечує антибактеріальну дію, протигрибкову та противірусну активність і сприяє посиленню специфічного й неспецифічного імунітету. Різні компоненти впливають на різні етапи патогенезу циститу. Комбінація Bacillus створює сприятливе середовище для захисту слизової оболонки, захищає від інфікування збудниками та від захворювань, запобігає дисбіозу й підвищує місцевий імунітет, а бетаїн і гіалуронова кислота у складі комплексу прискорюють загоєння.
Повертаючись до теми антибіотикотерапії, спікер нагадав, що цистит характеризується переважно бактеріальною етіологією, тому вирішальну роль має саме антибактеріальне лікування. Захворювання зазвичай лікують емпірично – без аналізу точної бактеріальної етіології чи чутливості до антибіотиків. Водночас антибіотики є не лише корисними: крім позитивних властивостей, вони мають і недоліки, як-от тривала зміна нормальної мікробіоти в сечостатевих органах, порушення мікробіоти в шлунково-кишковому тракті, поява мультирезистентних мікроорганізмів (останніми роками відіграє щоразу більшу роль). Крім того, антибіотикотерапія може мати значні побічні ефекти, пригнічувати імунну систему, збільшувати резистентність.
Найкращою альтернативою в такому разі є фітотерапія. Остання також має свої вимоги; зокрема, в лікуванні слід використовувати засоби рослинного походження, які мають низьку токсичність, поступове наростання та м’якість лікувального ефекту, відсутність побічних реакцій і комплексний механізм дії. Серед фітопрепаратів перевагу варто віддавати стандартизованим екстрактам, які гарантують сталість якості, характеризуються вищою концентрацією активних речовин, можуть зберігатися протягом тривалого періоду, мають високий рівень біоактивності, легко засвоюються організмом.
Таких рослин в Україні дуже багато: листя брусниці, толокнянка, квітки череди, плоди шипшини, листя кропиви, спориш, квітки звіробою, плоди журавлини, хвощ, шавлія. Доповідач наголосив, що EAU у своїх рекомендаціях ще у 2010 р. класифікувала журавлину (Vaccinium macrocarpon) у дозі проантоціанідинів 36-72 мг/добу як засіб профілактики інфекцій нижніх сечовивідних шляхів, адже журавлина має у своєму складі антиоксиданти, чинить бактерицидну дію, збагачена спектром вітамінів (зокрема, вітаміном С, який чинить антибактеріальну дію за рахунок створення кислішої реакції сечі), а також мікро- та макроелементів. Саме журавлина (англ. pembina) історично використовувалася індіанцями Північної Америки для лікування ІСШ [3]. Механізм її дії включає пригнічення адгезії бактерій (переважно Escherichia сoli) до уроепітеліальних клітин. У дослідженні I. Singh та співавт. (2016) у групи пацієнтів через 12 тиж прийому екстракту журавлини порівняно із плацебо зменшилася адгезія бактерій. Екстракт журавлини також перевершував плацебо щодо зниження рН сечі та запобігання таким симптомам ІСШ, як дизурія, бактеріурія, піурія [4].
Екстракт шавлії також має високу антибактеріальну активність стосовно основних уропатогенів; зокрема, його ефективність проти Escherichia сoli та Klebsiella становить 96 і 100% відповідно.
Метиленовий синій (метилтіонінію хлорид) використовують в урології як уроантисептик при інфекціях сечостатевих шляхів, для метафілактики сечокам’яної хвороби та з метою періопераційного контрастування. Він діє бактерицидно на грамнегативні бактерії, має гідрофільні властивості, малу молекулярну масу, проникає через канали зовнішньої мембрани бактерій; при циститі усуває збудника в слизовій оболонці та руйнує бактеріальні плівки. Метилтіонінію хлорид демонструє протимікробний ефект у сечостатевих шляхах, протизапальний ефект – у передміхуровій залозі, а також використовується з метою метафілактики сечокам’яної хвороби.
Склад комплексу Пембіна-Блю® базується на рекомендаціях EAU і включає екстракт сухий листя шавлії (Salvia officinalis) 100 мг, екстракт плодів журавлини великоплідної (Vaccinium macrocarpon) із 40% проантоціанідинів 200 мг і метилтіонінію хлориду 30 мг. Ці компоненти чинять пряму бактерицидну дію, забезпечують усунення збудника із глибоких шарів уротелію, боротьбу з адгезією, запобігаючи колонізації уропатогенами сечовивідних шляхів, а також зменшують ризик рецидивування. Показано, що комплекс достовірно зменшує частоту рецидивів ІСШ через 3 та 6 міс. Окрім того, частота рецидивів у пацієнтів із хронічним бактеріальним простатитом, які отримували Пембіна-Блю®, за період >3 міс була вдвічі нижчою, ніж в осіб контрольної групи.
Використання зазначеного комплексу у веденні рецидивуючих інфекцій нижніх сечовивідних шляхів у жінок було показано у 2022 р. [5]. Вживання Пембіна-Блю® курсом від 7 днів продемонструвало значний антибактеріальний, спазмолітичний та знеболювальний ефект. Зроблено висновок, що цей фітокомплекс може використовуватися як монозасіб або в комплексному веденні циститу з метою підкислення сечі. Кращі результати спостерігають у хворих із початковим показником рН сечі >7. В іншому дослідженні описано досвід використання Пембіна-Блю® у хворих на катетерасоційовані інфекції нижніх сечовивідних шляхів, яке виявилося ефективним у 86,7% пацієнтів [6].
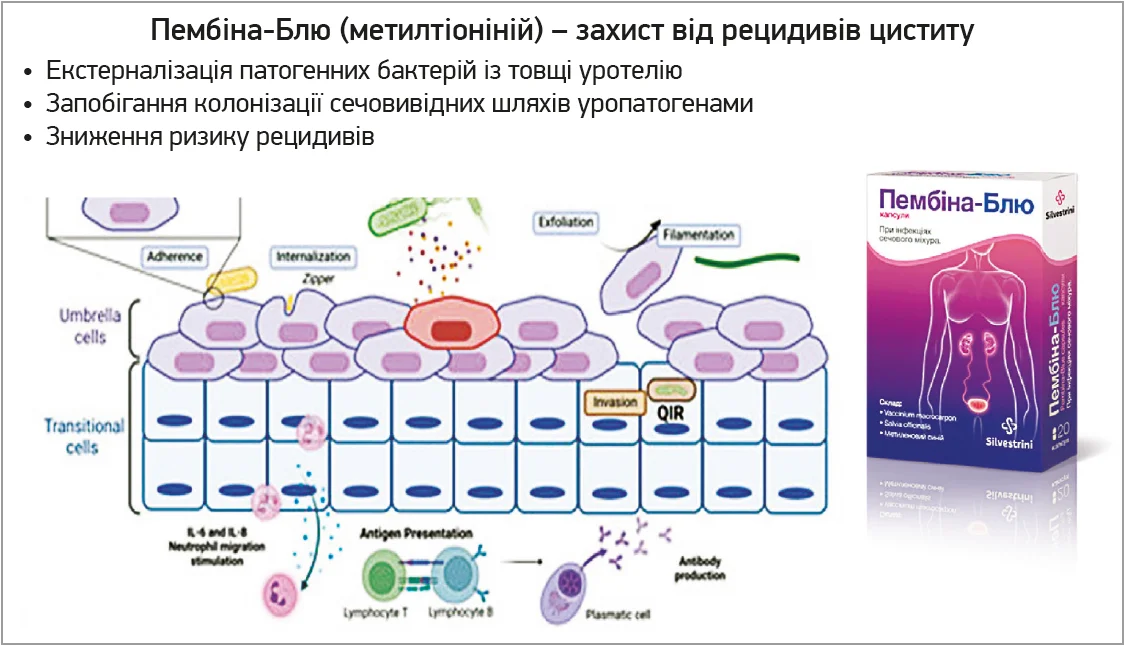
Доведена здатність компонентів Пембіна-Блю® проникати в біоплівки й екстерналізувати та нищити патогенні бактерії. Екстерналізація патогенних бактерій у товщі уротелію запобігає колонізації уропатогенами сечових шляхів, а також знижує ризик розвитку рецидивів (рис. 1). Це надає захист від повторного циститу.
Ще одним засобом є конкурентний інгібітор бактеріальної адгезії D-маноза – натуральний цукор із кукурудзи, який запобігає прилипанню бактерій до клітин. D-маноза сприяє зв’язуванню бактеріальних фімбрій. У результаті бактерії-збудники виводяться при сечовипусканні без шкоди для здоров’я. Захисні властивості D-манози виявляються, коли її концентрація в сечі становить >0,1%. Коли концентрація перевищує 2,5%, бактерії стають безпорадними і не можуть прикріплюватися до стінок СМ, тому необхідна доза D-манози становить 2000-6000 мг/добу. D-маноза засвоюється мікробіотою організму та частково розщеплюється в процесі гліколізу. Багато представників мікробіоти людини (лактобацили, біфідобактерії, непатогенні штами Escherichia сoli тощо) мають гени, що кодують білок XYZ-пермеази D-манози, необхідної для її усмоктування всередину бактерій для подальшої переробки.
Санлайф Д-маноза – німецький продукт, який містить D-манозу з порошком журавлинного соку й вітамінами С та В2. D-маноза здатна зв’язувати й блокувати адгезини FimH, розташовані на кінчику бактеріальних фімбрій типу I, відіграючи роль конкурентного інгібітора бактеріальної адгезії до рецепторів урогенітальних клітин.
Використання D-манози знижує ризик повторних ІСШ. Декілька досліджень продемонстрували, що в сечі Escherichia сoli приєднується до D-манози. Остання запобігає адгезії бактерій до стінки СМ за допомогою механізму конкурентного інгібування.
D-маноза виконує функцію уротеліального бар’єра, перешкоджаючи адгезії бактерій до уротелію. Зв’язуючи вільну D-манозу, бактерії блокуються в сечі, а потім виводяться сечовивідними шляхами. Цей ефект спостерігається і при одночасному застосуванні антибіотиків. Водночас тривале використання D-манози визнано безпечним. Декілька досліджень, оглядів і метааналізів демонструють, що використання D-манози знижує ризик рецидивів.
У рекомендаціях EAU D-маноза (поряд із журавлиною) розглядається як альтернатива антибіотикам у профілактиці хронічних рецидивуючих ІСШ.
Переваги Санлайф Д-манози включають наявність адекватного дозування (2000 мг), зручність прийому (у формі порошку в стіках) і високу німецьку якість. Продукт блокує адгезію мікроорганізмів до стінок СМ, забезпечує профілактику рецидивів циститу, а також підтримує імунну систему.
Ще один продукт, на котрий звернув увагу експерт, – патентований комплекс для підтримки функції нирок і сечостатевої системи, який містить суміш стандартизованих за вмістом рослинних екстрактів флавоноїдів, – сухий екстракт Креолесан™, 1 капсула якого містить олію ялиці 25,50 мг, сухий екстракт «Креолесан» (екстракт хмелю шишок, екстракт моркви дикої плодів, екстракт материнки трави, мальтодекстрин) 11,03 мг та олію м’яти перцевої 7,46 мг [7] (рис. 2).
Креолесан™ – комбінований продукт рослинного походження із широким спектром дії:
- сечогінна: збільшує утворення та виділення сечі, що сприяє виведенню піску й дрібного каміння з нирок та СМ;
- спазмолітична: усуває спазм гладких м’язів сечовивідних і жовчних шляхів, що зменшує біль;
- протизапальна: зменшує запалення в сечовивідних шляхах, що полегшує симптоми циститу та пієлонефриту;
- антимікробна: допомагає подолати ІСШ.
Комплекс може бути рекомендований як джерело біологічно активних речовин пацієнтам з інфекційно-запальними захворюваннями сечовидільної системи (цистит), у т. ч. пацієнтам із хронічною хворобою нирок, сечокам’яною хворобою та її попередником – сечокислим діатезом, жовчнокам’яною хворобою, для профілактики утворення конкрементів, до та після їхнього видалення. Завдяки своїм властивостям Креолесан™ сприяє покращенню функціонування нирок і сечостатевої системи. Спосіб вживання у дорослих – 1 капсула 3 р/день перед їдою, курс становить 1-2 міс (точна тривалість – за рекомендацією фахівця).
Методи профілактики рецидивів, згідно з рекомендаціями EAU (2025), включають приймання антибіотиків, зокрема фосфоміцину 1 раз на 10 днів, а також альтернативні методи (замісна гормональна терапія в жінок віком >40 років), фітотерапію (Пембіна-Блю®), методи неспецифічної профілактики (фітотерапія, підкислення сечі тощо). Водночас доповідач зауважив, що застосування антибіотиків для профілактики рецидивів ІСШ можливе тільки після розгляду заходів щодо зміни способу життя. Тривала або посткоїтальна антибактеріальна профілактика рецидивів ІСШ може застосовуватися лише в разі безуспішності профілактичних заходів без застосування антибіотиків.
Спікер також нагадав про важливість дотримання гігієни тіла та догляду за зовнішніми статевими органами, адже чистота є запорукою здоров’я. Завершив свій виступ він висловлюванням Александера Флемінга (Alexander Fleming): «Боротьба людства з мікробами – процес безкінечний. І потрібно все зробити для того, щоб частіше перемагала людина».
Список літератури знаходиться в редакції.
Підготувала Віталіна Хмельницька
Медична газета «Здоров’я України 21 сторіччя» № 19 (605), 2025 р